GP方案结合PD-1抑制剂治疗NSCLC的疗效及对Survivin蛋白、免疫细胞水平的影响
2021-01-26王利民
王利民,罗 敏,胡 萍,高 利
四川省成都市中西医结合医院医学检验科,四川成都 610041
肺癌是最常见的恶性肿瘤之一,已成为我国城市人口恶性肿瘤死亡原因的第1位[1-2]。非小细胞肺癌(NSCLC)包括鳞状细胞癌(鳞癌)、腺癌、大细胞癌,与小细胞肺癌相比,其癌细胞生长、分裂速度较慢,扩散、转移相对较晚。NSCLC约占所有肺癌的80%,约75%的患者发现时已处于中晚期,5年生存率很低[3-4]。化疗是肺癌的主要治疗方法,90%以上的肺癌患者需要接受化疗,尤其是NSCLC患者。化疗治疗NSCLC的肿瘤缓解率为40%~50%,但是化疗一般不能治愈NSCLC,只能延长患者生存时间和改善患者生活质量。程序性细胞死亡蛋白-1(PD-1)是一种重要的免疫抑制分子[5],通过向下调节免疫系统对人体细胞的反应,以及通过抑制T细胞介导的炎症活动来调节免疫系统并促进自身耐受。PD-1可以预防自身免疫性疾病,也可以阻碍免疫系统杀死癌细胞[6]。笔者采用PD-1抑制剂联合GP化疗方案治疗NSCLC,以探讨其对NSCLC患者疗效的影响,现报道如下。
1 资料与方法
1.1一般资料 选取2018年3月至2019年3月本院收治的105例NSCLC患者,按照随机数字表法将其分为对照组(52例)及观察组(53例)。对照组年龄31~75岁,平均(62.3±7.5)岁;体质量51~65 kg,平均(56.43±5.12)kg。观察组年龄31~76岁,平均(62.5±7.3)岁;体质量53~66 kg,平均(56.84±5.51)kg。两组患者性别、年龄、TNM分期比较,差异无统计学意义(P>0.05),具有可比性,见表1。以上患者均于本院确诊为NSCLC。本研究经本院伦理委员会批准,患者及家属均知情并同意本研究。
1.2纳入与排除标准 纳入标准:未合并严重营养不良及贫血;无严重传染性疾病;无精神系统疾病;符合内科学(第8版)中NSCLC的诊断标准[7]。排除标准:长期服用免疫抑制剂者;肝肾功能障碍者;合并急性感染者;入院前经系统性化疗者;无法耐受本研究化疗方案者;因各种原因无法完成本研究者;肿瘤肺外转移者。
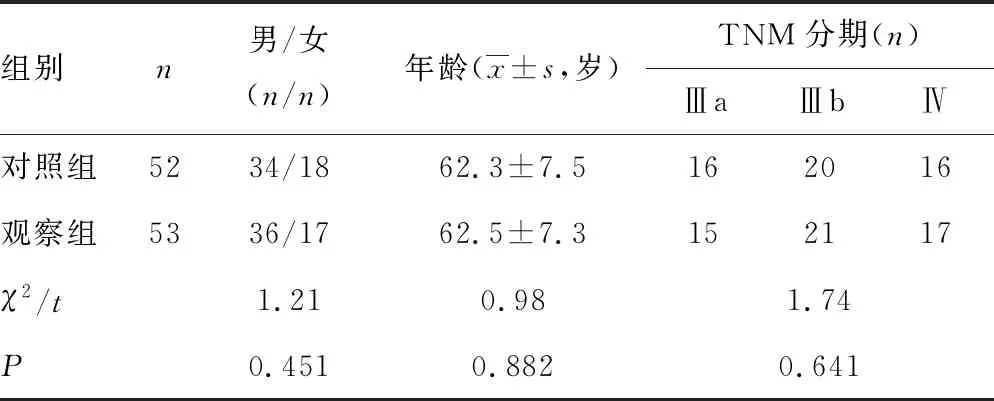
表1 两组患者一般资料比较
1.3方法 对照组患者给予吉西他滨(国药准字:H20123362;生产企业:连云港杰瑞药业有限公司;日剂量为1 000 mg/m2)+顺铂(国药准字:H20023461;生产企业:齐鲁制药有限公司;日剂量为75 mg/m2)进行治疗,静脉滴注。治疗周期为20 d,共治疗6个周期。观察组在对照组基础上给予PD-1抑制剂(国药准字:S20180019;生产企业:美国默沙东公司;2 mg/kg)静脉滴注,21 d为1个周期,共治疗6个周期。若患者出现不适及不良反应,应及时报告上级医师,并采取相应治疗措施。比较两组患者治疗前及治疗后6个月血清Survivin蛋白水平,治疗前及治疗后6个月CD4+、CD8+、CD4+/CD8+、自然杀伤(NK)细胞水平。观察两组患者治疗后6个月的疗效,治疗前及治疗后1、3、6个月的生存质量评分,以及不良反应发生情况。血清Survivin蛋白采用ELISA法进行测定。CD4+、CD8+、CD4+/CD8+、NK细胞采用流式细胞仪(HPC-150)进行检测。所有操作均由本院检验科医师按照说明书进行操作。
1.4疗效评价 根据世界卫生组织(WHO)实体瘤的效果评价标准进行评价[7],将疗效分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)和病情进展(PD)。疾病控制率=CR率+PR率+SD率;总有效率=CR率+PR率。
2 结 果
2.1两组患者治疗前后Survivin蛋白水平比较 两组患者治疗前Survivin蛋白水平比较,差异无统计学意义(P>0.05),治疗后6个月两组患者Survivin蛋白水平均明显降低(P<0.05),观察组患者Survivin蛋白水平明显低于对照组(P<0.05)。见表2。
2.2两组患者免疫功能比较 两组患者治疗前CD4+、CD8+、CD4+/CD8+、NK细胞水平差异无统计学意义(P>0.05),治疗后6个月两组患者CD4+、CD4+/CD8+、NK细胞水平与治疗前比较,均明显升高(P<0.05),观察组患者治疗后6个月的CD4+、CD4+/CD8+、NK细胞水平明显高于对照组(P<0.05)。见表3。
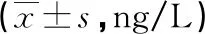
表2 两组患者治疗前后Survivin蛋白水平比较
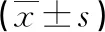
表3 两组患者免疫功能比较
2.3两组患者治疗后6个月的疗效比较 两组患者治疗后6个月的疗效差异有统计学意义(P<0.05),观察组总有效率及疾病控制率明显高于对照组(P<0.05)。见表4。
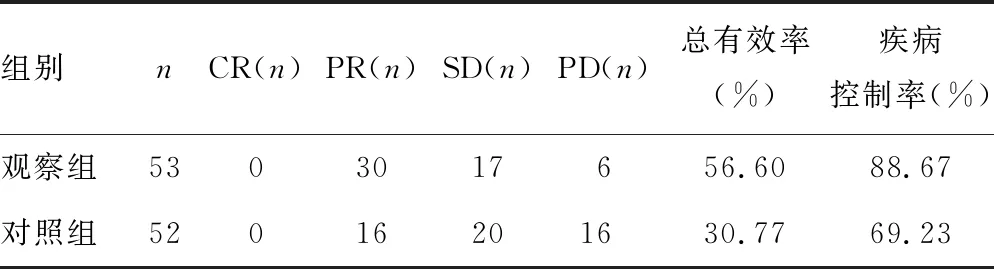
表4 两组患者治疗后6个月的疗效比较
2.4两组患者治疗前后的生存质量评分比较 治疗前,两组患者的生存质量评分差异无统计学意义(P>0.05),治疗后1、3、6个月的生存质量评分比较,差异有统计学意义(P<0.05)。随着治疗的进行,两组患者的生存质量评分均有明显改善。治疗后1、3、6个月观察组患者的生存质量评分明显高于对照组(P<0.05)。见表5。
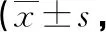
表5 两组患者的生存质量评分比较分)
2.5两组患者不良反应比较 两组患者均未出现严重不可逆不良反应。观察组出现骨髓抑制6例,肝功能损伤3例,肾功能损伤2例。对照组出现骨髓抑制5例,肝功能损伤5例,肾功能损伤6例。两组不良反应发生率比较,差异无统计学意义(P>0.05),且两组患者的不良反应经调整药物剂量后均得到显著改善。
3 讨 论
随着生活污染的加重,肺癌的发病率呈逐年升高的趋势[8-9]。近年来,化疗逐渐成为NSCLC治疗的重要手段,并取得了良好的治疗效果。随着分子生物学技术的不断发展,越来越多的分子生物学靶点被用于NSCLC的治疗,并被证明具有积极的治疗效果。PD-1是一种重要的免疫抑制分子,为免疫球蛋白超家族成员。有研究发现,以PD-1为靶点的免疫调节对抗肿瘤、抗感染、抗自身免疫性疾病及促进移植器官的存活等均具有重要的意义[10-11]。其配体PD-L1也可作为靶点,相应的抗体可以起到相同的作用。PD-1和PD-L1结合启动T细胞的程序性死亡,使肿瘤细胞获得免疫逃逸。PD-1抑制剂是阻断PD-1的一类新药,可激活免疫系统以攻击肿瘤,并用于治疗某些类型的癌症。
Survivin是凋亡抑制蛋白家族的新成员,Survivin具有肿瘤特异性,只表达于肿瘤和胚胎组织。有研究发现,Survivin与NSCLC患者肿瘤细胞的分化、增殖及浸润转移密切相关,其水平的升高提示肿瘤的快速增殖[12-13]。同时Survivin蛋白的表达也与NSCLC患者预后密切相关。为此,笔者将Survivin蛋白与CD4+、CD8+、NK细胞等免疫因子纳为NSCLC患者预后的评价指标。本研究中,两组患者治疗前Survivin蛋白水平比较,差异无统计学意义(P>0.05),治疗后6个月两组患者Survivin蛋白水平均明显降低(P<0.05),观察组患者Survivin蛋白水平明显低于对照组(P<0.05)。
两组患者治疗前CD4+、CD8+、CD4+/CD8+、NK细胞水平比较,差异无统计学意义(P>0.05),治疗后6个月两组患者CD4+、CD4+/CD8+、NK细胞水平与治疗前比较,均明显升高(P<0.05),且观察组明显高于对照组(P<0.05)。此结果表明,GP方案联合PD-1抑制剂相对于GP方案更能有效改善NSCLC患者的免疫功能。CHEN等[14]也在研究中得出相似结论,可能与PD-1抑制剂有效抑制了PD-1导致的自身免疫细胞功能下调有关,这在很大程度上改善了人体的自身免疫对肿瘤细胞的杀伤能力。两组患者疗效比较,差异有统计学意义(P<0.05),观察组总有效率及疾病控制率明显高于对照组(P<0.05)。随着治疗的进行,两组患者的生存质量评分均明显改善,治疗后1、3、6个月观察组患者的生存质量评分明显高于对照组(P<0.05)。此结果表明,GP方案联合PD-1抑制剂相对于GP方案更能有效提升NSCLC患者的疗效。CHEN等[15]也在研究中发现,GP方案联合PD-1抑制剂能显著改善NSCLC患者预后及生活质量,这可能与PD-1抑制剂有效减少了肿瘤细胞的免疫逃逸,显著改善患者自身免疫功能有关,与本研究结果基本一致。两组患者不良反应发生率比较,差异无统计学意义(P>0.05),且两组患者不良反应较轻,经调整药物剂量后均得到显著改善。此结果表明,PD-1并不会显著增加GP方案治疗患者的相关不良反应,具有较高的安全性。本研究还存在不足之处,需扩大样本量进一步证实其安全性。
综上所述,GP方案结合PD-1抑制剂治疗能有效提升NSCLC患者疗效及改善免疫功能,提高患者生活质量,值得临床推广。
