成人型神经元核内包涵体病相关视网膜病变的多模式影像学分析△
2021-01-22陈倩栾兴华冯超逸孙平曹煜雯邬静莹王诗格孙兴怀曹立田国红
陈倩 栾兴华 冯超逸 孙平 曹煜雯 邬静莹 王诗格 孙兴怀,3 曹立田国红,3
[1.复旦大学附属眼耳鼻喉科医院眼科 上海 200031;2.上海交通大学附属上海市第六人民医院神经内科 上海 201101;3.上海市视觉损害与重建重点实验室(复旦大学) 上海 200031]
神经元核内包涵体病(neuronal intranuclear inclusion disease,NIID)是一种罕见常染色体显性遗传性,慢性进展性神经退变性疾病,以神经元内嗜酸性透明包涵体形成为特征,涉及多器官。其临床表现多样,包括痴呆、肢体无力、小脑共济失调、肌张力障碍和自主神经功能失调[1]。根据发病年龄不同可分为儿童型、青少年型和成人型[2]。随着皮肤组织病理学及基因诊断技术的发展,近年来出现了较多临床报道,但眼部表现仅限于瞳孔缩小及夜盲、视网膜电图(electroretinogram, ERG)反应降低等[3-5]。目前国内尚未见到详尽的眼部检查及光学相干层析成像(optical coherence tomography, OCT)影像学研究报道。本文收集整理了5例国人散发成人型NIID的眼部临床表现及其特征,运用眼科多模式影像,首次提出该病视网膜病变特征及瞳孔缩小的眼部机制,以期为该病的早期诊断及筛查提供更多的临床手段,提高国内相关医师对于该病眼部特征的认识。
1 资料与方法
1.1 资料 2020年9~11月间经上海交通大学附属上海市第六人民医院神经内科确诊的成人散发型NIID患者5例,转诊复旦大学附属眼耳鼻喉科医院神经眼科门诊评估并行详尽眼科检查。所有病例均经影像学检查、皮肤活检及基因检测明确诊断。5例中男性1例、女性4例,神经系统表现包括痴呆、肢体无力、自主神经功能紊乱等。
1.2 方法 所有病例均行详细双眼裂隙灯眼部检查及各项辅助检查,收集其特征性病变。辅助检查包括最佳矫正视力(best corrected visual acuity, BCVA)、眼底照相、超广角眼底照相及自发荧光、中心视野、OCT、ERG、多焦ERG(multifocal ERG,mfERG)、超声生物显微镜(ultrasound biomicroscopy,UBM)等。
2 结果
2.1 一般特征 5例患者均表现为双眼一致性病变,病例一般特征见表1。
2.2 眼底及自发荧光改变 5例患者后极部及超广角眼底照片见图1左列及中列。双眼病变表现一致。病例1~4均表现为双眼视盘周围视网膜脉络膜萎缩脱色素,病例1伴有黄斑区脱色素改变,病例5眼底无明显异常。
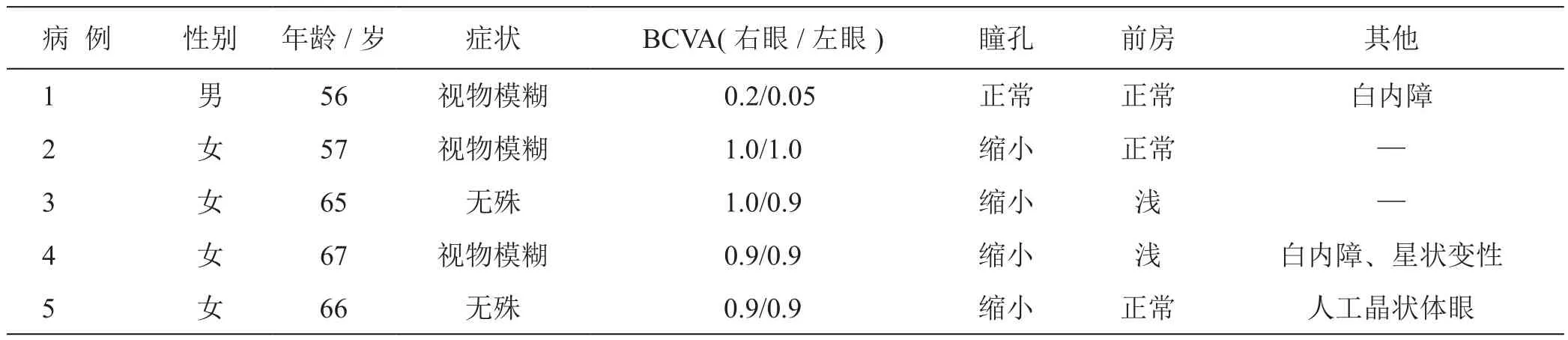
表1 5例NIID患者一般情况
5例患者眼底广角自发荧光表现见图1右列。双眼表现一致。病例1、4 表现为双眼视盘周围及黄斑区弱荧光,病例2、3表现为视盘周围荧光斑驳,病例5无明显改变。5例均未发现周边部异常自发荧光。
2.3 中心视野 病例1、4、5完成中心视野检查,均表现为不同程度的生理盲点扩大或中心视野缺损。
2.4 OCT 5例患者OCT黄斑区结构分析显示不同程度的椭圆体带缺失(图2),其中病例1、4为后极部弥漫性椭圆体带缺失,病例2、3为视盘旁椭圆体带缺失,视网膜内可见散在高反射细点。视乳头周围视网膜神经纤维层(retinal nerve fiber layer,RNFL)厚度无明显异常或局灶轻微变薄,黄斑区视网膜节细胞复合体(ganglion cell inner plexiform layer complex,GCIPL)显示弥漫性变薄(图2)。
2.5 ERG 病例3、4因明显浅前房未能进行ERG检测,其余3例均行ERG和mfERG检测。ERG:病例1、2显示明暗视反应均轻中度降低伴有隐含期延迟;病例5暗视反应基本正常,明视反应轻度降低(图3)。mfERG:均显示后极部不同程度振幅降低伴潜伏期延迟,且部分不以黄斑为中心 (图4)。
2.6 UBM检查 病例1、3、5完成了UBM检查。病例1显示前节完全正常;病例3浅前房窄角伴有睫状突肥大旋前;病例5白内障术后前房不浅,房角开放,但睫状突肥大旋前(图5)。
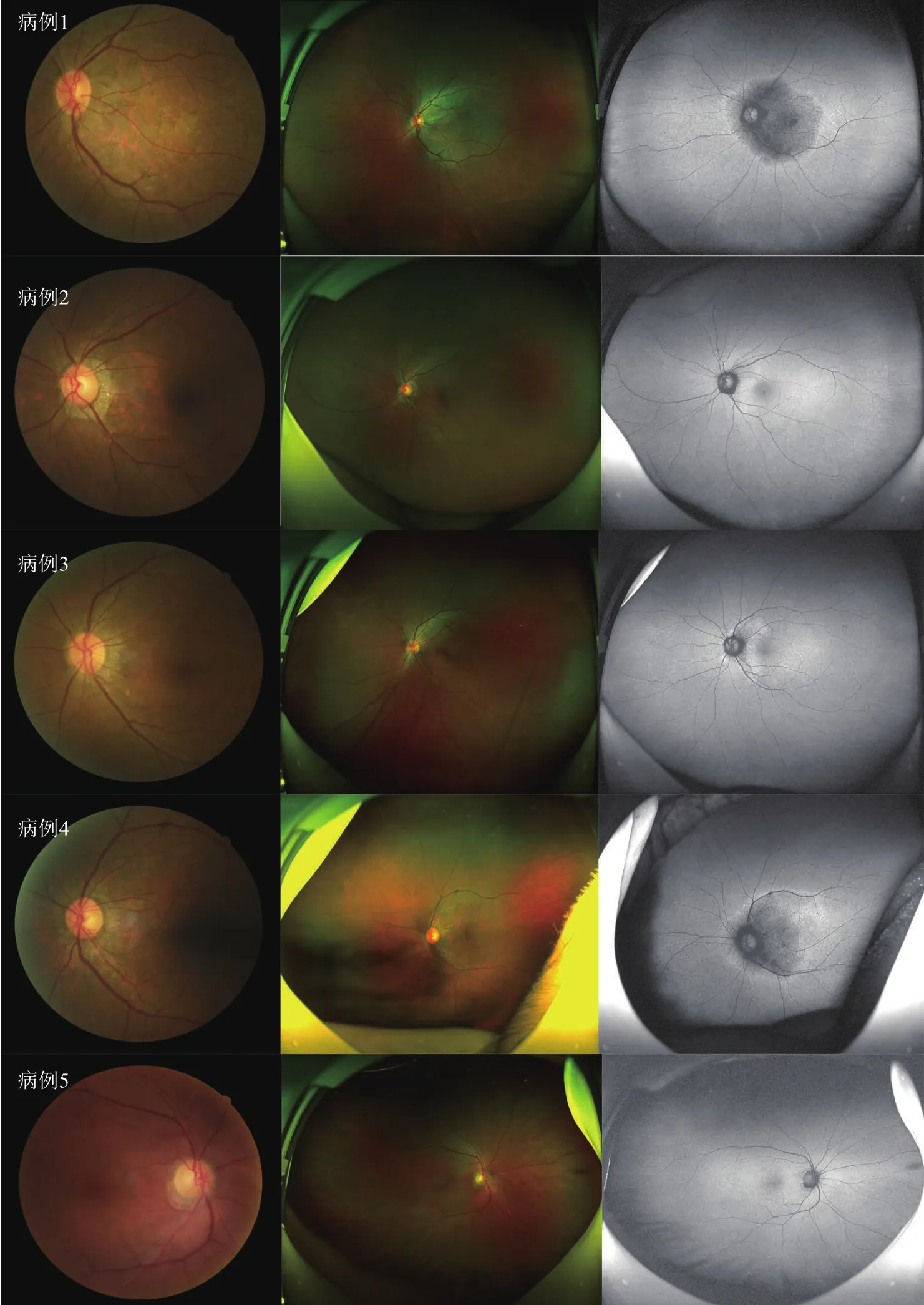
图1 5例NIID患者后极部眼底相、超广角眼底相及自发荧光改变
3 讨论
NIID是一种罕见病,由 Haltia 等[1]在1984年首次提出。由于该病缺乏特异性临床表现,且活检困难,给诊断带来巨大挑战。2016年Sone等[6]提出NIID的诊断流程并被广泛认可和采用:磁共振 成 像 (magnetic resonance imaging,MRI)DWI序列呈现皮髓质交界区特征性“绸带征”;皮肤活检见神经元核内嗜酸性包涵体;基因检测排除FMR1基因所致的脆性X染色体相关震颤/共济失调 (FXTAS)。2019年由中、日两国研究团队分别揭示了NIID 致病机制与NOTCH2NLC基因中GGC异常重复扩增相关,因此明确了其相关致病基因[7-10]。此后的国内外研究均表明,该基因突变除可导致NIID外,在少数阿尔茨海默病、额颞叶痴呆、帕金森综合征、多系统萎缩、特发性震颤、成年型白质脑病等神经系统变性病患者中也可被检测到。因此有学者[11]提出将NIID的疾病名称变更为NOTCH2NLC相关重复扩展性疾病(NRRED)更为合适。
国外已有少量病例报道显示NIID患者可发生进行性视网膜变性,但多为个案,总数仅十余例,临床表现具有相似性,病变以感光细胞为主,常发生于视盘旁和中周部区域[3-5]。本组病例是目前国内首次报道NIID相关视网膜病变,其OCT检查结果验证了感光细胞是视网膜主要受累部位,但本组病例超广角眼底照相及自发荧光结果显示5例病变均局限于视盘旁或累及后极部,并未发现诸如文献报道中的中周部及周边部病变。此外,在本组病例研究中GCIPL在受检患者均存在弥漫性变薄,即便患者病灶局限于视盘旁且改变轻微,这在国外以往报道中从未提及,因此提示神经节细胞可能也是NIID相关视网膜病变的受累部位。
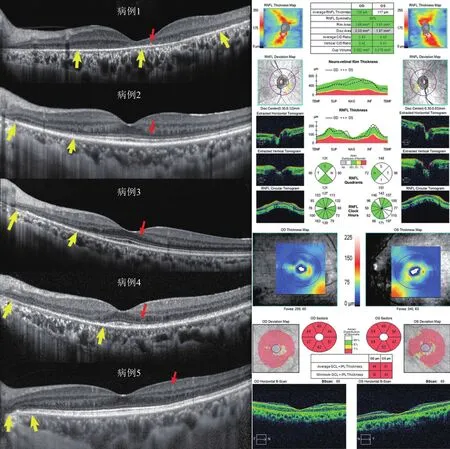
图2 5例NIID患者OCT、RNFL及GCIPL改变 黄斑区结构分析显示不同程度的椭圆体带缺失,黄箭头示各例椭圆体带缺失范围,红箭头示散布于视网膜各层中的高反射细点。右列上、下图分别显示基本正常的RNFL和同一患者弥漫性变薄的黄斑区GCIPL。

图3 3例NIID患者ERG结果 相比于正常人,各项反应呈不同程度振幅降低和隐含期延迟。
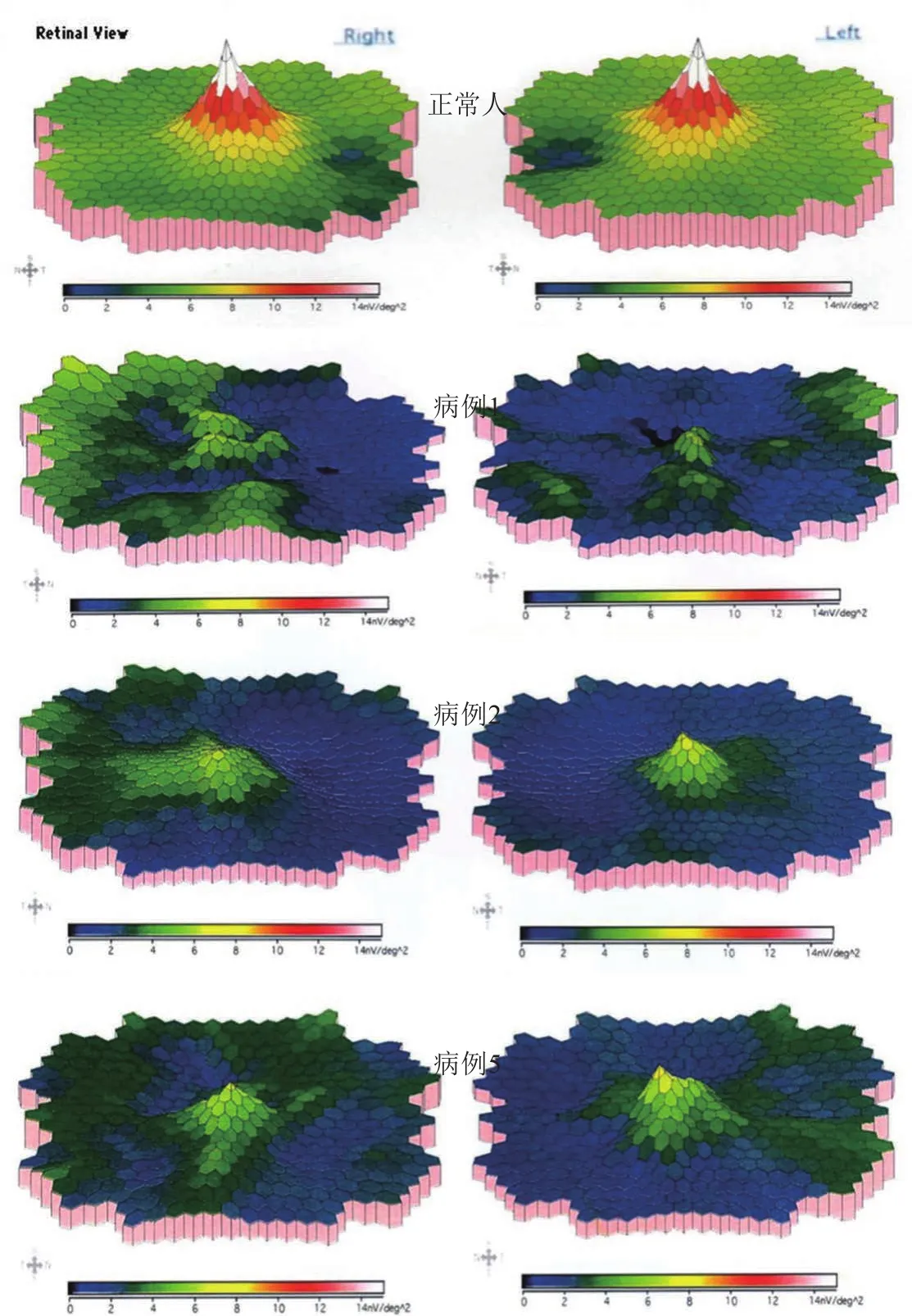
图4 3例NIID患者mfERG结果 与正常人相比,3例NIID患者表现为后极部不同程度振幅降低。
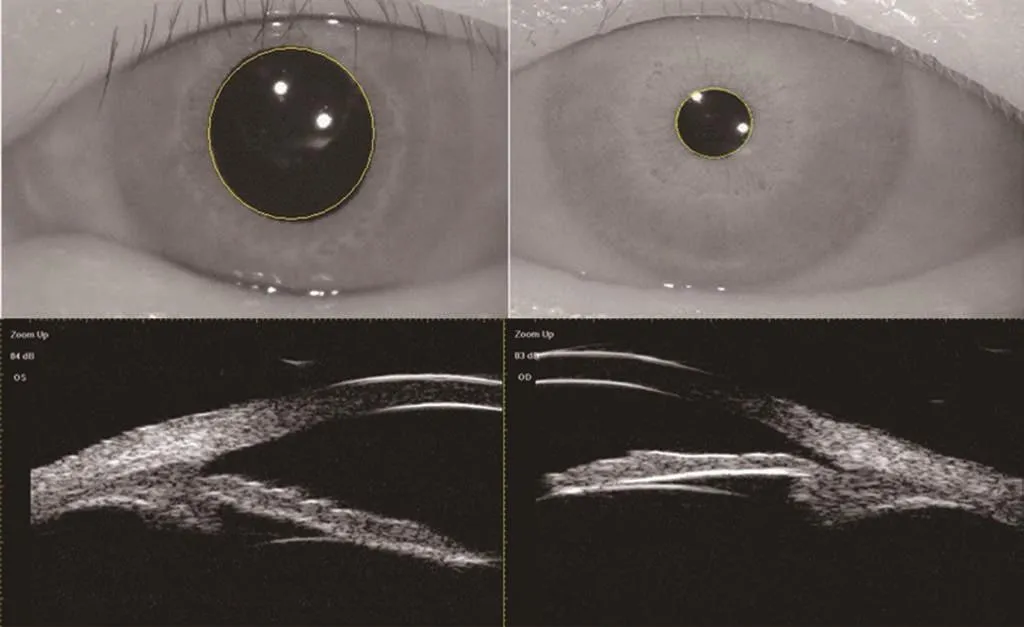
图5 瞳孔大小及UBM结果 左列显示正常大小瞳孔及睫状体,右列显示小瞳孔、肥大旋前睫状突及窄房角。
NIID眼组织病理分析极为罕见。1986年由Haltia等[12]报道的一对青少年型NIID双胞胎的眼组织病理结果成为研究NIID眼部相关病变的珍贵参考资料。病理结果揭示了后极部视网膜神经节细胞的缺失以及节细胞内典型包涵体结构,这可以为本组病例的黄斑区弥漫性GCIPL变薄提供佐证。该结果还显示视网膜星形胶质细胞增生,我们在OCT上观察到的视网膜内散布的高反射细点可能与此有关。但该病理报道的分型与本组病例不同,且当时无法进行基因检测确证,因此其结果尚不能与本组病例完全匹配。
ERG和mfERG结果均证实NIID患者存在视网膜功能不同程度异常,其改变异于临床常见的遗传性视网膜变性类疾病,诸如视网膜色素变性(retinitis pigmentosa,RP)和锥杆细胞营养不良。从目前几例结果看,视杆反应与视锥反应仅呈现轻中度降低,与RP的视杆反应重度降低和锥杆细胞营养不良的视锥反应重度降低均有不同,有益于鉴别诊断。
文献报道中NIID患者因自主神经功能失调常出现瞳孔缩小。本组小瞳孔发生比例较高(4/5)。同时,本组患者浅前房比例也较高(2/5)。由于瞳孔括约肌和睫状肌同受副交感神经支配,推测自主神经失调可能导致副交感神经相对亢进引起瞳孔缩小及睫状肌过度收缩,产生由UBM所证实的睫状突肥大现象,进而发生悬韧带松弛、晶状体前移;而小瞳孔会导致瞳孔阻滞力增加,二者相互作用使得这类患者容易产生浅前房、窄房角。这也提示对于小瞳孔的NIID患者应关注其潜在的闭角型青光眼风险。
本组病例就诊时4例视力尚佳,其中3例无明显视觉障碍主诉,但最终证实所有病例均存在不同程度视网膜病变。因此提示眼科医师对于NIID患者应进行细致的视网膜结构与功能检测;而对于具有典型眼底改变合并小瞳孔及全身多器官异常的患者也应考虑到NIID可能性,以尽早明确诊断。
总之,NIID会伴有视网膜变性改变,以感光细胞和神经节细胞受累为主,同时可伴有小瞳孔及睫状体肥大,部分患者存在潜在闭角型青光眼风险。
试题4.答案:A。目前国内外对于CSC合并CNV治疗方案还没有得到共识,但对于合并CNV的患者仍然是首选抗VEGF治疗。
试题5.答案:B。导致黄斑水肿的眼底病变排序:糖尿病视网膜病变,老年黄斑变性,视网膜静脉阻塞,CSC。
试题6.答案:C。对于部分VKH患者使用激素冲击后ICGA也可以表现为RPE破坏导致的荧光渗漏,故ICGA并不是唯一的方式,可以通过全身体征及多模式影像学,例如VKH出现耳鸣、头痛症状,也可以根据OCT观察是脉络膜中大血管扩张还是脉络膜基质的弥漫性增厚,或者可以根据口服激素前后OCT的改变而有助于鉴别两者。
试题7.答案:C。常染色体隐性遗传VMD,通常表现为眼底环视乳头多灶性改变,但需要注意的是它也可以表现为黄斑区病灶;这类患者通常会具有眼轴短、前房浅、房角发育不良等特点,所以遇到此类患者需要注意检查其房角形态,若遇到有窄房角或者浅前房,需要给予预防性LPI激光治疗。
试题8.答案:D。虽然文献报道具有浅前房及房角发育不良的风险很高,但是并不是所有的患者都具有。
试题9.答案:C。对于成人型VMD,年龄并不是定义的标准。主要判断还是依据家系中是否具有幼年发病、基因遗传、EOG等综合临床指标给予诊断。
试题10.答案:C。虽然常染色体隐性遗传VMD与浅前房具有相关性,但是并不是说BEST病不发生浅前房或青光眼,目前国内外有少数病例报道显示,常染色体显性遗传也可以引起青光眼的发生。
