负载纳米氧化锌的明胶/乙基纤维素气凝胶的制备及抑菌能力分析
2021-01-20潘晶晶刘雨雨
潘晶晶,张 宠,刘雨雨,张 辉
(浙江大学生物系统工程与食品科学学院,浙江 杭州 310058)
气凝胶通常是指以纳米级颗粒聚集而成的纳米级多孔结构,并以气态介质填充纳米孔洞的三维多孔低密度固体材料[1]。由于气凝胶材料特性优良(如孔隙率大、比表面积大、热导率低、电导率低等),在工业建筑、医疗、化工等领域被广泛应用,近年来其在食品领域也体现出巨大的应用潜力,例如包埋不饱和油脂、降低油的氧化敏感性[2]。最近,有研究者提出一种新型方案,即将静电纺丝技术与冷冻干燥技术相结合来构建气凝胶的三维结构[3],但这种制备技术在加工食品级气凝胶中仍然十分少见。
明胶因良好的生物相容性、生物可降解性而常被加工成气凝胶,在医药、材料等领域应用广泛。但是,由于存在机械性能弱、防水性差以及热力学不稳定等问题,明胶气凝胶在食品领域的应用受到了极大的限制。为了扩展这类材料的应用范围,通常添加具有良好机械性能的纤维素或纤维素衍生物以形成结构稳定的三维结构[4]。乙基纤维素因具有疏水性、高韧性、高生物相容性等特点,是共混材料的理想选择[5]。本课题组前期研究表明,利用明胶和乙基纤维素制成的共混薄膜材料有良好的疏水性和热稳定性,而且,由于乙基纤维素分子链上残留的羟基具有一定的持水能力,可增加材料的渗透性能,并装载疏水活性物质[5]。
纳米氧化锌是一种粒径范围为1~100 nm的多功能纳米金属氧化物,其来源广泛、价格低廉、结构稳定、安全无毒[6]。纳米氧化锌与细菌细胞之间的化学相互作用会产生光诱导的活性氧化物(reactive oxygen species,ROS),产生H2O2并且释放Zn2+离子,而其物理相互作用则会使细胞膜破裂、细胞内化或机械损伤,从而体现出杀菌效应[7]。目前,纳米氧化锌在食品中主要是作为抗菌类食品添加剂使用,尽管对哺乳动物细胞可能存在遗传毒性[8],但现有研究表明,纳米氧化锌不会对人体健康构成重大威胁[9]。
本研究采用静电纺丝与冷冻干燥相结合的新技术制备明胶/乙基纤维素气凝胶,用于装载纳米氧化锌。首先,通过静电纺丝技术制备明胶/乙基纤维素纳米纤维膜,再结合冷冻干燥技术将该膜制备成气凝胶,并添加海藻酸钠(sodium alginate,SA)和氯化钙(CaCl2)进行交联,分析交联前后气凝胶的形貌、物理性能、热稳定性、化学结构和水稳定性,并装载不同质量浓度的纳米氧化锌,分析其对大肠杆菌、金黄色葡萄球菌的抑菌效果。研究结果将为食品级气凝胶的制备提供新的思路。
1 材料与方法
1.1 菌株与试剂
大肠杆菌(ATCC 25922)、金黄色葡萄球菌(CMCC 26003)为食品营养与代谢实验室保藏。
乙基纤维素(3 ~7 c P,20~30 kDa)、明胶(TypeB,Bloom250,100 kDa)、海藻酸钠、纳米氧化锌上海阿拉丁公司;乙醇、乙酸 国药集团化学试剂有限公司;二水氯化钙 生工生物工程股份有限公司。以上试剂均为分析纯。
1.2 仪器与设备
分析天平 德国Sartorius公司;磁力搅拌器 上海司乐仪器有限公司;搅拌器 德国VMA公司;冷冻干燥器 北京博医康实验仪器有限公司;SU8010扫描电子显微镜 日本日立公司;差示扫描量热仪(differential scanning calorimeter,DSC) 美国PE公司;热重分析(thermogravimetric analysis,TGA)仪美国TA公司;X射线衍射仪 德国布鲁克公司;傅里叶变换红外光谱仪 美国Nicolet公司;Z020万能材料试验机 德国Zwick公司;TPS 2500 S热导系数测试仪凯戈纳斯仪器商贸(上海)公司。
1.3 方法
1.3.1 明胶/乙基纤维素气凝胶的制备
将质量比为1∶1的乙基纤维素与明胶溶于体积比为6∶2∶2的乙酸/乙醇/水混合溶剂中,配成总质量浓度为30 g/100 mL的溶液,置于60 ℃水浴中磁力搅拌2 h后,室温(25 ℃)搅拌至溶质完全溶解。参照Liu Yuyu等[5]的方法,使用食品营养与代谢实验室自行搭建的静电纺丝设备制备复合纤维膜,该设备主要由高压电源(Gamma高压仪表)、带泵注射器(LSP02-1B实验室推拉注射泵)和接地滚筒接收器3 个部分组成。电纺参数为电压15 kV、流速1.0 mL/h、接收距离为10 cm;环境参数为室温25 ℃和相对湿度50%。制备好的膜使用打孔机打成形状均匀的小圆片,浸泡于体积分数为10%的乙醇溶液中,使用搅拌器于104 r/min转速下搅拌15 min(分3 次,每次5 min),打碎成质量浓度为1 g/100 mL的糊状液体。用此糊状液体作为原料制备以下3 组气凝胶:1)将上述糊状液体装于6 孔板中,在超低温冰箱(-80 ℃)中放置24 h,待液体完全冻结,取出后在冷冻干燥机中放置24 h完全除去水分,所得气凝胶记为EG11;2)在上述糊状液体中加入0.5 g/100 mL海藻酸钠,置于磁力搅拌器上于500 r/min常温下搅拌1 h,按上述步骤所得气凝胶记为EG11-SA;3)将EG11-SA气凝胶浸泡于0.5%氯化钙(CaCl2)溶液4 h,取出后再冷冻干燥12 h,所得气凝胶记为EG11-SA/Ca。
1.3.2 形态分析和孔隙率的测定
采用SU8010扫描电子显微镜观察气凝胶样品的表面及截面微观形貌。扫描电子显微镜的加速电压为5~10 kV。用尺子量取每个样品的直径、高度与质量,计算其表观密度(ρA),根据以公式(1)计算样品的孔隙率,每个样品做3 组平行。其中,乙基纤维素和明胶的真实密度(ρR)分别为1.14 g/cm3和1.41 g/cm3。

1.3.3 热导率的测定
用TPS 2500 S热导系数测试仪测定气凝胶的导热系数(以热导系数表征热导率)。对于EG11、EG11-SA气凝胶,输出功率15 mW,升温时间20 s;对于EG11-SA/Ca气凝胶,输出功率10 mW,升温时间40 s。所有样品平行测定3 次,取平均值。
1.3.4 水稳定性的测定
将样品称质量并测定体积后,在蒸馏水中浸泡24 h,取出后拭去表面水分,再次称质量并测量表面尺寸。随后,将浸水的气凝胶放入烘箱,在50 ℃下烘干30 min,测定烘干后的质量,根据公式(2)、(3)、(4)分别计算气凝胶的尺寸稳定性、吸水能力与持水能力。

1.3.5 机械性能的测定
使用Z020万能材料实验机测定气凝胶的机械性能。实验采用压缩测试,弹性模量测试速率2 mm/min,压缩变形量为50%。
1.3.6 热稳定性的测定
气凝胶样品的热稳定性采用DSC和TGA仪进行分析。DSC分析条件:样品质量为6~8 mg;在0 ℃下平衡20 min;升温速率为10 ℃/min;氮气流速为50 mL/min;温度最高值为250 ℃。TGA条件:样品质量为2 mg左右;氮气环境;样品升温速率为10 ℃/min,升温范围为50~600 ℃。
1.3.7 X射线衍射分析
气凝胶样品的结晶特性采用X射线衍射仪进行分析。分析条件:光源Cu Kα(λ=1.540 6 Å),倾角0.02°,扫描速率1(°)/min,扫描范围2θ=4°~80°。所有样品均测定3 次。
1.3.8 傅里叶变换红外光谱分析
气凝胶样品的化学结构采用傅里叶变换红外光谱仪进行分析。将样品与KBr按照1∶50质量比混合压片后进行分析,分析条件:扫描范围4 000~400 cm-1,分辨率4 cm-1,光谱记录频率为16。所有样品均测定3 次。
1.3.9 气凝胶的抑菌实验
在乙基纤维素/明胶溶液中加入质量浓度分别为0、1、1.5、2 g/100 mL纳米氧化锌,采用1.3.1节方法制备气凝胶,分别记为Z0-EG11-SA/Ca、Z1-EG11-SA/Ca、Z1.5-EG11-SA/Ca、Z2-EG11-SA/Ca。采用打孔法[10]评估气凝胶对大肠杆菌(Escherichia coli)和金黄色葡萄球菌(Staphylococcus aureus)的抑菌活性。通过倾注平板法,将1 mL浓度为105CFU/mL的大肠杆菌、金黄色葡萄球菌菌液接种到已灭菌的培养基中,待培养基冷却凝固后使用已灭菌的钢管打出直径8 mm的圆孔,然后在孔中放入经紫外光(ultraviolet,UV)照射灭菌1 h、直径为8 mm的气凝胶,37 ℃下恒温培养24 h后,采用Nano Measurer 1.2软件计算抑菌圈的平均直径,每个气凝胶样品做3 组平行。
1.3.10 UV照射后的抑菌动力学分析
称取约11 mg气凝胶,UV(364 nm、250 W)灭菌0.5 h。然后将气凝胶加入到含有20 mL培养液的已灭菌离心管中。其中一组UV照射1 h,另一组避光处理1 h。随后向每支离心管中加入0.2 mL菌液(106CFU/mL),再置于恒温摇床进行37 ℃培养。使用酶标仪在600 nm波长处测定菌浓度,每隔2 h测一次,共测24 h。选取空白培养液和加入Z0-EG11-SA/Ca气凝胶的培养液分别作为空白和阴性对照。每个样品均做3 次平行。抑菌率按公式(5)计算。

1.4 数据处理与分析
使用Origin pro 9.0软件t分布检验单因素方差分析,后续使用Tukey分析进行检验,当P<0.05时表示结果间差异显著。绘图采用Origin pro 9.0软件。所有经过3 次重复测定的数据都采用平均值±标准差表示。
2 结果与分析
2.1 形态分析结果
图1为3 种气凝胶的外观,其中,EG11气凝胶质地蓬松,EG11-SA气凝胶质地较为紧密,EG11-SA-Ca质地最为紧密,体积相对最小。从图2扫描电子显微镜观察结果可以看出,3 种气凝胶的形态结构上有显著差异。EG11气凝胶由于未进行交联,表面呈现出粗糙的多孔状,截面的孔隙小且密集,孔径约分布在10~100 μm之间,纤维松散地缠绕在一起。EG11-SA气凝胶表面光滑致密,这与Meng Chihan等[11]制备的海藻酸钠气凝胶的表面结构相似。交联海藻酸钠后截面空隙直径明显增大,大致分布于50~200 μm之间,组织呈片状相互连接。EG11-SA/Ca气凝胶表面致密,空隙直径较EG11-SA气凝胶明显减小,组织间有薄层相互连接,结构稳定性大幅增强。

图1 EG11、EG11-SA、EG11-SA/Ca气凝胶的俯视图(A)与侧视图(B)Fig.1 Vertical view (A) and lateral view (B) of EG11, EG11-SA and EG11-SA/Ca aerogels

图2 EG11、EG11-SA、EG11-SA/Ca气凝胶的表面(A)与截面(B)扫描电子显微镜图Fig.2 Scanning electron micrographs of the surface (A) and cross-section (B) of EG11, EG11-SA and EG11-SA/Ca aerogels
2.2 孔隙率与热导率

表1 EG11、EG11-SA、EG11-SA/Ca气凝胶的孔隙率与热导率Table 1 Porosity and thermal conductivity of EG11, EG11-SA and EG11-SA/Ca aerogels
由表1可知,EG11、EG11-SA、EG11-SA/Ca气凝胶的孔隙率分别为99.46%、98.30%、97.15%。交联SA后,气凝胶的孔隙率降低,应该与SA本身形成的凝胶有关。再交联Ca2+后,孔隙率继续降低,证明Ca2+与SA交联产生稳定的鸡蛋盒(egg-box model)结构[12],在气凝胶结构中起到了一定的填充支持作用。通常,当孔隙度超过80%时即为高孔隙度体系,因此,本实验中各气凝胶材料的孔隙率均达到高孔隙率水准。
EG11、EG11-SA、EG11-SA/Ca气凝胶的热导率分别为0.033 04、0.034 40、0.035 46 W/(m·K)。结合孔隙率实验结果可以发现,孔隙率越低,材料的热导率越高。一般而言,隔热材料的热导率在0.03~0.17 W/(m·K)之间,因此,3 种气凝胶均属于隔热材料。
2.3 水稳定性分析结果
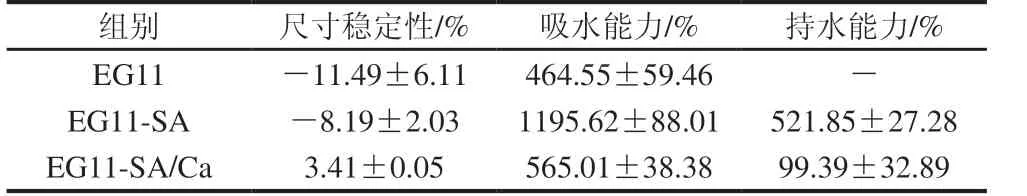
表2 EG11、EG11-SA、EG11-SA/Ca气凝胶的尺寸稳定性、吸水能力、持水能力Table 2 Dimensional stability, water-absorbing capacity, and water-holding capacity of EG11, EG11-SA, and EG11-SA/Ca aerogels
如表2所示,经过24 h水浸泡处理后,交联SA后的气凝胶尺寸稳定性比未交联气凝胶有所提升。赵谋明等[13]通过研究离子强度与明胶、海藻酸钠混合凝胶黏度之间的关系,发现明胶带正电的氨基与海藻酸钠上带负电的羧基存在较强的静电引力,二者同时存在时会增加体系的稳定性。EG11-SA/Ca气凝胶的尺寸稳定性最好,这是因为Ca2+与海藻酸钠的古洛糖醛酸单元结合,形成一种稳定的鸡蛋盒结构[12],导致整个体系更加不易破坏。从实验结果可知,24 h水浸泡处理后,EG11与EG11-SA两组气凝胶尺寸缩小,而EG11-SA/Ca气凝胶尺寸膨胀,这是由于在浸泡过程中,前两组气凝胶的表面成分从气凝胶体脱落,而交联紧密的第3组气凝胶则体现出了吸水膨胀的效果。
由表2可知,交联海藻酸钠后气凝胶吸水能力显著上升,这与SA具有较强的亲水性有关,但EG11-SA/Ca气凝胶吸水能力下降,这是由于Ca2+与海藻酸钠间形成交联作用,导致材料结构变得更加紧密。由表2可知,EG11气凝胶的持水能力数据不可测,因为该组样品测定过程中无法避免质量大幅损失,应用价值较低。交联SA之后气凝胶的持水性增强,但EG11-SA/Ca气凝胶持水能力有所下降,证明EG11-SA/Ca气凝胶具有较好的可重复利用性。
2.4 机械性能分析结果
气凝胶的应力-应变曲线如图3所示,3 种气凝胶表现出经典的应力-应变线性关系,这表明气凝胶在50%的应力下表现出弹性行为。在相同应变下,交联后的气凝胶(EG11-SA/Ca)具有更高的应力,表明其具有更好的机械性能。表3为3 种气凝胶的弹性模量以及变形量50%时的压强。相比EG11气凝胶,EG11-SA、EG11-SA/Ca气凝胶的弹性模量分别提高了33、50 倍,证实该交联方式可显著提高气凝胶的机械性能,具有实际应用意义。结合扫描电子显微镜观察结果可知,EG11气凝胶是纳米纤维通过相互缠绕搭建而成的,结构间没有支持与联结。交联海藻酸钠的气凝胶由于海藻酸钠与明胶间具有静电作用力,使其组织间相互连接,提高了整体结构的机械性能。然而,Ca2+与海藻酸钠交联可以形成更加稳定的结构,进一步提高气凝胶的机械性能。
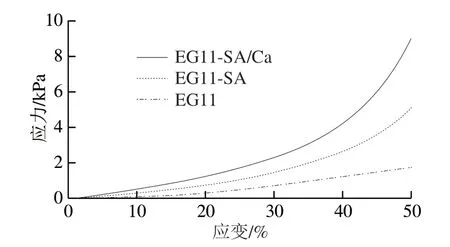
图3 EG11、EG11-SA、EG11-SA/Ca气凝胶的形变关系图Fig.3 Stress vs strain curves of EG11, EG11-SA, EG11-SA/Ca aerogels

表3 EG11、EG11-SA、EG11-SA/Ca气凝胶的压缩性能Table 3 Compression performance of EG11, EG11-SA, and EG11-SA/Ca aerogels
2.5 热稳定性分析结果

表4 EG11、EG11-SA、EG11-SA/Ca气凝胶的TGA参数Table 4 Mass loss rate and maximum degradation temperature of thermogravimetric analysis curves for EG11, EG11-SA, EG11-SA/Ca aerogels
气凝胶的热稳定性分析结果如图4和表4所示。依据图4A中TGA曲线,气凝胶的热重分析过程可分为4 个阶段:0~150 ℃是第一阶段,主要受易挥发成分脱离的影响[14];150~230 ℃为第二阶段,单纯明胶分子会在220 ℃会发生变性,但是由于与乙基纤维素进行复合电纺,明胶分子发生螺旋向无定型的结构转变,所以在加热过程中未检测到EG11的变性过程,这与Bigi等[15]的研究结果相似。而在该温度下的质量损失主要是海藻酸钠分子处于热降解阶段,海藻酸钠分子的糖苷键断裂,发生脱羧反应产生碳酸盐,并且释放出二氧化碳和水[16],从而导致质量减少;第三(230~390 ℃)与第四(390~600 ℃)阶段分别对应于多聚物的分解和碳化。微分热重(differential thermogravimetry,DTG)曲线在240 ℃的峰是由于海藻酸钠的变化所致,李博等[17]的研究认为这一阶段主要是由于海藻酸钠分子链断裂分解为稳定的中间产物,加入Ca2+后,这一温度有所提高,且质量损失比率明显降低[16]。如表4所示,第三阶段EG11-SA气凝胶的最大分解温度降低,稳定性变差,但是,交联Ca2+后稳定性重新提高。
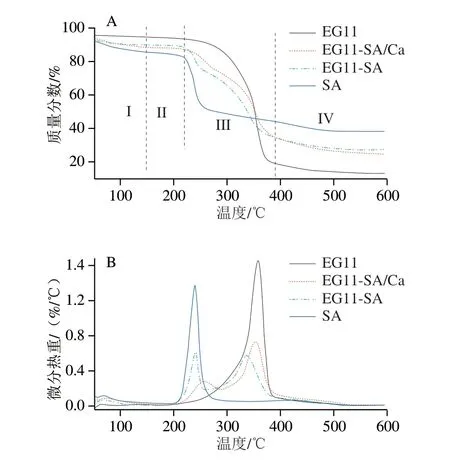
图4 EG11、EG11-SA、EG11-SA/Ca气凝胶的TGA(A)与DTG(B)曲线Fig.4 Thermogravimetric analysis (A) and differential thermogravimetry (B)curves of EG11, EG11-SA and EG11-SA/Ca aerogels
如表5和图5所示,DSC表征进一步证明了交联后气凝胶稳定性的提升。这主要体现在第三部分,明胶在220 ℃左右会热分解[18],经过交联后,该处的热分解峰消失,这是由于明胶经过电纺后螺旋结构部分解开,经过SA交联形成较多的无定形结构[19],相比于EG11气凝胶,在交联Ca2+后,焓变增加到249 J/g,证明气凝胶稳定性提升。而EG11-Ca/SA的tm高于EG11和EG11-SA的tm,表明经过Ca2+交联气凝胶的热稳定性显著增加。

表5 EG11、EG11-SA、EG11-SA/Ca气凝胶的DSC分析参数Table 5 Differential scanning calorimeter analysis parameters of EG11, EG11-SA and EG11-SA/Ca aerogels
2.6 X射线衍射分析结果

图6 EG11、EG11-SA、EG11-SA/Ca气凝胶的X射线衍射图谱Fig.6 X-ray diffraction curves of EG11, EG11-SA and EG11-SA/Ca aerogels
图6 为气凝胶的X射线衍射图谱,EG11气凝胶的衍射峰位在8°与22°左右,与其所含明胶与乙基纤维素的衍射峰位相一致。在交联之后,这些衍射峰强度发生明显下降,且交联的程度越高,衍射强度降低的越多,这是由于明胶与海藻酸钠之间的分子相互作用导致明胶螺旋晶体结构部分解开,特征峰消失。Sajjan等[20]也报道了相似的结果,他们认为明胶和海藻酸钠之间存在氢键或者静电作用力,导致明胶的三维螺旋结构减少,使明胶的特征峰发生显著降低。
2.7 傅里叶变换红外光谱分析结果
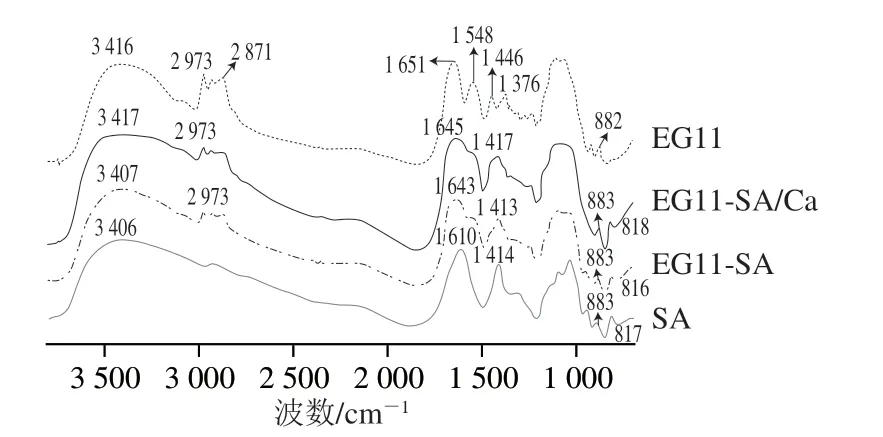
图7 EG11、EG11-SA、EG11-SA/Ca气凝胶的傅里叶变换红外光谱图Fig.7 Fourier transform infrared spectra of EG11, EG11-SA and EG11-SA/Ca aerogels
如图7所示,明胶的特征峰主要有1 650 cm-1的酰胺峰I(VC=O)、1 550 cm-1的酰胺峰II(δNH+VCN)以及1 241 cm-1的酰胺峰III(δNH)[21]。理论上氨基带的振动强度越高,明胶分子中的螺旋结构含量越多[22],从图7中可见,EG11气凝胶在交联以后,1 550 cm-1的酰胺峰II强度明显降低,说明明胶的螺旋结构减少。此外,交联后的气凝胶酰胺峰I出现了红移,说明明胶分子螺旋结构含量降低,与交联剂间形成了更多的氢键[23]。3 400 cm-1附近的峰代表了—OH的伸缩振动,证实EG11-SA气凝胶中明胶与海藻酸钠间的氢键形成,而Ca2+交联作用却减少了氢键作用,导致该峰又发生了蓝移[24]。
2.8 抑菌圈实验结果
装载纳米氧化锌的气凝胶对大肠杆菌和金黄色葡萄球菌的抑菌效果如表6所示。对于阴性对照组,该气凝胶没有抑菌能力,但纳米氧化锌装载量分别为1、1.5、2 g/100 mL时,气凝胶对大肠杆菌的抑菌圈直径分别为1.28、2.40、3.89 mm,对金黄色葡萄球菌的抑菌圈直径分别为1.00、1.52、1.88 mm。气凝胶的抑菌能力与纳米氧化锌的质量浓度呈正相关关系,且对于大肠杆菌的抑菌效果优于金黄色葡萄球菌。这与Diez-Pascual等[25]的研究结果相一致,他们将纳米氧化锌加入到3-羟基丁酸酯和3-羟基戊酸酯的共聚物中,发现纳米氧化锌对大肠杆菌的抗菌效果优于金黄色葡萄球菌。这可能与两种细菌的细胞壁厚度有关,革兰氏阳性菌的肽聚糖网层次较多且交联致密,革兰氏阴性菌的细胞壁更容易被纳米氧化锌颗粒穿透,达到杀死细菌的效果[26]。
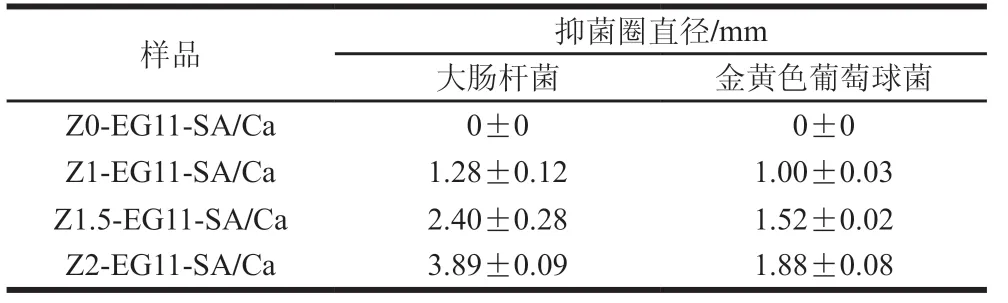
表6 EG11、EG11-SA、EG11-SA/Ca气凝胶的抑菌圈数据Table 6 Inhibition zones of EG11, EG11-SA and EG11-SA/Ca aerogels
2.9 UV照射后的抑菌动力学

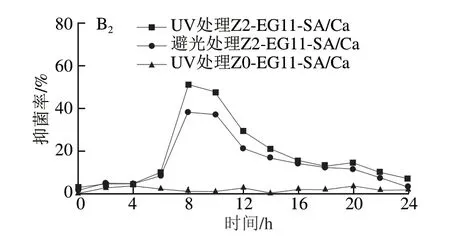
图8 UV辐射对Z2-EG11-SA/Ca气凝胶抑菌动力学的影响Fig.8 Effect of UV radiation on the antibacterial activity ofZ2-EG11-SA/Ca aerogel
如图8A所示,大肠杆菌和金黄色葡萄球菌的生长曲线可以分为3 个阶段:分别为迟滞阶段、指数生长阶段、稳定阶段。通过图8B可以看出,阴性对照组气凝胶几乎没有任何抑菌能力,但是Z2-EG11-SA/Ca气凝胶在指数生长阶段有连续抑制作用。相比于避光处理组,经UV照射的气凝胶组也显示出了更好的抑菌性能。对大肠杆菌的抑菌率最高达到63.85%,对金黄色葡萄球菌的抑菌率最高达到50.88%。因此,UV照射能够强化装载纳米氧化锌气凝胶的抑菌能力。Sirelkhatim等[27]认为UV照射强化纳米氧化锌抑菌能力的机理是其促进ROS的生成。Li Yang等[28]的研究也表明,氧化锌经UV照射后会生成3 种类型ROS,而且,ROS浓度越高,对大肠杆菌的抑菌能力则越强。
3 结 论
本实验以乙基纤维素、明胶为原料利用静电纺丝技术制备纳米纤维膜,经过冷冻干燥制备EG11气凝胶,并成功利用海藻酸钠、氯化钙对气凝胶进行交联,制备出EG11-SA、EG11-SA/Ca气凝胶,同时选取EG11-SA/Ca气凝胶装载抑菌物质纳米氧化锌测定其抑菌能力。EG11、EG11-SA、EG11-SA/Ca气凝胶都具有高孔隙率与良好的隔热性能。其中,明胶分子中的三维螺旋结构部分解开,与海藻酸钠形成了氢键,同时,海藻酸钠的羧基与明胶的氨基存在静电引力,使得两者能够相互交联,形成更加稳定的结构。在此基础上,添加Ca2+与海藻酸钠进一步交联,提高了整体结构的稳定性,在3 种气凝胶中具有最佳的机械性能和水稳定性。抑菌实验结果表明,EG11-SA/Ca气凝胶中的纳米氧化锌最佳添加量为2 g/100 mL,对大肠杆菌、金黄色葡萄球菌具有明显的抑菌效果。不仅如此,UV照射还可显著提高气凝胶的抑菌性能。
