重组人胰岛素原料药N末端氨基酸序列的测定
2021-01-16田沛霖张国林
田沛霖,张国林
(苏州市药品检验检测研究中心,苏州 215104)
胰岛素是广泛存在于人和动物体内的多肽类激素,经内源性或外源性物质刺激,由胰脏内的胰岛B细胞分泌。主要用于调节糖代谢,是已发现的机体内唯一可降低血糖的激素。胰岛素在临床上主要用于糖尿病治疗。早期的胰岛素主要从猪、牛等动物的胰脏中提取所得,存在浓度低、效期短和免疫原性强等缺陷,限制了其临床使用。随着分子生物学技术在生物医药领域的广泛应用,通过重组DNA技术合成的人胰岛素,不仅解决了上述问题,甚至可定向改变天然胰岛素的氨基酸序列,从而获得活性更高、作用时间更长、吸收更安全的胰岛素类似物产品[1-2]。
重组人胰岛素为重组技术生产的双链多肽类激素,由51个氨基酸残基组成,其中A链有11种(21个氨基酸),B链有16种(30个氨基酸),2条链通过2个二硫键相连,构成具有活性的胰岛素分子[3]。胰岛素在历年的《中国药典》中均有收载,但在2015年版及更早版本中,N末端氨基酸序列未涵盖在重组人胰岛素的产品检验标准中。作为重组蛋白类药物,其末端氨基酸残基存在被酶切或降解的可能性,从而影响生物学功能[4]。当胰岛素氨基酸序列与理论序列一致时,可以作为判定产品结构正确性、完整性以及稳定性的重要依据。而在《中国药典》(2020年版三部)人胰岛素的3.3.12项涵盖了“N末端氨基酸序列”[5]。可见,对重组人胰岛素原料药的N末端氨基酸序列进行测定,是其质量控制的必要手段。
本研究旨在建立重组人胰岛素原料药N末端氨基酸序列的测定方法,为完善质量标准提供参考。
1 材料与方法
1.1 仪器与试剂
PPSQ-53A蛋白质测序仪、LC-20AD高效液相色谱仪(HPLC,日本岛津公司);XSE205DU十万分之一电子天平(梅特勒-托利多仪器有限公司);Lab Dancer小舞灵旋涡混合器(德国IKA公司);微量移液器(德国Brand公司);Wakopak®Wakosil PTH-GR硅胶柱(日本和光纯药工业株式会社)。
PTH-氨基酸混合物标准品(批号TWK5776)、R1溶液(5%异硫氰酸苯酯,正庚烷溶液,批号KCG0760)、R2GR溶液(30%N-甲基哌啶溶液,批号KCF20206)、R3溶液(三氟乙酸,批号KCM6143)、R4GR溶液(25%三氟乙酸溶液,批号KCF2027)、S2溶液(乙酸乙酯,批号KCG0691)、S3溶液(1-氯丁烷,批号KCK4251)、S4B溶液(37%乙腈,批号APE3239)、PTH-氨基酸洗脱液A[批号KCQ5445,成分:水(浓度<90%)、乙腈(浓度<15%)、醋酸铵(浓度<1%)、1-己烷磺酸钠(浓度<1%)、醋酸(浓度<0.1%)]、PTH-氨基酸洗脱液B[批号KCQ5446,成分:水(浓度<60%)、甲醇(浓度28%)、2-丙醇(浓度14%)、醋酸(浓度<1%)],以上均购自日本和光纯药工业株式会社;聚凝胺试剂(polybrene,Sigma 试剂公司,批号SLBN6919V);醋酸(国药集团化学试剂有限公司,批号20170728);超纯水由Synergy制备;其余试剂为市售分析纯。
1.2 供试品溶液的制备
重组人胰岛素原料药(美国礼来公司,批号C514759-1,纯度经测定为99.9%)为重组DNA技术生产的由51个氨基酸残基组成的蛋白质,宿主为大肠杆菌。精密称取该样品适量,用1%醋酸溶液溶解稀释,制成浓度约为50 μmol/L的溶液,即得。
1.3 PTH-氨基酸混合标准液的制备
取PTH-氨基酸混合标准品1支,加入S4B溶液2 ml使其溶解,作为贮备液;取S4B溶液150 μl,加水450 μl涡旋混匀,作为稀释S4B溶液;取贮备液10 μl,加稀释S4B溶液490 μl,涡旋混匀,即得。
1.4 聚凝胺溶液的制备
取聚凝胺试剂1支,向配管内注入750 μl蒸馏水(HPLC级),振摇使完全溶解,即得(非立即使用时在低于-20 ℃条件下保存)。
1.5 分析条件
Edman降解后的PTH-氨基酸注入高效液相色谱仪进行分析,用Wakopak®Wakosil PTH-GR硅胶柱,以PTH-氨基酸洗脱液A作为流动相A,以PTH-氨基酸洗脱液B作为流动相B;柱温35 ℃,流速为0.3 ml/min,进样体积为50 μl,光电二极管阵列(PDA)检测器,检测波长为269 nm,按表1的条件进行梯度洗脱。

表1 高效液相色谱仪洗脱条件
1.6 实验操作步骤
1.6.1分析PTH-氨基酸混合标准样品
为了进行HPLC分析系统的校准,首先需对PTH-氨基酸混合标准样品进行分析。
量取“1.3”项下PTH-氨基酸混合标准液90 μl,放置于指定样品管内并安装封盖。仪器将通过样品管吸样,以半自动方式进行分析。分析其容量为50 μl。
所有检测出的PTH-氨基酸峰,可通过比对PTH-氨基酸标准色谱图进行识别并修正保留时间,从而获得校准后的各氨基酸标准定位图谱,确定分别为何种氨基酸。
1.6.2准备玻璃纤维膜
待测的供试蛋白溶液需加在玻璃纤维膜上进行分析反应,因此必须预先对玻璃纤维膜进行聚凝胺处理。
聚凝胺是一种多聚阳离子聚合物。在蛋白质测序时,添加小剂量的聚凝胺能够明显改善多肽的降解现象。而当玻璃纤维膜中加入聚凝胺后,还能有效提高膜的亲和性,从而更好地吸附样品。
取“1.4”项下聚凝胺溶液15 μl,用微量移液器加到玻璃纤维膜上,干燥后进行清洗处理,待用。
1.6.3样品的序列分析
量取“1.2”项下供试品溶液5 μl,用微量移液器点在已经过预处理的玻璃纤维膜上, 干燥后放入仪器指定位置,设置仪器参数开始序列分析,并对结果进行数据处理与分析。
2 结果
2.1 PTH-氨基酸混合标准品校准测试结果
对PTH-氨基酸混合标准品测试校准了20种PTH-氨基酸的出峰时间。见图1。

图1 PTH-氨基酸混合标准品校准测试图谱
2.2 重组人胰岛素N末端氨基酸序列结果
运行16个循环检测重组人胰岛素样品N末端氨基酸残基序列,前15个循环检测到的氨基酸见图2和表2。经分析,重组人胰岛素原料药样品N末端氨基酸的理论序列见表3。
2.3 实验室比对结果
委托岛津上海分析中心用PPSQ-53A蛋白质测序仪在等度洗脱模式下,对该样品的N末端氨基酸序列进行了测序,PTH-氨基酸混合标准品校准测试图谱见图3。重组人胰岛素供试品分析结果见图4。

表3 重组人胰岛素N末端理论氨基酸序列

图3 PTH-氨基酸混合标准品校准测试图谱(岛津上海分析中心比对结果)
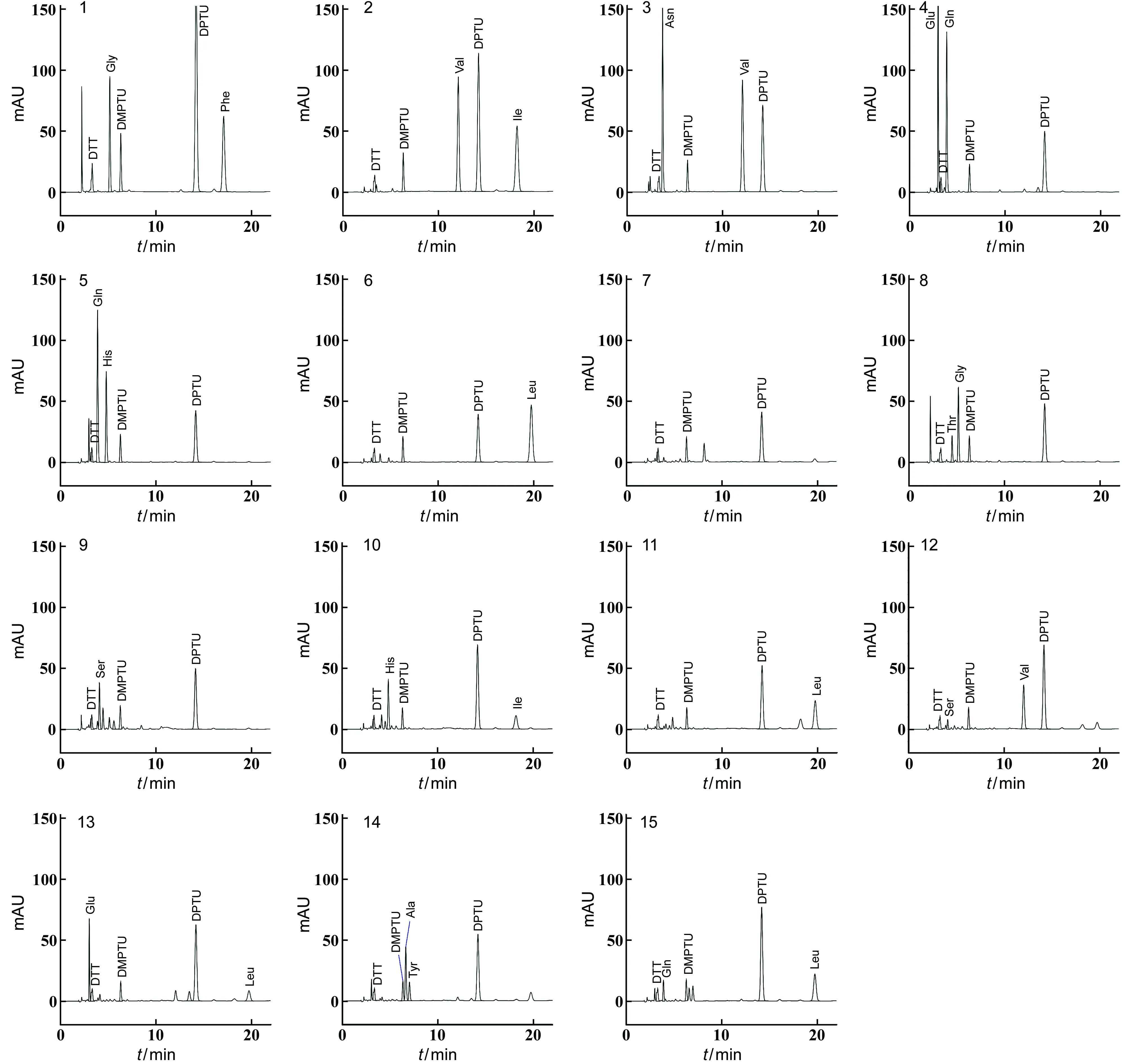
图4 重组人胰岛素N末端氨基酸序列完整图谱(岛津上海分析中心结果)
前15个循环检测到的氨基酸种类分别为Gly、Phe;Ile、Val;Val、Asn;Glu、Gln;Gln、His;(Cys)、Leu;(Cys)、(Cys);Thr、Gly;Ser;Ile、His;(Cys)、Leu;Ser、Val;Leu、Glu;Tyr、Ala;Gln、Leu,因此推断样品N末端氨基酸序列为A链Gly-Ile-Val-Glu-Gln-(Cys)-(Cys)-Thr-Ser-Ile-(Cys)-Ser-Leu-Tyr-Gln;B链Phe-Val-Asn-Gln-His-Leu-(Cys)-Gly-Ser-His-Leu-Val-Glu-Ala-Leu。结果与重组人胰岛素的理论氨基酸序列相符,实验室比对结果一致。
3 讨论
重组人胰岛素是含有可高效表达人胰岛素基因的基因工程菌,经发酵、分离、高度纯化、结晶和干燥制成[5],是目前糖尿病治疗的重要药物之一。在《中国药典》2020年版中,人胰岛素等多个品种正式由过去的二部品种转为三部品种,在三部中重组人胰岛素通用名称统一改为“人胰岛素”。此外,其质量标准也与以往有较大的修订。新增了N末端氨基酸序列等检查项,“人用重组DNA蛋白制品总论”的3.1.1中也明确提示“一级结构,即包括二硫键连接方式的氨基酸序列(包含二硫键的完整性和正确性、游离疏基)。应尽可能采用综合的方法测定目标制品的氨基酸序列,并与其基因序列推断的理论氨基酸序列进行比较”[5]。可见,这种一级结构的特性分析是确保产品安全有效、建立并确定制品质量标准的基础。作为验证蛋白类药物结构准确性的重要参数,N末端氨基酸序列的测定注定会越发普遍化,而这也为检验机构的检测能力提出了更新、更高的要求。
Edman降解是一种用于测定多肽和蛋白质氨基端序列的经典方法,其主要原理是通过异硫氰酸苯酯与蛋白质或多肽的N末端残基进行偶联、苯氨基硫甲酰酞(PTC-肽)环化裂解、噻唑啉酮苯胺(ATZ)转化为苯异硫脲-氨基酸(PTH-氨基酸)等化学反应,将氨基酸进行特异性修饰[6]。每次循环时,都会从蛋白质或多肽N末端裂解一个氨基酸残基,同时暴露出新的氨基酸进行下一个Edman降解。所有生成的PTH-氨基酸会通过液相色谱(LC)进行分析。而梯度洗脱的方式分离效果较好,能够提高检测的灵敏度[7];等度序列分析则基线较平稳,能提供更稳定的保留时间。
本研究基于Edman降解原理,将样品经1%乙酸溶液处理后,采用PPSQ-53A蛋白质测序仪依照序列切割N末端氨基酸后,注入高效液相色谱仪。使用Wakopak Wakosil®PTH-GR硅胶柱,通过梯度洗脱分离,PDA检测器分析证实供试品N末端氨基酸序列与理论序列一致。本方法操作简单、可行,能够较好地实现重组人胰岛素原料药的氨基酸序列测定。但本方法也存在着一定的局限性,如样品需要有比较高的纯度[4];N末端已发生修饰的蛋白难以进行Edman反应,因此当双链中有半胱氨酸时,由于结构中的半胱氨酸残基会发生二硫键交联而导致基团封闭,无法与异硫氰酸苯酯发生偶联,故而序列中的半胱氨酸无法检测出[8-10]。
本实验对样品N末端氨基酸序列进行分析时,是以液相图谱中的出峰时间作为依据,即是在每一个循环中分别找出与PTH-氨基酸混合标准品的出峰时间相一致的峰,从而加以确定。这种氨基酸匹配的方式,可能会因出峰时间的漂移而影响结果判断,并且无法精确定位已检测到的目标氨基酸到底是源自A链还是B链。在本实验的15个循环中,就有个别氨基酸峰的保留时间与混合标准品的出峰时间发生了偏离。因此,这只是一种半定性的方式,无法得到样品的氨基酸绝对序列。
致谢:感谢岛津上海分析中心对本实验给予的帮助与支持。
