超声造影对肝脏局灶性病变诊断的价值分析
2021-01-15
江苏省宝应县人民医院超声影像科,江苏 宝应 225800
肝脏局灶性病变在临床上极为常见,恶性病变以肝细胞肝癌(hepatocellular carcinoma,HCC)、胆管细胞性肝癌(hepatic cholangiocarcinoma,CC)及转移性肝癌(metastatic hepatic carcinoma,MLC)多见,而良性病变以肝血管瘤和局灶性增生结节(focal nodular hyperplasia,FNH)多见,由于良恶性病变预后及处理方法不一样,因而必须尽早明确诊断。传统超声和增强CT或磁共振成像(magnetic resonance imaging,MRI)是常用的诊断方法,但敏感性和特异性受到一定限制。超声造影(contrast-enhanced ultrasound,CEUS)可实时动态地显示微血管及组织灌注情况,具有良好的分辨率,且操作简便,无肾毒性及辐射的危险,广泛应用于临床肝脏病变的诊断[1],在定性诊断方面具有一定的优越性。本研究回顾并分析江苏省宝应县人民医院50例患者(共62个肝脏局灶性病变)CEUS表现,探讨CEUS在肝脏局灶性病变临床诊断中的应用价值。
1 资料和方法
1.1 研究对象
回顾并分析2018年7月—2019年12月于江苏省宝应县人民医院行CEUS检查的50例患者(62个肝脏局灶性病变)的临床资料,其中男性42例,女性18例,年龄9~84岁,平均年龄50岁。所有患者在进行肝脏CEUS前均行常规超声检查,单发病灶44例,多发病灶6例。62个病灶均经穿刺标本病理学检查证实,其中恶性病变23个,良性病变39个,病灶直径1.0~7.8 cm。
1.2 仪器与方法
使用荷兰Philips公司的EPIQ5超声诊断仪,造影剂为意大利Bracco公司生产的声诺维(SonoVue)。首先行常规超声检查观察患者肝内局灶性病变的数目、大小、边界、内部结构及内部血流情况,然后选取病灶的最佳观察切面后进行CEUS。经患者左侧肘静脉快速团注2.4 mL混悬液,随即推注入5 mL 0.9% NaCl溶液。在注射造影剂的同时持续地观察病灶在动脉期、门脉期及延迟期的灌注和回声强度的变化,包括病灶及其周围肝组织开始增强时间、增强的强度、病灶增强的形态及其范围,动态记录造影图6 min。多个病灶或同一病灶再次观察时注射造影剂需间隔10 min。8例诊断可疑的患者同期进行了增强CT或增强MRI检查。
1.3 超声诊断标准
依据《中国超声造影临床应用指南》[2]CEUS临床分期:动脉期一般开始于注射后30 s内;门脉期31~120 s,延迟期不超过240~360 s。依据肝组织增强程度分级:无增强,低增强,等增强,高增强。定性诊断:① 良性,动脉期等增强或高增强,门脉期及延迟期仍为等增强或高增强,或各期均为无增强。② 恶性,动脉期等增强或高增强,门脉期低增强,延迟期低增强或无增强。
1.4 统计学处理
采用SPSS 17.0软件进行统计学分析,计量资料比较采用t检验,用±s表示,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结 果
2.1 CEUS诊断与病理学诊断对照
50例患者进行CEUS检查,均无与造影剂相关的不良反应。以穿刺标本病理学检查结果为标准,62个病灶CEUS检出与病理学检查结果对照见表1。

表1 62个肝脏局灶性病变CEUS和病理学检查结果对照
2.2 CEUS时相
本组资料显示,恶性病变的始增时间早于良性病变组,差异有统计学意义(P<0.05)。恶性病变组的达峰时间、始消时间明显早于良性病变组,持续时间明显小于良性病变组,差异有统计学意义(P<0.01,表2)。
表2 62个肝脏良恶性局灶性病变CEUS时相比较(±s)
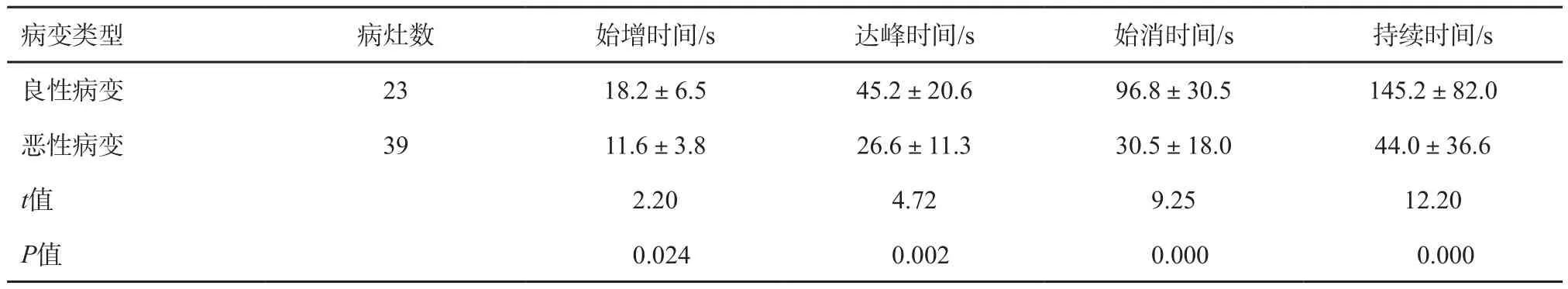
表2 62个肝脏良恶性局灶性病变CEUS时相比较(±s)
病变类型 病灶数 始增时间/s 达峰时间/s 始消时间/s 持续时间/s良性病变 23 18.2±6.5 45.2±20.6 96.8±30.5 145.2±82.0恶性病变 39 11.6±3.8 26.6±11.3 30.5±18.0 44.0±36.6 t值 2.20 4.72 9.25 12.20 P值 0.024 0.002 0.000 0.000
2.3 良恶性肝脏局灶性病变的CEUS表现
本组资料中7个HCC病灶表现为造影剂于动脉期快速整体充填,6个呈均匀性高增强,1个呈不均匀性高增强,其中6个门脉期及延迟期呈低增强,为快进快出特征,误诊1个表现为门脉期及延迟期为等增强。11个CC病灶中动脉期7个为环状高增强,4个为不均匀性高增强,均于门脉早期呈低增强,延迟期廓清,为快进快出特征。5个MLC病灶动脉期3个表现为均匀性高增强,2个表现为环状高增强,门脉期及延迟期均表现为明显的低增强,呈快进快出特征。17个肝血管瘤表现动脉期向心性充填,呈环状或不均匀性高增强,门脉期为持续的高增强,延迟期为高增强或等增强,呈快进慢出或慢进慢出特征。1个误诊表现动脉期呈环状高增强,结节内为无增强,门脉期及延迟期呈环状等增强,结节内为低增强。13个FNH中12个表现为动脉期呈离心性的快速高增强,8个呈轮辐样改变,门脉期多表现为持续的高增强或等增强,延迟期为高增强或等增强,呈快进慢出特征。1个误诊表现为动脉期呈不均匀性高增强,无明显轮辐状,门脉期呈低增强,延迟期廓清。3个肝硬化结节及3个肝局灶性脂肪缺损均表现与肝脏组织同步增强,呈等进等出特征。3个肝局部炎性病变2个表现为动脉期呈等增强,整体充填,内见多个无增强区,呈蜂窝状改变;1例肝脓肿表现为动脉期边缘呈厚薄不一的高增强,门脉期及延迟期边缘仍为高增强,内部为无增强。
62个肝脏局灶病变始增方式及峰值声像见表3、4。典型病例CEUS图像见图1~3。

表3 62个肝脏局灶性病变峰值声像(n)

表4 62个肝脏局灶性病变始增方式(n)

图1 典型病例1(男性,80岁)的CEUS图像

图2 典型病例2(男性,55岁)的CEUS图像
图3 典型病例3(男性,19岁)的CEUS图像
3 讨 论
CEUS能实时显示组织的微血管结构和各时相(动脉期、门脉期和延迟期)的血流灌注,不同性质的肝脏局灶性病变因其血供方式、血管数量及其分布的不同而具有不同的特征。
恶性肿瘤新生大量发育不成熟的血管,血管间存在着动静脉瘘,因而CEUS显示动脉期呈迅速的高增强。因缺乏网状内皮细胞,血管通透性增加而迅速廓清,表现为延迟期低增强,呈“快进快出”的声像图特征,而不同类型的肝脏恶性肿瘤CEUS表现略有差异。HCC为富血供肿瘤,且以肝动脉供血为主,因而动脉期快速整体强化,而门脉期病灶内部肝动脉因造影微泡补充不足呈低增强(图1)[2]。CC的滋养血管多分布在肿块周边,而内部的血管稀疏纤维组织丰富[3],因而CEUS表现为动脉期呈厚壁的环状高增强,内部为不均匀网络状增强。MLC因原发灶的不同而表现为富血管型和乏血管型两种类型,因而其增强方式也不同,富血管型动脉期呈均匀或不均匀高增强,而乏血管型动脉期呈环状高增强。本组资料显示恶性病变组间在增强时相上三者无明显差异。一直径约15 mm的HCC误诊为肝血管瘤,表现为“快进慢出”特征,可能与病灶较小、分化程度高有关。文献报道部分恶性肿瘤亦表现为造影剂廓清缓慢,门脉期表现为等增强,这与肿瘤较小、分化程度高及存在门静脉血供有关[4]。有研究[5]表明,HCC“快进快出”的典型CEUS增强模式多见于较大的肿瘤,在<20、20~50和>50 mm的结节中出现的比例分别为76.2%、90.3%和96.8%。这提示病灶越小、分化程度越高,出现非典型HCC造影模式的可能性越大。
良性病灶中血管瘤及FNH具有特征性的CEUS改变,这与病灶病理学变化有关。血管瘤由大小不等的血窦组成,血流缓慢,造影剂不易进出,因而表现出快进慢出或慢进慢出的增强特征,同时部分因存在血栓或大量的纤维组织出现充盈缺损现象,表现为环状的高增强,而内部可见不规则的无增强区(图2)。FNH因肝动脉血管畸形引起肝组织增生并由内向外构成纤维分隔,有动脉血供丰富等特点,因此典型的FNH表现为动脉期呈离心性的快速高增强,并于门脉期及延迟期持续高增强或等增强(图3),因而FNH的轮辐状改变,并于门脉期及延迟期持续高增强或等增强的特征是其与恶性病变区别的关键。肝硬化结节及肝内局灶性脂肪缺损可能因无肿瘤血管及异常增生的血管,CEUS无明显改变。肝局部炎性反应早期因局部血供丰富,表现为动脉期边缘呈高增强,内部伴有坏死液化时呈蜂窝状改变,而形成脓肿时表现为无增强。本组资料中一直径约15 mm的肝血管瘤误诊为HCC,分析其内部可能有血栓形成或存在大量的纤维组织,同时可能与笔者经验不足有关;一直径约12 mm FNH误诊为HCC,与结节较小、不典型、位置较深同时伴有大量的纤维组织有关。有学者[6]认为一些FNH轮辐状增强的特征并不明显,尤其是较小的FNH;部分非典型的FNH结节内的血流直接引流到肝静脉是其门脉相低回声的原因[7]。近年来许多学者[8-10]从肿瘤的大小、有无动脉相高增强、廓清情况等方面对肝脏局灶性结节进行LI-RADS分类诊断,可明显提高肝脏局灶性病变的良恶性诊断准确度。本研究证实,肝脏恶性病变的快进快出、快速增强的CEUS特点,其峰值持续时间明显小于良性病变,表明良恶性病变的血流动力学特点有较大差异,为肝脏良恶性病变的鉴别提供了可靠的依据。
综上所述,与增强CT及MRI相比较,CEUS通过实时动态观察,能捕捉到增强过程中的瞬间血流灌注特征,因此绝大部分肝内局灶性病变能够明确诊断;同时其费用低廉,无明显禁忌,可重复操作,因而实用性强。但因其缺乏全面了解其他部位病变的信息,同时二维超声显示困难的部位,CEUS效果常不理想,医师的业务能力也影响结果的判断。笔者认为,首先应加强从事CEUS工作的医师规范化培训,提升技术水平。而对于部分2 cm以下CEUS不能明确诊断的病灶,应同时结合增强CT或MRI综合分析,必要时应进行超声引导下穿刺活检,如无法进行穿刺活检或活检仍不能明确诊断的应定期随访观察。
