MRI 指导骨髓保护调强放疗在宫颈癌放化疗中的剂量及临床研究
2021-01-13罗建奇孙亚楠师卫华
罗建奇, 孙亚楠, 张 亮, 师卫华
(银川市第一人民医院,银川 750001)
以顺铂为基础的同步放化疗是局部晚期及术后具有高危因素的宫颈癌患者的标准治疗[1]。多项临床研究发现,在提高疗效的同时,同步放化疗患者的急性血液毒性也显著增加。严重的骨髓抑制会使患者治疗暂停甚至终止,从而降低疗效[2-4]。因此减轻血液毒性的发生是目前宫颈癌放化疗中亟待解决的问题。现有研究已证实骨髓内的造血干细胞对低剂量的照射非常敏感,放疗剂量10Gy 时即可在MRI 下观察到急性水肿和脂肪浸润,更高剂量可导致骨髓血管床的闭塞和放射性骨髓炎[5-6]。由于成年人造血活性骨髓分布不均匀且普通CT 无法区分,因此对整体骨盆及腰椎骨性结构进行限量意义有限,而且会增加IMRT 计划设计难度[7-8]。本研究采用MRI 来识别造血活性骨髓,通过融合配准,在模拟定位CT 图像上勾画出其体积并限量,在靶区剂量学参数达标及危及器官保护的前提下,分析该技术对放射治疗剂量学和急性血液毒性的影响,并观察近期疗效,为临床提供参考。
1 材料与方法
1.1 一般临床资料
选择2014年1月至2018年12月在银川市第一人民医院初诊的90例宫颈癌患者为研究对象,临床分期为ⅡB 期至ⅢB 期,采用骨髓保护调强放疗(BMS-IMRT)的44例,采用常规调强放疗(IMRT)的46例。所有入选患者均有明确病理诊断,放化疗前血常规及肝肾功能无异常,临床检查未发现远处转移,既往未接受放化疗。两组患者临床资料见表1。
1.2 定位及扫描
患者口服加入60%泛影葡胺20 mL 的适量温水,充盈膀胱并显影小肠。憋尿后仰卧于固定体架上,热塑模固定后行螺旋CT 增强扫描,层厚5 mm,扫描范围为双肾下极至坐骨结节下5 cm,图像传输至Varian Eclipse 10.0 治疗计划系统。

表1 两组患者的临床特征
1.3 靶区及危及器官的勾画
临床靶区(clinical target volume,CTV)包括大体肿瘤、宫体、宫颈、宫旁以及髂总、髂外、髂内、闭孔及骶前淋巴引流区,阴道1/2 至2/3、阴道旁软组织。CTV 在头脚方向上外扩1.0 cm,腹背及左右方向外扩0.8 cm 成计划靶区(planning target volume,PTV)。同时勾画膀胱、直肠、小肠等危及器官(organ at risk,OAR)。对BMS-IMRT 组患者同一体位下行MRI 扫描;TR 为500 ms,TE为25 ms,层厚6 mm。T1WI 显示信号强度介于同视野肌肉信号和皮下脂肪信号之间为造血活性骨髓(图1a),采用Eclipse 系统的Registration 配准模块将MRI 图像和CT 模拟定位图像融合,确定造血活性骨髓。BMS-IMRT 组患者根据MRI识别的活性骨髓(图1c)和骨盆外轮廓(图1b)定义的骨髓体积,分别制订BMS-IMRT 和常规IMRT 计划。
1.4 处方剂量及计划设计
两组患者外照射放疗计划均采用7 野共面照射,PTV 处方剂量为50.4Gy/1.8Gy×28 次。BMSIMRT 组每例患者均针对同一PTV 设计活性骨髓限量和不限量两套计划。造血活性骨髓限量为V10<85%,V20<70%,V30<60%。
1.5 计划评价
利用剂量体积直方图(dose volume histograms,DVH)对BMS-IMRT 组每例患者的两个计划进行比较。(1)均匀性指数(homogeneity index,HI)和适形指数(conformity index,CI);(2)盆骨、膀胱、直肠等危及器官剂量体积百分比的差异。HI=D2-D98/D50(D2 表示2%的PTV 接受的剂量,D98 表示98%的PTV 接受的剂量,D50 表示50%的PTV 接受的剂量),均匀性指数表示靶区剂量分布情况,数值越小表示靶区剂量分布越均匀。CI=Vt,ref/Vt×Vt,ref/Vref(Vt、ref 为参考等剂量线面所包绕的靶区体积,Vt 为靶区体积,Vref 为参考等剂量线面所包绕的所有区域的体积)。适形度指数表示等剂量线面所包绕的区域与靶区的一致性,越接近1 适形度越好[9]。
1.6 同步化疗及后装治疗
两组患者化疗方案均采用顺铂40 mg·m-2,每周1 次,共4~5 次;后装治疗采用192Ir 高剂量率腔内后装治疗机,待同步放化疗结束后进行,6Gy/次,共4~5 次。
1.7 急性毒性反应和疗效评价
采用RTOG 急性放射损伤分级[10]进行急性毒性反应评估。治疗结束后3月根据患者结合妇科检查及影像学资料进行完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD)的近期疗效评价,其中CR+PR 为有效,有效率=(CR+PR)÷总例数×100%。
1.8 统计学方法
采用SPSS 17.0 统计软件进行分析,计量资料用t 检验;计数资料用χ2检验,P≤0.05 为差异有统计学意义。
2 结果
2.1 两种计划方法勾画的骨髓体积比较
BMS-IMRT 计划的活性骨髓体积为(144.31±22.78)cm3,IMRT 计划的骨髓体积是(922.97±19.43)cm3,两种计划的骨髓体积比较差异有统计学意义(P<0.05)。
2.2 两种计划的PTV 参数比较
在反应靶区剂量均匀性及适形度的指标方面,BMS-IMRT 计划和IMRT 计划的HI、CI 比较差异均无统计学意义(P均>0.05)(表2)。

表2 BMS-IMRT 和IMRT 两种计划的HI、CI 比较
2.3 危及器官的受照剂量和体积
DVH 分析显示BMS-IMRT 组的造血活性骨髓10、20、30、40、50 Gy 所接受的照射体积低于IMRT 组(P<0.05);但二者在5 Gy 时活性骨髓受照体积差异无统计学意义(P>0.05)。膀胱及直肠在中高剂量30、40、50 Gy 范围内接受照射体积两种计划差异均无统计学意义(P>0.05)(表3)。
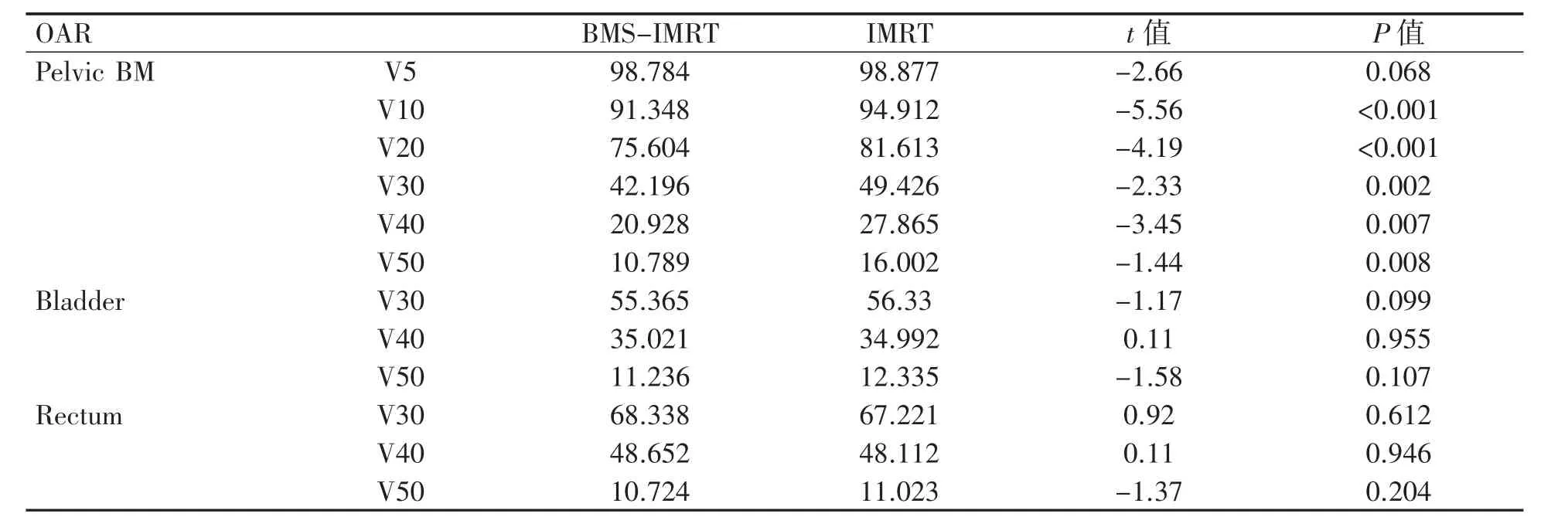
表3 两种计划危及器官剂量体积百分比比较(%)
2.4 急性血液毒性反应
两组均没有发生4 级骨髓抑制,BMS-IMRT组2 级及2 级以上骨髓抑制的发生率为34.09%,IMRT 组为58.70%,两组患者急性血液毒性反应比较差异有统计学意义(P<0.05)(表4)。

表4 两组患者急性血液毒性反应比较[例(%)]
2.5 近期疗效分析
PBM-IMRT 组有效率为95.45%(42/44);IMRT 组有效率93.48%(43/46),两组比较差异无统计学意义(P>0.05)(表5)。

表5 两组患者近期疗效比[例(%)]
3 讨论
同步放化疗在宫颈癌、直肠癌等盆腔恶性肿瘤治疗中占有重要地位。常规AP—PA 对穿照射难以使肿瘤靶区获得理想的剂量分布,但骨髓受照体积和剂量较低。调强放疗技术由于其明显的剂量学优势,在保证靶区剂量的同时能最大限度地降低正常组织损伤,由于其显著增加了骨髓低剂量照射区域,导致严重血液毒性反应明显增加。严重的骨髓抑制常导致治疗的中断甚至终止,使局部控制率和长期生存率均明显下降[9]。
Klopp 等[11]利用PET 扫描发现成人具有造血活性的骨髓超过50%位于盆骨及腰骶骨中,而这部分骨髓正好处于放射治疗的照射范围之内。研究证实造血干细胞对低剂量的射线非常敏感,尤其是在同步放化疗时,急性血液不良反应的发生率是单纯放疗的2~10 倍[12]。放化疗对造血活性骨髓的损伤具有叠加作用,所以临床上同步放化疗导致的骨髓持续程度较重,且短期内不易恢复。
目前国内外多项研究均已证实,盆腔恶性肿瘤行同步放化疗时,采用骨髓保护的调强放疗技术可以显著降低急性血液毒性的发生[1,13-14]。骨髓保护调强放疗技术需要解决的第一个问题是如何准确界定造血活性骨髓。由于造血活性骨髓分布不均匀且有个体差异,普通定位CT 无法区别造血活性骨髓,所以对整体盆骨限量并不可靠且会增加计划设计难度。在目前现有技术中,FDGPET 及FLT-PET 在造血活性骨髓的区分中有一定价值,但由于费用昂贵、辐射损伤等缺点难以在一般医疗机构中实施[15]。而核磁共振的T1WI上红骨髓和无造血活性的黄骨髓存在较明显的信号差异,容易识别,和模拟定位CT 进行图像融合后,可以指导勾画。国内外已有学者对直肠癌的放疗进行研究,结果发现此技术对剂量学参数没有明显影响[16-17]。黄荣等利用SPECT 定义活性骨髓,发现能明显降低高剂量辐射的剂量体积[18]。
另一个问题是骨髓剂量学参数与急性血液毒性的相关性。目前现有研究中对于造血活性骨髓的限量尚无统一标准。Albuquerque 等[12]研究发现骨髓V20>80%是骨髓抑制发生的独立预测因子。Rose 等对宫颈癌同步放化疗患者进行研究后提出骨髓V10>95%、V20>76%者易发生严重骨髓抑制[7,9]。综合以上结果,本研究界值为V10<85%,V20<70%,V30<60%,在IMRT 计划设计中对其进行保护。在剂量学方面,降低了造血活性骨髓的照射剂量的同时,没有增加其他危及器官的受照体积和剂量,明显降低了2 级及以上骨髓抑制的发生,近期疗效方面,BMS-IMRT 与传统IMRT 相比,未发现明显统计学差异。
在本研究中,我们首先注意到,MRI 识别造血活性骨髓存在一定的局限性,比如对于活性与非活性骨髓的信号值没有定量标准,实际操作中容易受到MRI 成像质量和放疗医师主观因素的干扰。另外,活性骨髓限量参数有待进一步明确,国内外学者尚未达成一致。本研究发现,BMSIMRT 计划和常规IMRT 计划相比,靶区HI 和CI差异无统计学意义,分析原因可能是对活性骨髓限量的约束条件比较宽松。
综上,MRI 能够比较清晰地反映造血活性骨髓的体积,为临床靶区勾画提供帮助。BMS-IMRT 技术对于降低造血活性骨髓受照体积和减轻急性血液毒性有明确作用。下一步需明确其剂量体积参数,同时观察对患者远期疗效的影响。
