基于数据挖掘和网络药理学的丹参配伍规律及其防治冠心病作用机制研究❋
2021-01-09周文静郭怡含李志勇周荣荣王永辉
周文静,朱 彦,郭怡含,李志勇,周荣荣,,柴 智,王永辉△
(1. 山西中医药大学基础医学院,山西 晋中 030600; 2. 中国中医科学院中医药信息研究所,北京 100700;3. 山东中医药大学中医学院, 济南 250355; 4. 中央民族大学药学院,北京 100081)
丹参为唇形科植物丹参(SalviamiltiorrhizaBge)的干燥根和根茎,首载于《神农本草经》,其味苦、性微寒,归心、肝经,具有活血化瘀、通经止痛、清心除烦、凉血消痈等功效[1]。主要化学成分为丹参酮、丹参酚酸类、挥发油及无机元素[2]。丹参有保护血管内皮细胞、抗心律失常、抗动脉粥样硬化、改善微循环等作用[3],常用于心脑血管病,是临床治疗冠心病(coronary heart disease,CHD)的主要中药之一,疗效肯定[4]。中药发挥作用的一大优势就是药物配伍,丹参应用历史悠久,方剂众多,因此挖掘丹参的配伍应用规律,突出丹参配伍后的多成分协同作用,对进一步提高丹参临床应用率具有重要意义。
近年来,随着计算机技术的高速发展,孕育而生的数据挖掘技术[5]与网络药理学[6]等技术方法在医药各方面发挥着越来越重要的作用。本研究采用数据挖掘和网络药理学相结合的方法,挖掘与分析丹参在方剂中的配伍规律,进一步从网络药理学微观角度探讨丹参药对防治冠心病的分子机制,为系统化研究丹参这一药物并将其更好地运用于临床提供科学依据。
1 资料与方法
1.1 文献检索
方剂来源于中国中医科学院信息研究所中国中医药数据库(http://cowork. cintcm. com/ engine/windex.jsp)。
1.2 数据清洗[7]
所选方剂为1911年前古代医籍收载方剂,且明确是内服(汤剂、丸剂、散剂)方剂,选取时剔除只有1味药的方剂以及组成中药物不明确的方剂。参照《中国药典》2015年版[1]与十三五规划教材《中药学》[8]对所录入中药名称进行规范化处理,剔除剂量、药物炮制信息、描述性前缀词,将药名规范化纳入进行数据整理。
1.3 数据挖掘
采用开源工具R (V3.4.0)语言arules包(https://cran.r-project.org/web/ packages/arules/)对含丹参方剂进行关联规则分析。其中支持度(Support)高的对药为频繁对药数据集;置信度(Confidence)越高药对关系越紧密,满足提升度(Lift)大于1,关联规则才有意义[9]。本研究以Lift>1,Confidence≥ 93%,按Support值降序排列选取丹参高频药对数据。
1.4 丹参药对作用靶标预测
在中药系统药理学分析平台(TCMSP)数据库[10](http://ibts. hkbu. edu. hk/LSP/ tcmsp. php),搜集含丹参高频对药的中药化学成分,以口服生物利用度(OB)≥30%、类药性(DL)≥ 0.18为中药活性成分筛选条件,并获得活性成分的预测靶标。利用Uniprot数据库(http:// www. Uniprot.org)查询、验证靶标信息,并统一为基因名称。
1.5 疾病靶标获取
采用人类基因数据库Gene Cards(http://www.genecards.org/)和在线人类孟德尔遗OMIM(http://omim.org/)数据库,以“coronary heart disease”为检索词,获取冠心病的疾病靶标。并在Uniprot数据库设定生物物种为homo sapiens (human),统一基因名称,删除重复项。
1.6 靶点相互作用及核心靶点筛选
在1.5基础上,将丹参药对化合物对应的所有靶标通过软件Cytoscape 3.2.1中“Network analyzer”功能进行拓扑属性分析,按度值Degree值取中位数。进一步利用STRING数据库(https://string-db.org)获取蛋白相互作用(PPI)网络,通过Cytoscape 3.2.1软件进行可视化展示,寻找关键靶点。
1.7 基因本体与通路富集分析
利用R Project中的org.Hs.eg.db包(http://www. bioconductor. Org/packages/release/ data/annotation/html/ org.Hs.eg.db.html),将基因symbols转变为Entrez IDs ,进而利用cluster Profiler包3.6版(http://bioconductor. org/packages/release/ bioc/ html/cluster Profiler. html)对核心靶标进行GO(gene ontology)注释和KEGG(Kyoto encyclopedia of genes and genomes)通路富集分析,将P值设置为小于0.01。
1.8 分子对接验证
在1.6基础上,选择拓扑参数度值前5的关键靶标,与相对应的活性成分以及治疗冠心病的阳性对照药洛伐他汀(Lovastatin)进行分子对接验证。在Systems Dock Web Site(http:// systems dock. unit. oist.jp/iddp/ home/ index)分析平台输入活性成分3D结构,按照提示步骤进行分子对接并保存结果,对docking score进行分析。
2 结果
2.1 关联规则分析
表1示,经过文献整理筛选出含丹参方剂共773首,利用R语言从中筛选获得550组对药数据。按Support≥ 1%且Confidence≥ 93%、Lift> 1,筛选含丹参的对药数据115个。根据Support值由大到小排序,排名前5位的高频对药分别是{人参}=>{丹参}、{防风}=>{丹参}、{川芎}=>{丹参}、{芍药}=>{丹参}、{肉桂}=>{丹参},将这5组对药中的药物认为是与丹参作用密切的药物。其中芍药有赤芍、白芍2种,由于明代以前的医籍中没有明确赤白之分[11],在进一步的网络药理学分析中,选取活血化瘀作用较好的赤芍与丹参进行配伍研究。
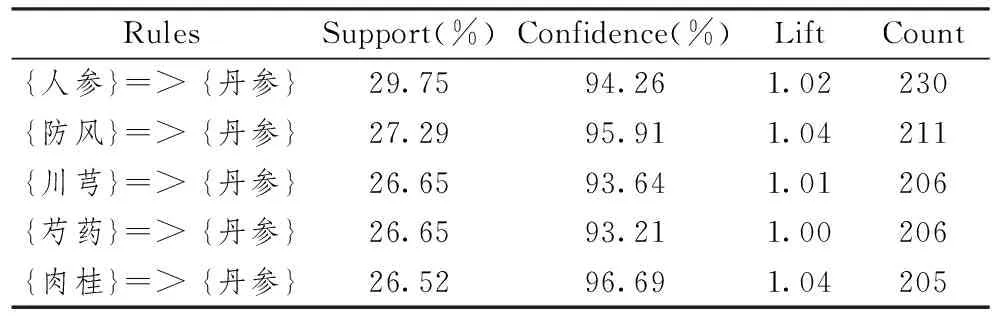
表1 含丹参高频药对之间的关联规则分析
2.2 丹参药对潜在靶点与冠心病已知靶点筛选
表2图1示,预测丹参药对化合物的潜在作用靶点,其中丹参作用靶点1763个,人参562个,川芎1039个,防风1096个,赤芍528个,肉桂448个,发现丹参与其他药物均有共性靶点。其中丹参与防风、赤芍、川芎共性靶点较多,说明有较强的协同作用;而丹参与肉桂共性靶点最少,协同作用较低。与此同时,检索到冠心病疾病靶标63个,其中丹参药对与疾病共有靶标12个,分别是MMP3、IL10、ALOX5、INS、CETP、IGF2、SELP、GLB1、AKR1B1、AR、CRP、NR3C1,推测丹参药对可能通过上述靶点发挥协同治疗作用。使用Cytoscape 3.2.1软件,构建丹参药对“药对-靶点”关系图,反映各药对间的共同靶点关系。“防风-丹参”“川芎-丹参”与疾病共有靶点交互较多,所以丹参通过与川芎、防风等药物配伍在治疗冠心病中可能发挥重要作用。而“肉桂-丹参”与疾病共有靶点交互最少,治疗作用较弱,进一步机制研究中将其剔除。

表2 丹参的高频药对之间共同靶点分析

图1 丹参药对与疾病共有靶点交互图(浅色代表中药,深色代表靶点)
2.3 丹参药对防治冠心病关键靶点预测
图2示,选取丹参分别与赤芍、川芎、防风、人参等对药,按网络拓扑中位数值选取255个潜在靶点,及已知靶点在STRING数据库构建PPI网络。使用Cytoscape 3.2.1软件进行可视化处理,将Degree值前100位的靶点进行展示,越接近红色表明网络中节点与节点相连的数目越多,即Degree值越大。网络拓扑值前10位靶点包括共有靶点INS(胰岛素),已知靶点TNF(肿瘤坏死因子),潜在靶点MAPK1(丝裂原活化蛋白激酶1)、AKT1(RAC-α丝氨酸/苏氨酸-蛋白激酶)、IL6(白细胞介素-6)、CAT(氯霉素乙酰转移酶)、VEGFA(血管内皮生长因子A)、CASP3(半胱天冬酶3 )、JUN(转录因子AP-1)、MAPK1(丝裂原活化蛋白激酶1)、MMP9(基质金属蛋白酶-9)。这些靶点可能是丹参药对发挥作用的关键靶点,且靶点之间的关系密切,存在相互协同作用。
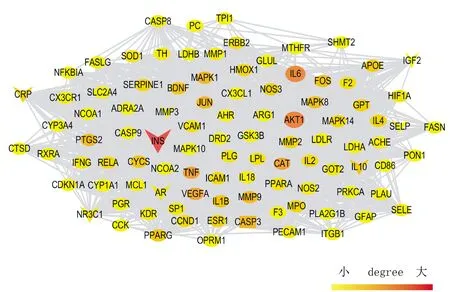
图2 关键靶标网络比较(三角形为共有靶点,圆形为潜在靶点,颜色越深表示越重要)
2.4 关键靶点GO、KEGG通路富集分析
图3示,将丹参药对治疗冠心病关键靶标进行GO和KEGG通路分析。结果显示,丹参药对主要通过类固醇激素反应、羧酸生物合成、有机酸生物合成、氧化应激反应等生物过程(biological process,BP),并结合辅酶、羧酸、有机酸、G蛋白偶联乙酰胆碱受体活性、类固醇激素受体活性等分子功能(molecular function,MF)发挥作用。涉及KEGG通路包括流体剪切应力和动脉粥样硬化通路(Fluid shear stress and atherosclerosis)、晚期糖基化终末产物及其受体(AGE/RAGE)信号通路(AGE-RAGE signaling pathway in diabetic complications);免疫相关信号通路包括肿瘤坏死因子信号通路(TNF signaling pathway),信号传导通路包括血管内皮生长因子信号通路(VEGF signaling pathway)、IL-17信号通路(IL-17 signaling pathway);感染性疾病信号通路如乙型肝炎(Hepatitis B),癌症信号通路如前列腺癌(Prostate cancer)。具体分析用Graph Pad Prism 5.0绘图,提示丹参药对的主要活性成分靶点通过多种生物过程、分子功能、不同的代谢途径发挥作用。
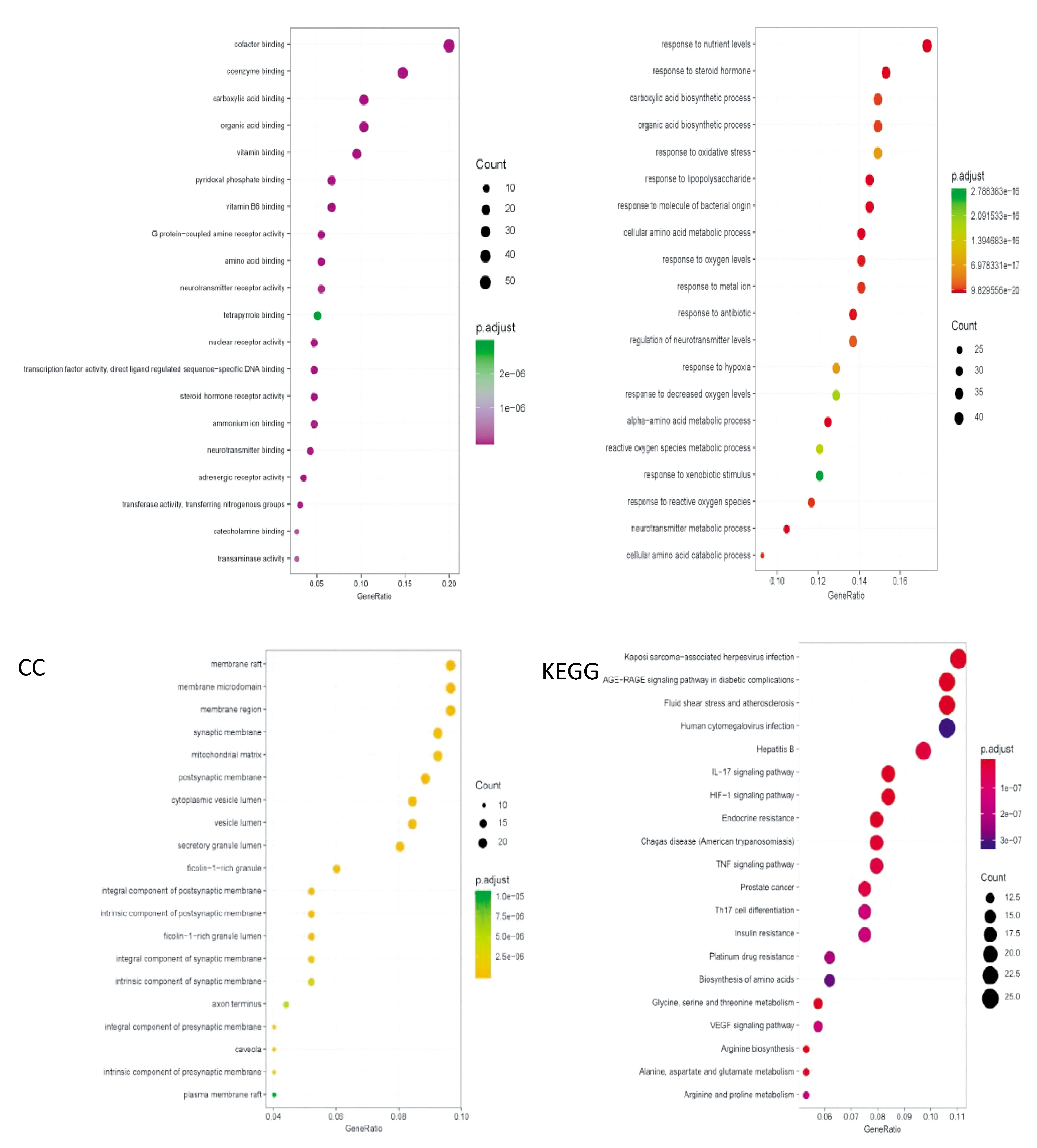
图3 GO富集分析和KEGG通路分析
2.5 分子对接验证
图4示,采用Systems Dock Web Site分析平台进行分子对接验证,其中对接结果评分docking score代表小分子与靶蛋白结合强度,一般认为docking score值在4.25以上表示分子与靶点之间有一定的结合活性,大于5.0分表明有较好的结合活性,大于7.0表明具有强烈的结合活性[16]。将排名前5的靶点INS、TNF、AKT1、IL6、CAT进行分子对接,由于TNF缺少相应的晶体结构未进行分子对接,结果显示多数丹参药对活性成分与重要靶点有较好的结合性,与阳性对照药Lovastatin的docking score分值接近,证明预测靶点的可靠性及丹参药对活性成分与靶点的良好结合活性。

图4 丹参药对主要化学成分和具体靶点对接结果
2.6 构建“中药-成分-关键药靶-通路”网络
图5示,最后构建“中药-成分-关键靶点-通路”网络图。为更清晰直观,仅选取KEGG通路富集分析结果前20名的通路以及网络拓值前10位的靶点进行可视化展示,提示丹参药对中同一药物有多种化合物,不同药物又有相同的化合物;同一化合物可以调节不同靶点,同一靶点也会参与不同的代谢通路,形成多靶点和多通路协同作用的特点。

图5 “中药-成分-靶点-通路”网络比较
3 讨论
冠心病属于中医学“胸痹”“心痛”等范畴,表现为“胸痹不得卧,心痛彻背”者,为一种临床常见病、多发病,严重危害人类健康。中医药在改善冠心病临床症状、延缓演变、改善预后方面具有独特优势和良好作用[3]。文献研究治疗冠心病方剂用药规律,得出治疗冠心病最常用的单药就是丹参(共143次占54.40%)[13],而与丹参配伍治疗冠心病的药物组成即是以活血化瘀药为主,佐以益气、祛瘀、通脉药,如人参、川芎、赤芍[14],而丹参与防风、肉桂用于冠心病治疗报道较少。通过网络药理分析发现,“丹参-防风”为冠心病疾病靶点交互最多的药对,可能在冠心病治疗中发挥重要作用。从发病病因来看,冠心病多因痰瘀互结、日久郁而化热、暗耗真阴,进而导致阳亢风动、风与痰瘀互结在一起形成风痰内动的病理证候[15]。风邪特性善行而数变,病人会出现病情反复发作、发病急剧、症状多种多样的表现,类似于冠心病心绞痛“不稳定”型的特点[16]。防风功用祛风解表、胜湿止痛止痉,为风药之润剂,用于治疗冠心病取其祛风以胜湿祛痰之功,且现代药理研究防风可影响红细胞和纤维蛋白的原量及功能,发挥活血化瘀作用[17],所以防风既可祛风治标又可活血治因,可见丹参与防风的配伍亦是治疗冠心病的重要组合。
网络药理学预测,丹参药对防治冠心病关键靶标有INS、TNF、MAPK1、AKT1、IL6、CAT、VEGFA、CASP3、JUN、MAPK1、MMP9等。研究报道,INS抵抗是CHD等心血管疾病的病理基础,不同区域的CHD患者其INS抵抗水平存在明显差异[18]。同时局部或全身的炎症反应在动脉粥样硬化及其并发症的发生发展中起重要作用[19]。TNF-α是一种有效的促炎细胞因子,IL-6为一种多效的细胞因子,在炎症反应中起中枢性调节作用,并且IL-6与相应受体结合后可诱导基质金属蛋白酶MMP-9的表达和释放,促进平滑肌细胞的增殖[20-21],而释放MMP-9可提高炎症单核细胞聚集与浸润,又会刺激补体、TNF等物质生成,从而加重血管粥样硬化及钙化[22]。CAT是一种关键的抗氧化酶,可以抵御氧化应激反应,而氧化应激反应贯穿动脉粥样硬化斑块形成的始终[23]。KEGG通路分析主要涉及流体剪切应力和动脉粥样硬化信号通路、AGE/RAGE、TNF、IL-17、VEGF信号通路以及感染性疾病通路等,形成多靶点、多途径的作用特点,且相应的靶标又会映射于相关通路。以VEGF信号通路为例,血管内皮细胞功能障碍发生于动脉粥样硬化的全过程[24]。网络药理学预测,映射于VEGF信号通路的关键靶点有AKT1、MMP9、MAPK1。研究表明,抑制内皮细胞Akt1加剧了缺氧诱导的体内血管重构[25]。VEGF可以增加MMP的表达,促进冠脉侧支循环的形成[26]。VEGF诱导MAPK活化,在大鼠心脏缺氧模型中,p38MAPK被激活导致心肌细胞凋亡[27],说明这些关键靶点在与冠心病相关的VEGF通路中确有作用。丹参药对防治冠心病化学成分众多,进一步分析化合物与关键靶点的关系。如与AKT1存在相互作用的化合物有丹参中木犀草素(luteolin)、丹酚酸A (salvianolic acida)、芹菜素(apigenin);防风中的汉黄芩素(wogonin);赤芍中黄芩素(baicalein)、芍药酮(paeonol);人参中的4,5,7-三羟黄酮醇(kaempferol),且通过分子对接验证,除汉黄芩素与芍药酮与靶点AKT1对接得分小于4.0外,其余均大于5.0,有较好的结合活性且作用密切,体现了丹参药对防治冠心病“中药-化学成分-靶点-通路”增效协同的完整作用过程。
综上所述,本研究通过数据挖掘得到5组丹参高频药对。网络药理学方法预测丹参高频药对防治冠心病的分子机制,丹参药对主要作用于INS、TNF、MAPK1、AKT1、IL6等靶点,干预多种生物过程与分子功能,主要通过动脉粥样硬化通路、TNF、AGE-RAGE、VEGF、IL-17等信号通路发挥作用。本研究不足之处,未对丹参药对与冠心病的不同证型进行对应研究,且相关分子机制尚需基础实验验证。
