腹腔镜下Dixon与Miles手术对低位直肠癌根治保肛术后患者手术应激反应及肛门功能的影响
2021-01-06张玉麒刘明亮
张玉麒,刘明亮
(浚县人民医院普外二科,河南 浚县 456250)
低位直肠癌是指发生在距肛缘3~6 cm左右的直肠恶性肿瘤,发病率占所有直肠癌的70%,临床以手术切除治疗为主[1]。但对于直肠癌患者来说,传统手术术后由于人工肛门的存在使患者心理和生活质量受到极大影响。目前认为保留完整的肛管直肠黏膜对维持患者肛门括约肌功能以及排便反射功能正常具有重要的生理意义[2]。目前临床上低位直肠癌根治保肛术常用的术式包括腹会阴联合直肠癌根治术(Miles)和直肠低位前切除术(Dixon)。Miles手术主要切除患者的全部直肠、部分乙状结肠、肠系膜下动脉及区域淋巴结、直肠系膜、肛提肌等的基础上做一单腔造口。Dixon手术在切除病变直肠的基础上,较好地保留了部分直肠、肛管、肛门括约肌、肛提肌等和一部分排便功能。鉴于此,笔者采用对比研究的方法探讨腹腔镜下Dixon与Miles手术治疗对低位直肠癌根治保肛术后患者手术应激反应及肛门功能的影响,报告如下。
1 资料与方法
1.1 一般资料
选取2014年5月至2017年5月浚县人民医院收治的低位直肠癌患者108例,根据手术方案不同,分为2组:观察组54例,男33例、女21例,年龄36~75岁、平均(55.64±19.28)岁;对照组54例,男31例、女23例,年龄38~79岁、平均(56.12±16.69)岁。2组患者的性别、年龄等一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经本院医学伦理委员会审批批准。
1.2 入选及排除标准
入选标准:1)所选患者均符合《胃肠病学》中关于直肠癌的诊断标准[3];2)所有患者术前临床分期为T2-4N0-2;3)年龄35~80岁;4)符合低位直肠癌保肛术的适应证;5)患者自愿参与本研究并签署知情同意书。
排除标准:1)肿瘤已转移或转术中开腹者;2)急性肠穿孔、出血、梗阻者;3)心、肝、肾等重要器官功能严重障碍者;4)血液及免疫系统疾病者;5)伴有其他恶性肿瘤者;6)有精神疾病史者。
1.3 手术方法
所有患者手术均由同一组经验丰富的胃肠外科专科医师团队完成,手术严格遵循全直肠系膜切除(TME)原则[4]。
对照组予以Miles手术,具体操作方法如下:行气管插管、全身麻醉,体位放置头低足高截石位,建立人工气腹,常规做操作孔,置入腹腔镜探查病灶,游离直肠,切除肛门周围5 cm处皮下至肛提肌、肛尾韧带,将切断后的近端肠管拉出,扩张肛口,吻合肛管残端,于左下腹部麦氏点操作孔处作乙状结肠造口,结束关腹。
观察组予以Dixon手术,具体操作方法如下:行气管插管、全身麻醉,体位放置头低足高截石位,建立人工气腹,常规做操作孔,置入腹腔镜探查病灶,离断肿瘤下方1~2 cm处范围的直肠,离断肿瘤上方10~15 cm处的近端肠管,于左下腹划一5 cm左右的切口,于腹腔内取出病变直肠及部分乙状结肠,用弯型吻合器吻合直肠与结肠,常规放置引流管,结束关腹。
1.4 观察指标及评价标准
1)比较2组术中出血量、胃肠功能恢复时间等临床相关指标。2)比较2组术前及术后3 d炎症因子白细胞介素-6(IL-6)水平变化。3)术后3个月随访2组排便困难、切口感染、吻合口瘘等并发症发生情况。4)术后6个月,对患者的肛门功能进行随访。比较2组患者肛门功能的优良率。评价标准:按照“五项十分制”让患者从0~10分进行评分;综合得分后,将肛门功能划分为4个等级;其中优:9~10分;良:7~8分;一般:5~6分;差:4分及以下。优良率=(优+良)例数/总病例数×100%。5)随访2年后,比较2组术后复发率。
1.5 统计学方法
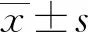
2 结果
2.1 2组临床相关指标比较
2组术中出血量、胃肠功能恢复时间等临床相关指标比较,差异无统计学意义(P>0.05)。见表1。
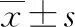
表1 2组临床相关指标比较
2.2 2组炎症因子IL-6水平比较
观察组术前、术后3 d IL-6水平分别为(17.86±4.58)pg·mL-1、(54.27±9.63)pg·mL-1;对照组术前、术后3 d IL-6水平分别为(18.04±4.36)、(74.89±10.26)pg·mL-1。与对照组比较,观察组术后3 d的IL-6水平上升幅度明显减小,差异有统计学意义(t=10.768,P<0.05)。
2.3 2组术后并发症比较
随访2年,观察组发生排便困难、切口感染、吻合口瘘的例数为1、0、1,分别对应对照组的3、3、2。观察组排便困难、切口感染、吻合口瘘等并发症总发生率为3.70%,显著低于对照组的14.81%,差异有统计学意义(χ2=3.967,P=0.046)。
2.4 2组肛门功能优良率比较
与对照组比较,观察组术后6个月肛门功能优良率显著升高,差异有统计学意义(P<0.05)。见表2。

表2 2组肛门功能优良率比较 例
2.5 2组术后复发率比较
随访2年后,观察组有2例复发,复发率为3.70%,对照组有5例复发,复发率为9.26%。2组复发率比较,差异无统计学意义(χ2=0.611,P=0.434)。
3 讨论
低位直肠癌由于其部位较深且解剖结构层次复杂,加大了手术的难度,同时对术者提出了更高的要求。近年来,随着对肠癌生物学研究的深入和腹腔镜技术的不断进步,其在治疗直肠癌患者中的优势越来越突出,同时也使直肠癌患者保肛的实现成为可能。Miles手术全名为腹会阴联合直肠癌根治术,主要切除患者的全部直肠、部分乙状结肠、肠系膜下动脉及区域淋巴结、直肠系膜、肛提肌等的基础上做一单腔造口。Dixon手术全名为直肠低位前切除术,多应用于直肠癌保肛手术中,该手术方案在切除病变直肠的基础上,较好地保留了部分直肠、肛管、肛门括约肌、肛提肌等和一部分排便功能。
本研究中,2组术中出血量、胃肠功能恢复时间等临床相关指标及术后2年复发率比较,差异无统计学意义,说明两种手术方式对患者的术后恢复及生存质量的远期效果均较高。分析其原因可能与腹腔镜使局部手术视野更清晰,帮助医生更加准确地辨认血管及神经组织有关[4];术中超声刀分离和止血作用效果好,有利于减少术中出血及医源性种植,降低术后转移和复发。本研究经3个月的随访后发现,观察组术后并发症发生率显著低于对照组,与周启军等人[5]的研究结果一致,表明腹腔镜下Dixon手术相比于Miles手术治疗低位直肠癌的安全性较高。本研究中观察组术后3 d的IL-6水平上升幅度明显小于对照组,表明腹腔镜下Dixon手术可有效减轻直肠癌患者的炎症因子水平,从而减轻手术带来的应激反应,保护患者的肠道功能[6]。可能与Miles手术切除范围更广、对患者身体的损伤程度更大,造成切口感染的风险更高有关。本研究结果显示,观察组术后6个月肛门功能优良率为74.07%,显著高于对照组的53.70%,表明应用Dixon手术方式较Miles手术方式治疗对低位直肠癌根治保肛术后患者肛门功能的恢复效果较好。可能与Dixon手术中弯型吻合器的使用,将直肠与结肠进行吻合有关,此步骤尽可能保留了患者的肛门功能[7]。
综上所述,腹腔镜下Dixon手术相比Miles手术治疗低位直肠癌总体效果明显,可以显著降低术后患者的应激反应,改善肛门功能,且术后并发症较少。
