基于UHPLC-QTOF MS的肉桂枝叶蒸油剩余物化学成分研究
2020-12-31毕良武曾维星赵振东陈玉湘张笮晦
程 贤, 毕良武*, 曾维星, 赵振东, 陈玉湘, 张笮晦
(1.中国林业科学研究院 林产化学工业研究所;生物质化学利用国家工程实验室;国家林业和草原局林产化学工程重点实验室;江苏省生物质能源与材料重点实验室;江苏省林业资源高效加工利用协同创新中心,江苏 南京 210042; 2.广西中医药大学 药学院 广西中药药效研究重点实验室,广西 南宁 530200; 3.广西庚源香料有限责任公司,广西 东兴 538100)
肉桂(CinnamomumcassiaPresl)主要分布在我国的广西、广东,此外,印度、老挝以及越南等地也有种植[1]。肉桂中挥发性活性成分主要为肉桂醛等组成的肉桂油[2],精油提取后的剩余物中含有大量的非挥发性活性成分,如酚酸、黄酮、苷等。酚酸类成分主要有原儿茶酸、香豆酸和香草酸等,占非挥发性活性成分的17.5%[3];黄酮类成分主要有槲皮素、山柰酚和木犀草素等,占非挥发性活性成分的4.47%[4]。这些非挥发性成分具有抗菌、抗氧化、抗肿瘤等作用,具有广阔的应用前景[5-7],但并没有得到充分的利用,大多数肉桂蒸油剩余物被当做废水直接排放,不仅容易造成资源浪费,还会导致环境污染。近年来,针对肉桂蒸油剩余物化学成分的研究主要集中在紫外分光光度法测定含量及其生物活性的测定[8]。对肉桂蒸油剩余物化学成分的结构表征未见报道,该研究难点在于肉桂蒸油剩余物化学成分复杂,并且具有极性大和难挥发等特点,常规的分析方法较难实现对其化学成分的全面表征。液相色谱质谱联用技术可以快速分析植物提取物复杂体系内结构的化学成分,在提取物化学成分的全面表征中已被广泛应用[9]。其中,四极杆飞行时间质谱(QTOF MS)能够测得化合物的精确分子质量而不降低灵敏度,通过精确分子质量可以获得化合物的分子式,是提取物化学成分表征研究的有力工具。韩金美等[10]采用超高效液相色谱-高分辨飞行时间质谱(UHPLC-QTOF MS)从苏格木勒-3水提物中鉴定出42个成分,为其质量控制研究奠定了基础。陈嘉慧等[11]基于UHPLC-QTOF MS技术指认了丹参水提物中的72个成分,为筛选丹参活性成分提供了科学依据。本研究采用UHPLC-QTOF MS对肉桂蒸油剩余物的化学成分进行了全面的定性分析,同时对酚类、黄酮类、糖苷类、醇类、醛类和酸类化合物在电喷雾质谱中的裂解路径进行研究。由于同一类化学成分往往具有相同的骨架结构或亚结构,因此这些成分在质谱裂解过程中会丢失相同的中性碎片或者形成相同的特征离子,所以本研究不仅能为肉桂蒸油剩余物中化学成分鉴定提供重要参考,还能为肉桂资源的开发与利用提供理论基础。
1 实 验
1.1 材料与试剂
干燥的肉桂枝叶,由广西庚源香料有限责任公司提供,粉碎后过筛,取粒径0.15~0.25 mm的部分备用;乙腈和甲醇均为色谱纯,购自美国Merck公司;甲酸为质谱级,购自Sigma-Aldrich公司。
1.2 仪器与设备
Milli-Q纯水仪,美国Millipore公司;Waters Acquity BEH C18(2.1 mm×100 mm,1.7 μm)色谱柱,美国Waters公司;Shimadzu LC-30A Series UHPLC系统,配备SIL-20AC自动进样器、LC-20AD 二元泵、CTO-20A柱温箱和SPD-M20A二极管阵列检测器,日本岛津公司;AB SCIEX QTOFTM 5600+质谱仪,美国SCIEX 公司;移液枪、 5424高速离心机,德国Eppendorf公司。
1.3 样品制备
1.3.1肉桂蒸油剩余物的制备 取粉碎、过筛后的干燥肉桂枝叶,转移到水蒸气蒸馏装置中,按照料液比1 ∶50(g ∶mL)加入蒸馏水,于100 ℃电热套中加热8 h,采用抽滤方式分离,分离所得滤液减压浓缩后真空干燥,得到肉桂蒸油剩余物,干燥器内储存备用。
1.3.2供试品溶液配制 取肉桂蒸油剩余物2.50 g,置具塞锥形瓶中,精密加入50%甲醇水溶液50 mL,超声波(功率250 W,频率25 kHz)溶解0.5 h,放冷,摇匀,转移至离心管并13 000 r/min离心10 min,将上清液转移至进样小瓶中并进行UHPLC-QTOF MS分析。
1.4 色谱和质谱条件
1.4.1色谱条件 Shimadzu LC-30A Series UHPLC系统,柱温为35 ℃,流速为0.2 mL/min,流动相A为0.1%甲酸水溶液,流动相B为乙腈。梯度洗脱条件为:0~3 min,95%流动相A,5%流动相B;3~10 min,95%~40% 流动相A,5%~60%流动相B;40~45 min,40%~5%流动相A,60%~95%流动相B;45~55 min,5%流动相A,95%流动相B;55~56 min,5%~95% 流动相A,95%~5%流动相B;56~60 min,95%流动相A,5%流动相B,进样体积为2 μL。
1.4.2质谱条件 AB SCIEX QTOF TM 5600+质谱仪,电喷雾离子源(ESI)喷雾电压3 000 V;雾化气N2,1.5 L/min;干燥气N2,140 kPa;诱导碰撞解离(CID)碰撞气为氩气,50 kPa;解簇电压90 V;碰撞电压45 V;离子源温度350 ℃;毛细管温度300 ℃;扫描范围m/z100~1 000。所有样品数据采集均在正离子模式和负离子模式2种模式下进行,首先通过全扫模式描获取一级质谱信息,然后采用非靶向模式获得MS/MS二级碎片。
1.5 数据处理
应用Peak View 软件(AB公司,美国)进行数据分析,并通过分子式预测功能推测化合物的可能分子式。
2 结果与讨论
2.1 肉桂蒸油剩余物主要化学成分
肉桂枝叶蒸油剩余物来自水蒸气蒸馏法提取精油后的水溶液,其主要化学成分均具有非挥发性,因此采用超高效液相色谱-高分辨飞行时间质谱(UHPLC-QTOF MS)仪能对肉桂蒸油剩余物的主要化学成分进行全面的表征。本研究在文献中肉桂乙醇提取物的液相分离条件基础上稍作调整[12]。鉴于前期研究已经表明,肉桂中的非挥发性成分以酚酸和黄酮类成分为主,酚酸类成分在质谱检测中容易丢失H+产生[M-H]-,黄酮类成分在质谱检测中容易加和H+产生[M+H]+,因此本研究在质谱检测过程中采用了正离子和负离子2种检测模式。首先利用全扫描模式获取主要化学成分的一级质谱信息,然后采用非靶向扫描模式获取二级质谱信息。基于二级质谱信息和相关文献,进一步分析了化合物的质谱裂解路径。最终,综合考虑保留时间、精确分子质量、分子式、特征性离子碎片及文献数据,共鉴定了26个化学成分,总离子流色谱图见图1,化合物定性分析结果见表1。26个化合物在图1中的出峰顺序表明,所使用的液相分离条件使肉桂蒸油剩余物的主要化学成分得到充分的分离,有利于进一步的质谱检测。肉桂油中含量较高的挥发性成分如肉桂醛、肉桂酸容易残留在肉桂蒸油剩余物中,由于质谱分析灵敏度高,上述物质会在肉桂蒸油剩余物中被检测到,如表1中的化合物23和24。
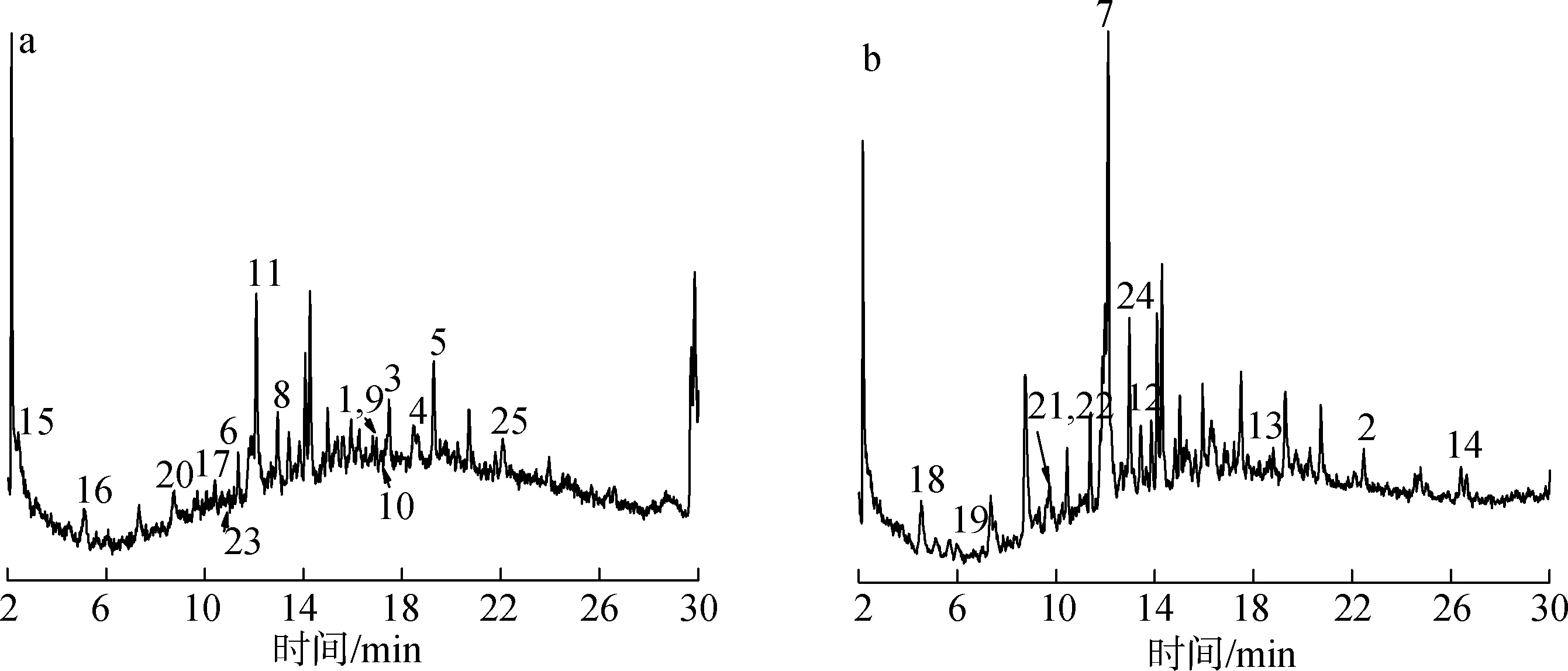
a.正离子检测模式positive mode; b.负离子检测模式negative mode
2.2 不同类型化合物结构表征
2.2.1酚类化合物 酚类化合物种类众多,其结构特点为芳环上直接连接了羟基,由于羟基的取代使酚类化合物通常具有抗氧化活性的潜力。
化合物1准分子离子峰是m/z165.1,通过软件计算其分子组成,推测该化合物分子式为C10H12O2,加和离子为[M+H]+,m/z105.1推断为准分子离子先丢失一个CH4O(32 u)后继续丢失一个CO(28 u)所产生,上述碎片与丁香酚连续丢失CH4O、CO所得碎片完全一致,结合相关文献[12],推断化合物1为丁香酚,推测的质谱裂解路径见图2路径I。
化合物2准分子离子峰是m/z417.1,通过软件计算其分子组成,推测该化合物分子式为C22H26O8,加和离子为[M-H]-,m/z387.1推断为准分子离子丢失2个CH3(15 u)所产生,m/z181.0推断为醚键断裂所产生,m/z166.0推断为m/z181.0碎片继续丢失1个CH3所产生,上述碎片与丁香脂素连续丢失CH3以及醚键断裂所得碎片完全一致,结合相关文献[13],推断化合物2为丁香脂素,推测的质谱裂解路径见图2路径II。

表1 肉桂枝叶蒸油剩余物中化学成分的定性分析

图2 酚类化合物质谱裂解路径
2.2.2黄酮类化合物 黄酮类化合物指具有2-苯基色原酮结构的化合物,天然黄酮类化合物母核上常含有羟基、甲氧基等取代基,很多黄酮类化合物具有药用价值,不仅具有止咳、祛痰、平喘及抗菌的活性,同时能用于防治心脑血管疾病。
化合物3准分子离子峰是m/z303.0,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C15H10O7,m/z229.0推断为准分子离子A环丢失一个H2O(18 u)和CO(28 u),B环继续丢失一个CO(28 u)所产生,m/z153.0推测为C环C—C的断裂,即逆狄尔斯-阿尔德反应(RDA),该碎片也是黄酮类物质的特征离子碎片。m/z153.0碎片与槲皮素分子在正离子模式下C环C—C的断裂所产生的碎片完全一致,结合相关文献[14],推断化合物3为槲皮素,推测的质谱裂解路径见图3路径I。
化合物4准分子离子峰是m/z287.0,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C15H10O6,同化合物3类似,m/z153.0推测为黄酮类物质的特征离子碎片,m/z165.0推测为准分子离子A环(C6H6O,94 u)断开后,B环丢失1分子CO(28 u)所产生。m/z153.0碎片与山柰酚分子在正离子模式下所产生的碎片完全一致,结合相关文献[14],推断化合物4为山柰酚,推测的质谱裂解路径见图3路径II。
化合物5准分子离子峰是m/z287.0,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C15H10O6,同化合物4为同分异构体,m/z153.0推测为黄酮类物质的特征离子碎片,m/z241.0推测为准分子离子A环丢失1分子H2O(18 u)和1分子CO(28 u)所产生,m/z213.0推测为m/z241.0 碎片继续丢失1分子CO(28 u)所产生,m/z153.0碎片与木犀草素分子在正离子模式下所产生的碎片完全一致,结合相关文献[14],推断化合物5为木犀草素,推测的质谱裂解路径见图3路径III。
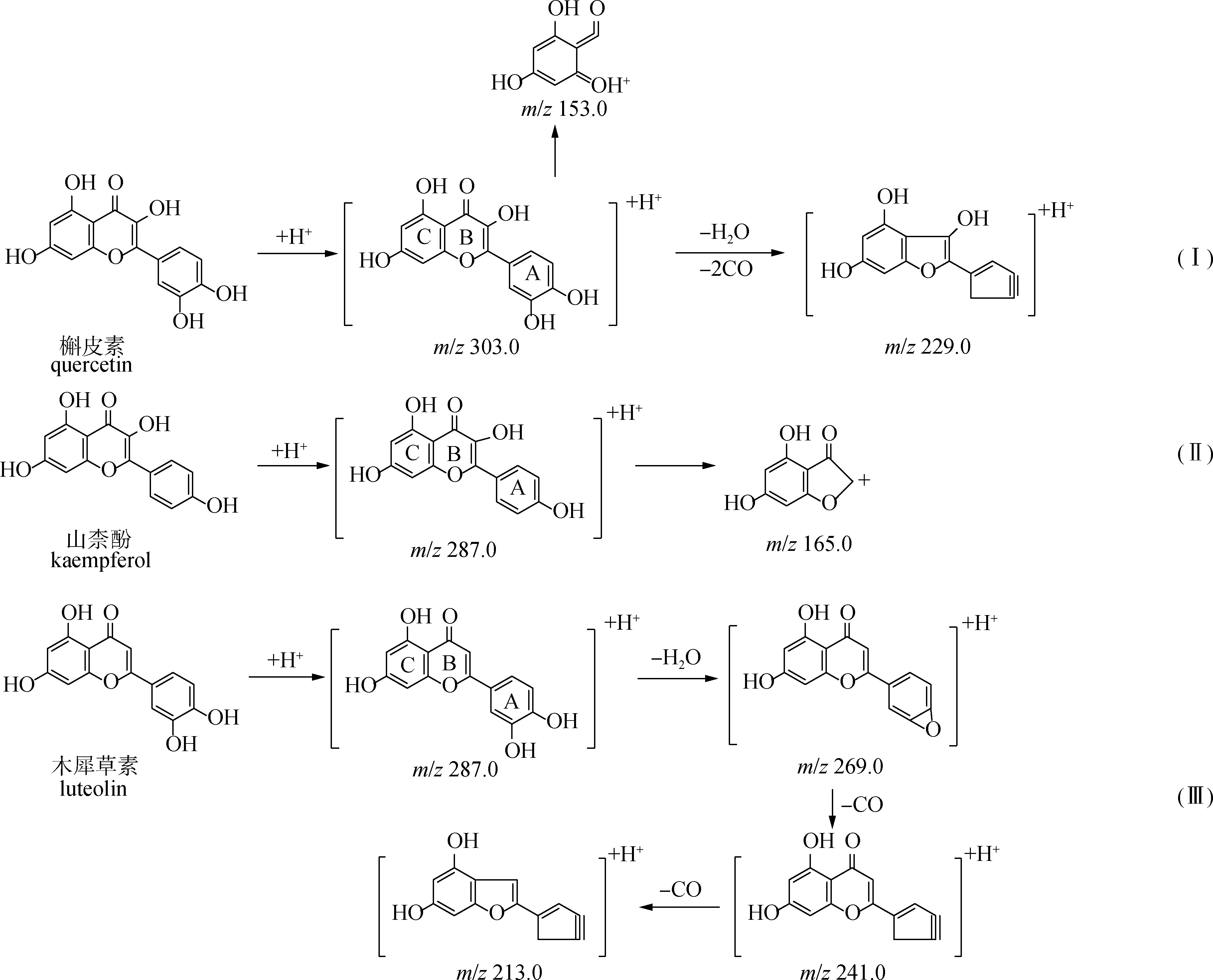
图3 黄酮类化合物质谱裂解路径
肉桂蒸油剩余物中黄酮类化合物的质谱行为研究表明:化合物3、 4和5的结构区别在于A/B环上的羟基位置或数量不同,在正离子模式下都可以通过RDA反应产生m/z153的特征碎片。
2.2.3糖苷类化合物 糖苷类化合物是由糖或糖衍生物的端基碳原子与另一类非糖物质连接形成的化合物,如黄酮类化合物在植物体中通常与糖结合成糖苷类。
化合物6准分子离子峰是m/z611.1,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C27H30O16,m/z303.0推测为准分子离子连续丢失1分子鼠李糖和1分子葡萄糖所产生,因此推测化合物6为双糖苷。m/z303.0碎片与化合物3的分子离子峰相同,因此推测化合物6的母核为槲皮素,同时,上述碎片与芦丁分子丢失葡萄糖和鼠李糖所产生的碎片完全一致,结合相关文献[15],推断化合物6为芦丁,推测的质谱裂解路径见图4路径I。同理,推测化合物9以槲皮素为母核并连接了1分子半乳糖,推测化合物9为金丝桃苷。同理,推测化合物10以槲皮素为母核并连接了1分子木糖,推测化合物10为槲皮素-3-O-木糖苷,推测的质谱裂解路径见图4路径I。
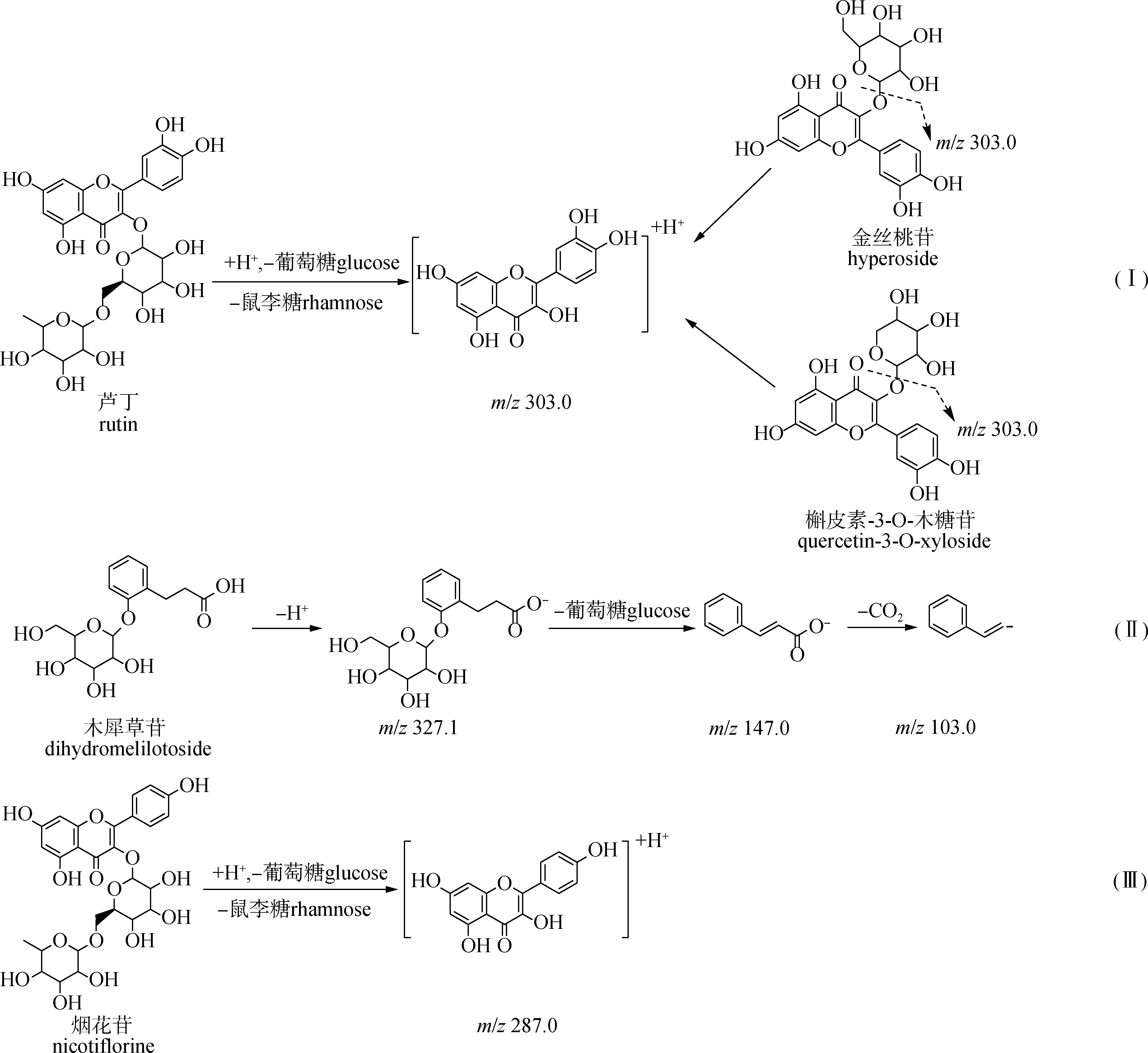
图4 糖苷类化合物质谱裂解路径
化合物7准分子离子峰是m/z327.1,加和离子为[M-H]-,通过软件计算其分子组成,推测该化合物分子式为C15H20O8,m/z147.0推测为准分子离子丢失1分子葡萄糖(C6H12O6,180 u)所产生,m/z103.0 推测为准分子离子丢失1分子葡萄糖后继续丢失1分子CO2(44 u)所产生,上述2种碎片与木犀草苷分子连续丢失葡萄糖和CO2所产生的碎片完全一致,结合相关文献[16],推断化合物7为木犀草苷,推测的质谱裂解路径见图4路径II。
化合物8准分子离子峰是m/z595.1,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C27H30O15,m/z287.0推测为准分子离子连续丢失1分子鼠李糖和1分子葡萄糖所产生,因此推测化合物8为双糖苷。m/z287.0碎片与化合物4、 5的分子离子峰相同,由于黄酮苷的糖基取代位点通常在B环的羟基,因此推测化合物8的母核为山柰酚,同时,上述碎片与烟花苷分子丢失葡萄糖和鼠李糖所产生的碎片完全一致,结合相关文献[17],推断化合物8为烟花苷,推测的质谱裂解路径见图4路径III。
2.2.4醇类化合物 化合物11准分子离子峰是m/z135.1,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C9H10O,m/z103.1推测为准分子离子连续丢失1分子H2O(18 u)和1分子CH2(14 u)所产生,上述碎片与肉桂醇分子连续丢失H2O和CH2所产生的碎片完全一致,结合相关文献[12],推断化合物11为肉桂醇,推测的质谱裂解路径见图5路径I。
化合物12准分子离子峰是m/z381.2,加和离子为[M-H]-,通过软件计算其分子组成,推测该化合物分子式为C20H30O7,m/z271.0推测为准分子离子丢失1分子C7H10O(110 u)所产生,m/z167.1推测为准分子离子丢失1分子C11H18O4(214 u)所产生,上述2种碎片与肉桂萜醇A分子在五碳环处断裂所产生的2种碎片完全一致,结合相关文献[17],推断化合物12为肉桂萜醇A,推测的质谱裂解路径见图5路径II。
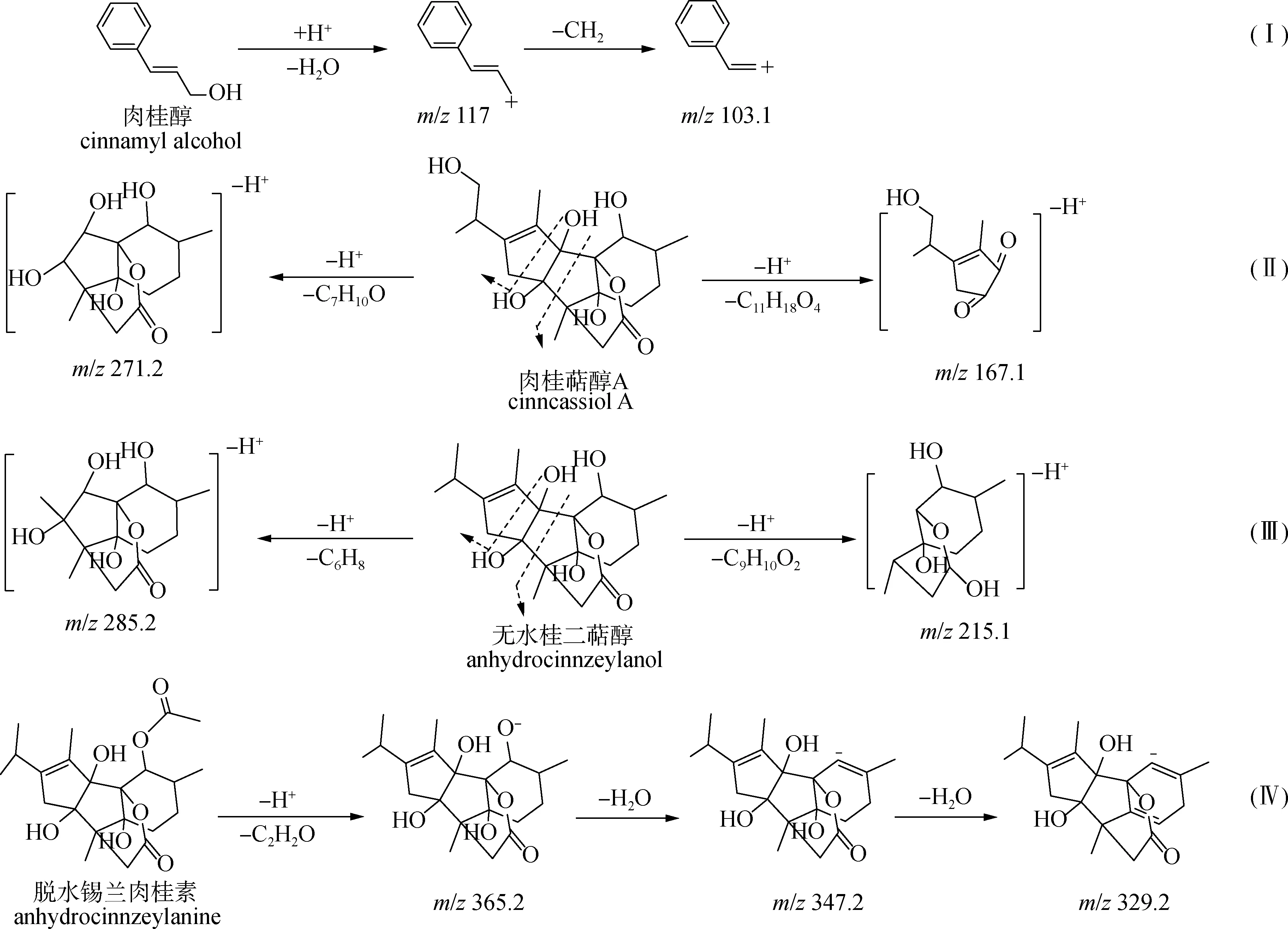
图5 醇类化合物质谱裂解路径
化合物13准分子离子峰是m/z365.2,加和离子为[M-H]-,通过软件计算其分子组成,推测该化合物分子式为C20H30O6,m/z285.2推测为准分子离子丢失1分子C6H8(80 u)所产生,m/z215.1推测为准分子离子丢失1分子C9H10O2(150 u)所产生,上述2种碎片与无水桂二萜醇分子在五碳环处断裂所产生的2种碎片完全一致,结合相关文献[18],推断化合物13为无水桂二萜醇,推测的质谱裂解路径见图5路径III。
化合物14准分子离子峰是m/z407.2,加和离子为[M-H]-,通过软件计算其分子组成,推测该化合物分子式为C22H32O7,m/z365.2推测为准分子离子丢失1分子C2H2O(42 u)所产生,m/z347.2推测为准分子离子丢失1分子C2H2O后脱H2O(18 u)所产生,m/z329.2推测为m/z347.2的碎片继续脱水所产生,m/z365.2的碎片从精确分子可以推测与化合物13的准分子离子峰一致,同时也检测到m/z215.1和m/z285.2的碎片,因此可以推测化合物14的化学结构与化合物13相似,结合相关文献[13],推断化合物14为脱水锡兰肉桂素,推测的质谱裂解路径见图5路径IV。
2.2.5醛类化合物 化合物15准分子离子峰是m/z179.1,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C10H10O3,m/z147.1推断为准分子离子丢失一个CH4O(32 u)所产生,m/z119.1推断为继续丢失一个CO(28 u)所产生,上述2种碎片与松柏醛分子丢失CH4O、CO所得碎片完全一致,结合相关文献[16],推断化合物15为松柏醛,推测的质谱裂解路径见图6中路径I,因为H+加和位点的不同,分别产生醛基的丢失或醚键的断裂。
化合物16准分子离子峰是m/z133.1,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C9H8O,m/z105.1推断为准分子离子丢失一个CO(28 u)所产生,该碎片与肉桂醛的醛基部位丢失CO所得碎片完全一致,结合相关文献[12],推断化合物16为肉桂醛,推测的质谱裂解路径见图6路径II。同理,结合相关文献,推断化合物17为邻甲氧基肉桂醛,推测的质谱裂解路径见图6路径III。

图6 醛类化合物质谱裂解路径
2.2.6酸类化合物 化合物18准分子离子峰是m/z167.0,加和离子为[M-H]-,通过软件计算其分子组成,推测该化合物分子式为C8H8O4,m/z137.0推断为准分子离子丢失一个CH2O(30 u)所产生,m/z108.0推断为准分子离子连续丢失CO2(44 u)和CH3(15 u)所产生,上述2种碎片与香草酸分子丢失CH2O、CO2、CH3所得碎片完全一致,结合相关文献[19],推断化合物18为香草酸,推测的质谱裂解路径见图7中路径I。
化合物19准分子离子峰是m/z153.0,加和离子为[M-H]-,通过软件计算其分子组成,推测该化合物分子式为C7H6O4,m/z109.0推断为准分子离子丢失一个CO2(44 u)所产生,该碎片与原儿茶酸分子的羧基部位丢失CO2所得碎片完全一致,结合相关文献[20],推断化合物19为原儿茶酸,推测的质谱裂解路径见图7中路径II。同理,结合相关文献,推断化合物22为咖啡酸(C9H8O4),推测的质谱裂解路径见图7中路径III。
化合物20准分子离子峰是m/z225.1,通过软件计算其分子组成,推测该化合物分子式为C11H12O5,加和离子为[M+H]+,m/z193.0推断为准分子离子丢失一个CH4O(32 u)所产生,m/z165.1推断为继续丢失一个CO(28 u)所产生,上述2种碎片与芥子酸分子丢失CH4O、CO所得碎片完全一致,结合相关文献[19],推断化合物20为芥子酸,推测的质谱裂解路径见图7中路径IV。

图7 酸类化合物质谱裂解路径
化合物21和化合物24准分子离子峰都是m/z163.0,加和离子为[M-H]-,通过软件计算其分子组成,推测该化合物分子式为C9H8O3,推断化合物21和24为同分异构体,且2个化合物碎片相同,m/z119.1推断为准分子离子丢失一个CO2(44 u)所产生,m/z117.0推断为继续丢失一个H2(2 u)所产生,上述2种碎片与香豆酸分子丢失CO2、H2所得碎片完全一致,结合相关文献[12],推断化合物21和24为香豆酸,结合相关文献可以推测肉桂的化学成分中通常包括对香豆酸和邻香豆酸,2个化合物由于苯环羟基的取代位置不同,导致化合物极性有差异,其中对香豆酸极性较强,在反相色谱中优先被洗脱出来,因此推测化合物21(保留时间9.90 min)为对香豆酸,化合物24(保留时间12.97 min)为邻香豆酸,推测的质谱裂解路径见图7路径V。
化合物23准分子离子峰是m/z355.1,通过软件计算其分子组成,推测该化合物分子式为C16H18O9,加和离子为[M+H]+,m/z193.0推断为准分子离子丢失一个咖啡酸(180 u)所产生,m/z163.0推断为准分子离子丢失一个奎宁酸(192 u)后继续丢失一个H2O(18 u)所产生,上述2种碎片与绿原酸酯键断裂所得碎片完全一致,结合相关文献[19],推断化合物23为绿原酸,推测的质谱裂解路径见图7路径VI。
化合物25准分子离子峰是m/z149.1,加和离子为[M+H]+,通过软件计算其分子组成,推测该化合物分子式为C9H8O2,m/z131.0推断为准分子离子丢失1个H2O(18 u)所产生,m/z103.1推断为准分子离子丢失一个H2O后继续丢失1个CO(28 u)所产生,上述碎片与肉桂酸在羧基位点连续丢失 H2O 和CO所得碎片完全一致,结合相关文献[12],推断化合物25为肉桂酸。推测的质谱裂解路径见图7路径VII。
化合物26准分子离子峰是m/z339.3,加和离子为[M-H]-,通过软件计算其分子组成,推测该化合物分子式为C22H44O2,m/z183.0推断为准分子离子丢失1个C11H24(156 u)所产生,上述碎片与山嵛酸在碳链中间断裂所得碎片完全一致,结合相关文献[12],推断化合物26为山嵛酸。推测的质谱裂解路径见图7路径VIII。
肉桂蒸油剩余物中酸类化合物的质谱行为研究表明: 1) 具有甲氧基的取代酸类化合物,如化合物18、 20,在正离子模式下容易丢失CH4O和CO,在负离子模式下容易丢失CH2O和CO2。2) 无甲氧基的取代酸类化合物,如化合物19、 21、 22、 23、 24,在正离子模式或负离子模式下容易直接丢失CO2或CO。
3 结 论
3.1本研究采用UHPLC-QTOF MS技术在肉桂蒸油剩余物中鉴定出26个化学成分,包括2个酚类成分,3个黄酮类成分,5个糖苷类成分,4个醇类成分,3个醛类成分和9个酸类成分。其中,多数肉桂黄酮类成分在治疗心血管疾病、糖尿病等方面具有一定的药用价值,在开发天然防腐剂、抗菌剂和抗氧化剂方面具有广阔的应用前景。肉桂醛、邻甲氧基肉桂醛等少数化合物属于肉桂油的成分,但高温蒸油环境增加了其在水中的溶解度,因此在肉桂蒸油剩余物中被高灵敏度的质谱检测器检出。
3.2肉桂蒸油剩余物中种类最丰富的为酸类成分,并且以酚酸类化合物为主。有甲氧基取代的酚酸类化合物在正离子模式下容易丢失CH4O和CO,从而产生32 u和28 u的中性丢失,在负离子模式下容易丢失CH2O和CO2,从而产生30 u和44 u的特征性中性丢失。无甲氧基取代的酚酸类化合物则容易直接丢失CO2或CO。
3.3肉桂蒸油剩余物中黄酮类化合物数量仅次于酸类,包括槲皮素、山柰酚和木犀草素和4个黄酮苷,结构区别在于A/B环上的羟基位置或数量不同,在正离子模式下都可以通过RDA反应产生m/z153的特征碎片。
