乳粉中大肠菌群测定能力验证的结果与分析
2020-12-26袁晓丽杨延峰清远市食品检验中心
□ 袁晓丽 杨延峰 清远市食品检验中心
大肠菌群指的是具有某些特性的一组与粪便污染有关的细菌,包括大肠杆菌、产气克雷伯氏菌和阴沟肠杆菌等。食品中检出大肠菌群,表明食品受到人和温血动物的粪便污染,其中典型大肠杆菌为粪便近期污染。大肠菌群在结晶紫中性红胆盐琼脂(VRBA)培养基上呈现出直径为0.5 mm 或者更大的紫红色菌落特征,并且菌落周围有红色的胆盐沉淀环。该典型菌落在煌绿乳糖胆盐(BGLB)肉汤管中37 ℃条件下培养能够产气[1]。因此,实验室一般采用VRBA 平板初筛,并通过BGLB 肉汤验证方式检测食品中是否存大肠菌群。
能力验证是指利用实验室之间的比对,按照预先制定的准则来评价实验室的检测能力的活动。通过参加能力验证活动,不仅可以对实验室进行质量控制、完善实验室的管理制度,而且可以评判实验室相关项目检测人员的检验技术水平是否维持在正常的水平,从而确保日常检验报告检测数据的准确性和可信性[2]。2019 年,本实验室参加了由国家食品药品监督管理总局组织,中国食品药品检定研究院提供样品的乳粉中大肠菌群的计数检验能力验证活动,通过分析和总结此次能力验证的实验结果,为日常的微生物检验工作提供技术支持。
1 材料与方法
1.1 培养基及试剂
结晶紫中性红胆盐琼脂(VRBA):批号1072991,厂家:广东环凯;煌绿乳糖胆盐(BGLB)肉汤:批号1066081,厂家:广东环凯;氯化钠:批号20180504—2,厂家:广州广试。大肠杆菌:菌株编号 ATCC25922,来源:广东环凯;弗氏柠檬酸杆菌:菌株编号ATCC43864,来源:广东环凯;所有培养基和试剂均在有效期内,并通过验收验证。
1.2 仪器散设备
全自动蒸汽灭菌器(型号:GI54DS厂家:厦门致微);电热恒温培养箱(型号:HKP—9172A,厂家:广东环凯);生物安全柜(型号:BSC—1600IIA2,厂家:苏净安泰);电热恒温干燥箱(型号:DHG—9123A,厂家:广东环凯);电热恒温水浴锅(型号:DKZ—3B 厂家:上海一恒)。
1.3 测试样品
样品1:来源于中国食品药品检定研究院的乳粉中大肠菌群计数的能力验证样品,编号TF2240147。
样品2:来源于中国食品药品检定研究院的乳粉中大肠菌群计数的能力验证样品,编号TF2240052。
1.4 检验方法
按照中国食品药品检定研究院下发的NIFDC—PT—224《乳粉中大肠菌群计数作业指导书》和国家标准GB 4789.3—2016《食品安全国家标准食品微生物学检验 大肠菌群计数》的要求进行实验。
1.5 大肠菌群平板计数的报告
1.5.1 大肠菌群数的计算
经证实实验确定,大肠菌群阳性的试管比例乘以VRBA 平板上计数的典型菌落数,再乘以稀释倍数,即为每1 g 样品中的大肠菌群数[3]。
1.5.2 z 值的计算
样品的测试结果采用“z-比分数”评价,z—比分数计算公式如式(1)所示。
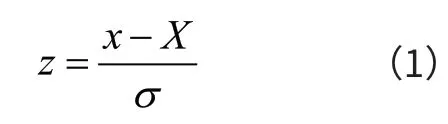
式(1)中:x-测试人所提供的测试结果;X-指定值/对数值(即中位值);σ-标准差(样品的标准化四分位间距)。
当|z|≤2 时,结果判定为“满意”;当2 <|z|<3 时,结果判定为“可疑”;当|z|≥3 时,结果判定为“不满意”。
2 结果与分析
2.1 VRBA 平板观察和计数
选取菌落数在15 ~150 的平板,分别计数平板上出现的典型和可疑大肠菌群菌落(如菌落直径较典型菌落小)。典型菌落为紫红色,菌落周围有红色的胆盐沉淀环,菌落直径为0.5 mm,或更大[3]。
样 品CODE147、CODE052 及 空白对照在VRBA 平板上的计数结果见表1。其中,空白对照平板上均无菌落生长;样品TF2240147 在10—1和10—2稀释度的平板上形成了可计数的分散的 单 一 菌 落,而 在10—3、10—4、10—5稀释度的平板上均无菌落生长;样品TF2240052 在10—2和10—3稀释度的平板上形成了可计数的分散的单一菌落形态,在10—1稀释度平板上菌落数量较多无法计数,而在10—4和10—5稀释度均无菌落生长。

表1 VRBA 平板计数结果(cfu/g)
样 品CODE052 和CODE147 不 同稀释度在VRBA 平板上的菌落形态,如图1 所示。为了防止表面有迁徙性细菌蔓延生长,并确保菌落在VRBA 平板上能形成可计数的单一散落的菌落,在第一次倾注VRBA 培养基后,应小心水平晃动平皿,使得培养基与待测样液充分混匀,待琼脂凝固之后,再加入3 ~4 mL VRBA 覆盖平板表层即可。VRBA 培养基的制备,不需要121 ℃高温灭菌,只需微波煮沸使其中的琼脂充分溶解即可,长时间的高温会使结晶紫中性红胆盐琼脂中的抑制其它其他菌生长的抑制物成分降解,从而使其选择性降低。
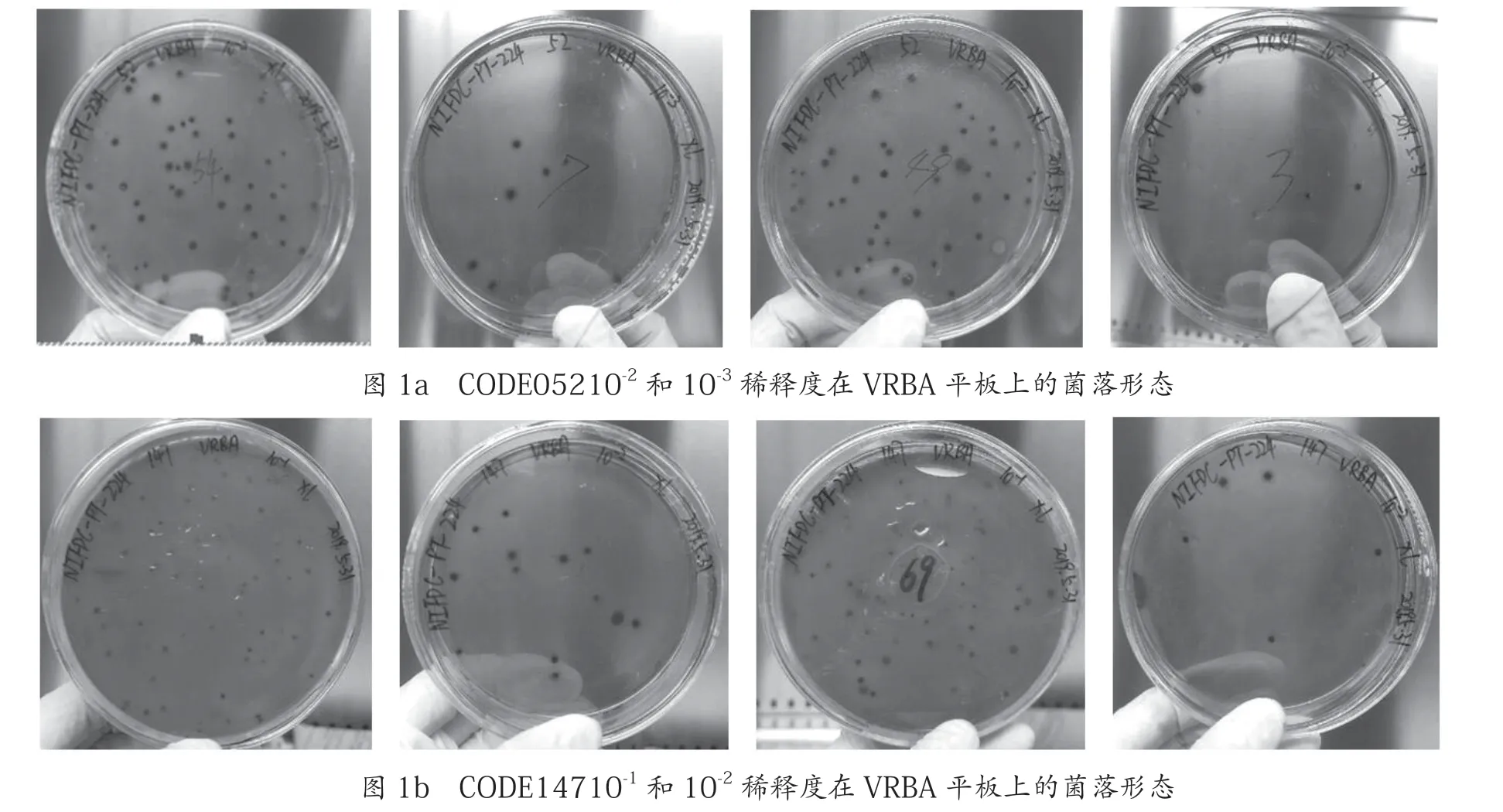
图1 样品在VRBA 平板上的菌落形态
2.2 特征菌落的确证性实验
为了确保确证性实验结果的准确性,BGLB 肉汤在接种前,要首先确定玻璃小导管内是否有气泡,经常会由于过早打开灭菌锅、试管塞塞的太紧或者小导管口太小等,使得小导管内气体未充分排出,如果直接使用其进行后续验证实验,则会得出假阳性结果。本实验之前,均已检查未有上述情况。
样 品CODE147:从10—1稀 释 度VRBA 平板上挑取10 个不同的类型的典型和可疑菌落,移种于BGLB 肉汤管中,(36±1)℃培养24 ~48 h,观察产气情况。凡BGLB 肉汤管产气,即可报告为大肠菌群阳性[3]。
样 品CODE052:从10—2稀 释 度VRBA 平板上挑取10 个菌落,其他同样品CODE147。
由表2、3 可知,挑取10 个样品CODE147 和CODE052 在VRBA 平 板上的特征菌落接种到BGLB 肉汤管中培养之后均产生气泡,说明平板上的所有典型和可疑菌落均确证为大肠菌群阳性。样品CODE147 的报送结果为700 CFU/g,样品CODE052 的报送结果为5 200 CFU/g。
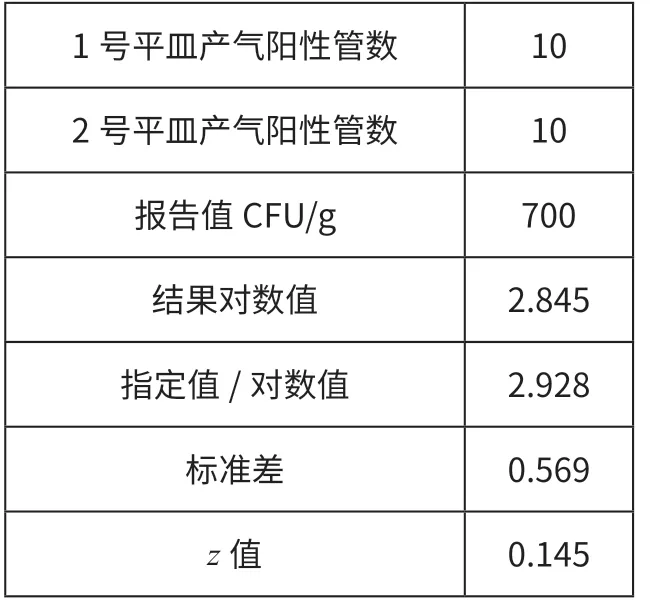
表2 样品CODE147 的特征菌落证实实验结果
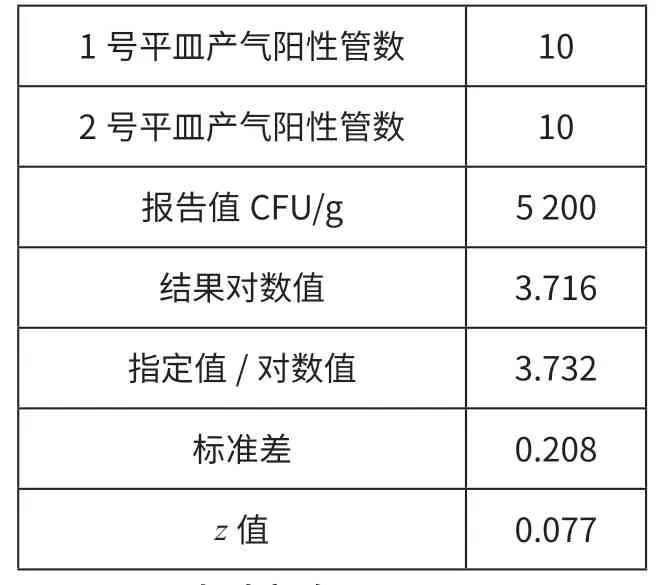
表3 样品CODE047 的特征菌落证实实验结果
2.3 人员比对实验
由表1 中的数据计算可知,CODE147 实验员A 和实验员B 比对的结果平均值相对偏差为11.3%,CODE052 人员比对的结果平均值相对偏差为16.7%。人员比对结果偏差较大,最终以实验员A 的结果上报。主要是由于实验员B 在稀释取样的过程中,没有充分混匀样品,正确操作为先用量器反复吹吸样液2 次,再吸取1 mL 样液于平皿中或9 mL 生理盐水中进一步稀释。
2.4 实验结果的确定与评价
本次能力验证共有51 家实验室报名参加,其中5 家实验室结果不满意,3 家实验室结果可疑。本实验室CODE147 大肠菌群的测定结果为700 CFU/g,z 值为0.145;CODE052大肠菌群的测定结果为5 200 CFU/g,z 值为0.077;两个样品的结果评价均为满意(具体见图2 ~3)。
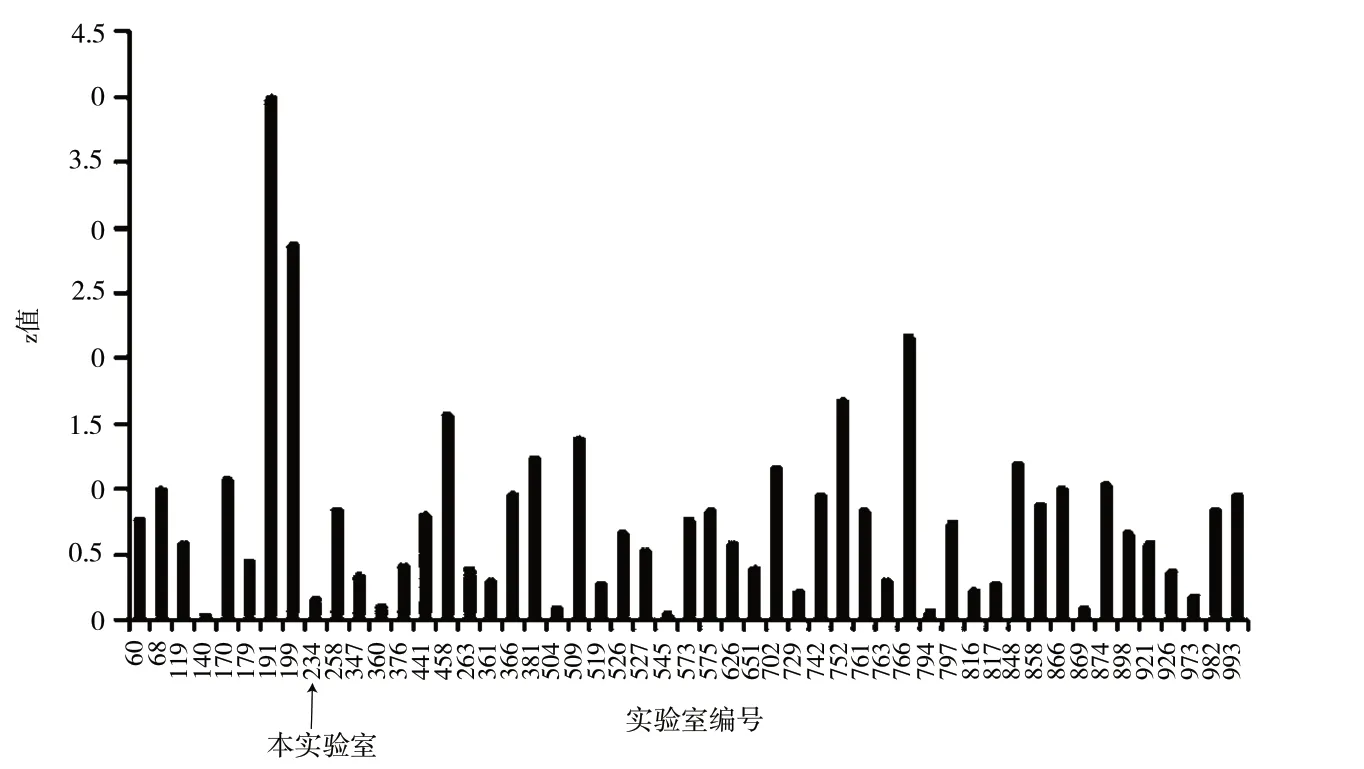
图2 TF2240147 中大肠菌群z 值柱状分析图
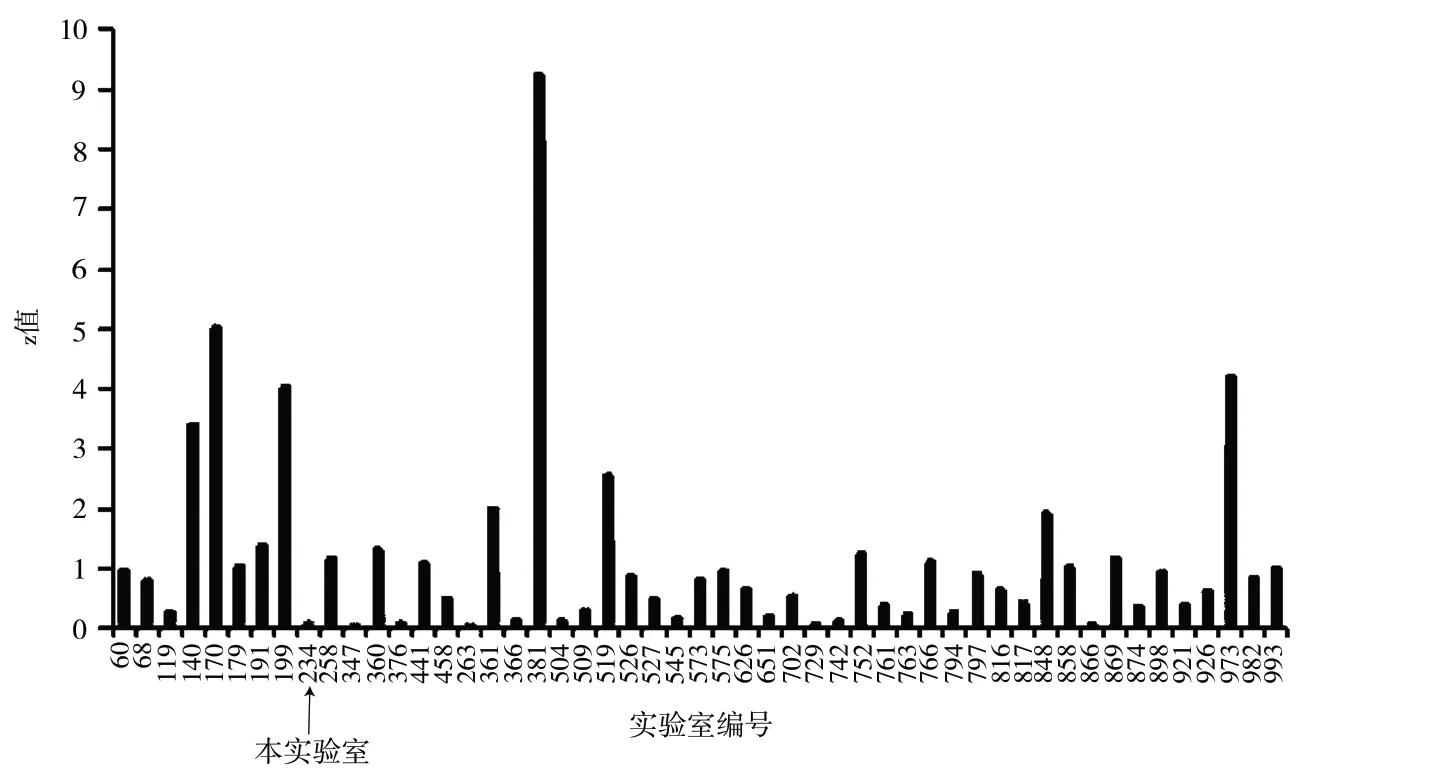
图3 TF2240052 中大肠菌群z 值柱状分析图
3 结果与讨论
本实验室参加了国家食品药品监督管理总局组织,由中国食品药品检定研究院提供样品的乳粉中大肠菌群的计数检验能力验证,依据能力验证的作业指导书及GB 4789.3—2016 对样品进行检测,两个样品中大肠菌群的计数结果均为满意。说明本实验室具备检测大肠菌群的能力。
本实验室采用多个稀释度、平行样、人员比对和阴/阳性菌株对照的手段,为样品中大肠菌群确证和计数的准确性提供强力保障。今后,还可加入质控样品实验,以对实验结果进行进一步的验证,使检验结果更加准确。
