次氯酸钠脱色考马斯亮蓝G-250废液的优化研究
2020-12-22刘海平吴玉芬吴梁莹张敬虎张国广
刘海平,吴玉芬,吴梁莹,张敬虎,张国广*
(1.闽南师范大学生物科学与技术学院,福建漳州363000;2.闽台特色园林植物福建省重点实验室,福建漳州363000)
目前人们对良好生态环境的要求越来越高,食品工业生产单位都加大了对排放三废的治理.学校实验室是教学单位开展教学和研究工作的重要场所,在教学实验开展过程中也面临着三废的处理问题.在生物学和食品相关实验中,使用考马斯亮蓝G-250(后文简称G-250)对蛋白质进行定量测定是一种适用广泛的经典实验方法.G-250测试溶液主要是由考马斯亮蓝G-250,乙醇,85%(W/V)的磷酸和蒸馏水配置而成[1],实验后产生的废液色度大,pH值低,若直接排放将对环境产生不利影响.
次氯酸钠是弱酸盐,分子式NaClO,分子量74.44,室温呈现无色或淡黄色的液体,有类似氯气的刺激性气味,其溶液属于一种复杂不稳定的化学系统.次氯酸钠作为一种强烈的氧化剂,可以破坏有机色素基团,从而使有色物褪色,因此被应用到一些有色废液的脱色处理中[2-4],但尚未有次氯酸钠对实验室G-250废液的脱色研究报道.本研究拟优化次氯酸钠对G-250废液脱色处理条件,为该废液的无害化处理提供参考.
1 材料与方法
1.1 材料、仪器和药品
材料:G-250废液是动物营养、生物科学、园艺等专业进行生物化学实验教学中产生的废液,该方法按照文献[1]考马斯亮蓝结合法测定蛋白质浓度的步骤开展,教学实验产生的废液按照要求进行单独收集.
仪器:TP-114电子天平丹佛仪器;STARTER 3100 pH计奥豪斯仪器;T9紫外可见分光光度计普析通用;TGL-16台式高速离心机湘仪仪器.
药品:考马斯亮蓝G-250(A.R)、95%乙醇(A.R)、85%(W/V)磷酸(A.R)、牛血清白蛋白、硫酸亚铁(A.R)、30%H2O2(A.R)、NaOH(A.R)、高铁酸钾(A.R)等购自国药集团化学试剂有限公司.次氯酸钠溶液 次氯酸钠含量(以有效氯计算)≧8.0%购自西陇化工股份有限公司.
1.2 实验方法
在预实验的基础上探讨次氯酸钠溶液投加量、脱色反应时间和pH 对G-250 废液脱色的影响,同时测定了G-250光谱、G-250结合蛋白后光谱.
1.2.1 NaClO溶液的投加量对G-250废液降解效果的影响
在室温条件下,取5 支试管,分别加入10 mL 的G-250 废液,再每支试管分别依次加入5、7.5、10、12.5、15 μL 的次氯酸钠溶液,震荡摇匀.脱色反应10 min 后,离心,依次测定并记录反应后溶液的OD 值,计算脱色率.
1.2.2 不同pH值对G-250废液降解效果的影响
在室温条件下,取若干G-250废液测定原始溶液的pH值,取5支试管,分别加入10 mL的G-250废液,其它反应条件保持一致,分别调节废液的pH值为2、3、4、5、6,再依次加入7.5 μL的次氯酸钠溶液,震荡摇匀.反应10 min后,离心,依次测定并记录反应后溶液的OD值,计算脱色率.
1.2.3 反应时间对次氯酸钠溶液降解效果的影响
在室温条件下,调节G-250废液pH为4,取5支试管,分别加入10 mL的pH为4的G-250废液,再分别加入7.5 μL 的次氯酸钠溶液,震荡摇匀.分别反应5、10、15、20、25 min 后,离心,依次测定并记录反应后溶液的OD值.计算脱色率.
1.2.4 脱色率的计算
次氯酸钠的氧化降解G-250 废液效果主要以脱色率大小体现.脱色率=(A0−A)/A0×100%,式中:A0—废液处理前的吸光度;A—废液处理后的吸光度.
1.2.5 响应面实验设计
在单因素实验基础上,把G-250 废液的脱色率作为响应值,根据Box-Behnken 实验的设计原理,应用Design Expert 8.0 软件设计三因素三水平响应面实验,检验NaClO 溶液的投加量、脱色反应时间、pH 及因素间交互作用对G-250废液的脱色率的影响,以+1,0,−1分别代表自变量的高、中、低水平,见表1.
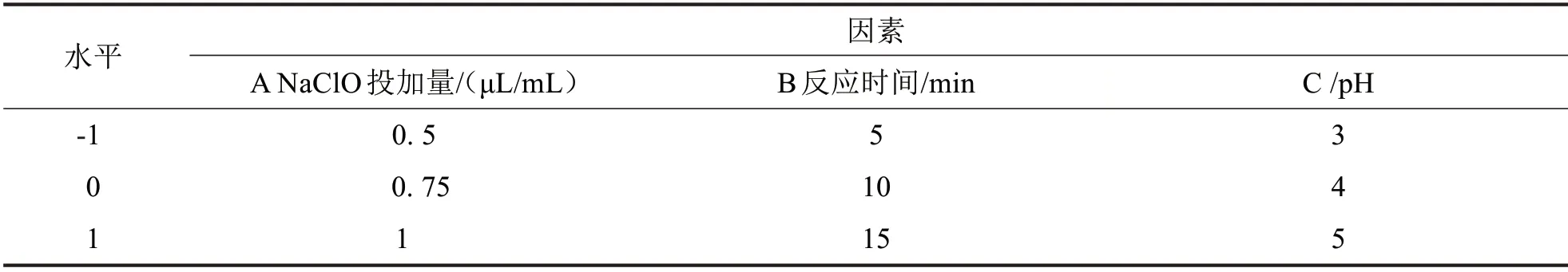
表1 响应面分析因素水平表Tab.1 Level table of response surface analysis factor
1.3 次氯酸钠降解G-250废液的原理
紫外可见光光谱:使用紫外可见光分光光度计扫描用次氯酸钠脱色过的G-250废液,在次氯酸钠脱色过的废液中按照体积比10︰1的比例加入5%的高铁酸钾,振荡30 min后再次扫描记录光谱变化.
2 结果与分析
2.1 G-250及其结合蛋白质后的光谱
图1中曲线1和2分别表示在200~800 nm之间,G-250和G-250与蛋白质结合后的光谱.在可见光区域内,G-250 在465 nm 和650 nm 处有两个波峰,G-250 与蛋白质结合之后,在640 nm 处有最大吸收峰值,但此处在G-250 第二个波峰的附近,为了尽可能减少G-250 自身的干扰,蛋白质浓度测定时选取595 nm,此波长处G-250自身吸光值处于一个低点,G-250结合蛋白质后的吸光值处于相对的高峰,尽可能的降低了游离G-250的干扰,光谱扫描结果和文献[5]相符合.
2.2 单因素实验结果
2.2.1 NaClO溶液的投加量对G-250废液脱色效果的影响
本实验结果(图2)表明:NaClO 溶液的投加量对G-250废液脱色率有较大影响,随着NaClO 溶液的投加量的增加,G-250 废液脱色率逐渐升高.当投加量大于10μ L 后废液脱色率逐渐趋于平缓.当NaClO 溶液的投加量为7.5μL 时的脱色率已高达93.11%,废液几乎变为无色.在后面的单因素试验中,NaClO 溶液的投加量均取7.5μL.
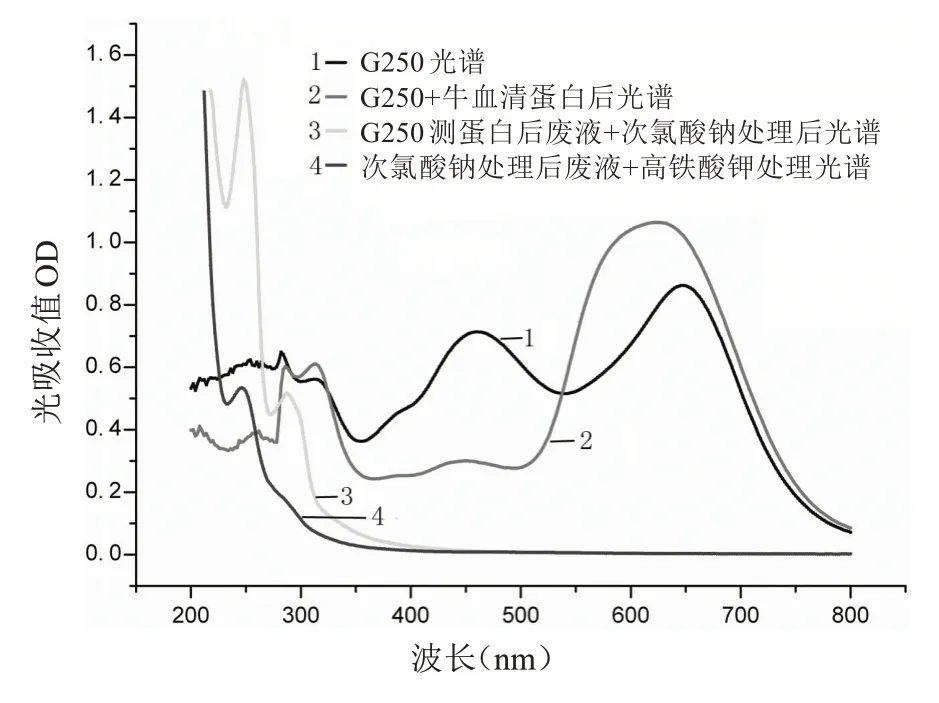
图1 G250、G250 结合蛋白、次氯酸钠处理G250 废液和处理后废液加入高铁酸钾处理后光谱图Fig.1 Spectra of G250, G250 binding protein, sodium hypochlorite treatment G250 waste liquid and discolored waste liquid added with potassium ferrate
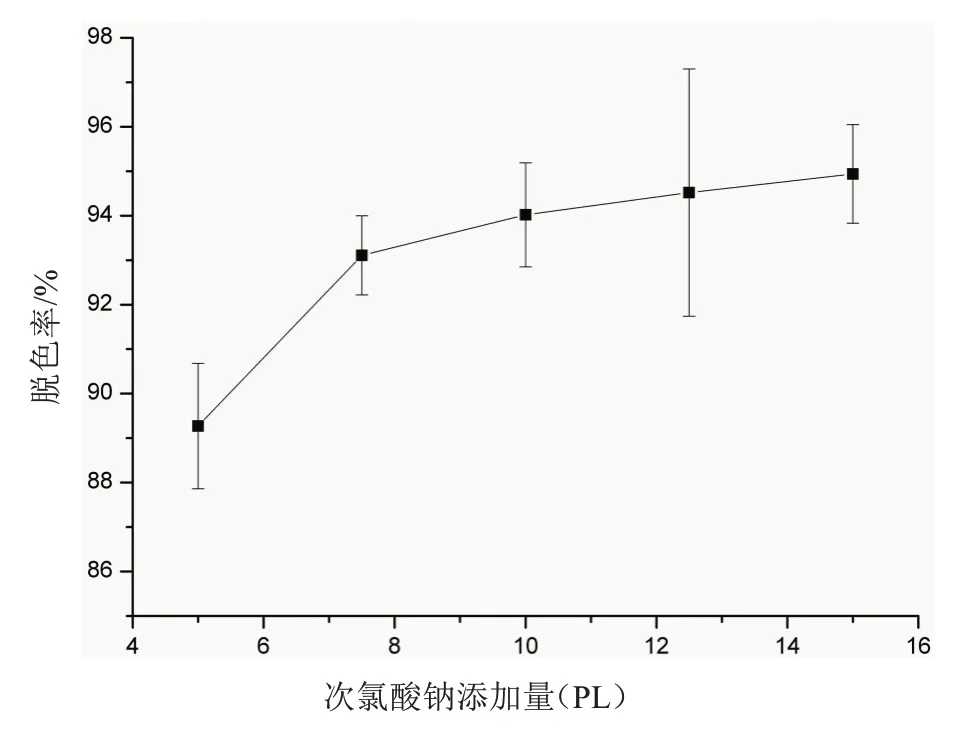
图2 NaClO的投加量对G-250废液脱色效果的影响Fig.2 Effect of dosage of NaClO on decolorization of G-250 waste liquid
2.2.2 不同pH对G-250废液脱色效果的影响
G-250 废液pH 值约在1~2 之间,但不同批次收集的废液因实验过程中清洗比色皿等原因,其pH 有所波动.脱色处理结果表明,pH 对次氯酸钠脱色有较大影响(图3),在pH 为4 时,脱色率最佳,可达97.48%.其原因可能在于:pH为4时,NaClO主要以HClO形态存在,而HClO放出的新生氧具有很强的氧化作用;pH大于4时,主要以NaCIO形态存在,二种分子氧化能力不同[2].考虑到处理完的废液,pH要调到中性才能排放,故pH选取4比较合适.
2.2.3 脱色反应时间对次氯酸钠废液脱色效果的影响
本组实验结果(图4)表明:随着反应时间的增加,G-250 废液脱色率逐渐增加,反应时间为10 min 时的脱色率可以达到80.21%.
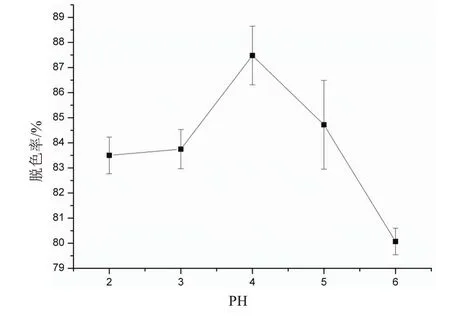
图3 pH对G-250废液脱色效果的影响Fig.3 Effect of pH on the decolorization effect of G-250 waste liquid
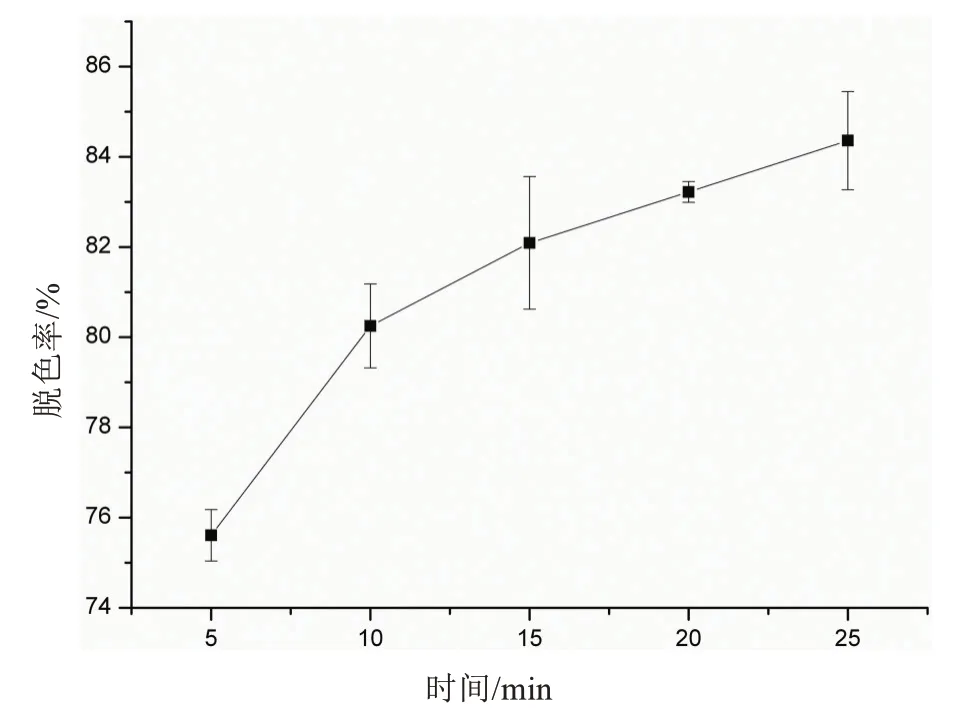
图4 反应时间对G-250废液脱色效果的影响Fig.4 Effect of reaction time on the decolorization of G-250 waste liquid
2.3 响应面优化G-250废液脱色率的结果
2.3.1 回归模型的建立与分析
在单因素实验的基础上,将NaClO 溶液的投加量、反应时间、pH 值进行三因素与三水平中心组合实验,利用Box-Benhnken 中心组合实验的设计原理,应用响应面优化G-250 废液脱色、设计,进行17 次试验,其中析因试验共计12 次,中心组合试验共计5 次重复.实验设计方案与结果见表2,相应的方差分析数据见表3.
应用Design-Expert 8.0 软件对表2中的数据进行二次多项式回归拟合,得到回归方程:Y=85.80+4.87A+2.06B −2.20C+3.37AB+3.24AC+2.36BC −3.25A2−2.97B2−2.19C2.根据表3的方差分析可以得出,该模型极显著(p<0.01),预测值和试验值有相关性;失拟项不显著(p=0.601 3>0.05),表明残差均由随机误差所引起,该模型对G-250废液脱色率实际值与预测值有很好的拟合度,可以利用该模型对G-250 废液脱色率进行较好地分析、预测及确定G-250 废液脱色率最佳的反应条件.从表3还可以看出:3个因素对G-250废液脱色率有显著影响.而由相应pH 值可看见,对G-250废液脱色率影响的大小顺序为:次氯酸钠投加量>pH>反应时间.
2.3.2 G-250废液脱色率响应面分析与优化
响应曲面反映了氯酸钠投加量、脱色反应时间和pH 三个因素中的其中一个变量取零点水平时,另外两个因素交互作用对G-250 废液脱色率的影响情况(图5—7).曲面陡表示该因素对脱色率的影响显著,曲面平缓表示该因素对脱色率的影响不显著[6-7];等高线形状则反映两因素交互作用的强弱,椭圆形表示交互作用强,影响显著,圆形则相反[6-7];等高线密集表示对脱色率影响较大,稀疏表示影响较小[6-7].从图中可看出次氯酸钠投加量比pH、反应时间的曲线陡峭,说明次氯酸钠投加量对G-250 废液脱色率的影响最大;三组三维图的投影(即等高线)呈椭圆状,表明两因素的交互作用对脱色率的影响显著,同回归方差分析的结果(表3)一致.
2.3.3 最佳工艺的预测与验证
应用Design-expert 8.0软件的optimization功能,把G-250废液脱色率的目标选项设定成maximize,取得一个最优的方案:10 mL的G-250废液体系中次氯酸钠投加量10 μL、反应时间15 min、pH 为4.78,此时的理论脱色率达91.19%.考虑到实际操作的便利,将优化方案设置为:次氯酸钠投加量10 μL,反应时间15 min,pH为5,进行了五次验证试验所得的G-250废液脱色平均得率为92.55%,与预测值之间的相对偏差为1.36%,表明用响应面法对G-250废液脱色的3个因素进行优化研究是可行的.
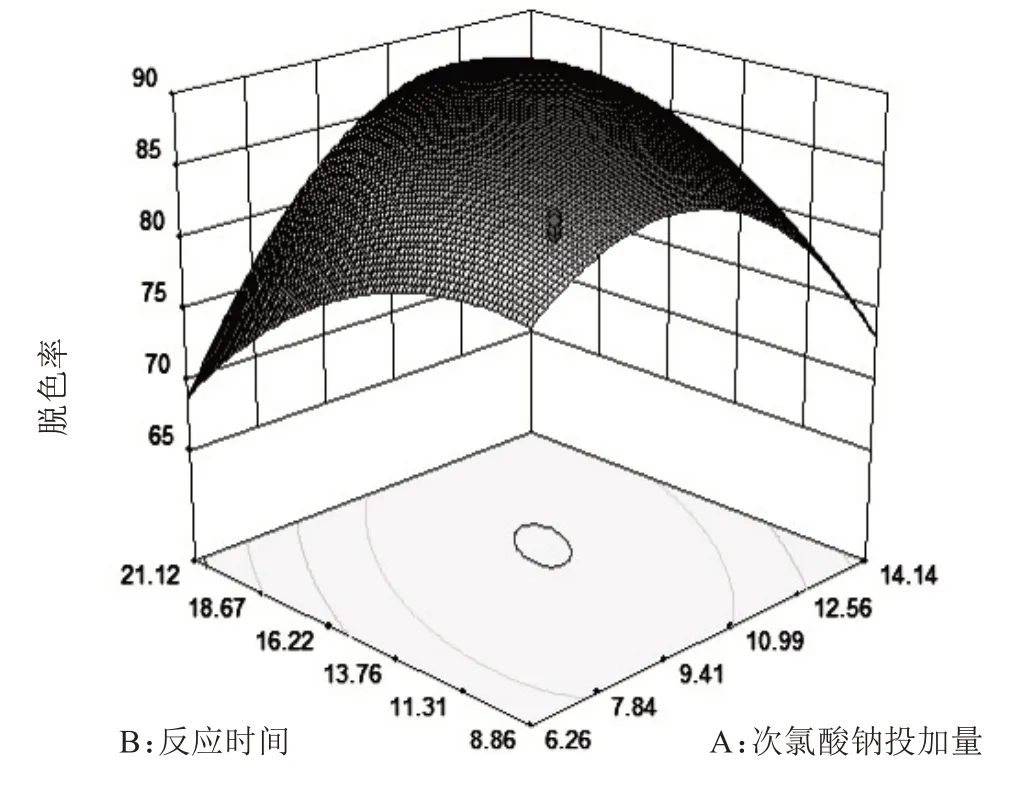
图5 反应时间与次氯酸钠投加量交互作用响应面Fig.5 Response surface of interaction between reaction time and sodium hypochlorite dosage
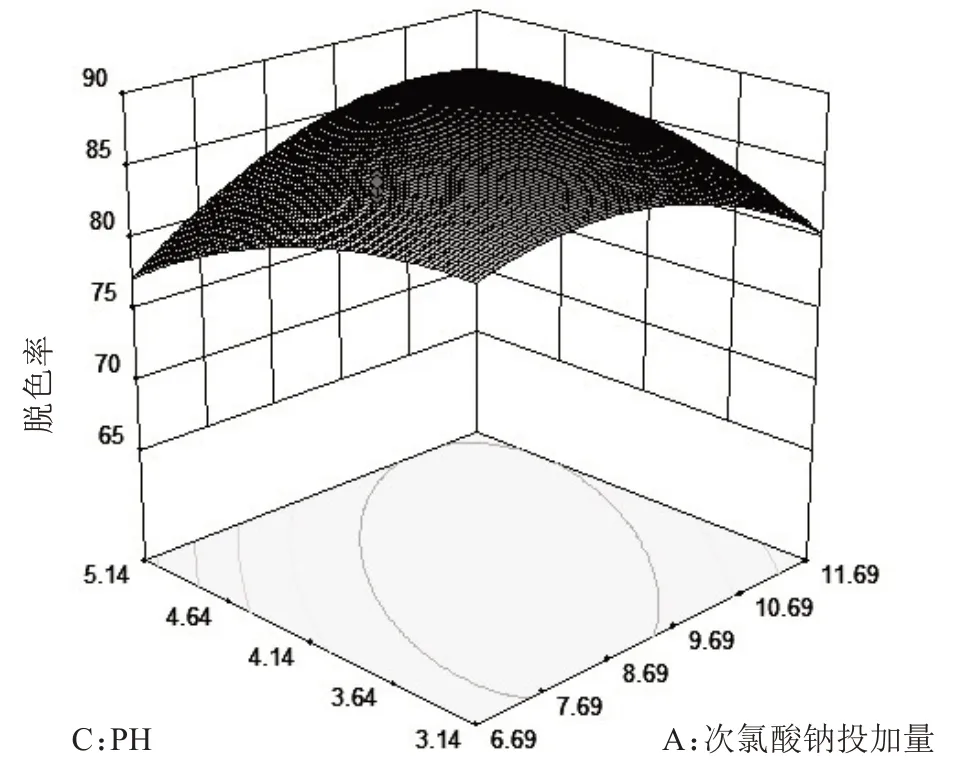
图6 pH与次氯酸钠投加量交互作用响应面Fig.6 Response surface of interaction between pH of solution and sodium hypochlorite dosage
2.4 次氯酸钠氧化褪色G-250废液的原理
G-250 废液被次氯酸钠溶液氧化脱色后扫描到的光谱(图1线3)表明,在400~800 nm 的可见光区域内,没有吸收峰的出现,因此次氯酸钠法可以使G-250 废液脱色.在紫外区240 nm 和290 nm 处分别出现了光吸收峰,240 nm处的光吸收波峰出现,说明溶液中有苯环结构存在,290 nm处的波峰说明化合物具有较大的共轭体系[8].观察用高铁酸钾处理脱色后的废液测得的光谱图(图1线4)在290 nm 处的波峰消失,且240 nm处的光吸收值也大大降低,因为高铁酸钾可以使苯环开环,生成的产物主要有顺丁烯二酸、反丁烯二酸、草酸和甲酸[9-11],这些小分子化合物在240 nm处几乎没有光吸收.
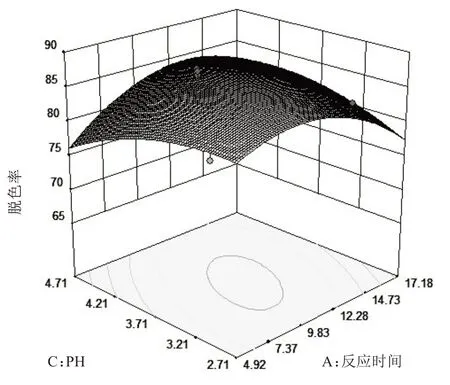
图7 pH与反应时间交互作用响应面Fig.7 Response surface of interaction between pH of solution and reaction time
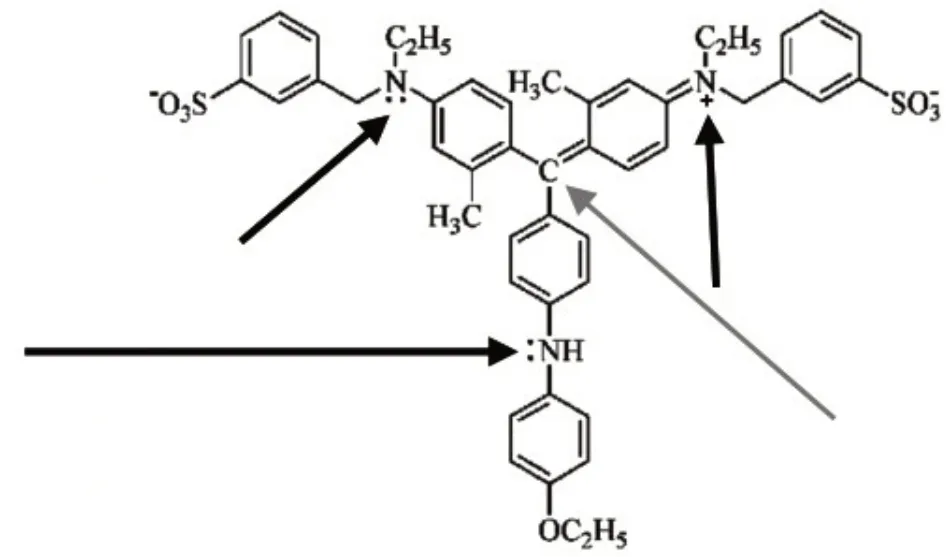
图8 G-250结构图及其可能被降解化学键示意图Fig.8 G-250 structure diagram and its possible degradation of chemical bonds
由以上分析推测次氯酸钠优先攻击考马斯亮蓝G-250 分子结构[12]中的三个带电N 原子处(图8较粗的黑色箭头所示),作为氧化剂,带电子的N 原子处是最容易因失去电子而被氧化的,从而化学键被打断,也应该能够攻击核心的C 原子(图8较细绿色箭头所指)和三个苯环结构形成的共价键,主要生成一些游离的带苯环结构的分子和部分仍然连接在核心C 原子上的三个苯环的大的共轭结构分子,因此在光谱扫描中在240 nm和290 nm处有2个吸收波峰存在.用高铁酸钾处理后290 nm处的吸光值消失,表明高铁酸钾不但能够打开单个游离的苯环结构,也能够氧化断裂与核心C 原子连接的3个共价键(图8较细箭头所指),使原来具有较大共轭结构的大分子变成游离的单苯环结构的分子,从而导致处理后废液的290 nm处的吸收峰消失.
因此G-250 废液在次氯酸钠的氧化下,色素分子分解生成了游离的含苯环的分子,这样考马斯亮蓝G-250的结构被破坏,从而达到脱色的目的.但脱色的废液中还富含具有苯环结构的分子,该脱色后废液是否具有生物毒性还需要进一步探究.
3 结论
次氯酸钠法氧化降解G-250 废液具有脱色效果好,操作经济简单等优点.根据单因素实验及响应曲面分析优化的反应条件,结合实际操作确定氧化降解G-250废液的最佳条件为:10 mL的废液体系中次氯酸钠投加量为10 μL,反应时间为15 min,pH 为5,此时的脱色率最高,结果可为考马斯亮蓝G-250 废液的脱色提供参考依据.经光谱扫描后可知脱色后的废液仍然具有大量含苯环结构的化合物分子,还需要进一步的无害化处理.
