基于母亲孕前肥胖与子代注意缺陷多动障碍风险队列研究的Meta分析
2020-12-16石奇琪
王 冉 石奇琪 贾 兵
注意缺陷多动障碍(ADHD)是儿童期最为常见的神经、行为障碍,主要临床表现是与发育水平不相符的注意力不集中,不分场合的过度活动和情绪冲动,伴有学习困难和品行障碍,临床上分为注意缺陷型、多动/冲动型和混合型。流行病学调查研究显示全球儿童青少年ADHD总患病率为2%~7%(平均约5%)[1]。Meta分析显示我国儿童青少年ADHD总患病率为6.3%,且患病率从20世纪90年代的5.5%上升至6.7%[2]。近年前瞻性队列研究表明,母亲孕前体重过大,其子代发生ADHD、孤独症谱系障碍(ASD)、认知障碍等神经发育障碍的风险增加[3,4],但尚缺乏相关的系统评价。本文通过系统文献检索和Meta分析,探讨母亲孕前体重状态与子代发生ADHD的关联。
1 方法
1.1 文献纳入标准 ①母亲孕前超重/肥胖子代发生ADHD的队列研究;②暴露因素为研究者不施以任何有意识地降低和控制体重的措施下的母亲孕前体重状态;③体重状态以BMI作为定义,不同研究的超重、肥胖的BMI判断标准可能不同是被接受的;④结局变量为子代ADHD,文献中给出明确的ADHD诊断标准和随访时间,且不存在ASD、抑郁症等其他精神心理疾病的伴随诊断;⑤文献中能提取和导出ADHD与暴露因素效应量,或比值比(OR)或相对危险度(RR)或风险比(HR)及其95% CI;⑥语种为中文和英文。
1.2 文献排除标准 ①数据库中重复发表的文献,以最后发表的文献为准;②不能获取全文;③会议论文;④ADHD治疗或干预的临床研究;⑤暴露因素BMI为连续变量,不能做出超重、肥胖BMI的判断截断值;⑥述评和综述。
1.3 文献检索策略
1.3.1 检索数据库和起止时间 计算机检索,中文数据库(中国知网数据库、万方数据库、中国生物医学文献数据库),英文数据库(PubMed、Embase、Cochrane)。均从建库到2020年2月11日。
1.3.2 检索词和检索式 以CBM为例。(1) "孕期" OR "妊娠期";(2) "肥胖"OR "超重" OR "体重" ;(3) "子代" OR "后代" OR "子女";(4) "注意缺陷障碍" OR "多动症" ;(5) #4 AND #3 AND #2 AND #1。
以Embase为例。ADHD OR adhd OR attention deficit disorder with hyperactivity OR syndrome hyperkinetic OR hyperkinetic syndrome OR hyperactivity disorder OR hyperactive child syndrome OR childhood hyperkinetic syndrome OR attention deficit hyperactivity disorders OR attention deficit hyperactivity disorder OR attention deficit hyperactivity disorder OR addh OR overactive child syndrome OR attention deficit hyperkinetic disorder OR hyperkinetic disorder OR attention deficit disorder hyperactivity OR child attention deficit disorder OR hyperkinetic syndromes OR syndromes hyperkinetic OR hyperkinetic syndrome childhood AND weight/obesity/overweight/underweight/obese/body mass index/BMI/body size AND maternal/ mother/prenatal/perinatal/pregnancy/prepregnancy。
1.4 文献筛选 由共同第一作者分别按照初筛和全文筛选标准独立筛选文献,如有争议,讨论协商统一。Endnote软件去除重复文献。初筛阅读文献题目和摘要,排除述评、会议论文、动物实验文献、与主题无关综述、与主题明显不相关的文献。全文筛选,排除会议论文、不能提取母亲孕前BMI或其子代ADHD评价数据的文献。阅读与主题相关综述,追溯其后参考文献。基于同一人群不同研究阶段的文献,取队列病例数较大的文献。
1.5 资料提取 由共同第一作者采用事先设计的资料提取表分别提取如下信息,如有争议,讨论协商统一。提取作者、出版年份、研究类型、随访年龄、队列人数,病例数、暴露因素判断标准、结局指标判断标准、效应指标(HR或OR或RR及其95%CI)。如果同一文献采用不同的ADHD诊断量表,每个诊断量表视为单纯提取项。同一文献中父母和/或家长分别报告ADHD临床分型,视为单纯提取项。
1.6 文献偏倚风险评价 根据NOS量表对文献行偏倚风险评价,≤5颗星为低质量研究,6~7颗星为中等质量研究,~9颗星为高质量研究。如评价意见不统一,协商解决。
1.7 GRADE证据评价 队列研究的起始评价为低质量证据,分别从局限性、不一致性、间接性、精确性和发表偏倚行降级因素考量,分为无(不降级)、严重(降1级)、非常严重(降2级)、极严重(降3级)。根据效应量大的程度和可能导致疗效显著性降低偏倚因素存在多少和程度考虑升1~2级,剂量-效应关系可考虑升1级。
1.8 统计学方法 采用Stata15.0软件进行Meta分析。采用卡方检验行统计学异质性分析,P≤0.1为研究之间存在显著异质性,采用I2对异质性进行定量,I2≤50%为中低度异质性,采用固定效应模型;I2>50%为高度异质性,采用随机效应模型。通过计算效应指标自然对数使其满足近似正态分布。通过亚组分析探究研究间异质性的来源以识别重要的潜在混杂因素。采用Begg秩相关法、Egger直线回归法及绘制漏斗图进行发表偏倚检验。合并统计量的检验评估结果,P<0.05为差异有统计学意义。
2 结果
2.1 文献检索结果 根据检索策略共检索到文献1 120篇,经过筛选最终纳入文献13篇[4-16],筛选流程见图1。
2.2 纳入文献基本特征 13篇队列研究中,1 篇[13]为回顾性,12篇为前瞻性。表1显示,13篇中文献[14]和[4]分别含2和3个独立队列,故共16个队列,50项消瘦、超重和肥胖数据。队列来自北美洲4个(美国3个,加拿大1个)、欧洲12个(丹麦、瑞典和英国各3个,芬兰2个,西班牙1个)。队列总人数801 834(511~649 043,中位数3 803)。除文献[11,12]外,其他均校正了主要混杂因素。母亲孕前BMI来源于自我报告9篇,来源于医疗信息系统数据4篇。10篇根据WHO标准将母亲孕前BMI(kg·m-2)分为消瘦(<18.5)、正常(~24.99)、超重(~29.99)、肥胖(≥30);3篇分别根据美国国家体重分类标准[11]、美国CDC标准[9]、美国医学研究所(IOM)标准[4]对母亲孕前体重进行分组。2篇[9,10]将正常体重组与消瘦组合并作为对照组。1篇[14]将超重、肥胖合并分析(肥胖组)。儿童随访年龄3~18岁。3篇[8,11,14]采用父母和教师2种评估量表行ADHD评估。11篇[4-14]报道了ADHD总体患病率,其中1篇文献[8]同时对注意力缺陷型和多动冲动型ADHD进行了报告。2篇[15,16]对ADHD亚型进行了分别报告。

图1 文献筛选流程图

表1 纳入文献基本特征

续表1 文献国家随访年龄/岁孕前BMI来源BMI分类标准ADHD诊断标准ADHD症状报告者调整的混杂因素ADHD/队列人数效应量OR/HR/RR2017[11]荷兰10自我报告美国国家CSI-4父母/教师NA父母153+教师168/764超重OR&:1.9(1.1~3.3);超重OR$:1(0.6~1.8);肥胖OR&:2.3(1.4~3.9);肥胖OR$:1(0.6~1.6)2018[5]丹麦13.3自我报告WHODSM-Ⅳ父母4,10,12,17,22,252 417/81 892消瘦HR:1.05(0.87~1.28);超重HR:1.28(1.15~1.41);肥胖HR:1.47(1.26~1.71)2018[13]芬兰11岁止2)医疗信息WHOICD-10父母1,6,7,10,12,17,19,20,29,25,26,275 263/649 043超重HR:1.15(1.06~1.24);肥胖HR:1.44(1.28~1.63)2019[10]加拿大18自我报告WHOICD-9父母1,5,6,11,12,17,191 257/38 211超重RR:1.09(0.95~1.26);肥胖RR:1.45(1.24~1.69)
2.3 偏倚风险评价 表2显示,中等风险9篇,低风险4篇,文献总体偏倚风险中等偏上。
2.4 母亲孕前体重状态与子代发生ADHD的Meta分析 图2显示,母亲孕前消瘦纳入了6篇文献(11项数据),I2=0(P=0.781),随机效应模型,OR=1.05(95%CI: 0.97~1.13),差异无统计学意义;母亲孕前超重共纳入了12篇文献(18项数据),I2=18.3%(P=0.234),随机效应模型,OR=1.21(95%CI: 1.16~1.27),差异有统计学意义;母亲孕前肥胖纳入了13篇文献(21项数据),I2=84.0%(P<0.01),随机效应模型,OR=1.35(95%CI: 1.19~1.55),差异有统计学意义。
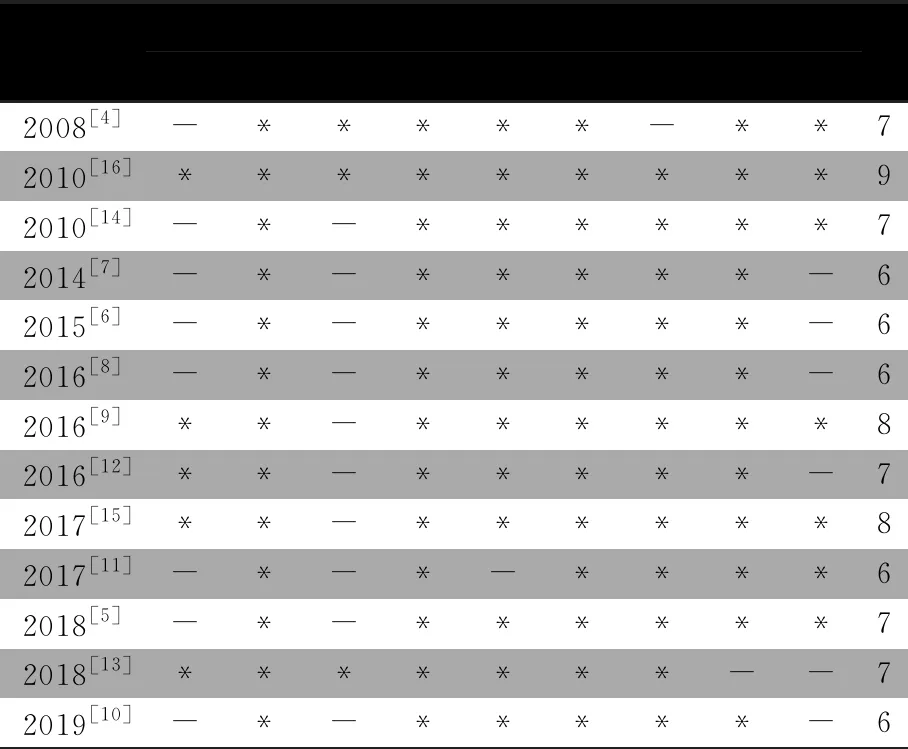
表2 纳入的30个队列研究文献的NOS评分
2.5 亚组分析 表3显示,①根据队列地区来源亚组分析,欧洲队列显示,母亲孕前超重、肥胖均可增加子代ADHD风险;北美队列显示,母亲孕前肥胖增加子代ADHD风险,母亲孕前超重与子代ADHD发生风险无关。②根据BMI报告亚组分析,无论孕前BMI来自医疗信息还是母亲自述,母亲孕前超重、肥胖均可增加子代ADHD风险。③根据儿童随访年龄(学龄前期、学龄期和未提供随访年龄)亚组分析,母亲孕前超重增加子代各个年龄段ADHD发生风险,母亲肥胖与学龄前期子代ADHD发生风险之间不相关,可增加学龄期和未说明年龄子代ADHD发生风险。④根据ADHD诊断标准亚组分析,无论采用何种诊断标准,母亲孕前超重、肥胖均可增加子代ADHD风险。⑤根据ADHD症状汇报者亚组分析,父母汇报儿童ADHD症状,母亲孕前超重、肥胖增加子代ADHD风险;教师汇报儿童ADHD症状,母亲孕前超重增加子代ADHD风险,母亲孕前肥胖与子代ADHD风险无关。⑥根据ADHD不同临床分型亚组分析,母亲孕前超重、肥胖增加子代混合型ADHD发生风险;母亲孕前超重增加子代注意缺陷型ADHD发生风险;母亲孕前超重、肥胖与多动/冲动型ADHD的风险不相关。

图2 母亲孕前体重状态与子代ADHD的关系Meta分析

表3 亚组Meta分析结果
2.6 敏感性分析 对母亲孕前超重(图3A)、肥胖(图3B)与子代ADHD关系文献逐一去除行敏感性分析,前后合并效应量未发生明显变化(超重组OR值波动于1.19~1.23;肥胖组OR值波动于1.30~1.39),母亲孕前体重状态与子代发生ADHD的Meta分析总体结果稳健可靠。
由于母亲孕前肥胖与子代ADHD发生风险关系的研究异质性较大(I2=84.0%),行敏感性分析,文献[11]和[12]未调整混杂因素,文献[13]为回顾性队列研究,去除这3篇后的分析结果显示,母亲孕前肥胖(OR=1.33,95%CI:1.13~1.57)与基础分析肥胖(OR=1.35,图2)子代发生ADHD的风险一致。
2.7 发表偏倚 Begg秩相关法结果显示,母亲孕前消瘦(Z=1.09,P=0.276)、超重(Z=0.15,P=0.880)和肥胖(Z=0.18,P=0.856)发表偏倚较小; Egger直线回归法结果显示,母亲孕前消瘦(t=0.81,P=0.439)、超重(t=0.06,P=0.949)和肥胖(t=-1.0,P=0.332)发表偏倚较小;母亲孕前消瘦(图4A)、超重(图4B)和肥胖(图4C) 漏斗图显示发表偏倚较小。

图3 母亲孕前超重、肥胖与子代ADHD关系的敏感性分析

图4 发表偏倚漏斗图
2.8 GRADE证据评价 表4显示,母亲孕前消瘦和超重有非常严重局限性,纳入的6项和12项队列研究中等质量文献≥50%;母亲孕前肥胖有严重局限性,纳入的13项队列研究中等质量文献38%; 母亲孕前消瘦、超重和肥胖不一致性均非常严重:母亲孕前BMI自我报告比例分别为67%、73%和69%,ADHD诊断量表由教师和家长共同评定比例分别为33%、27%和31%,没有升级因素存在。

表4 GRADE证据质量评价
3 讨论
本文Meta分析纳入的13篇文献均为队列研究,12项为前瞻性研究,1项为回顾性研究,采用NOS评分评估偏倚风险中等偏上,文献[8]研究人群含酗酒、吸毒人群,文献[11]为早产儿队列,余11篇文献均为人群出生队列研究,暴露组真正或一定程度上代表某一地区人群中的暴露组特征,部分研究[4,5,6,7,10,14]未能明确描述队列纳入总人数详细排除标准,且总人数与最终参与分析人数相差较大(超过10%);4项研究的暴露数据来自档案记录,9项研究的暴露数据来自于自我报告。13项研究的暴露组和非暴露组均来自同一人群,11项研究调整了混杂因素及主要混杂因素,13项研究随访时间均足够长。
本文Meta分析结果显示,母亲孕期超重和肥胖子代患ADHD的风险分别增加21%和35%;敏感性分析发现,剔除纳入的任意1篇文献OR值分别为1.19~1.23和1.30~1.39,与基础分析结果一致,因此本文结果稳健可靠。
本文纳入队列研究,队列的起点是母亲孕期BMI,队列的终点为生后3~18岁ADHD评估,涉及母亲和儿童2代人,影响的因素可以来自于母亲(神经精神疾病、ADHD、受教育水平、怀孕时年龄、健康状况、情绪等),也可以来自于儿童(出生方式、性别、出生体重、胎龄、体重),也可以来自于母亲和儿童之外的残余混杂因素(家庭环境、营养水平、遗传易感性、父亲因素等)。本文纳入的13篇文献,8篇控制了母亲、儿童及残余混杂因素,2篇未控制任何混杂因素,2篇未控制儿童因素,1篇未控制残余因素,去除2篇未控制任何混杂因素的文献再行敏感性分析,结果与基础分析一致,也提示本文结果稳健可靠。
母亲孕前肥胖文献的异质性大(I2=84.0%,P<0.001),为探索异质性来源,行亚组分析结果显示:队列来源于不同地域、随访年龄、量表评定者及ADHD临床分型均为其可能的异质性来源。不同ADHD临床类型分析发现,母亲孕前超重、肥胖增加子代未分型的发生风险,而与注意缺陷型、多动冲动型无相关性,可能与通过单一型判断ADHD导致假阴性率增加有关。随访年龄的亚组分析发现,母亲孕前肥胖与子代ADHD发生风险呈现时间依赖性,母亲孕前肥胖对学龄前期子代ADHD影响相对较小,母亲孕前超重、肥胖显著增加学龄期儿童ADHD发生风险,这可能与儿童ADHD临床特点相关,即ADHD临床症状初现的平均年龄是3~4岁,至学龄期症状最为突出,因此学龄前期随访可能会增加假阴性率[19]。
本文不足与局限性:①纳入的研究人群主要为欧、美洲人群,结果的外推性受到限制[20],因种族差异,结论可能不适合其他国家和地区人群。②ADHD临床症状初现于3~4岁,但学龄前儿童诊断ADHD仍具有挑战性[21]。③只纳入中英文文献,可能带来语种选择偏倚;且并未检索到基于我国人群的队列研究,结果推广需谨慎。
