山茶油中不同形态酚类化合物的分离提取及抗氧化能力评价
2020-12-15裘芳成刘睿杰金青哲王兴国
裘芳成,张 涛,常 明,刘睿杰,金青哲,王兴国
(江南大学 食品学院,食品安全与营养协同创新中心,江苏 无锡 214122)
山茶油被誉为“东方橄榄油”[1],除高油酸外,山茶油还富含各种脂质伴随物[2],其中酚类化合物含量较高,且具有抗氧化、抗炎等多种生理活性[3-4],是山茶油中重要的功能性成分。
植物中酚类化合物可分为游离态酚类化合物(Free phenolic compound,FP)、酯化酚类化合物(Esterified phenolic compound,EP)、糖苷态酚类化合物(Glycosylated phenolic compound,GP)及不溶性结合态酚类化合物(Insoluble-bound phenolic compound,IBP)4种形态。目前,国内外众多对果蔬、谷物等酚类化合物的研究已证实不同形态酚类化合物提取物在含量及生物活性上存在较大差异[5-7],但山茶油中各形态酚类化合物种类及含量尚未得知。
本研究对山茶油中4种形态酚类化合物进行提取方法的优化,并且通过DPPH、ABTS、FRAC和ORACFL4种方法评价山茶油中4种形态酚类化合物的抗氧化能力,以期为山茶油酚类化合物的进一步研究提供参考。
1 材料与方法
1.1 实验材料
1.1.1 原料与试剂
山茶籽,购自浙江杭州,50℃烘干备用;山茶油,小型家用榨油机压榨山茶籽,经自然沉降过夜分离残留的饼渣后制得,密封避光保存于-20℃冰箱中备用。
无水甲醇、正己烷、乙酸乙酯、乙醚、盐酸、氢氧化钠、抗坏血酸、乙二胺四乙酸、氯化铝、没食子酸、Folin酚试剂、碳酸钠、亚硝酸钠、硝酸铝、芦丁、儿茶素、香兰素、溴化钾、无水磷酸氢二钠、无水磷酸二氢钾、冰乙酸、荧光素钠盐标准品,国药集团化学试剂有限公司;6-羟基-2,5,7,8-四甲基色烷-2-羧酸(Trolox)、2,2′-二氮-双(3-乙基苯并噻唑-6-磺酸)(ABTS)、偶氮二异丁脒盐酸盐(AAPH)、荧光素钠酸性黄(FL)、2,4,6-三吡啶基三嗪(TPTZ)、1,1-二苯基-2-三硝基苯肼(DPPH),美国 Sigma-Aldrich 公司。
1.1.2 仪器与设备
UV-2100分光光度计,上海Unico公司;VX-2500型涡旋振荡器,美国Henry Troemner 有限公司;Centrifuge 5415R高速冷冻离心机,德国Eppendorf公司;AL104型电子分析天平,上海Mettler Toledo仪器有限公司;HH-2型数显恒温水浴锅,江苏省金坛市荣华仪器制造有限公司;XD-5203型真空旋转蒸发器,上海贤德实验仪器有限公司。
1.2 实验方法
1.2.1 可溶性酚类化合物提取物的制备
取15 g山茶油,用50 mL正己烷与100 mL 70%甲醇溶液进行提取,室温下超声处理30 min后,加入0.04 g/mL氯化铝溶液对可溶性酚类物质进行沉降,并添加20 mL一定浓度的NaHCO3溶液以调节pH。静置,待完全沉淀后过滤,取沉淀物用1.0 mol/L盐酸溶液溶解,4 000 r/min离心5 min以除去多余沉淀物,用于后续3个形态(游离、酯化和糖苷态)可溶性酚类化合物的分级提取。剩余滤液中的正己烷层用于提取不溶性结合态酚类化合物。
1.2.2 游离态酚类化合物的提取
将1.2.1中酸水溶液用乙醚-乙酸乙酯(体积比1∶1)在溶剂与水相体积比为1∶1下提取3次。将有机相合并,加无水硫酸钠脱除多余水分后,于-20℃下冷冻静置2 h,过滤除去多余的基质共提物。而后将处理过的样品在35℃下旋转蒸发至干,得到游离态酚类化合物,用5 mL HPLC级甲醇溶解备用。
1.2.3 酯化酚类化合物的提取
取1.2.2中游离态酚类化合物提取后的剩余酸水相,按体积比加入一定量含有10 mmol/L EDTA和1%抗坏血酸的4 mol/L NaOH溶液,室温下在水浴振荡器150 r/min转速下水解一定时间以释放酯化酚类。使用6 mol/L HCl将水解产物的pH调节至2,然后如1.2.2中对游离态酚类化合物所述,将释放的酚类化合物用有机溶剂提取3次,并蒸干复溶备用。
1.2.4 糖苷态酚类化合物的提取
取1.2.3中酯化酚类化合物提取后的剩余酸水相,按体积比加入一定量 6 mol/L HCl,在75℃下使用水浴振荡器在150 r/min转速下水解一定时间以释放糖基化的酚类,然后如1.2.2中对游离态酚类化合物所述,将从可溶性糖苷释放的酚类化合物用有机溶剂提取3次,并蒸干复溶备用。
1.2.5 不溶性结合态酚类化合物的提取
取1.2.1中的正己烷层,加入一定量含有10 mmol/L EDTA和1%抗坏血酸的4 mol/L NaOH,在室温下使用水浴振荡器在150 r/min转速下水解一定时间以释放不溶性结合态酚类化合物。使用6 mol/L HCl将水解产物的pH调节至2,并在5℃下以4 000 r/min离心5 min。然后,用等体积的正己烷将上清液萃取3次以除去干扰的脂质,再如1.2.2对于游离态酚类化合物所述,将释放的不溶性结合态酚类化合物用有机溶剂提取3次,并蒸干复溶备用。
1.2.6 总酚含量(TPC)的测定
以没食子酸为标准品,采用Folin-Ciocalteu比色法测定总酚含量(TPC)。总酚含量用没食子酸当量GAE表示,具体测定参考Gouvinhas等[8]的方法。
1.2.7 总黄酮含量(TFC)的测定
以芦丁为标准品,采用NaNO2-Al(NO)3比色法测定总黄酮含量(TFC)。总黄酮含量用芦丁当量RE表示,具体测定参考梁杏秋[9]的方法。
1.2.8 缩合单宁含量(CTC)的测定
以(+)-儿茶素为标准品,采用香草醛比色法测定缩合单宁含量(CTC)。缩合单宁含量用(+)-儿茶素当量CE表示,具体测定参考覃宇等[10]的方法。
1.2.9 酚类化合物抗氧化能力测定
采用DPPH、ABTS、FRAP及ORACFL4种方法对山茶油不同形态酚类化合物进行抗氧化能力比较,其结果均以Trolox当量表示,具体操作参考谢丹[11]的方法。
2 结果与分析
2.1 山茶油不同形态酚类化合物提取条件优化
目前,关于山茶油酚类化合物的研究多集中在通过有机溶剂可直接萃取的可溶性酚类化合物,而植物中还存在大量与植物基质化学键合的结合态酚类,需要通过水解等手段破坏化学键后提取[12]。研究表明,碱、酸水解分别能够有效破坏结合态酚类化合物的酯键和糖苷键,可通过不同水解方法释放多种形态的酚类化合物[13]。本实验借鉴Arruda等[5]对水溶性体系中不同形态酚类化合物的样品前处理方法,优化了结合态酚类化合物提取过程中的水解条件(水解时间、液料比),对山茶油中不同形态酚类化合物的提取方法进行探索,结果如图1~图3所示。
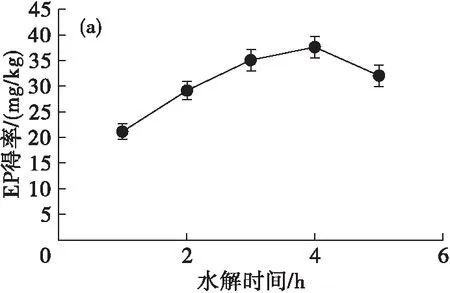
注:液料比2∶1。
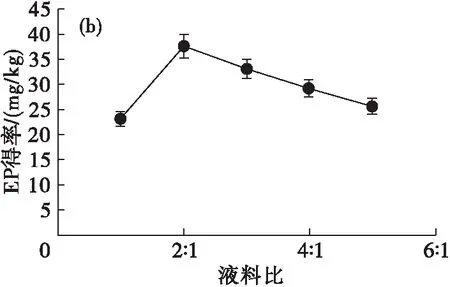
注:水解时间4 h。
由图1可见:酯化酚类化合物得率随着水解时间的延长而逐渐增加,在4 h时达到最高,超过4 h后,酯化酚类化合物得率呈下降趋势,因此确定最佳水解时间为4 h;在水解时间4 h下,酯化酚类化合物得率随液料比的增大呈先增加后降低趋势,在液料比为2∶1时酯化酚类化合物得率最高,因此确定最佳液料比为2∶1。
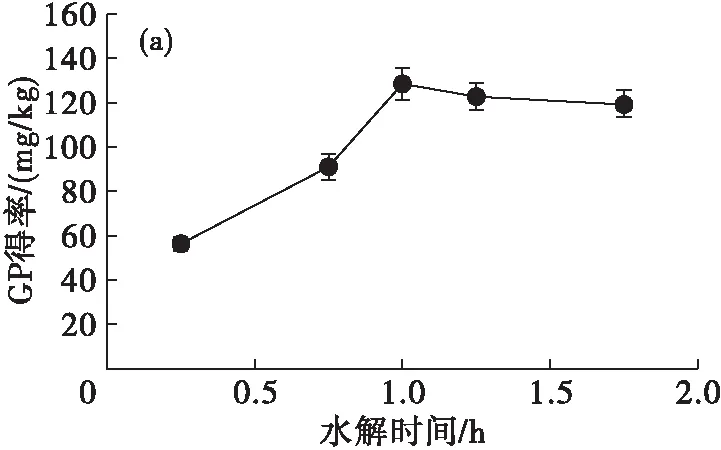
注:液料比1∶1。

注:水解时间1 h。
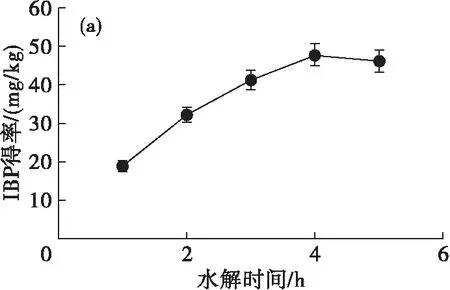
注:液料比4∶1。
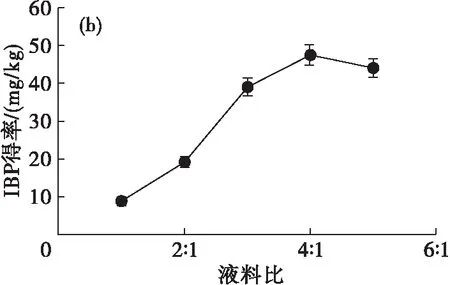
注:水解时间4 h。
由图2可见:糖苷态酚类化合物得率在水解时间为1 h时最高,之后随水解时间延长呈下降趋势,因此确定最佳水解时间为1 h;在水解时间1 h下,糖苷态酚类化合物得率随液料比的增大呈先增加后降低趋势,在液料比为1∶1时糖苷态酚类化合物得率达到峰值,因此确定最佳液料比为1∶1。
由图3可见:不溶性结合态酚类化合物得率随着水解时间的延长而逐渐增加,在4 h时达到最高,因此确定最佳水解时间为4 h;在水解时间4 h下,不溶性结合态酚类化合物得率随液料比的增大呈先增加后降低趋势,在液料比为4∶1时不溶性结合态酚类化合物得率达到峰值,因此确定最佳液料比为4∶1。
由图1~图3可知,随着水解时间的不断延长,山茶油中酯化酚类化合物、糖苷态酚类化合物及不溶性结合态酚类化合物得率均呈现先增加后降低的趋势。可能的原因是:当水解时间较短时,山茶油中结合态酚类化合物还未被完全释放,而随着水解时间的延长,山茶油中酚类化合物逐渐被释放,得率上升;当水解时间过长时,过碱或过酸的环境中酚类化合物结构被破坏,从而使得率有所下降。同样,当碱液或酸液的加入量增加时,山茶油中酚类化合物得率也呈先增加后降低的趋势,这可能是由于当碱液或酸液的加入超过一定量时,过碱或过酸环境下酚类化合物的稳定性下降所造成的。
2.2 山茶油中提取的4种形态酚类化合物中总酚、总黄酮和缩合单宁含量
在最佳条件下对山茶油中4种形态酚类化合物进行提取,并测定了其总酚含量(TPC)、总黄酮含量(TFC)及缩合单宁含量(CTC),结果如表1所示。

表1 山茶油中提取的4种形态酚类化合物中TPC、TFC及CTC μg/g
由表1可见,山茶油TPC为225.74 μg/g。其中,酚类化合物主要以糖苷态存在,占TPC的57.02%,而游离态酚类化合物的TPC最低,为11.92 μg/g,仅占总含量的5.28%。山茶油TFC为106.67 μg/g,其总体形态分布趋势与TPC较为相似。黄酮类化合物主要以糖苷态和不溶性结合态存在,分别占TFC的38.76%和39.52%。而山茶油CTC较低,仅为31.71 μg/g。缩合单宁主要以不溶性结合态存在,占CTC的49.32%。
2.3 山茶油中4种形态酚类化合物的抗氧化能力
已有研究表明,谷物中结合态酚类化合物比游离态酚类化合物具有更强的清除自由基活性[14-15]。本实验通过DPPH、ABTS、FRAP和ORACFL4种方法,评价山茶油中4种形态酚类化合物抗氧化能力的差异,结果如图4所示。
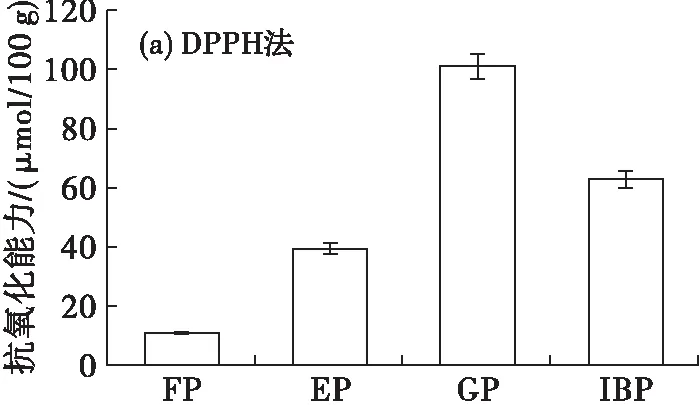
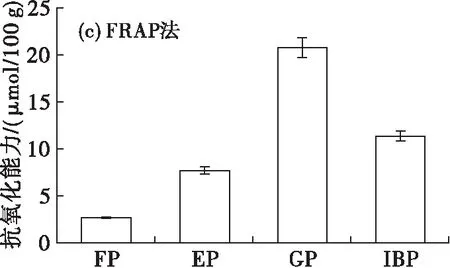
由图4可知,山茶油中4种形态酚类化合物DPPH、ABTS、FRAP和ORACFL4种方法抗氧化能力分别为11.49~101.17、5.53~37.65、2.64~20.68、44.12~184.96 μmol/100 g。4种方法评价的山茶油中4种形态酚类化合物抗氧化能力的总体趋势均为糖苷态酚类化合物>不溶性结合态酚类化合物>酯化酚类化合物>游离态酚类化合物,糖苷态酚类化合物的抗氧化能力明显优于其他形态的酚类化合物。
3 结 论
(1)通过单因素实验优化了山茶油中酯化酚类化合物(碱水解法)、糖苷态酚类化合物(酸水解法)及不溶性结合态酚类化合物(碱水解法)提取过程中的水解时间和液料比,结果表明这3种酚类化合物的最佳水解时间分别为4、1、4 h,最佳液料比(体积比)分别为2∶1、1∶1、4∶1。
(2)利用优化的提取方法对山茶油中4种形态酚类化合物进行提取并测定,其中TPC、TFC及CTC分别为(225.74±0.10)μg/g、(106.67±0.06)μg/g及(31.71±0.23)μg/g。其中,糖苷态是山茶油酚类化合物的主要存在形式,占TPC的57.02%;山茶油中黄酮类化合物主要以糖苷态和不溶性结合态形式存在,占TFC的38.76%和39.52%;而山茶油酚类化合物提取物中CTC较低,且主要以不溶性结合态的形式存在,占CTC的49.32%。
(3)采用DPPH、ABTS、FRAC和ORACFL4种方法对山茶油中4种形态酚类化合物抗氧化能力进行比较,结果表明,4种形态酚类化合物抗氧化能力的强弱顺序均为糖苷态酚类化合物>不溶性结合态酚类化合物>酯化酚类化合物>游离态酚类化合物。
该结果为进一步研究山茶油中不同形态酚类化合物提供了一定的理论基础,为更好地开发植物油酚类化合物提供一定的参考。
