喷雾干燥可控制备生物玻璃微球及其体外生物活性研究
2020-12-11胡亚萍田正芳朱钰方
胡亚萍,田正芳,朱 敏,朱钰方
(1. 上海理工大学 材料科学与工程学院,上海 200093; 2. 黄冈师范学院 化学化工学院,催化材料制备及应用湖北省重点实验室,湖北 438000)
SiO2-CaO-P2O5体系的硅酸盐基生物玻璃(Bioglass,BG)能与人体体液发生化学反应而与骨组织形成界面结合[1]。BG具有优异的生物相容性、成骨能力和降解性能,因此自1969年被发明以来,已得到广泛应用和深入研究[1-4]。
传统制备BG粉体的方法有高温熔融法、溶胶-凝胶法等。高温熔融法制备BG粉体具有高温耗能、混料不匀和生物活性较低等特点[5-6]。因此,为了克服这些缺点,研究人员提出溶胶-凝胶法,可在室温下成功制备出BG粉体[6-9]。与高温熔融法相比,溶胶-凝胶法制备的BG粉体生物活性更好,但其存在制备周期长、需用有机溶剂[10],且块状BG还需要进一步研磨等缺点。
喷雾干燥是一种快速加热和冷却的连续过程。在制备微球方面,喷雾干燥法具有耗时短、可批量生产、干燥过程还能方便调节微球大小和形状等优点[11-17]。例如,Yamauchi等[11]采用结构导向剂F127、1,2-双(三乙氧基甲硅烷基)乙烷和正硅酸四乙酯混合后喷雾干燥制备了具有良好球形形貌和粒径在0~2.5 μm的有机硅微球。Fiorilli等[12]采用正硅酸四乙酯为原料预水解后结合三嵌段表面活性剂P123进行喷雾干燥制备出粒径为2~5 μm,孔径约8 nm的二氧化硅微球。近年来,研究人员采用喷雾干燥法替代传统工艺制备BG粉体。例如,Shih等[18]采用溶胶-凝胶法结合喷雾干燥可快速制备平均孔径为6 nm,比表面积为260 cm2/g的BG微球。Ostomel等[19]采用三嵌段表面活性剂(P123)、正硅酸四乙酯、磷酸三乙酯、四水硝酸钙和乙醇溶剂混合后喷雾干燥,成功制备出球形介孔BG微球,颗粒粒径为1 nm~1 mm,表现出良好的体外诱导磷灰石沉积能力。Arcos等[20]采用不同的结构导向剂(P123、CTAB、F127)与正硅酸四乙酯、磷酸三乙酯、四水硝酸钙和乙醇溶剂制备前驱体溶液,喷雾干燥后制备得到不同孔径的BG微球,发现氧化钙含量的提高有利于提高其生物活性。虽然上述研究都表明前驱体溶液结合喷雾干燥方法可制备不同的BG微球,但是前驱体溶液通常含有大量易燃溶剂(主要为体积含量约60%的乙醇),前驱体溶液雾化干燥过程需考虑安全问题而不能长时间连续工作,限制了BG粉体的连续批量化制备。
因此,为克服高温耗能、制备周期长、原料成本高、连续批量制备不安全等缺点,本研究提出以水溶液作为溶剂,在酸性条件下制备BG前驱体溶液,采用喷雾干燥方法快速、连续、可控制备球形BG微球,研究了喷雾干燥过程中不同工艺参数(进气风量、前驱体溶液浓度和进料速率)对BG微球粒径的影响; 通过调节原料配比制备不同化学组成的BG微球,研究了不同化学组成BG微球的体外诱导磷灰石沉积能力。
1 实验方法
1.1 材料
硝酸(HNO3,≥68%)、正硅酸四乙酯(TEOS,98%)、磷酸三乙酯(TEP,99.8%)、氯化钠(NaCl,99.5%)、碳酸氢钠(NaHCO3,99.8%)、氯化钾(KCl,99.8%)、磷酸氢二钾(K2HPO4·3H2O,99%)、氯化镁(MgC12·6H2O,98%)、盐酸(HCl,36%~38%)、氯化钙(CaC12,96%)、硫酸钠(Na2SO4,99%)和三羟基氨基甲烷(NH2C(CH2OH)3,99%)购自中国国药化学试剂有限公司(中国上海); 硝酸钙(Ca(NO3)2·4H2O,99%)购自天津市大茂化学检测厂。所有化学药品未经进一步纯化。
1.2 制备方法
1.2.1 制备前驱体溶液
室温下,取一定量的去离子水,滴加硝酸调节水溶液至pH为2,接着往水溶液中加入TEOS并磁力搅拌至溶液透明澄清[21],然后将TEP加入上述澄清溶液并搅拌30 min,最后加入四水合硝酸钙(CaNT)并搅拌20 min,得到澄清的前驱体溶液备用。配制的不同浓度前驱体溶液如表1所示,不同化学组成的前驱体溶液如表2所示。
1.2.2 制备BG微球
采用Buchi-290喷雾干燥仪(喷头直径2.8 mm)喷雾干燥BG前驱体溶液制备BG微球。固定设置仪器的循环率为100%,进口温度为220 ℃。前驱体溶液浓度分别为5wt%、15wt%、25wt%和35wt%; 进气风量为283、439、667和1052 L/h; 进料速率为1.5、3、4.5和6 mL/min。将不同喷雾干燥工艺条件下收集得到的微球置于马弗炉中,从室温开始以2 ℃/min的速率升温至700 ℃并保温5 h,自然冷却得到BG微球。
1.2.3 体外诱导磷灰石沉积
为研究不同化学组成BG微球的体外生物活性,本研究采用实验室自制的模拟体液(SBF)进行体外矿化实验以验证其体外诱导磷灰石沉积能力。SBF中各无机离子的浓度与人体血浆中各离子的浓度相近,根据Kukubo方法配制[22]。实验将BG微球以0.1 g/100 mL的比例浸泡SBF,静置于37 ℃烘箱中,分别浸泡2 h、4 h、8 h、12 h、1 d、2 d、3 d、5 d和7 d后取出,过滤干燥得到矿化的BG微球。采用扫描电镜和附带的能谱仪观察和分析BG微球表面的羟基磷灰石(HA)生长情况; 用粉末X射线衍射仪分析物相组成; 用红外光谱仪分析化学结构变化。
为了研究不同化学组成BG微球对周围pH环境的影响,将BG微球以0.1 g/100 mL的比例浸泡于Tris-HCl(pH7.4)溶液并静置于37 ℃烘箱中,分别浸泡2 h、4 h、8 h、12 h、1 d、2 d、3 d、5 d和7 d后测试溶液的pH,三组平行实验同时进行。
1.3 样品表征
用扫描电镜(SEM,Zeiss SIGMA300)观察BG微球形貌,用所附能谱仪(EDS)分析微球元素成分、组成及分布,另用SEM照片配合Imaje J软件对BG微球粒径进行统计; 用粉末X射线衍射仪(XRD-6100,SHIMADZU)和红外光谱仪(FT-IR,Nicolet 6700)分别对BG微球进行物相和化学结构分析。
2 结果与讨论
2.1 BG微球结构表征
煅烧处理后77SBG微球的SEM、粉末XRD图谱以及能谱仪分析得到的元素分布如图1所示。由图1(A)可以看出,喷雾干燥法得到的BG粉体为光滑的球形颗粒,粒径分布较窄; 粉末XRD图谱显示BG粉体只在2θ=15°~35°范围有宽化的馒头峰,表明700 ℃煅烧处理后的BG粉体为无定型态(图1(B));能谱仪分析的元素分布图表明BG微球的O,Si,Ca,P元素分布均匀(图1(C))。由此可知,采用喷雾干燥BG前驱体溶液方法可以制备化学组成分布均匀、粒径分布较窄的无定型态BG微球。

表1 不同质量浓度的前驱体溶液的配制Table 1 Preparation of precursor solutions with different mass concentrations
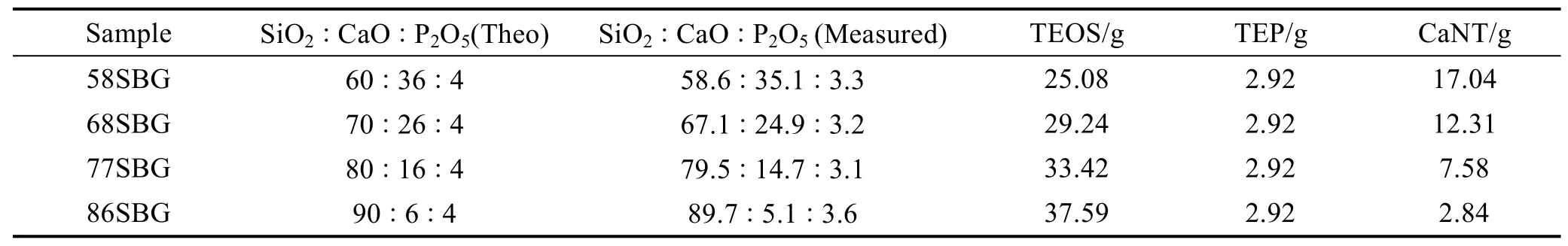
表2 不同化学组成BG微球的理论、实际化学组成和反应物用量Table 2 Theoretical and measured chemical composition,amounts of the reactants of BG microspheres

图1 喷雾干燥法制备的77SBG微球的SEM照片(A)、粉末XRD图谱(B)以及元素分布图(C)Fig. 1 SEM image (A),XRD pattern (B) and elemental mappings (C) of 77SBG microspheres obtained via spray-drying method
2.2 进气风量对BG微球粒径的影响
图2是固定进料速率为6 mL/min时,浓度为5wt%的前驱体溶液通过调节进气风量分别为283、439、667和1052 L/h时得到BG微球的SEM照片和相应的粒径分布直方图。当进气风量为283 L/h时,粒径范围为5~30 μm; 而当进气风量为1052 L/h时,粒径几乎都在10 μm以下。说明当进料速率恒定不变时,单位时间内进气风量越大,BG微球的粒径变小,而且粒径分布变窄。
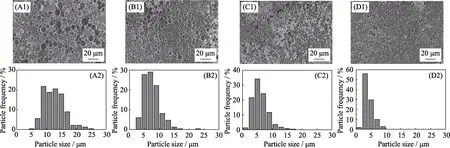
图2 进料速率为6 mL/min时,5wt%的前驱体溶液在进气风量分别为283 (A1,A2)、439 (B1,B2)、667 (C1,C2)和1052 L/h(D1,D2)时得到的77SBG微球的SEM照片以及运用Imaje J统计得到的粒径直方图Fig. 2 SEM images and the particle size histogramms obtained by Imaje J statistics of 77SBG microspheres prepared with 5wt% precursor solution at inlet air volume of 283 (A1,A2),439 (B1,B2),667 (C1,C2) and 1052 L/h(D1,D2) when the feed rate was 6 mL/min
这是因为单位时间内通过喷嘴风量增大,气流速率加快,会将进料的前驱体溶液快速冲散,从而使得雾化液滴尺寸变小。另一方面,气流速率加快将增加快速转移到溶液流中的能量(动能),这使得气液接触面积增大,被雾化液滴很快达到饱和,成核速率加快; 随着成核数量增多,BG微球沉积加快,BG微球的整体粒径减小,粒径范围也相应变窄[23-25]。因此,进气风量的增加与雾化流的液滴尺寸成反比,与最终得到的BG微球的整体粒径大小成反比。
2.3 前驱体溶液浓度对BG微球粒径的影响
图3是进料速率为6 mL/min、进气风量为667 L/h,前驱体溶液浓度分别为5wt%、15wt%、25wt%和35wt%时得到BG微球的SEM照片和粒径分布直方图。由图可以看出,前驱体溶液浓度为5wt%时,BG微球的粒度范围在15 μm以下; 而当前驱体溶液浓度增加到35wt%时,BG微球的粒度范围扩大到40 μm以下。表明当前驱体溶液浓度增高,BG微球整体粒径变大,同时粒径分布变宽。
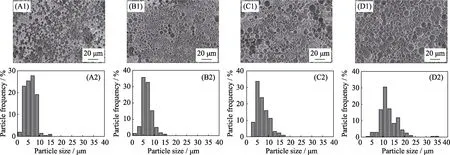
图3 进气风量为667 L/h,5wt% (A1,A2)、15wt% (B1,B2)、25wt% (C1,C2)和35wt% (D1,D2)的前驱体溶液在进料为6 mL/min时77SBG微球的SEM照片及运用Imaje J统计得到的粒径直方图Fig. 3 SEM images and the particle size histogramms obtained by Imaje J statistics of 77SBG microspheres prepared with 5wt% (A1,A2),15 wt% (B1,B2),25wt% (C1,C2) and 35wt% (D1,D2) precursor solutions at the feed rate of 6 mL/min when the inlet air volume was 667 L/h
当其他工艺参数不变时,前驱体溶液浓度增加,造成溶液粘度增大,使得雾化液滴变大,导致气液接触面积缩小,传热效率降低。因此,前驱体溶液浓度增大,BG微球的粒径变大且粒度分布也变宽。前驱体溶液浓度增大,BG微球会出现小颗粒团聚附着在大颗粒表面的现象,这可能由于溶液粘度增大使得雾化液滴不均匀所致。
另一方面,从溶剂去离子水的含量分析,当其他工艺参数不变时,前驱体溶液浓度越小,意味着前驱体溶液中的去离子水含量越大。喷雾干燥形成BG微球的球形形貌很大程度上取决于溶液的表面张力[26]。在喷雾干燥过程中,每种原料都会降低雾化液滴的表面张力,从而影响最终颗粒的形貌。相反地,去离子水具有大的表面张力(72.7 mN/m),高含量的水会增加雾化液滴整体的表面张力而有利于形成BG微球的球形形貌。因此,去离子水含量越高,喷雾干燥过程中雾化液滴的表面张力越大,雾化液滴干燥固化成颗粒时发生的变形越小,使得形成的BG微球球形度越好,整体颗粒变小且粒径分布也会变窄(颗粒更均匀)。
2.4 进料速率对BG微球粒径的影响
图4是前驱体溶液浓度为5wt%、进气风量为1052 L/h,调节进料速率分别为1.5、3、4.5和6 mL/min时得到BG微球的SEM照片和粒径分布直方图。当进料速率增加时,得到的BG微球的粒径范围主要为10 μm以下,但是通过Imaje J统计的粒度分布直方图可以看出,BG微球的中间粒径会随着进料速率的增加而略有增大。这是因为在喷雾干燥过程中,进气风量不变,增大进料速率意味着单位时间内需要更多能量将前驱体溶液雾化成液滴并干燥。所以进料速率越大,雾化液滴的尺寸也会缓慢增大,液滴干燥后形成的BG微球的中间粒径也会略有增大。因此,喷雾干燥过程中进料速率对BG微球的粒径范围影响较小,但是进料速率增大会使BG微球的中间粒径略有增大。
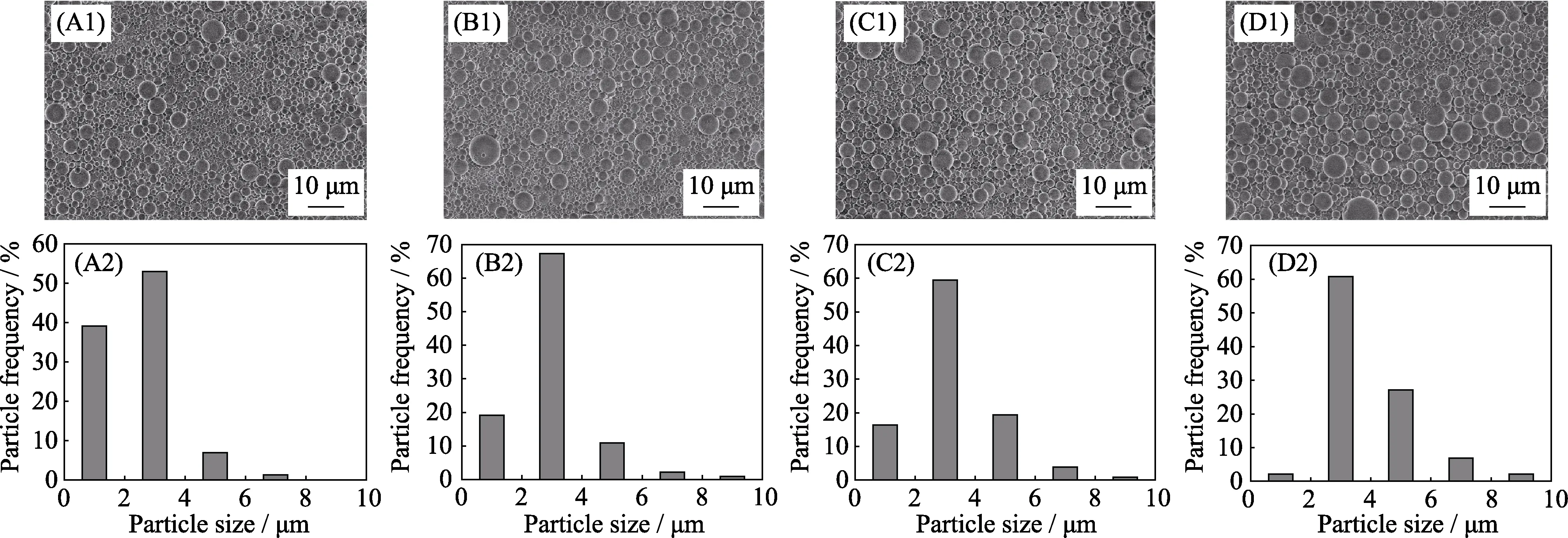
图4 进气风量为1052 L/h时,5 wt%的前驱体溶液在进料速率为1.5 mL/min (A1,A2)、3 mL/min (B1,B2)、4.5 mL/min (C1,C2)和6 mL/min(D1,D2)时得到的77SBG微球的SEM照片及运用Imaje J统计得到的粒径直方图Fig. 4 SEM images and the particle size histogramms obtained by Imaje J statistics of 77SBG microspheres prepared with the 5wt% precursor solution at the feed rates of 1.5 mL/min (A1,A2),3 mL/min (B1,B2),4.5 mL/min (C1,C2) and 6 mL/min (D1,D2) when the inlet air volume was 1052 L/h
2.5 不同化学组成BG微球的结构表征
图5是58SBG、68SBG、77SBG和86SBG微球在700 ℃煅烧处理后的SEM照片。可以看出,不同化学组成的前驱体溶液都能采用喷雾干燥方法制备得到表面光滑的BG微球,并且相同的喷雾干燥过程得到粒径范围相似的BG微球。图6是58SBG 68SBG、77SBG和86SBG微球在700 ℃煅烧处理后的XRD图谱和FT-IR图谱。由XRD图谱可以看出,86SBG和77SBG微球为典型的无定型态生物玻璃,而68SBG微球出现了较弱的Ca2SiO4(PDF#86-0399)物相宽化衍射峰,58SBG则显示出明显的Ca2SiO4衍射峰,表明随着Ca/Si比例的增大,700 ℃煅烧处理得到的BG微球由完全的无定型态到逐渐有Ca2SiO4物相生成。由FT-IR图谱可看出,58SBG、68SBG、77SBG和86SBG微球在800和1083 cm-1左右处出现了较强的Si-O-Si的伸缩振动峰; 在460 cm-1左右处出现了Si-O-Si的弯曲振动峰;58SBG和68SBG微球在590 cm-1左右处出现微弱的肩峰属于无定型态P-O的弯曲振动双峰; 从图中可看出四种组分的BG微球在3500 cm-1左右处出现了-OH峰,这是吸收了空气中水分的缘故。另外,58SBG微球在1480 cm-1处出现了CO32-的振动峰,这是因为相对于68SBG、77SBG、86SBG微球、58SBG微球氧化钙含量最大,表征时暴露在空气中更容易吸收水分和二氧化碳的缘故。
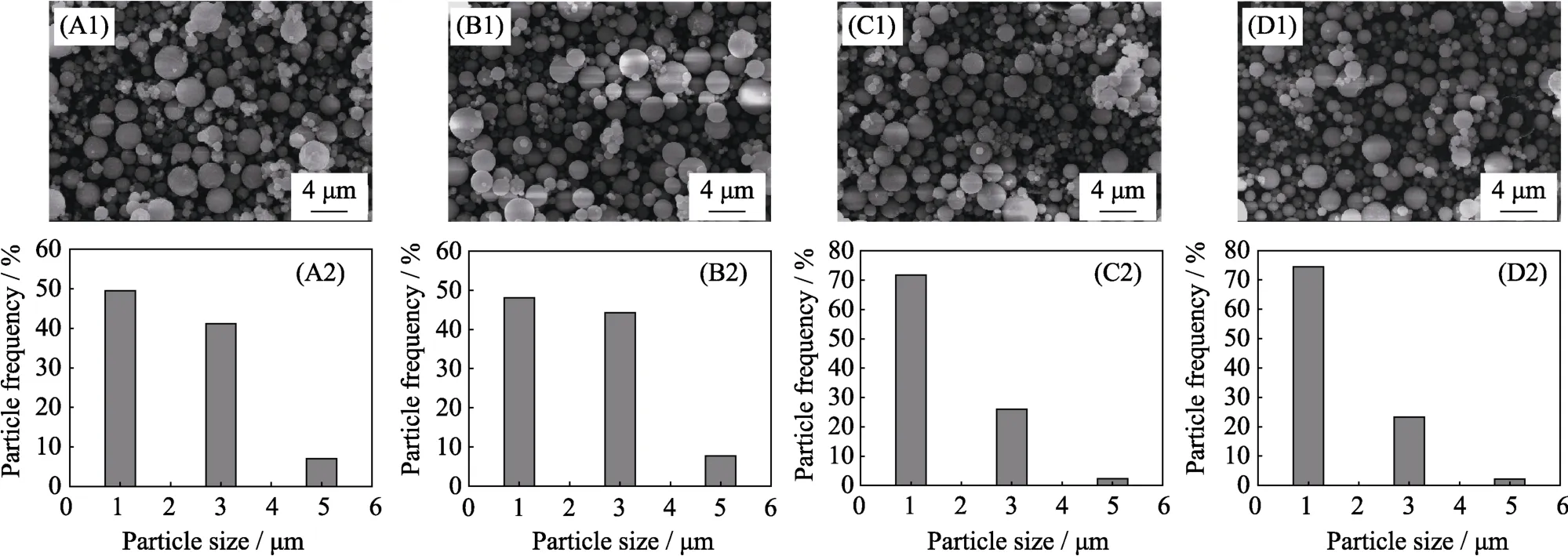
图5 58SBG(A1,A2)、68SBG(B1,B2)、77SBG(C1,C2)和86SBG(D1,D2)微球经700 ℃煅烧处理后的SEM照片及运用Imaje J统计的粒径分布直方图Fig. 5 SEM images and the particle size histogramms obtained by Imaje J statistics of 58SBG (A1,A2),68SBG (B1,B2),77SBG (C1,C2) and 86SBG (D1,D2) microspheres after calcination at 700 ℃

2.6 不同化学组成BG微球的体外诱导磷灰石沉积能力
图7是58SBG、68SBG、77SBG和86SBG微球在SBF中浸泡7 d后的SEM照片和EDS分析图谱。由SEM照片可以看出,原本光滑的BG微球表面都覆盖了一层厚厚的沉积物。根据EDS能谱分析得到58SBG、68SBG、77SBG和86SBG微球的Ca/P比值分别为2.048、1.597、1.520和1.712,这些比值都较接近于羟基磷灰石的Ca/P=1.67,表明BG微球表面的沉积物为羟基磷灰石。因此,喷雾干燥前驱体溶液制备的BG微球具有良好的体外诱导磷灰石沉积能力,主要是因为快速加热和快速冷却的喷雾干燥过程使得制备的BG颗粒的表面保留了更多的亚稳硅氧烷基团[18],而这些基团则充当成核位点有助于羟基磷灰石形成[9]。
图8为58SBG、68SBG、77SBG和86SBG微球在SBF中浸泡不同时间前后的XRD图谱。可以看出,不同化学组成的BG微球在SBF中浸泡不同时间后在2θ=25.8°、31.7°、39°和47°处都出现了羟基磷灰石的特征衍射峰(PDF#09-0432),表明不同化学组成的BG微球都具有体外诱导磷灰石沉积能力。另一方面,不同化学组成的BG微球矿化生成羟基磷灰石的能力有所不同。其中,86SBG微球在矿化3 d后出现明显的羟基磷灰石特征衍射峰,而58SBG、68SBG和77SBG微球则在矿化4 h后就出现了羟基磷灰石的特征衍射峰,并且随着矿化时间延长,羟基磷灰石的特征衍射峰强度逐渐增强; 58SBG微球在浸泡5 d后出现了较强的CaCO3物相衍射峰[27],这归因于58SBG微球表面较高的Ca/P比使58SBG微球溶于SBF后的钙离子溶出较多,在SBF中矿化形成羟基磷灰石的同时还形成了CaCO3。
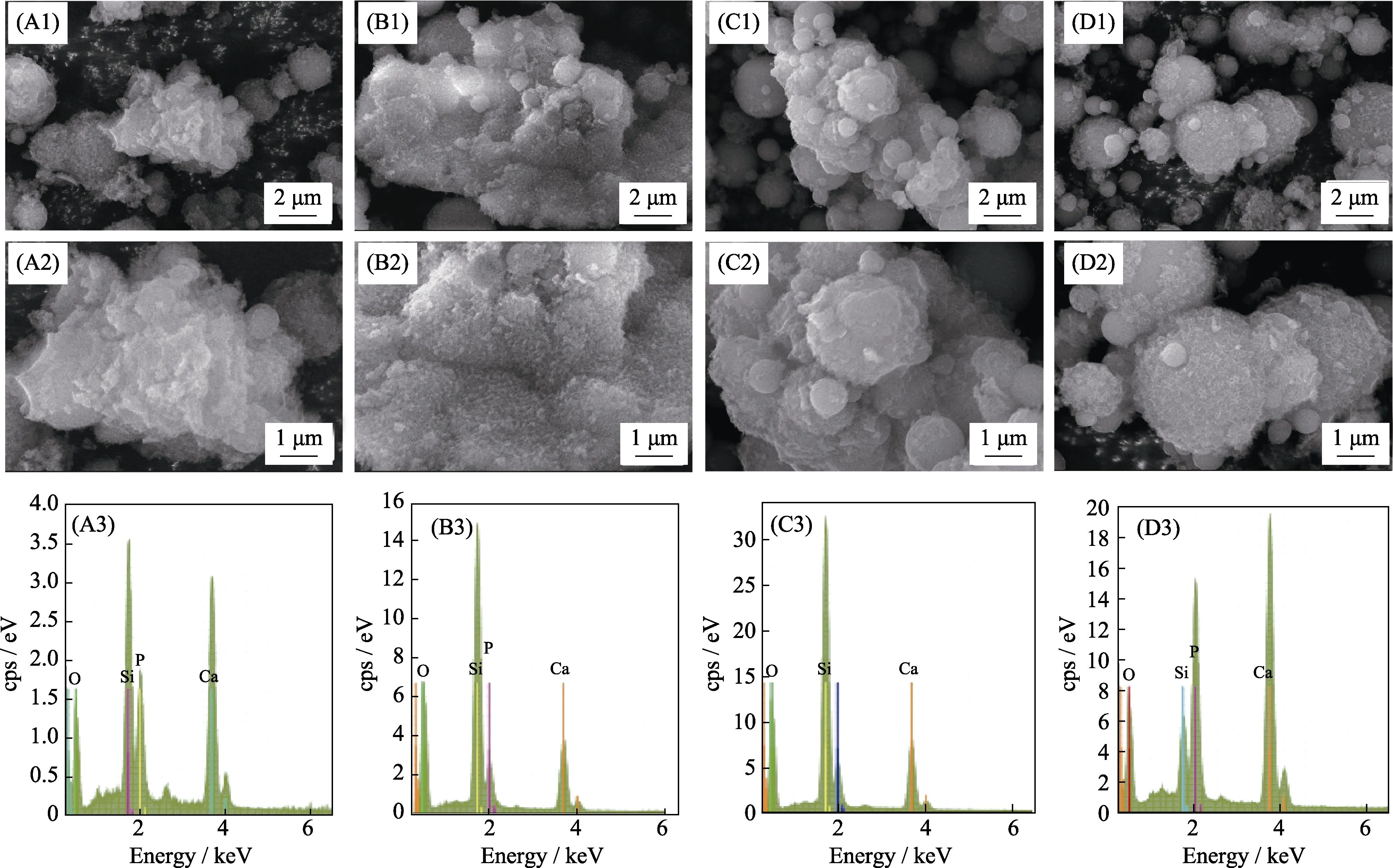
图7 58SBG(A)、68SBG(B)、77SSBG(C) 和 86SBG(D)微球在SBF中浸泡7 d后的SEM照片和EDS分析图谱Fig. 7 SEM images and EDS analysis of 58SBG (A),68SBG (B),77SSBG (C),and 86SBG (D) microspheres after soaking in SBF for 7 d
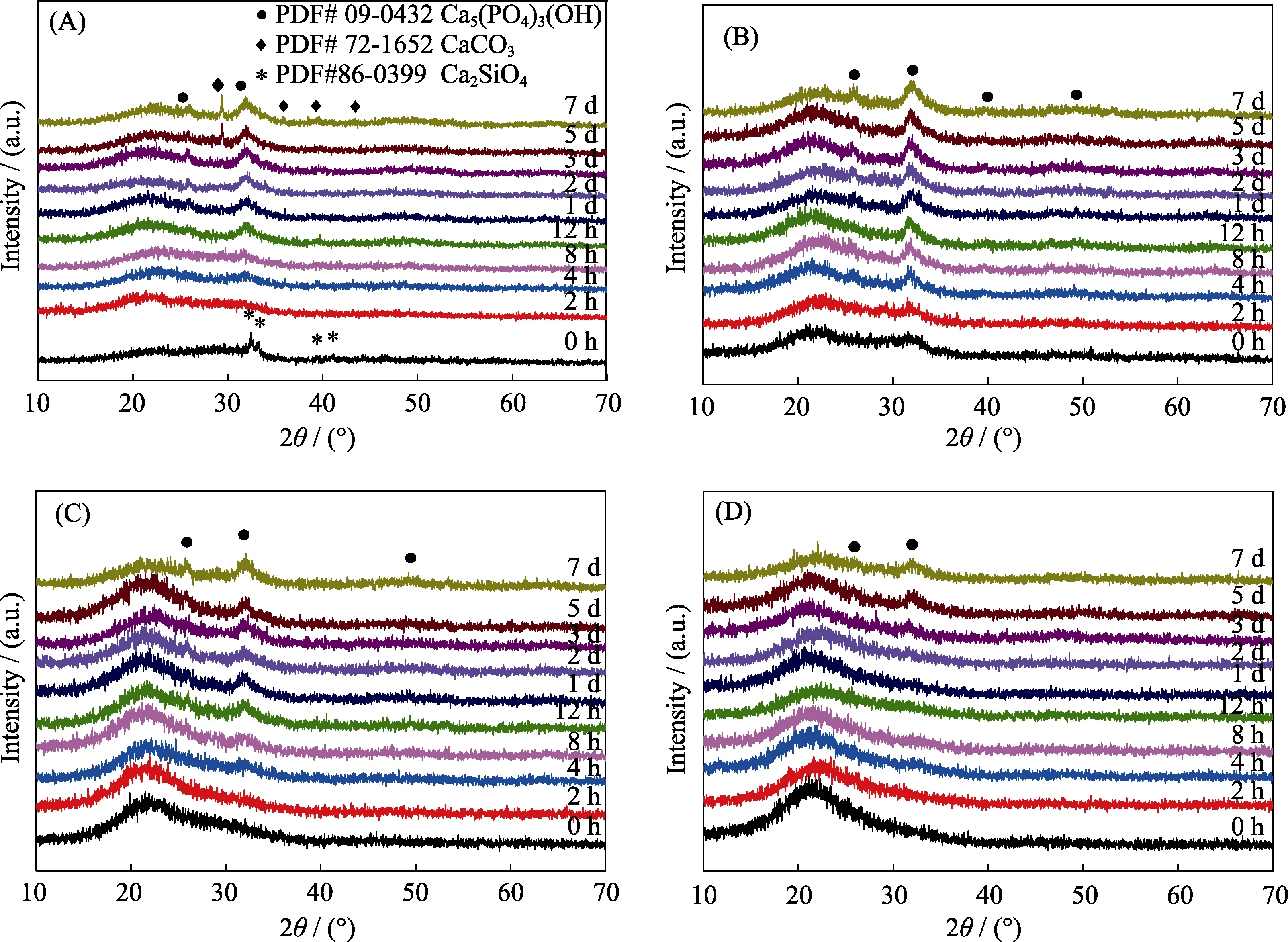
图8 58SBG(A)、68SBG(B)、77SSBG(C)和86SBG(D)微球在SBF中浸泡不同时间前后的广角XRD图谱Fig. 8 Wide-angle XRD patterns of 58SBG (A),68SBG (B),77SSBG (C) and 86SBG (D)microspheres before and after soaking in SBF for different periods
图9为58SBG、68SBG、77SBG和86SBG微球在SBF中浸泡不同时间前后的FT-IR谱图。可以看出,不同化学组成的BG微球在SBF中浸泡不同时间后,在560和610 cm-1左右都出现了晶态的P-O弯曲振动双峰; 在1033 cm-1附近出现P-O伸缩振动峰,而且随着矿化时间延长,振动峰强度也逐渐增强,表明BG微球在矿化过程中,羟基磷灰石在BG微球表面的逐渐形成和晶化。另一方面,从图9中还可以观察到58SBG微球浸泡SBF后在1410和1450 cm-1附近出现CO32-振动峰[28-29],随着浸泡时间延长,其振动峰更明显; 不仅如此,在浸泡2 d时,明显观察到在870 cm-1左右也出现CO32-中C-O振动峰,这表明58SBG微球表面矿化形成碳酸羟基磷灰石[30-31]; 同理也可看出68SBG和77SBG微球在浸泡3 d时,在1410和1450 cm-1附近也出现比较微弱的CO32-振动峰,表明在68SBG和77SBG微球的表面也生成很少量的碳酸羟基磷灰石。

图9 58SBG(A)、68SBG(B)、77SSBG(C)和86SBG(D)微球在SBF中浸泡不同时间前后的FT-IR谱图Fig. 9 FTIR spectra of 58SBG (A),68SBG (B),77SBG (C) and 86SBG (D) microspheres before and after soaking in SBF for different periods
图10是58SBG、68SBG、77SBG和86SBG微球浸泡Tris-HCl溶液中的pH变化曲线。由图可以看出,不同组成的BG微球浸泡Tris-HCl溶液后,其溶液pH随着浸泡时间的延长而升高,且浸泡小于24 h的pH均增大较快,随后缓慢增大,最终pH分别稳定在7.63、7.73、8.49和9.29左右。其中,58SBG微球在浸泡前24 h增加最快,最终达到的pH最高。这主要因为58SBG微球的Ca含量最大,当BG微球浸泡在Tris-HCl溶液中后,微球会发生降解并溶解出大量的Ca2+,而Ca2+会在溶液中发生水化反应产生OH-,从而使溶液pH升高而呈现碱性环境[32]。
3 结论
本研究以正硅酸四乙酯、磷酸三乙酯和四水硝酸钙为原料,采用喷雾干燥前驱体溶液方法可控制备出球形、组成分布均匀且无定型的BG微球。通过调节喷雾干燥过程中的工艺参数(进气风量、前驱体溶液浓度和进料速率)可得到粒径可控的BG微球。进气风量增大,BG微球的整体粒径减小、粒径分布变窄; 前驱体溶液浓度增大,BG微球的整体粒径增大、粒径分布变宽; 进料速率增大,BG微球的整体粒径略有增大、粒径分布基本不变。另一方面,喷雾干燥方法还可以制备不同化学组成的BG微球,且都具有良好的诱导磷灰石沉积能力,BG微球中钙含量增加有利于提高BG微球的体外诱导磷灰石沉积能力。因此,本研究提出的喷雾干燥法制备BG微球可实现粒径、化学组成可控并有望快速、批量制备BG微球。
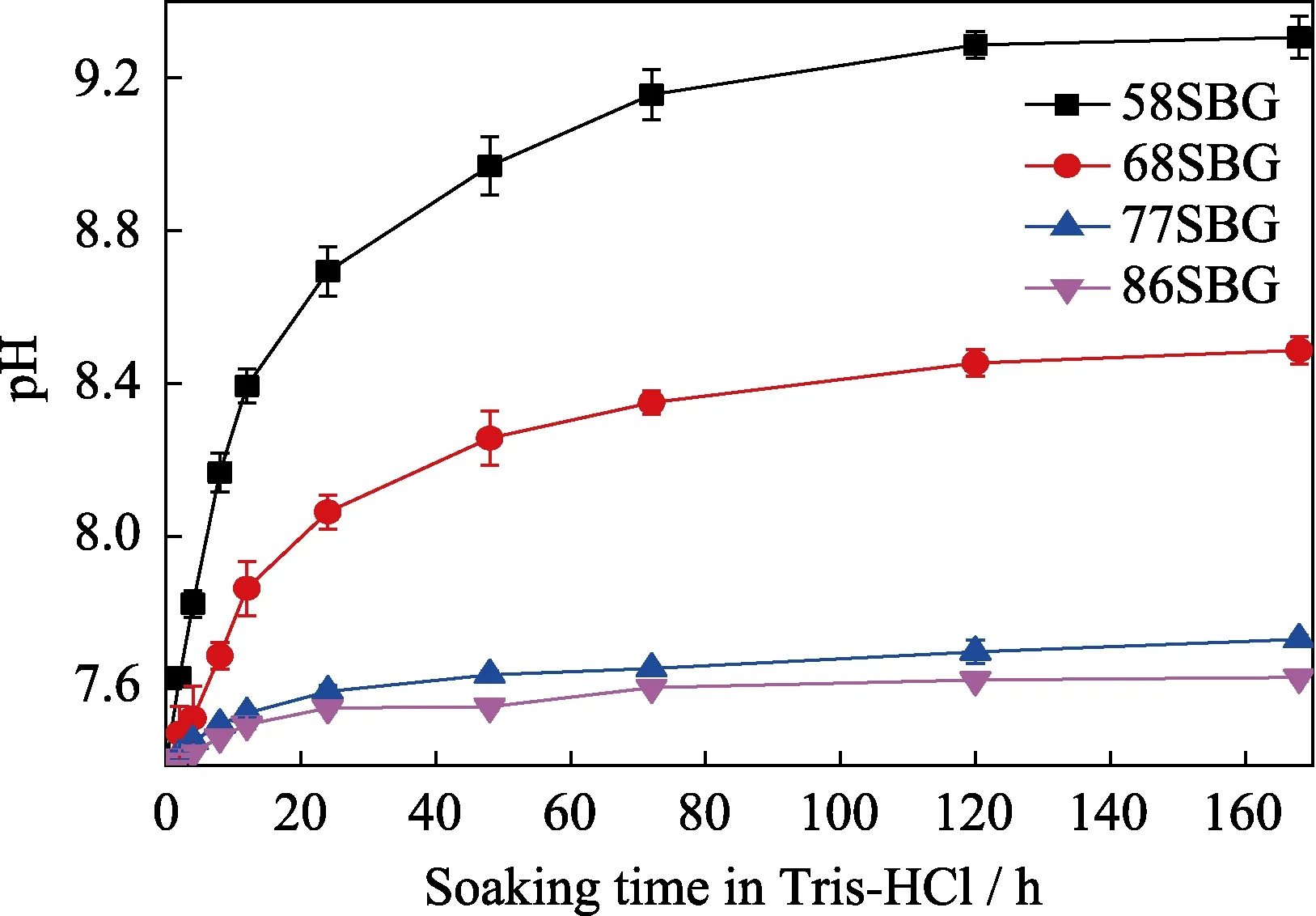
图10 58SBG、68SBG、77SBG和86SBG微球在Tris-HCl溶液中浸泡不同时间的pH变化曲线Fig. 10 pH changes of Tris-HCl solutions after 58SBG,68SBG,77SBG and 86SBG microspheres soaking in Tris-HCl for different periods
