α-Ni(OH)2/g-C3N4复合材料合成及其电化学性能研究*
2020-12-08黄誓成陆映东张倍维方志杰曾纪术
黄誓成,陆映东,黄 作,张倍维,方志杰,曾纪术
(1. 广西晶联光电材料有限责任公司,广西 柳州 545006; 2. 广西科技大学 材料科学与工程研究中心,广西 柳州 545006)
0 引 言
近年来,电催化分解水制备氢气和氧气因原料来源广泛、操作简便、产品纯度高、无污染等优点已成为研究热点。作为水分解半反应之一,阳极氧析出反应(OER)因动力学缓慢,严重制约了电解水制氢的效率,因此开发高效、廉价、稳定的OER电催化剂是一个亟待解决的课题[1]。贵金属催化剂如IrO2和RuO2是目前公认为最优异的OER催化剂,但稀少的储量和高昂的成本限制了其大规模应用[2],因此寻找性能优异的廉价电催化剂对电催化水分解制氢具有重要的现实意义。
过渡金属催化剂中镍基催化剂因活性高,价格低廉,稳定性较好被认为极有潜力的非贵金属催化剂[3-4]。氢氧化镍由于其成本低廉、易于合成、稳定性较好和电化学活性高等优点在制作电池、电容器以及电化学催化等方面均具有很好的应用[5-7]。研究表明Ni(OH)2尤其是纳米化的α-Ni(OH)2具有令人期待的OER潜力[8-13],但易于团聚和碱性条件不稳定的缺陷,制约了其活性进一步提升。石墨化氮化碳(g-C3N4)合成条件简单、成本低廉、耐酸/碱环境能力强、化学稳定性强和热稳定性强[14-15],但导电性差、活性点位少[16-18]。本文拟通过水热法将α-Ni(OH)2纳米片生长于g-C3N4基底上得到α-Ni(OH)2/g-C3N4复合材料,期望改善α-Ni(OH)2易于团聚,稳定性差的缺陷,同时改善g-C3N4的导电性,得到成本低、稳定性好且活性高的碱性析氧催化剂。
1 实 验
1.1 材料制备
(1)α-Ni(OH)2纳米片的制备:烧杯中加入30 mL去离子水,5 mmol尿素((NH2)2CO),1.25 mmol乙酸镍(Ni(CH3COO)2·4H2O)和1.25 mmol十六烷基三甲基溴化铵(CTAB)(C16H33(CH3)NBr)。在加热搅拌器上48 ℃加热搅拌40 min,之后将反应物倒入50 mL反应釜中,将其放入烘箱加热至120 ℃保温12 h,自然冷却到室温。将收集的绿色粉末先用去离子水洗3遍,7 500 转离心3 min。然后用乙醇洗两遍,9 000转离心3 min,再放入烘箱50 ℃干燥12 h,收集粉末得到α-Ni(OH)2纳米片。
(2)g-C3N4材料的制备:10 g尿素((NH2)2CO)在马弗炉中以2 ℃/min的升温速率升至550 ℃,保温2 h,然后以5 ℃/min的降温速率降到室温,得到的g-C3N4材料为淡黄色粉末。
(3)α-Ni(OH)2/g-C3N4复合材料的制备:将0.03g g-C3N4加入装有30 mL去离子水的烧杯中,将其超声处理30 min形成均一溶液。随后向溶液中加入5 mmol尿素((NH2)2CO),1.25 mmol乙酸镍(Ni(CH3COO)2·4H2O),1.25 mmol十六烷基三甲基溴化铵(CTAB, C16H33(CH3)NBr),在加热搅拌器上48 ℃加热搅拌40 min,之后将反应物放入50 mL反应釜中。将反应釜放入烘箱加热至120 ℃并保温12 h,然后自然冷却到室温。干燥后的粉末先用去离子水离心沉淀洗3遍,转速为7 500 r/min,再用乙醇清洗两遍,转速为9 000 r/min,放入烘箱50 ℃干燥12 h。采用上述方法分别制备了g-C3N4含量为8%,20.6%和56.6%(质量分数)的g-C3N4/α-Ni(OH)2复合材料, 初步进行电催化碱性析氧测试后发现含量为20.6%(质量分数)-g-C3N4/α-Ni(OH)2的样品具有最好的OER性能,因此进一步对 20.6%(质量分数)-g-C3N4/α-Ni(OH)2样品的形貌与性能进行表征测试。
1.2 材料表征与性能测试
(1)材料表征:采用日本株式会社理学公司的Miniflex 600型X射线衍射仪分别测定g-C3N4,α-Ni(OH)2以及α-Ni(OH)2/g-C3N4样品衍射峰的出峰位置和出峰强度,与XRD标准卡片特征峰对比,得到样品的物质组成。扫描范围为 5°~80°,步长为0.02°。g-C3N4,α-Ni(OH)2以及α-Ni(OH)2/g-C3N4样品经干燥以后,采用美国FEI公司的FEI Nova NanoSEM 230型扫描电子显微镜(SEM)观察样品表面形貌。
(2)电化学性能测试:称取10 mg样品α-Ni(OH)2/g-C3N4加入1 mL去离子水,1 mL乙醇,20 μL萘酚,搅拌12 h,将得到的样品涂到玻碳电极上空冷干燥12 h。所有电化学性能测试在上海辰华 CHI760E 电化学工作站上进行,电极电化学性能测试采用三电极体系,参比电极为汞/氧化汞(Hg/HgO)电极,石墨碳棒对电极,制备所得电极作为工作电极。电解液为1 mol/L KOH水溶液。在电化学性能测试前以30 mV/s的扫描速率用循环伏安法在0~0.7 V区间内扫描至曲线稳定,析氧极化曲线扫描区间为0~0.8 V,扫描速率为5 mV/s。电化学活性面积(ECSA)的分析通过测定不同扫描速率(2,0, 10,15,20,30,40,50 mV/s)下的CV曲线的2Cdl值来比较材料的ECSA,选取的测试区间为0.5~0.6 V。交流阻抗测试(EIS)在开路电压0.66 V下进行,振幅为5 mV,工作频率为0.1 Hz~100 kHz。采用计时电位法进行电化学稳定性测试,以10 mA·cm-2电流密度进行恒电流测试,测得计时电位曲线,测试时长为12小时。α-Ni(OH)2,g-C3N4测试方法相同。
2 结果与讨论
2.1 X射线衍射分析
图1为g-C3N4,α-Ni(OH)2/g-C3N4复合材料以及α-Ni(OH)2的XRD谱图。通过一步煅烧法所得g-C3N4样品在2θ角为13.1°和27.2°出现衍射峰,其分别为CN衍生物(即melon类物质)和共轭芳香物层间堆积的特征峰,分别对应(100)和(002)晶面,表明所合成样品为类石墨状结构。图中纯α-Ni(OH)2的XRD衍射图谱中衍射峰的位置与相对强度与标准α-Ni(OH)2的标准PDF卡片(JCPDS No. 38-0715)完全吻合,表明所得样品为纯相α-Ni(OH)2。在α-Ni(OH)2/g-C3N4复合材料的XRD测试结果中,在11.3°,22.9°,33.7°,35.2°位置的特征峰分别对应α-Ni(OH)2的(003),(006),(101),(012)晶面,位于27.4°的特征峰对应g-C3N4的(002)晶面(JCPDS No.87-1526)。除此之外,样品无其它杂峰。通过对比可以看出,复合材料的峰位置分别与g-C3N4和α-Ni(OH)2的衍射峰一一对应,峰的位置与种类无明显变化,证明复合后材料未发生明显的结构或相改变。
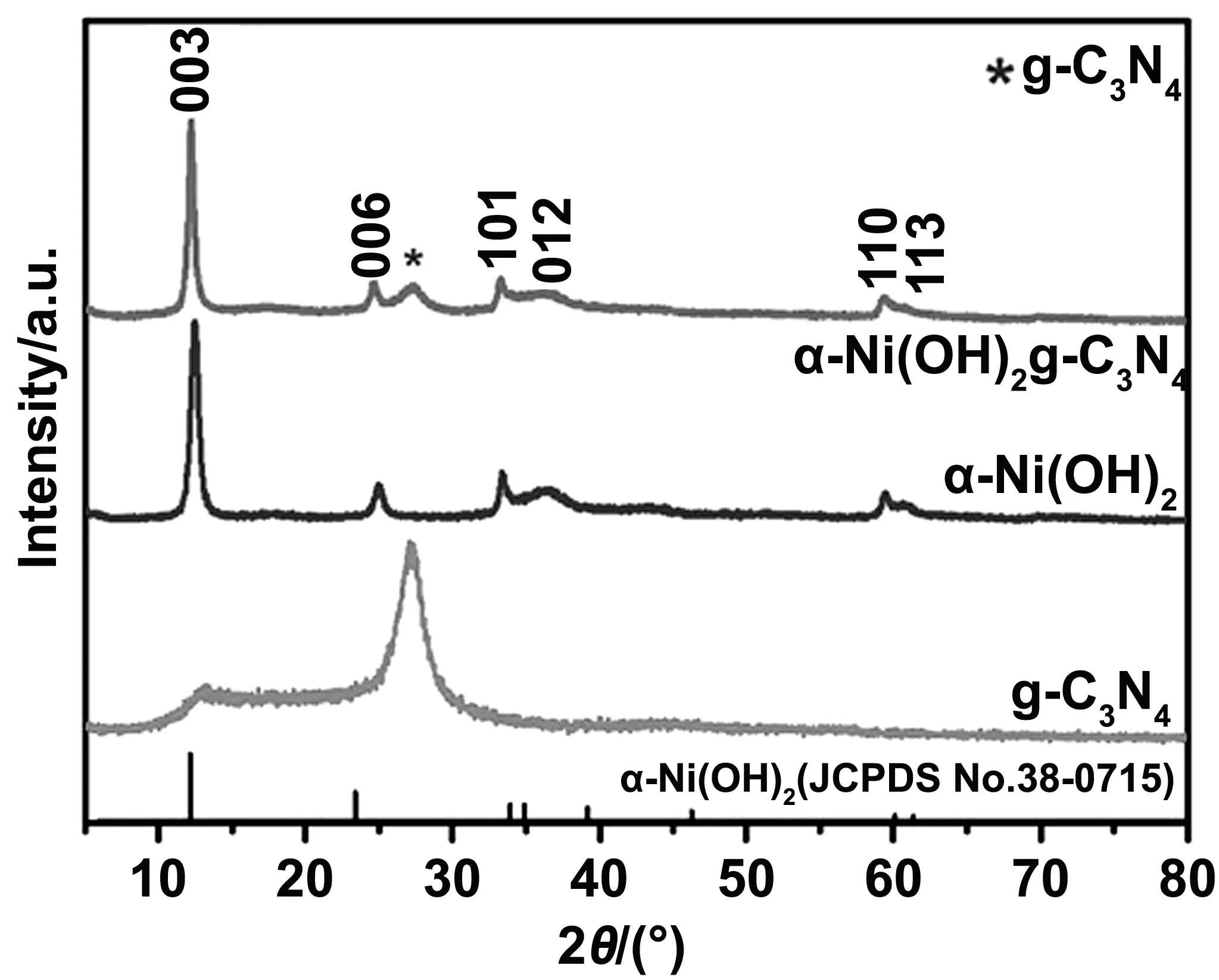
图1 α-Ni(OH)2/g-C3N4,g-C3N4及α-Ni(OH)2的X射线衍射图谱Fig 1 X-ray diffraction patterns of α-Ni(OH)2/g-C3N4, g-C3N4 and α-Ni(OH)2
2.2 扫描电镜分析
图2(a)为采用水热法合成的α-Ni(OH)2的SEM图像。由图可以看到合成的α-Ni(OH)2呈表面光滑的方片状,尺寸约1-4 μm,厚度约50 nm,大小不均一且呈堆叠状,不利于活性位点的暴露。图2(b)为g-C3N4的SEM图像,可以看出g-C3N4为微米级的表面褶皱众多的二维片状结构,这种形貌使其具有较大的比表面积。图2(c)为同样方法合成的 α-Ni(OH)2/g-C3N4复合材料。从图中可以看出细小的α-Ni(OH)2纳米片均匀地分散在g-C3N4表面,尺寸约100 nm。对比图2(a)与(c)可以看出,α-Ni(OH)2与g-C3N4具有很高的结合度,形成了高效复合的 α-Ni(OH)2/g-C3N4纳米复合结构,比表面积较大,三维立体结构明显,有利于电化学性能的提升。此外,与g-C3N4复合后α-Ni(OH)2片尺寸明显减小且大小均一,分散性明显变好,证明复合后的材料有效解决了水热合成的Ni(OH)2尺寸较大、易堆积的问题。

图2 (a) α-Ni(OH)2、(b) g-C3N4 (c)α-Ni(OH)2/g-C3N4(摩尔比为1/0.24)复合材料扫描电镜图Fig 2 SEM images of α-Ni(OH)2, g-C3N4 and α-Ni(OH)2/g-C3N4(1/0.24)
2.3 电化学性能测试
图3(a)为在5 mV/s扫描速率下,g-C3N4,α-Ni(OH)2及α-Ni(OH)2/g-C3N4(20.6%(质量分数))线性扫描极化曲线。可以看出,α-Ni(OH)2/g-C3N4在电化学测试过程中电流随电压的增加上升最快,表现出最优异的电催化性能,明显优于g-C3N4和α-Ni-(OH)2。图3(b)为3种样品在10 mA/cm2电流密度下所对应的过电位,其中α-Ni(OH)2/g-C3N4的析氧过电势为333.5 mV,g-C3N4为474.5 mV,αNi(OH)2为376.5 mV,α-Ni(OH)2/g-C3N4复合材料的过电位与α-Ni(OH)2相比降低了43 mV。为探究催化剂析氧反应过程中的动力学特征,通过LSV曲线,根据塔菲尔公式拟合得到的塔菲尔曲线如图3(c)。Tafel公式为η=a+blgj,其中b为斜率,斜率越小表示样品动力学性能越好,反应越易进行[19]。由图3(c)中可以看出α-Ni(OH)2/g-C3N4复合材料的塔菲尔斜率为92.1 mV/dec,明显小于g-C3N4的147.6 mV/dec和α-Ni(OH)2的126.6 mV/dec,表明α-Ni(OH)2/g-C3N4复合材料具有较快的反应动力学速率,证实其性能的提高。进一步对3种材料进行电化学交流阻抗测试,如图3(d)所示。可以看到,三者的电解质溶液电阻Rs非常接近,表明所有的催化剂在电化学过程中所处的测试环境基本相同。从阻抗结果来看,α-Ni(OH)2/g-C3N4复合材料具有最小的电荷转移电阻,表明其在电化学反应中电子与质子的传输速率最快。结合Tafel斜率和EIS分析可知,α-Ni(OH)2与g-C3N4复合能够加快反应动力学过程和提高电子传输速率,这主要是由于α-Ni(OH)2分散于g-C3N4表面上能有效降低团聚作用,暴露更多的活性位点,有益于提高催化效率;同时,α-Ni(OH)2/g-C3N4纳米复合结构拥有较大的比表面积,电解液能够对电极表面进行有效浸润与渗透,加快电荷转移,有利于反应中间体的吸附脱附,进一步表现为更优异的OER催化性能。此外,α-Ni(OH)2与g-C3N4的可能存在协同作用,有助于加速析氧过程的电荷转移,提高材料导电性,进而使反应速率提升。表1为其他报道中基于Ni(OH)2的电催化剂析氧性能,对比可知α-Ni(OH)2/g-C3N4与商用RuO2[21]相比仍有较大差距,其性能优于与泡沫镍复合的Ni(OH)2[20],与α-Ni(OH)2空心球[21]相当。

表1 本工作所制备样品与其他报道中基于Ni(OH)2的电催化剂OER性能比较结果
为进一步探究所制备催化剂的显著催化性能差异,通过双电层电容的循环伏安法测试,研究三种样品的电化学活性面积(ECSA)。在无法拉第电流的电位范围内进行不同扫速的CV测试,通过计算充电电流密度与放电电流密度的差值(Δj=ja-jc)。Δj与扫描速率之间呈现出线性关系,它们的斜率是双电层电容的2倍(2Cdl),对于理想的双电层电容而言,2Cdl与ECSA呈线性关系,因此,可用2Cdl来代表电化学活性面积。所得的双电层电容曲线如图4(a)所示,计算得出α-Ni(OH)2/g-C3N4复合材料的2Cwdl值为9.37 mF/cm2,比起α-Ni(OH)2的7.16 mF/cm2有明显提升,表明复合后的α-Ni(OH)2/g-C3N4具有更大的电化学活性面积,其活性位点数较多,这也是其电催化析氧性能提高的一个重要原因。
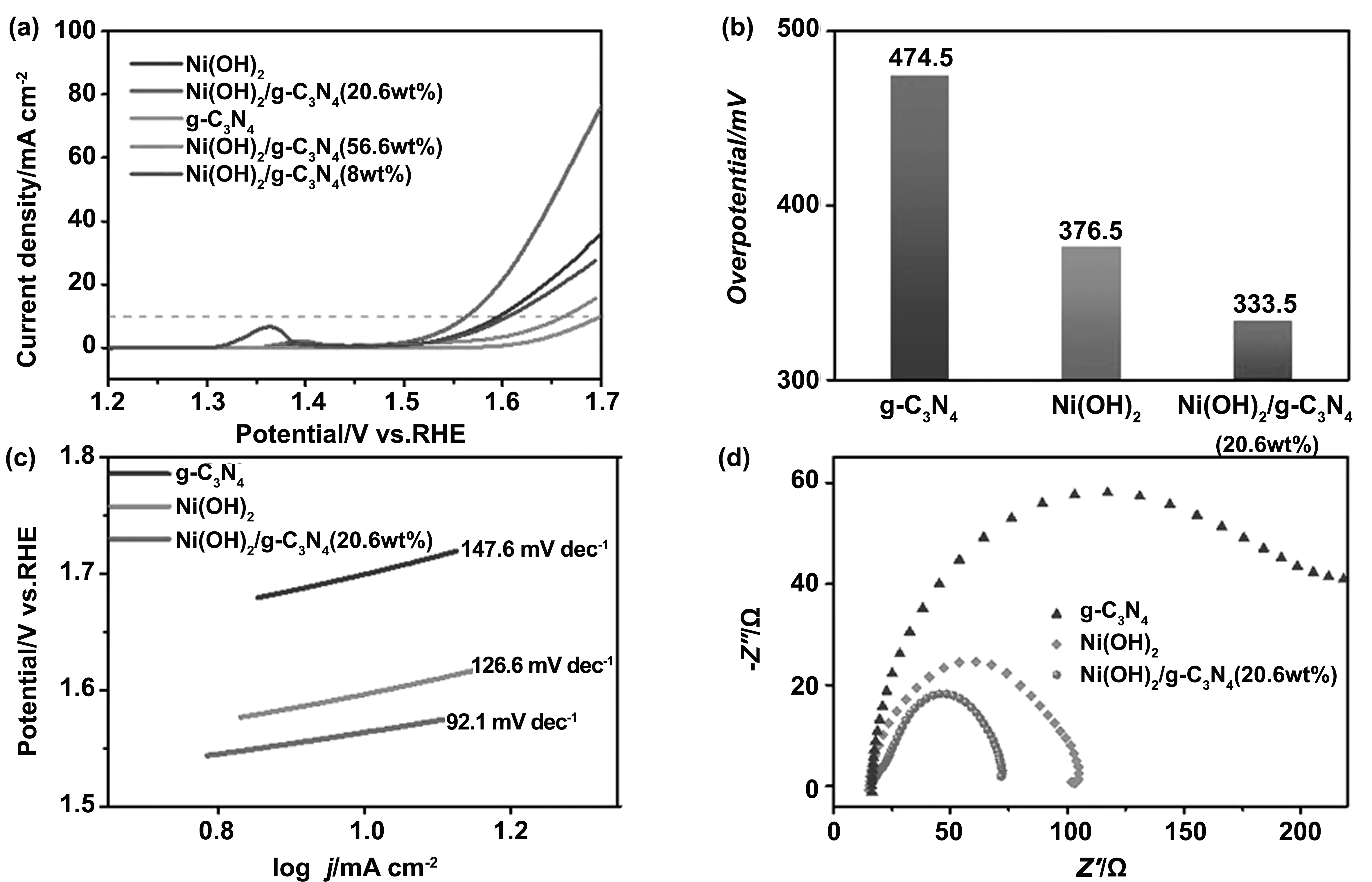
图3 (a)g-C3N4,α-Ni(OH)2/g-C3N4,α-Ni(OH)2线性扫描极化曲线(扫描速率:5 mV/s,电解液:1 mol/L KOH;(b)过电势柱状图; (c)塔菲尔斜率图; (d) g-C3N4,α-Ni(OH)2/g-C3N4,α-Ni(OH)2奈奎斯特曲线(电压条件: 1.65 V(相对可逆氢电极),工作频率:105~0.1 Hz)Fig 3 (a) Polarization curves for g-C3N4, α-Ni(OH)2/g-C3N4, α-Ni(OH)2 on glassy carbon(Sweep rate: 5 mV/s. Electrolyte: 1mol/L KOH); (b) overpotentials to yield 10 mA/cm2; (c) Tafel plots; (d) Nyquist plots of g-C3N4, α-Ni(OH)2/g-C3N4(20.6 wt%), α-Ni(OH)2 (105 Hz to 0.1 Hz)
对于析氧催化剂,稳定性也是重要参数之一。通过计时电位法在10 mA/cm2的电流密度下进行恒电流测试来验证电极材料的电催化稳定性。如图4(b)所示,在10 mA/cm2的电流密度下,α-Ni(OH)2的电位在1.6V处保持6h后急速上升,说明此时材料可能发生氧化反应而变性。α-Ni(OH)2/g-C3N4复合材料则在1.56 V保持9 h后开始缓慢上升,在12 h后达到1.6 V,说明α-Ni(OH)2/g-C3N4复合材料碱性条件下稳定性明显优于α-Ni(OH)2。原因可能是g-C3N4具有较强的耐酸/碱环境能力[19],且具有较好的机械强度,对整个纳米复合结构起到支撑作用,减缓催化过程中α-Ni(OH)2团聚的同时还防止催化剂从工作电极脱落,从而提高了催化剂的稳定性与耐久性。
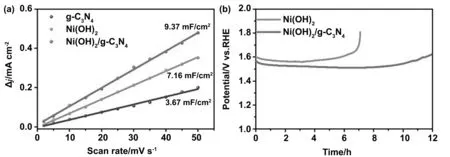
图4 (a)充电电流密度与放电电流密度差值与扫描速率之间的线性关系图;(b)电流密度为10 mA/cm2的条件下,α-Ni(OH)2/g-C3N4(20.6wt%),α-Ni(OH)2计时电位分析曲线Fig 4 Current density differences plotted against scan rates and chronopotentiometric curves for α-Ni(OH)2/g-C3N4(20.6 wt%) and α-Ni(OH)2 to yield 10 mA/cm2
3 结 论
(1)通过水热法合成了α-Ni(OH)2/g-C3N4复合材料,将α-Ni(OH)2纳米片生长于g-C3N4基底,能够明显降低α-Ni(OH)2的尺寸,分散性明显变好,比表面积增大;
(2)复合材料α-Ni(OH)2/g-C3N4具备优越的电催化性能,其中g-C3N4含量为20.6%(质量分数)的样品在10 mA/cm2电流密度下的析氧过电势为333.5 mV,显著优于纯相g-C3N4和α-Ni(OH)2,OER性能优异;
(3)复合材料α-Ni(OH)2/g-C3N4结构拥有较大的比表面积,能减缓团聚,暴露更多的活性位点,增强电化学活性面积以及催化剂的稳定性,使得α-Ni(OH)2/g-C3N4具有较低的塔菲尔斜率和较小的电化学阻抗,提高了其电催化析氧性能。
