传统及趁鲜加工工艺对荆芥饮片质量的影响
2020-12-08刘雨晴许凤清吴德玲廖延武赵宏苏
刘雨晴,许凤清,2,吴德玲,2,廖延武,张 伟,2,赵宏苏
(1.安徽中医药大学药学院,安徽 合肥 230012;2.中药饮片制造新技术安徽省重点实验室,安徽 合肥 230012)
荆芥始载于《神农本草经》,来源于唇形科植物荆芥SchizonepetatenuifoliaBriq. 的干燥地上部分[1],是临床常用辛温解表药。其性温、味辛,以全草入药,具有解表散风、透疹、消疮之功效,主治风寒感冒、咽喉肿痛及多种皮肤病[2-3]。荆芥主要含有挥发油、黄酮、单萜苷类、甾体等化学成分[4-5]。现代药理研究[6-7]表明,荆芥在抗感染和抗病毒方面具有较好的疗效。
传统荆芥饮片生产加工过程中涉及清洗、软化工序,与水较长时间接触,一方面会导致荆芥中亲水性有效成分流失,另一方面软化切制后的二次干燥也会使荆芥中挥发性成分丢失,从而影响荆芥饮片的质量[8]。因此,荆芥作为一种富含挥发油类成分的全草类药材,其饮片的切制加工工艺对保证其质量优劣起决定性作用。有研究[9]表明,新鲜药材在产地采收后就趁鲜加工成饮片,对于提高中药饮片的质量具有十分重要的意义。2015年版《中华人民共和国药典》以挥发油和胡薄荷酮作为荆芥质量控制的主要指标。现有研究[10-11]表明,荆芥中黄酮类成分之一的橙皮苷具有抗感染、抗病毒、抗氧化等多种药理活性,荆芥总黄酮亦具有抗肿瘤等作用[12-13]。因此,本研究以荆芥饮片挥发油、胡薄荷酮、橙皮苷及总黄酮含量作为指标,通过综合评分法建立荆芥药材及饮片的质量评价标准,并利用正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)比较传统加工与趁鲜加工方式对荆芥饮片质量的影响,旨在探讨趁鲜加工的合理性与可行性。
1 仪器与试药
1.1 仪器 水分测定装置:湘潭市三星仪器有限公司;挥发油测定器:湘潭市三星仪器有限公司;岛津LC-2030C 3D型高效液相色谱仪:日本岛津公司;ME204E电子天平:梅特勒·托利多仪器有限公司;TU-1810紫外可见分光光度计:北京普析通用仪器有限公司;RHP-100型高速多功能粉碎机:浙江永康市荣浩工贸有限公司;HH-6型数显恒温水浴锅:常州普天仪器制造有限公司;KQ-500DE型数控超声波清洗器:昆山市超声仪器有限公司。
1.2 试药 胡薄荷酮对照品(批号 YBF18052406,纯度≥98%)、橙皮苷对照品(批号 YBF18052412,纯度≥98%):购于南京元宝峰医药科技有限公司;芦丁标准品(批号 100080-201610,纯度≥92.6%):购于中国食品药品检定研究院;甲醇、乙腈为色谱纯:德国默克公司;水为纯净水;其他试剂均为分析纯。
荆芥药材于2018年9月13日采自国家中药标准化荆芥种植基地——安徽省亳州市十八里荆芥种植基地,经安徽中医药大学刘守金教授鉴定为唇形科植物荆芥SchizonepetatenuifoliaBriq新鲜地上部分。将原药材割取荆芥地上部分,除去杂质,晒干。传统加工饮片:将原药材喷淋清水,洗净润透,于50 ℃烘1 h,切段,阴干干燥后即得。趁鲜加工饮片:将荆芥新鲜植株除去杂质,经过自然干燥至五成干,切段,阴干干燥即得。
2 方法与结果
2.1 挥发油及胡薄荷酮含量测定 依照2015年版《中华人民共和国药典》,分别取荆芥原药材、传统加工饮片、趁鲜加工饮片对挥发油及胡薄荷酮进行含量测定[3],结果见表1。
2.2 总黄酮的含量测定
2.2.1 对照品溶液的制备 取芦丁对照品适量,置于50 mL量瓶中,加甲醇溶解,配制成每1 mL含228.84 μg的对照品溶液。
2.2.2 供试品溶液的制备 取荆芥饮片粉末(过2号筛)0.5 g,精密称定。置于100 mL具塞磨口三角瓶中,加入甲醇25 mL,密塞,称定质量。水浴加热回流30 min,放置室温,加甲醇补足减失的质量,滤过,取续滤液,即得。
2.2.3 测定方法 取芦丁对照品溶液或供试品溶液,置于25 mL量瓶中,加水至10 mL,加5%亚硝酸钠溶液1 mL,摇匀,放置6 min,再加10%硝酸铝溶液1 mL,摇匀,放置6 min,续加4%氢氧化钠溶液10 mL,加水定容至刻线,摇匀,放置15 min[13],以相应试剂为空白,进行全波长扫描,结果表明供试品溶液的最大吸收在500 nm处,且阴性对照品无干扰。在该条件下测定吸收度A,计算总黄酮的含量,结果见表1。
2.2.4 线性关系的考察 精密吸取“2.2.1”项下的对照品溶液2、3、4、5、6、7 mL,自“置于25 mL量瓶中”起,按“2.2.3”方法制备系列浓度的芦丁对照品溶液,以浓度(ρ)为横坐标,吸光度(A)为纵坐标,绘制标准曲线,标准曲线为A=0.011 6ρ+0.012 9,r=0.999 9,线性范围为18.307~64.075 μg/mL。
2.3 橙皮苷含量的测定
2.3.1 色谱条件 色谱柱:SinoChrom ODS-BP(4.6 mm×250 mm,5 μm)。流动相采用乙腈-0.05%磷酸水梯度洗脱程序:0~19 min,20%乙腈;19~20 min,20%→85%乙腈;检测波长为283 nm,柱温30 ℃,流速为1.0 mL/min。色谱图见图1。
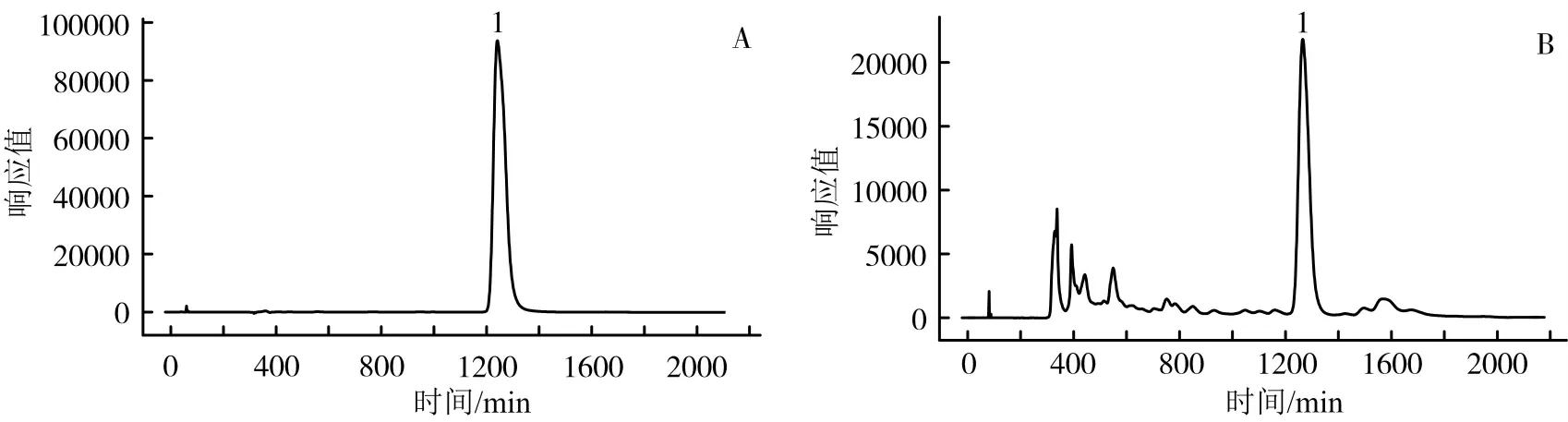
图1 橙皮苷标准品(A)及荆芥样品(B)的高效液相色谱图(1代表橙皮苷)
2.3.2 对照品溶液的制备 精密称取橙皮苷对照品适量,加甲醇制成每1 mL含121.48 μg的对照品溶液。
2.3.3 供试品溶液的制备 精密称取荆芥饮片样品粉末(过2号筛)0.5 g,置于三角锥形瓶中,加甲醇25 mL,密塞,称定质量,回流30 min,放冷,称定质量,加相应溶剂补足减失的质量,摇匀,经0.45 μm滤膜滤过,取续滤液制成供试品溶液。
2.3.4 线性关系的考察 精密吸取橙皮苷对照品溶液,以甲醇稀释成不同浓度按“2.3.1”项下色谱条件进样10 μL,以橙皮苷进样浓度(ρ)为横坐标,以峰面积(A)为纵坐标,进行线性回归分析,得线性方程A=19.11ρ+17.328,r=0.999 9(n=6),表明橙皮苷在3.80~121.48 μg/mL的范围内线性关系良好。
2.3.5 含量测定 取18批荆芥样品,按照“2.3.3”项下方法制备供试品溶液,按照“2.3.1”项下色谱条件进行测定,计算样品中橙皮苷的含量,结果见表1。
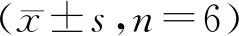
表1 不同加工方式荆芥饮片及药材挥发油、胡薄荷酮、总黄酮、橙皮苷含量
2.4 综合评分法分析 将上述各组样品的挥发油、胡薄荷酮、总黄酮及橙皮苷含量测定结果进行加权综合评分。以各指标的最大值为参照,对各组数据进行归一化处理,再按各指标的重要性,给出权重系数。以挥发油含量(A,%,权重系数0.3)、胡薄荷酮含量(B,%,权重系数0.3)、总黄酮含量(C,%,权重系数0.2)、橙皮苷含量(D,%,权重系数0.2)为综合考察指标,计算各组样品综合评分值,结果见表2。由表中结果可知,原药材综合评分最高,趁鲜加工次之,最后是传统加工,表明不同加工方式的荆芥质量存在一定的差异。
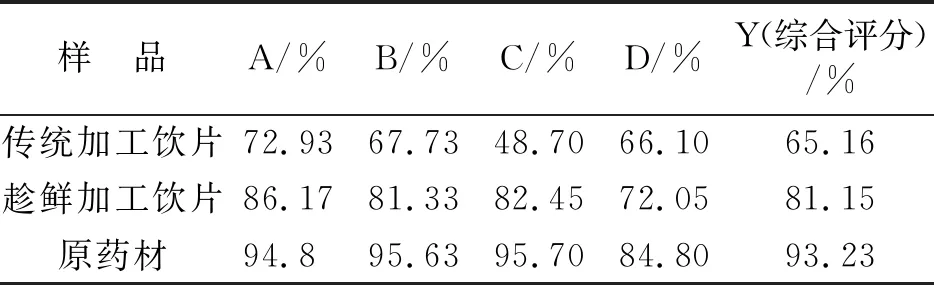
表2 不同加工方式荆芥饮片及药材
2.5 OPLS-DA 将归一化处理后的各组数据,采用SIMCA14.1软件进行OPLS-DA研究,散点得分图见图2。图中趁鲜加工饮片与原药材聚为一类,传统加工饮片单独聚为一类,说明相比传统加工工艺而言,趁鲜加工饮片与原药材的质量更为接近,更大程度上保留了药材中有效成分。此外,对模型中变量重要性投影(variable importance projection,VIP)参数进行分析,发现挥发油、总黄酮、橙皮苷3个指标VIP值均大于1,说明3种成分是形成荆芥各组样品间差异的主要因素,且贡献率大小依次为总黄酮、橙皮苷、挥发油,表明荆芥中黄酮类成分在加工过程中变化较为显著。见图3
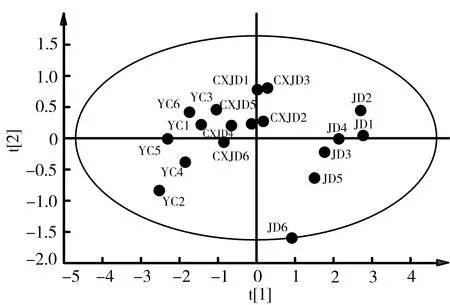
注:JD:传统加工饮片;CXJD:趁鲜加工饮片;YC:原药材
3 讨论
本实验考察了趁鲜加工与传统加工工艺对荆芥中挥发油、胡薄荷酮、总黄酮和橙皮苷含量的影响,利用综合评分法对各样品质量进行评价。荆芥原药材总体质量最好,其次是趁鲜加工饮片,最后是传统加工饮片。
比较传统加工与趁鲜加工结果可以发现,两种工艺所制得的饮片中挥发油和胡薄荷酮含量均符合《中华人民共和国药典》的要求,趁鲜加工饮片各指标成分的含量和综合评分均高于传统加工饮片,说明趁鲜加工饮片总体质量优于传统加工饮片;利用OPLS-DA法对数据分析可以得知,趁鲜加工饮片质量更接近原药材质量,而传统加工饮片质量橙皮苷、总黄酮、挥发油等多种成分均有显著差异,与原药材质量差距较大,模型中的VIP参数表明加工过程中橙皮苷和总黄酮在区分三者中起到重要作用。
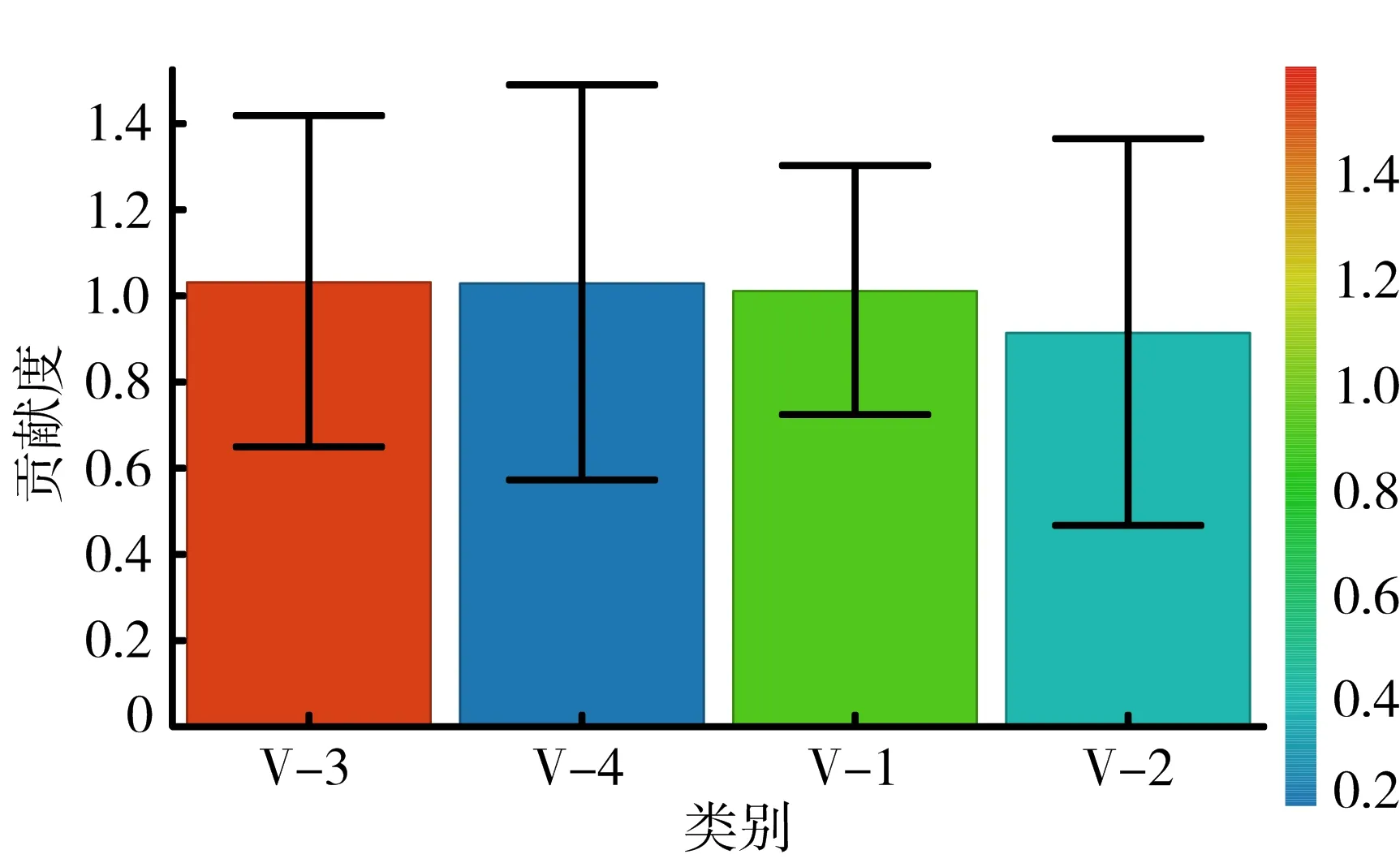
注:V-1.挥发油;V-2.胡薄荷酮;V-3.总黄酮;V-4.橙皮苷
上述结果表明,荆芥饮片趁鲜加工在保证饮片质量上具有较高的可行性。综合生产成本、生产效率及不同指标的质量评价结果,荆芥趁鲜加工工艺可行性最高。后期应利用现代分析检测技术和统计分析方法,在继承传统经验鉴别指标的基础上,引入表征荆芥内在品质的指标,还需对趁鲜加工的加工干燥方式,产地趁鲜加工工艺条件开展进一步研究进一步优化,对干燥方法等方面进一步开展深入研究,完善并规范趁鲜加工荆芥饮片生产工艺流程,保障荆芥饮片质量均一、稳定、可控,从而进一步完善荆芥药材趁鲜加工工艺流程,以期为荆芥饮片趁鲜加工生产提供理论依据。
