亚麻籽油增强小鼠免疫功能的研究
2020-12-07董和亮郭嘉欣白坤颖赵娟
董和亮 郭嘉欣 白坤颖 赵娟


摘 要:目的:研究亚麻籽油对小鼠免疫力功能的影响。方法:测定亚麻籽油中亚麻酸的含量,以高、中、低剂量组给予小鼠30 d灌胃实验,分析测定碳粒廓清实验,迟发型变态反应,抗体生成细胞实验,腹腔巨噬鸡红细胞实验,淋巴细胞转化实验,NK细胞活性测定。结果:亚麻籽油对小鼠的体重、脏器/体重比值、血清溶血素以及单核巨噬细胞功能无显著影响(P>0.05);与对照组比较,高剂量组能够显著提高小鼠的细胞免疫功能,如淋巴细胞转化、迟发型变态反应、NK细胞活性(P<0.05)。结论:亚麻籽油对小鼠具有增强免疫力的功能。
关键词:亚麻籽油;小鼠;免疫功能;亚麻酸
Abstract:Objective: To study the effect of linseed oil on the immune function of mice. Method: The content of linolenic acid in linseed oil was analyzed, and linseed oil were used as high, medium and low dose groups to give mice a 30 d gavage experiment to analyze and determine carbon Clearance test, delayed type allergy, antibody-producing cell test, chicken macrophage cell test, lymphocyte transformation test, NK cell activity determination. Results: Linseed oil had no significant effect on the body weight, organ/weight ratio, serum hemolysin and mononuclear macrophage function of mice (P>0.05); compared with the control group, the high-dose group could significantly improve the mice Cellular immune function, such as lymphocyte transformation, delayed type allergy, NK cell activity (P<0.05). Conclusion: Linseed oil has the function of enhancing immunity in mice.
Key words:Linseed oil; Mice; Immune function; Linolenic acid
中圖分类号:TS201.4
亚麻籽油中的亚麻酸对维持和提高正常的生理功能、预防疾病及患病风险具有积极的作用[1-3]。随着人们健康意识的提高,各类营养补充剂不断兴起,亚麻酸已成为重要的食品与保健品原料[4]。亚麻籽油富含人体所需的必需脂肪酸,可弥补日常饮食中脂肪酸摄入量不足,解决比例失衡的问题[5-7]。鉴于饮食中不饱和脂肪酸的缺乏,市场上出现了各种脂肪酸保健品。亚麻籽油作为丰富亚麻酸的植物来源,目前关于其对免疫力的影响尚处于空白阶段,亟需理论研究支持[8-10]。
基于亚麻籽油表现出的功能特性,本文分析测定了亚麻籽油中亚麻酸的含量,并以小鼠为研究对象,依据保健食品检验与技术评价规范,采用碳粒廓清实验,迟发型变态反应,抗体生成细胞实验,腹腔巨噬鸡红细胞实验,淋巴细胞转化实验,NK细胞活性测定等方法,研究分析亚麻籽油对小鼠免疫力的影响,以期阐明亚麻籽油的免疫调节过程及调节途径,为其全面利用和开发亚麻籽油提供科学指导和理论依据,为开发功能保健食品提供借鉴。
1 材料与方法
1.1 实验材料与动物
亚麻籽油,由山西五台山沙棘制品有限公司提供,为浅黄色至黄色液体。体重18~22 g清洁级ICR雌性小鼠200只,由上海莱斯克实验动物有限责任公司提供,许可证号:SCXK(沪)2012-0002。饲料,由上海普路腾生物科技有限公司提供,许可证号:沪饲证(2014)04001
1.2 仪器设备
8 mm直径打孔器,微量血凝试验板,2-16K通用离心机,RT-6100酶标仪,96孔培养板,Co-150 CO2培养箱,UV-1800紫外可见分光光度计,OlympusIX71倒置显微镜,电子天平,显微镜。
1.3 主要试剂
注射用墨汁,刀豆蛋白A(ConA),MTT,DNFB,丙酮,麻油,SRBC,生理盐水,鸡红细胞,羊红细胞,甲醇,Giemsa染色,YAC-1细胞,Hanks液(pH7.2~7.4),RPM11640完全培养液,乳酸锂,碘硝基氯化四氮唑(INT),吩嗪二甲酯硫酸盐(PMS)、NAD、Tris-HCL缓冲液(pH8.2),1%NP40,台酚兰,1 mol·L-1盐酸,酸性异丙醇等。
1.4 方法
1.4.1 亚麻酸含量的测定
(1)待测样品制备。准确称取油脂样品50 mg移入10 mL小容量瓶内,向其中加入3 mL正己烷与苯混合溶液(1∶1比例),并轻轻摇晃使其混合均匀。再加入2 mL NaOH-CH3OH溶液,充分振荡使其混合均匀后,在常温下静置30 min,向容量瓶内添加一定量去离子水使容量瓶内原有的有机溶剂升至瓶口,静置5 min待稳定后,吸取上清液进行气相色谱-质谱联用仪分析[11]。
(2)测定方法。将100 m×0.25 mm×0.20 μm的HP-88型号毛细管柱连接到6890/5973安捷伦气质联用仪上。氦气作为载气,载气压力保持在100 kPa,进样模式选择split,分流比设为1∶30,流速为1 mL·min-1,注射温度定为250 ℃,EI作为为离子源(温度设为230 ℃),将四级杆温度设为150 ℃,传输温度设为250 ℃,并在50~550 amu的范围、电离压力为70 eV的条件下进行扫描。扫描升温过程如下:将仪器的初始温度设为80 ℃并保持5 min;以10 ℃·min-1的速度升至150 ℃,保持2 min;再以5 ℃·min-1的速度升至230 ℃,保持10 min;整个分析过程持续40 min。采用外标法测定油样,每个样品重复测定3次。根据脂肪酸甲酯标准品保留时间及面积归一法计算脂肪酸的相对含量。
1.4.2 受试样品及配制
亚麻籽油的成人日推荐量为3 g,即0.05 g·kg-1 BW(成人体重以60 kg计)。按日推荐量的5倍、10倍、30倍配制受试样品浓度分别为0.15、0.05和0.025 g·mL-1的高、中、低剂量组,以食用大豆油作为对照组。临用前称取亚麻籽油15 g与食用大豆油混合均匀至100 mL,为高剂量组;取高剂量组样品40 mL,与食用大豆油混合均匀至120 mL,为中剂量组,取中剂量组样品40 mL,与食用大豆油混合均匀至80 mL,作为低剂量组。
1.4.3 动物分组与给药
参照韩飞方法,200只小鼠随机分成5大组,再分成4小组,每小组10只小鼠,分别进行体重、空斑、溶血素测定、脏器指数,NK活性、淋转试验,DTH试验,小鼠碳粒廓清试验,小鼠腹腔巨噬鸡红细胞试验。按每日10 mL·kg-1 BW连续灌胃30 d后,分别进行试验。
1.4.4 小鼠体重的测定。
标记每只小鼠,记录小鼠的初始体重和终期体重。
1.4.5 碳粒廓清实验测定
在最后一次给予受试物24 h后,称小鼠体重,小鼠尾部静脉注入稀释的印度墨汁,2 min、10 min后,取内眦静脉血20 μL,并立即加入2 mL 0.1%NaCO3溶液中,以NaCO3溶液为空白对照,在600 nm处测定OD值,将小鼠处死后,取出肝脏、脾脏后称重,计算吞噬指数a[12]。
式(1)(2)中:K-碳粒廓清指数,表示吞噬速率;OD1-t1时的吸光度值;OD2-t2时的吸光度值;t1-给墨汁后第2次取血的时间;t2-给墨汁后第2次取血的时间;a-吞噬指数,反映每单位组织质量的吞噬活性。
1.4.6 迟发型变态反应(DTH)检测
在最后一次给予受试物24 h后,对小鼠腹部皮肤约3 cm×3 cm进行脱毛处理,用50 μL的DNFB溶液涂抹均匀致敏;5 d后,再以10 μL的上述溶液均匀涂抹小鼠右耳。24 h后,颈椎脱臼处死小鼠,剪下左右耳,用打孔器取下直径8 mm的耳片称重[13]。
1.4.7 体液免疫功能测定
在最后一次给予受试物24 h后,腹腔注射0.2 mL 2%(V/V)SRBC悬液。5 d后,进行血清溶血素检测和抗体生成细胞检测。
(1)抗体生成细胞的测定。颈椎脱臼处死小鼠,取脾脏,经磨碎、过滤、离心,洗涤后悬浮于8 mL Hanks液中。取25 μL脾细胞悬液、50 μL 10%SRBC、0.5mL 0.5%的琼脂糖Hanks液混合培养基迅速混匀,倾倒于6 cm已刷琼脂薄层的平皿上,于CO2培养箱中温育1.5 h,然后用SA缓冲液稀释的补体(1∶8)加入,温育3 h后,统计溶血空斑数[14]。
(2)血清溶血素的测定。将小鼠摘除眼球采血,2 000 r·min-1离心10 min进行血清的分离,用生理盐水稀释不同倍数并置于微量血凝板内,每孔100 μL,加入同体积的0.5%(v/v)的SRBC悬液,混匀,37 ℃温箱孵育3 h,观察血球凝集程度[15]。
1.4.8 小鼠腹腔巨噬鸡红细胞实验(半体内法)和脏器/体重比值
在最后一次给予受试物24 h后,腹腔注射1 mL 20%鸡红细胞悬液。30 min后,颈椎脱臼处死动物,固定在鼠板上剪开腹壁皮肤,经腹腔注入2 mL生理盐水,转动鼠板1 min。吸出1 mL腹腔洗液,滴于2片载玻片上,移置37 ℃温育30 min。生理盐水漂洗、晾干、固定、染色、蒸馏水漂洗晾干。在油镜下阅片计数,计算吞噬率和吞噬指数。
吞噬率(%)=(吞噬鸡红细胞的巨噬细胞数/计数的巨噬细胞数)×100 (3)
吞噬指数=被吞噬的鸡红细胞总数/计数的巨噬细胞数 (4)
取脾脏及胸腺,称重,计算胸腺指数和脾指数[16]。
胸腺指数=胸腺重量(mg)/体重(g) (5)
脾脏指数=脾脏重量(mg)/体重(g) (6)
1.4.9 ConA诱导的小鼠淋巴细胞转化实验和小鼠NK细胞活性测定
在最后一次给予受试物24 h后,颈椎脱臼法处死小鼠,无菌取脾,置于无菌的适量Hanks液的小平皿中,用镊子轻轻将脾撕碎,过200目筛网,为单细胞悬液。
(1)ConA诱导的小鼠淋巴细胞转化实验。参照杨迪[17]的方法,并做适当修改,将上述细胞悬液经离心,调整浓度为3×106个/mL。分两孔加入24孔培养板中,每孔1 mL,一孔加75 μL ConA液,另一孔为对照,培养72 h。培养68 h时,每孔吸去0.7 mL上清液,并加入同体积不含小牛血清的RPMI 1640培养液与50 μL的MTT,继续培养。培养结束后,分装于96孔培养板,3个平行孔,于570 nm处测定OD值。
(2)小鼠NK细胞活性测定(乳酸脱氢LDH测定法)。参照王晓林的方法[18]。试验前24 h将靶细胞传代培养,Hanks液洗3次,RPMI1640培养液调整细胞浓度为4×105个/mL。弃上清液将细胞浆弹起,加入0.5 mL灭菌水20 s,裂解红细胞后再加入0.5 mL 2倍Hanks液及8 mL Hanks液,离心10 min(1 000 r·min-1),用1 mL完全培养液重悬,用1%冰醋酸稀释后计数,染色计数,调整细胞浓度为2×107个/mL。取靶细胞和效应细胞各100 μL(效靶比为50∶1),加入96孔培养板中;靶细胞自然释放孔加靶细胞和培养液各100 μL、靶細胞最大释放孔加靶细胞和1%NP40各100μL,上述各项均设3个平行孔,于37 ℃、5% CO2培养箱中培养4 h,然后将培养板1 500 r·min-1离心5 min,每孔吸取上清液100 μL置于96孔培养板中,并加入同体积的LDH基质液,反应3min,每孔加入30 μL 1 moL·L-1的HCl,于490 nm处测定OD值。
1.5 数据处理
实验数据以Origin作图,SPSS软件进行单因素方差分析。经方差齐性检验,方差齐的实验数据采用LSD法进行统计分析,方差不齐的实验数据采用Tamnane法进行统计分析。
2 结果与分析
2.1 亚麻籽油中亚麻酸含量测定
亚麻籽油中含丰富的营养成分如维生素E、甾醇等[3-6]。另外,亚麻籽油中亚麻酸含量较高,大量研究认为,亚麻酸具有降低心血管疾病的作用,对提高身体机能具有积极的影响,是目前最理想的单一植物油脂[7-9],因此,测定分析样品中亚麻酸的含量。图1为亚麻籽油脂肪酸气相色谱图,经测定分析本实验中采用的亚麻籽油中亚麻酸含量高达44.0%。
2.2 亚麻籽油对小鼠体重的影响
亚麻籽油对小鼠体重的影响见表1。由表1可知,30 d灌胃试验结束后,低剂量组小鼠的体重最高为33.2 g,与对照组比较,高、中、低各剂量组小鼠的体重均无显著差异(P>0.05),说明亚麻籽油对小鼠体重无影响。
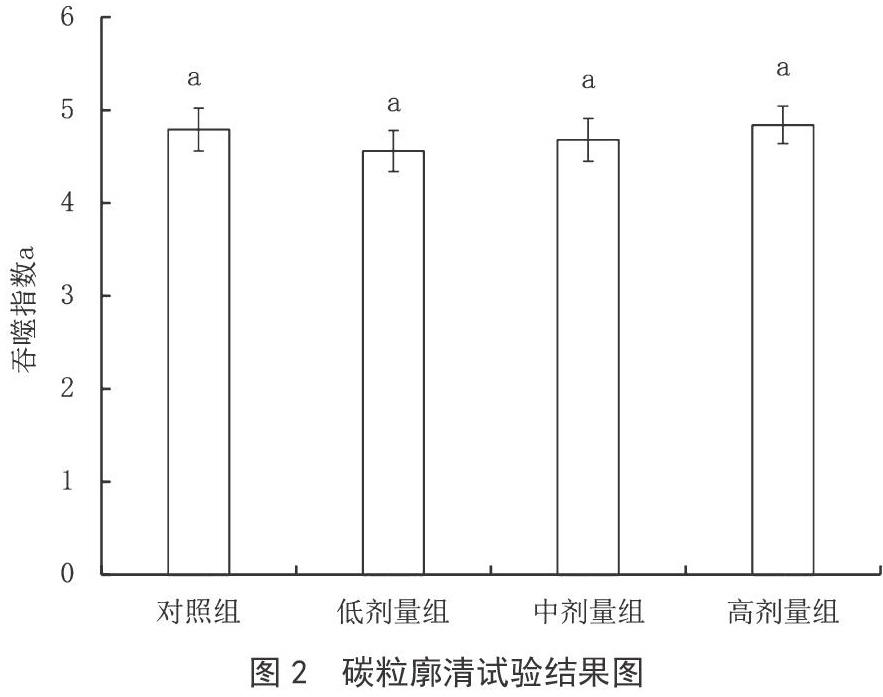
2.3 小鼠碳粒廓清试验
图2为小鼠的碳粒廓清试验,由图2可知,高、中、低各剂量组小鼠碳粒廓清吞噬指数a与对照组比较,差异均不显著(P>0.05)。其中,高剂量组的吞噬指数a最高为4.82,低剂量组的吞噬指数a最低为4.56。
2.4 迟发型变态反应实验
表2为DTH测定结果,由表2可知,高剂量组小鼠左右耳肿胀度差最高为22.2 mg,明显高于对照组,差异显著(P<0.05),而中、低剂量组与对照组相比,差异不显著(P>0.05)。
2.5 体液免疫功能测定
2.5.1 抗体生成细胞检测试验
小鼠抗体生成细胞检测试验结果如图3所示。由图3可知,与对照组比较,高剂量组与中剂量组具有显著的差异(P<0.05),低剂量组与对照组比较,差异不显著(P>0.05)。
2.5.2 血清溶血素试验
血清溶血素试验结果如图4所示。由图4可知,各剂量组小鼠抗体积数与对照组比较,差异均不显著(P>0.05)。
2.6 小鼠腹腔巨噬细胞吞噬鸡红细胞试验
巨噬细胞功能主要为吞噬作用,其代表着多个器官的免疫潜能。巨噬细胞吞噬试验结果见表3。由表3可知,高、中、低各剂量组小鼠腹腔巨噬细胞吞噬鸡红细胞的吞噬率、转换值及吞噬指数与对照组比较,差异不显著(P>0.05)。
2.7 脏器/体重比值的测定
正常时各脏器与体重的比值比较恒定。当动物染毒后,受损脏器重量可能发生改变,从而引起脏体比的变化。各剂量组胸腺指数、脾指数的测定结果见表4,由表4可知,与对照组比较,高、中、低各剂量组均无显著差异(P>0.05)。说明亚麻籽油对小鼠的脏器/体重比值无影响。其中P为概率值,取值在0~1之间,其数值越小,说明置信度就越高。由表4可知,P值均大于0.05,说明实验各组无差异,进一步说明受试样品亚麻籽油对小鼠的脏器/体重比值无影响。
2.8 细胞免疫功能测定
表5为ConA诱导的小鼠淋巴细胞转化试验结果,由表5可知,与对照组比较,低剂量组和中剂量组小鼠淋巴细胞转化OD值差异不显著(P>0.05),而高剂量组小鼠淋巴细胞转化OD差值明显高于对照组,差异显著(P<0.05)。说明亚麻籽油具有增强细胞免疫的功能。
2.9 NK细胞活性测定
NK细胞活性测定结果见表6。由表6可知,高剂量组小鼠NK细胞活性明显高于对照组,NK细胞活性提高了21.6%,差异显著(P<0.05),而中、低剂量组与对照组比较,差异不显著(P>0.05)。
3 结论
经30 d灌胃试验后,与对照组比较,高、中、低各剂量组小鼠体重,胸腺指数,脾指数,小鼠血清溶血素水平,碳粒廓清能力,小鼠腹腔巨噬细胞吞噬鸡红细胞的吞噬率和吞噬指数均无统计学意义(P>0.05),而亚麻籽油高剂量组能够明显增强ConA诱导的小鼠脾淋巴细胞增殖能力和DNFB诱导的小鼠迟发型变态反应,能显著提升小鼠抗体生成能力及小鼠NK细胞活性,说明亚麻籽油可提高小鼠的细胞免疫和体液免疫功能。根据《保健食品检验与评价技术规范》(卫生部2003)的规定,说明亚麻籽油具有增强小鼠免疫功能的作用,其可用于食品、保健食品提高免疫力等功能產品的开发和应用。
参考文献:
[1]禹晓,黄沙沙,程晨,等.不同品种亚麻籽组成及抗氧化特性分析[J].中国油料作物学报,2018,40(6):879-888.
[2]吕俊丽,马雪慧,王华.微波预处理对亚麻籽油得率及其贮藏稳定性的影响[J].中国油脂,2020,45(6):13-17.
[3]左洋,陆学茸,滕英来,等.亚麻籽环肽HPLC分析和氧化还原产物研究[J].中国油脂,2015,40(8):32-36.
[4]Addis C C,Koh R S,Gordon M B. Preparation and Characterization of a Bio-based Polymeric Wood Adhesive Derived from Linseed Oil[J].Elsevier Ltd,2020,102:102655.
[5]Ferlay A,Chilliard Y.Effect of linseed, sunflower, or fish oil added to hay-, or corn silage-based diets on milk fat yield and trans-C18:1 and conjugated linoleic fatty acid content in bovine milk fat[J]. Livestock science,2020,235:104005.
[6]利嘉祥,连莹君,张参,等.乙醇萃取-HPLC法快速分析亚麻籽油中四种环肽研究[J].粮食与食品工业,2016,23(2):8-12,18.
[7]Kazemi-Bonchenari M,Dehghan-Banadaky M,Fattahnia F,et al. Effects of Linseed Oil and Rumen Undegradable Protein:Rumen Degradable Protein Ratio on Performance of Holstein Dairy Calves[J]. Pubmed,2020,123(11):1-35.
[8]Gou Z Y,Cui X Y,Li L.Effects of Dietary Incorporation of Linseed Oil with Soybean Isoflavone on Fatty Acid Profiles and Lipid Metabolism-Related Gene Expression in Breast Muscle of Chickens[J]. Pubmed,2020,14(11):2414-2422.
[9]Szyd?owska-Czerniak A,Tymczewska A,Momot M. Optimization of the Microwave Treatment of Linseed for Cold-Pressing Linseed Oil - Changes in Its Chemical and Sensory Qualities[J].Elsevier Ltd,2020,126:109317.
[10]Sevda S G,Mohammad A,Hamed J,et al.
Effect of Flaxseed oil Supplementation on the Erythrocyte Membrane Fatty Acid Composition and Endocannabinoid System Modulation in Patients with Coronary Artery Disease:a Double-Blind Randomized Controlled Trial[J].Genes & nutrition,2020,15(1):59-69.
[11]廖麗萍,肖爱平,冷鹃,等.不同产地亚麻籽冷榨油脂肪酸的GC-MS分析[J].中国麻业科学,2018,40(5):234-238.
[12]Kanchan S,Balwinder S,Amritpal K,et al.Influence of Microwave Roasting on Chemical Composition,Oxidative Stability and Fatty Acid Composition of Flaxseed (Linum usitatissimum L.) oil[J]. Pubmed,2020,326(6):82-93.
[13]韩飞,马广强,熊魏,等.牛至油增强小鼠免疫功能的实验研究[J].中国医院药学杂志,2020(10):1106-1110.
[14]陈小英,曾晏萍,刘汉儒,等.太子参须多糖粗提物对小鼠免疫功能的调节作用[J].西南大学学报(自然科学版),2020,42(4):56-64.
[15]刘威良,吴白芬,黄艾祥.两种提取工艺的辣木籽油对小鼠免疫活性的影响[J].中国油脂,2020,45(6):92-96.
[16]喻建辉,周明良,余春涛,等.蜂胶对调节小鼠免疫功能的影响[J].农产品加工,2020(10):22-26.
[17]杨迪,李丽杰,张曾亮,等.南极磷虾油灵芝孢子油纳米乳复合物提高小鼠的免疫功能[J].现代食品科技,2020,36(5):14-21,50.
[18]王晓林,戴鹂莹,邸松,等.刺芪参胶囊对小鼠免疫功能的影响[J].现代食品,2020(5):162-166.
