γ刀分次立体定向放射治疗对非小细胞肺癌脑转移瘤的临床疗效及剂量学探讨
2020-12-05李亚杰郭少贤吕冠群韩世强宋桂芳
李亚杰 郭少贤* 吕冠群 韩世强 宋桂芳 赵 媛
脑转移瘤是指在患者中枢神经系统之外的肿瘤细胞经过转移而移至脑组织,是一种比较常见的恶性肿瘤,约占脑部肿瘤的13%左右[1]。据统计,约有20%~40%的癌症患者会出现脑转移,因此需要探索一种对脑转移瘤更加安全高效的治疗方法[2]。全脑放射治疗(whole brain radiation therapy,WBRT)是目前临床中对脑转移瘤进行治疗的一种标准方法,但因受到正常脑组织的耐受量限制,使其临床应用明显受限,依旧有30%~50%的患者因为颅内病变未能得到有效控制或复发,约50%~70%的患者因为颅外病灶发生进展而死亡[3]。目前,临床中对肺癌脑转移瘤的治疗依旧存在部分争议,并无标准的诊治规范[4]。因此,如何维持患者生存质量的同时有效避免或者延缓复发,使患者获得较长的生存期,依旧是目前临床中对肺癌脑转移患者进行治疗的重点及难点[5]。
γ刀立体定向放射外科(stereotaxic radio surgery,SRS)治疗能够显著增加肿瘤病灶靶区的局部照射剂量,降低其对周围正常组织的照射剂量,其优势为低损伤、高疗效、高剂量及高精度等,且具有适形的特点,逐渐成为临床肿瘤学界的一项研究热点[6]。γ刀SRS治疗对术后复发、不能进行手术切除或者很难耐受手术的患者都能够有效缩小瘤体,改善患者的临床症状,延长生存期,提高局部控制率[7]。为此,本研究对非小细胞肺癌(non-small cell lung cancer,NSCLC)脑转移瘤患者使用γ刀SRS分次进行治疗,取得了比较满意的效果。
1 资料与方法
1.1 临床资料
选取2017年10月至2019年5月解放军联勤保障部队第981医院住院治疗的64例NSCLC脑转移瘤患者,其中男性37例,女性27例;年龄34~76岁,平均年龄(56.8±5.6)岁;腺癌患者36例,鳞癌患者21例,混合型癌、大细胞癌或者其他病理类型癌患者7例。所有患者均进行γ刀SRS分次治疗。患者及家属均知情同意本研究,一般资料具有可比性,本研究经医院伦理委员会批准。
1.2 纳入与排除标准
(1)纳入标准:①患者均为原发病NSCLC,术前经影像学技术确诊脑转移,且颅内病灶可测量;②患者转移瘤总体积≤15 cm;③患者未接受头颅放射治疗。
(2)排除标准:①患者存在其他重大疾病,如免疫系统、血液系统;②患者存在精神障碍;③患者不能进行手术。
1.3 仪器设备
采用SGS-I型γ刀设备(深圳海波公司);Unicorn 3D的计划系统(深圳市海博科技有限公司)。
1.4 治疗方法
对64例NSCLC脑转移瘤患者进行WBRT,使用6 MV X射线在全脑的两侧对穿野等进行中心照射,剂量为30~40 Gy,对肿瘤靶区进行γ刀分次SRS[3]。采用超级伽马刀以及Unicorn 3D的计划系统。对患者进行头部固定面模的制作,定位X射线计算机断层扫描(computed tomography,CT)并增强扫描,层厚为3 mm,使用工作站将扫描的资料进行三维重建[8]。患者体内肿瘤的体积测量使用磁共振成像(magnetic resonance imaging,MRI)图像并进行再定位增强CT的勾画,其中计划靶体积是在肿瘤的体积基础之上进行三维外放3 mm[9]。根据患者的身体状况、肿瘤最大直径以及肿瘤位置等病情进行个体化治疗方案的制定,采取分次治疗的方法,单次靶区周边的剂量为3~5 Gy,总剂量为15~20 Gy,分3~5次完成。在患者治疗期间以及治疗完成后的3~5 d使用地塞米松以及20%的甘露醇进行颅内降压。
1.5 观察与评价指标
患者脑部局部控制情况评价标准[10]:在患者进行治疗后的1个月之后使用MRI进行复查,当患者的已知病灶全部消失,则视为完全缓解(complete remission,CR);当患者的体内肿瘤的最大垂直径以及最长直径的乘积之和减少为治疗前的50%以及以上,则视为部分缓解(partial response,PR);患者的病灶无明显变化则视为病灶稳定(stable disease,SD);当患者肿瘤的最大垂直径以及最长直径的乘积之和在原来的基础之上增加了25%或出现了新的病灶,则视为疾病进展(progressive disease,PD)。
观察患者的年龄、性别脑转移瘤的治疗方案、脑转移灶的数量、原发病灶是否被控制、卡氏功能量表(Karnofsky performance scale,KPS)评分、递归分隔分析(recursive partitioning analysis RPA)分级以及放射治疗得分指数(score index for radiotherapy,SIR)等因素对患者预后的影响[11]。观察患者在治疗过程中以及预后出现的不良反应。
1.6 统计学方法
应用SPSS18.0统计软件进行数据处理,正态分布的计量资料采用均数±标准差()表示,非正态分布的计量资料转化后采用均数±标准差()表示,采用独立样本t检验;计数资料以例数和百分率(%)表示,采用x2检验。多组间比较采用单因素方差分析,实施F检验,以P<0.05为差异有统计学意义。
2 结果
2.1 NSCLC脑转移患者近期治疗效果比较
(1)不同转移病灶直径疗效:64例NSCLC脑转移患者转移病灶直径≤3 cm(47例),CR为24例(占51.06),PR为17例(占36.17),SD为5例(占10.64),PD为1例(占2.13),治疗有效率为87.23%;直径>3 cm的(17例),CR为4例(占23.53),PR为6例(占35.29),SD为6例(占35.29),PD为1例(占58.82),治疗有效率为58.82%,两者比较差异有统计学意义(x2=5.269,P<0.05),见表1。

表1 64例不同脑转移病灶直径的NSCLC脑转移患者近期治疗效果比较[例(%)]
(2)不同转移病灶近期疗效:脑转移灶≤3个的治疗(51例),CR为25例(占49.02),PR为19例(占37.25),SD为5例(占9.80),PD为2例(占3.92),有效率为86.27%;脑转移灶>3个的(13例),CR为3例(占23.08),PR为4例(占30.77),SD为5例(占38.46),PD为1例(占7.69),治疗有效率为53.85%,两者比较差异有统计学意义(x2=5.526,P<0.05),见表2。

表2 64例不同脑转移病灶的NSCLC脑转移患者近期治疗效果比较[例(%)]
2.2 NSCLC脑转移患者生存时间因素比较
根据对64例患者1~24个月的随访结果,患者死亡34例,生存30例,中位生存期为10个月,其中患者年龄、性别病变数量、放射治疗剂量大小以及是否WBRT与患者的生存时间无明显影响,KPS、原发病灶是否被控制、是否存在其他转移、SIR以及RPA分级与患者生存时间存在相关性(r=0.124,r=0.136,r=-0.289,r=-0.262,r=-0.217;P<0.05),见表3~5。
2.3 NSCLC脑转移患者治疗后不良反应比较
在治疗过程中,64例患者有5例出现轻度恶心,7例食欲不振,4例头痛,经过激素治疗以及脱水治疗基本好转,未出现Ⅲ级神经系统的不良反应、脑梗死以及颅内出血等严重的并发症。
3 讨论
人颅脑内比较常见的一种恶性肿瘤是脑转移瘤,是癌症致死以及治疗失败的主要原因[12-13]。近年来,主要采用WBRT的方式对脑转移瘤患者进行治疗,但该种治疗方式只适合中位生存期为3~6个月的患者,对中位生存期较短的患者不适合[14]。NSCLC约占肺癌的80%,随着医学的发展,患者的生存时间随之延长,这也导致了NSCLC脑转移瘤的发生率提高。随着MRI技术的应用,在脑转移早期诊断、延长生存时间以及改善治疗效果方面被广泛应用,这一技术的应用也增加了癌症患者脑转移的发生率[15]。患者一旦出现脑转移瘤则表示患者的病情加剧,生存质量急剧下降,生存时间缩短,其自然生存时间只有1个月,使用常规的放射治疗和激素治疗已经起不到良好的效果,有些患者则不适合手术治疗,需要联合其他治疗方法。
表3 影响NSCLC脑转移患者生存时间的因素比较()
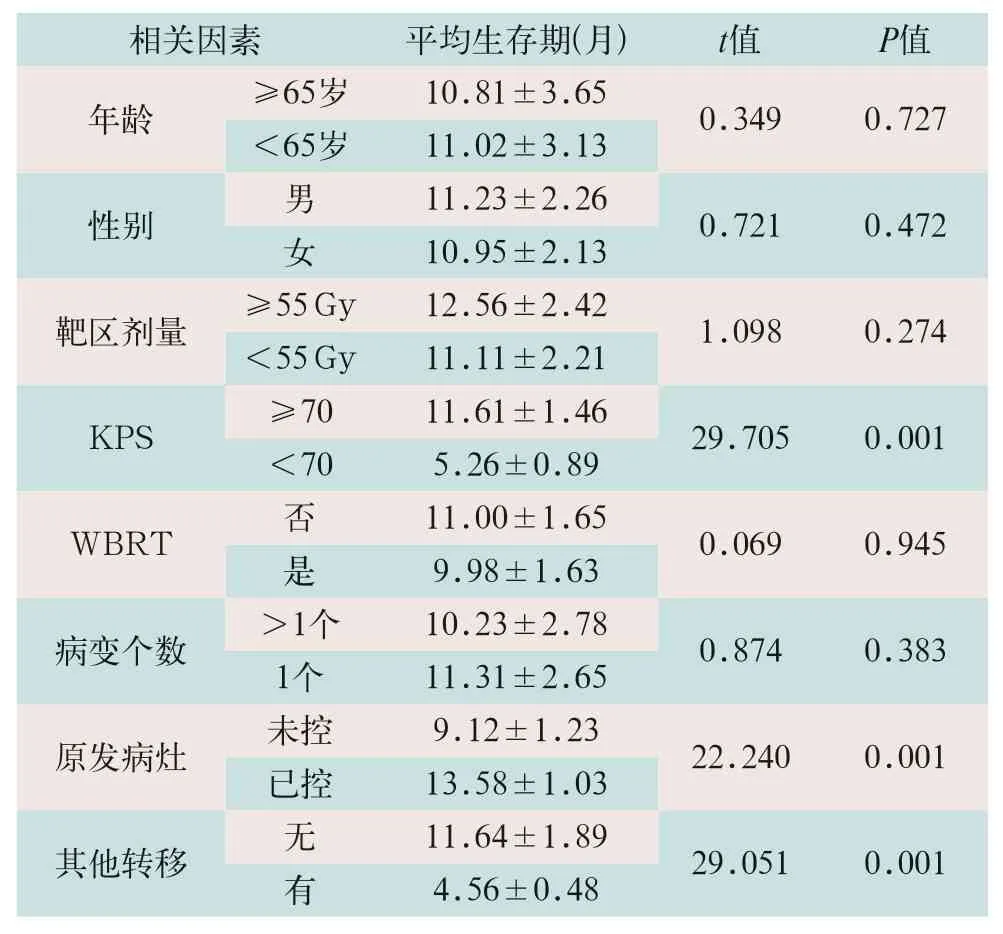
表3 影响NSCLC脑转移患者生存时间的因素比较()
注:表中KPS为卡氏功能量表;WBRT为全脑放射治疗
表4 影响NSCLC脑转移患者生存时间的单因素比较()
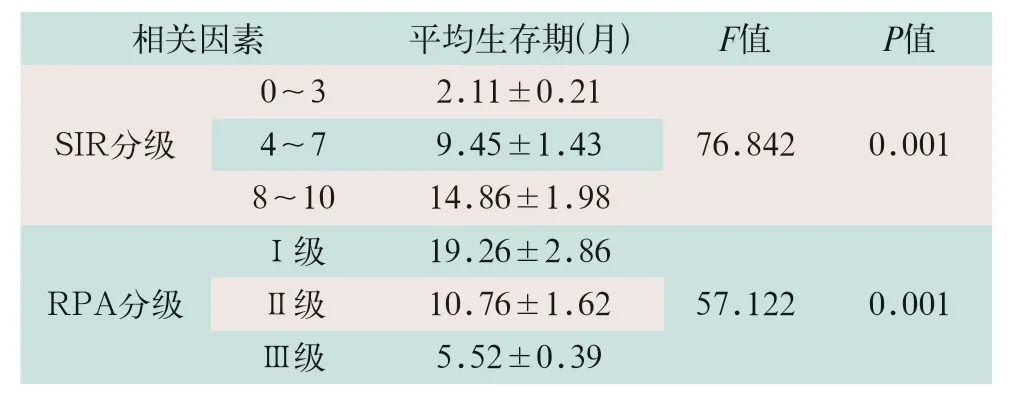
表4 影响NSCLC脑转移患者生存时间的单因素比较()
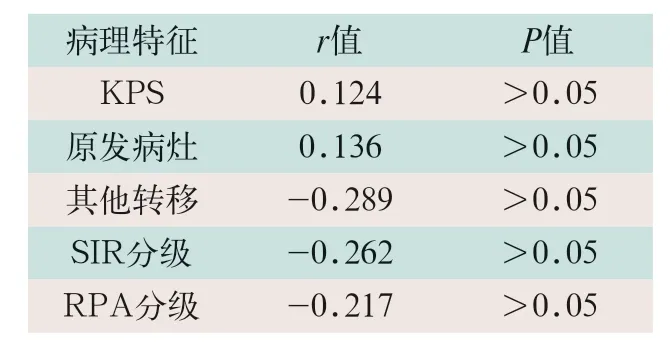
表5 影响患者生存相关性
NSCLC患者中约有70%会发生脑转移瘤,且肺癌的脑转移瘤治疗效果相对比较差,对于已经发生了脑转移的患者,目前主要采用WBRT进行治疗[16]。有资料表明,使用立体定向放射治疗能够减少患者的脑组织损伤,可以在一定程度上延长患者的中位生存期。在本研究中,对NSCLC脑转移瘤的患者使用γ刀分次立体定向放射治疗,使用6 MV X射线在全脑的两侧对穿野等进行中心照射,剂量为30~40 Gy,并在治疗期间以及治疗完成后使用地塞米松以及20%的甘露醇进行颅内降压。经过治疗后,64例NSCLC脑转移患者的病情呈现出不同程度的改善。使用WBRTL联合立体定向放射治疗,能够有效的改善患者的生活质量,改善神经症状以及功能,能够精确的对病变部位进行定位和放射治疗,缩短治疗时间,提高治疗有效率。
NSCLC脑转移瘤的发展速度相对较快,一旦发生转移,病情会急速恶化,中位生存期约为1~3个月[17]。在本次研究中,根据对患者随访1~24个月的结果,64例患者中34例死亡,生存30例,中位生存期为10个月,其中患者年龄、性别、病变数量、放射治疗剂量大小以及是否WBRT与患者的生存时间无明显影响,而影响患者生存的因素有KPS、原发病灶是否被控制、是否存在其他转移、SIR分级以及RPA分级。γ刀分次立体定向放射治疗能够给予病灶更大的生物剂量,提高了病灶的空置率和生存率,对患者的年龄、性别、病变是否WBRT与放射治疗剂量以及病变数量等因素要求不大,能够有效的提高中位生存期,延长患者的生存时间[18]。
NSCLC脑转移瘤患者在治疗过程中多存在预后效果不佳,出现多种不良反应[19]。使用手术和普通放射治疗进行治疗的患者虽然能够适当的延长生存时间,但是其风险较高,大多会出现脑水肿、恶心、头痛以及神经功能性障碍[20]。本研究患者治疗过程中,未出现Ⅲ级神经系统的不良反应、脑梗死以及颅内出血等严重的并发症。使用γ刀分次立体定向放射治疗,能够精准定位病灶,误差较小,产生的不良反应比较轻,在一定程度上提高患者的生活质量,减轻疾病带来的痛苦[21]。
4 结论
影响患者生存的因素有KPS、原发病灶是否被控制、是否存在其他转移、SIR以及RPA分级,而使用γ刀分次立体定向放射治疗对NSCLC脑转移瘤进行治疗,能够提高患者的治疗有效率,延长患者的生存时间,减轻不良反应的症状,有效改善患者生活质量。