柠檬籽粒中柠檬苦素离子液体双水相提取体系的优化与抗氧化活性分析
2020-12-04汪开拓蒋永波王富敏张帮奎
汪开拓 蒋永波 王富敏 张帮奎 马 莉 顾 欣
(1 重庆三峡学院生物与食品工程学院,重庆 404000;2 重庆汇达柠檬科技集团有限公司,重庆 402660)
柠檬[Citruslimon(L.)Burm.F.]为芸香科柑橘属常绿小乔木植物,其果实呈翠绿或亮黄色,果汁酸涩,富含维生素、矿物质、氨基酸和酚类等各种微量元素,兼具良好的食品加工特征和保健价值[1]。柠檬苦素是近年来被广泛研究的柠檬呈苦物质,属氧化性四环三萜类有机物。动物试验证实该化合物具有有效降低血脂、促进肠道菌落平衡、提高神经兴奋性、预防肿瘤和改善免疫力等功能,富集和开发价值极高[2]。但是,柠檬果实深加工过程中产生大量的碎籽,由于缺乏成熟的开发策略,现阶段只能被迫填埋或丢弃,造成巨大的资源损耗和环境污染。因此,高效分离和提取柠檬籽粒中的苦素类物质,对于柠檬资源综合开发极富现实意义[3]。
离子液体(ionic liquid)是由有机阳离子和无机或有机阴离子所构成的低沸点缓冲盐溶液,具有溶解性强、熔融优良和电离缓冲范围大等优点[4]。但单一离子液体性状稳定性差,通常将其与无机盐形成离子液体双水相体系,该体系具有挥发度和乳化性低、回收率高、平衡度高、易于放大等优点,可有效克服单一离子液体的缺点,现已被广泛用于高分子有机物的分离和纯化操作[5]。本研究拟首先从弱酸性离子液体双水相体系[BMG][BF4]/KH2PO4、[PHMG][PF6]/KH2PO4、[TMG][Br]/NaH2PO4和[TMG][Cl]/NaH2PO4中初筛出柠檬苦素最优提取体系,再优化相关操作工艺,以期获得从柠檬籽粒中高效提取柠檬苦素的方法,为柠檬苦素的工业化分离和纯化奠定基础。
1 材料与方法
1.1 材料与试剂
柠檬籽粒,由重庆市潼南区某柠檬深加工企业提供,以柠檬果实深加工后的破碎籽粒居多,粒径区间4.83±0.68 mm,含水量58.59%±3.73%;焦性没食子酸、绿原酸、芦丁、杨梅黄酮、槲皮素-3-o-芸香苷、柠檬苦素标准品(≥95%),美国Sigma公司;AB-8大孔吸附树脂,昆山市东鸿化工有限公司;乙腈、四氢呋喃,均为色谱纯,上海吉至生化科技有限公司;四甲基胍盐酸盐([TMG][Cl])、四甲基胍的溴酸盐([TMG][Br])、甲基丁基胍的四氟硼酸盐([BMG][BF4])、聚六亚甲基胍的六氟磷酸盐([PHMG][PF6]),上海彩佑实业有限公司;无水乙醇、石油醚、丙酮、磷酸二氢钠(NaH2PO4)、磷酸二氢钾(KH2PO4)、硫酸铵,均为分析纯,成都市科龙化工试剂厂;试验用水为重蒸水。
1.2 仪器与设备
HMB-700S小型研磨式超微粉碎机,弘荃机械企业有限公司;DH-300T试验筛,新乡市大汉振动机械有限公司;R201D旋转蒸发仪,上海锦赋实验仪器设备有限公司;DK-98-ⅡA电热恒温水浴锅、FW135中草药粉碎机,天津市泰斯特仪器有限公司;85-2数显恒温磁力搅拌器,金坛市双捷实验仪器厂;JC101电热鼓风干燥箱,南通嘉程仪器有限公司;PS-40Ultrasonic cleaner,深圳市洁康洗净电器有限公司;TDL-5-A低速大容量离心机,上海安亭科学仪器厂;752型紫外可见分光光度计,上海舜宇恒平科学仪器有限公司;Agilent 1100高效液相色谱仪,美国安捷伦公司。
1.3 试验方法
1.3.1 样品预处理 将柠檬籽粒在40~45℃条件下缓慢烘干至水分含量约10%,用超微粉碎机研磨粉碎,过300目筛得到干燥的柠檬籽粉末。然后将柠檬籽粉末加入10%乙醇溶液,调节液料比至15∶1,再加入0.5 mol·L-1柠檬酸调节pH值至4.8。最后加入0.15%混合水解酶(果胶酶∶纤维素酶∶淀粉酶=1∶1∶2)于35℃下水解8 h[6]。酶解结束后过滤得到酶解滤液转移到8 000~14 000截留分子量的透析袋中,置于2 000 倍体积以上的无菌蒸馏水中静置24 h以脱去微量无机盐,再将酶解液在40℃下减压(0.02~0.03 MPa)浓缩至原体积的10%,备用。
1.3.2 离子液体双水相提取方法及评价 选择4种弱酸性离子液体双水相体系,即[BMG][BF4]/KH2PO4、[PHMG][PF6]/KH2PO4、[TMG][Br]/NaH2PO4和[TMG][Cl]/NaH2PO4,这些溶液均为胍盐离子液体,具有一定分子识别能力,选择性较好。参考Lin等[7]的方法,配制浓度为1.5~2.5 mol·L-1[BMG][BF4]/1.8~2.0 mol·L-1KH2PO4、1.8~2.8 mol·L-1[PHMG][PF6]/0.8~1.0 mol·L-1KH2PO4、1.0~1.5 mol·L-1[TMG][Br]/1.2~1.5 mol·L-1NaH2PO4和0.5~1.5 mol·L-1[TMG][Cl]/1.2~1.5 mol·L-1NaH2PO4等4种胍盐离子液体双水相萃取体系,随后加入KBr,调节pH值至6.0。在1.3.1制备的浓缩酶解液中加入10倍上述各离子液体双水相溶液,随后置于40~80℃水浴锅中保温提取60~120 min,最后用0.5 mol·L-1柠檬酸调节溶液pH值至3.5(使柠檬苦素电离平衡后带正电并向离子相富集),在10℃下静置12 h待提取溶液分层,下层为水相,上层为离子相,分离上层离子相备用。向离子相溶液中加入30%~70%乙醇溶液进行萃取(液料比1∶15~1∶30),分离上层有机相,冷冻干燥(40 Pa、-50℃)后得到柠檬苦素粗粉,用40%乙醇溶液复溶,再用醋酸调节pH值至5.0,离心得到上清液再冷冻干燥后得到高纯度柠檬苦素粉末。
计算无机相和离子水相体积比(R)、柠檬苦素在双水相体系中的分配系数(KLimonin)及萃取率(YLimonin)[8]。比较各双水相系统对应分配系数和萃取率的大小,确定最佳的提取体系。相关计算公式如下:
KLimonin=CILimonin/COLimonin
(1)
YLimonin=[1/(1+R×KLimonin)]×100%
(2)
式中,CILimonin为无机相中柠檬苦素的质量浓度(mg·mL-1); COLimonin为有机相中柠檬苦素的质量浓度(mg·mL-1)。
1.3.3 单因素试验 根据1.3.2试验结果选择最优离子液体双水相萃取体系提取柠檬籽粒中柠檬苦素,分别以乙醇浓度50%、液料比20∶1、提取时间120 min、提取温度70℃为固定水平,提取温度设置为40、50、60、70、80℃,提取时间设置为60、90、120、150、180 min,萃取离子相柠檬苦素的乙醇溶液体积浓度设置为30%、40%、50%、60%、70%、80%,液料比设定为5∶1、10∶1、15∶1、20∶1、25∶1、30∶1,以乙醇萃取液中柠檬苦素含量为考察值,分析各因素对该离子液体双水相体系提取效率的影响。
1.3.4 响应面试验优化提取条件 在单因素试验结果的基础上,应用Design Expert 10.1软件中的Box-Behnken程序对提取工艺进行优化。以提取温度(X1)、提取时间(X2)、乙醇溶液体积浓度(X3)和液料比(X4)为自变量,以柠檬苦素含量为响应值(Y),设计试验因素与水平交互表(表1)。各组试验均重复3次,取平均值。
1.3.5 柠檬苦素含量测定 参照陈静等[9]的高效液相色谱法。使用Agilent 1100高效液相色谱仪测定,色谱柱reverse Nova-Pak C18分析柱(250 mm× 4.6 mm, 10 μm)。流动相为乙腈-四氢呋喃-水(体积比为17.5∶17.5∶65),流速0.5 mL·min-1,柱温30℃,进样量10 μL,在207 nm波长处检测,应用外标法定量

表1 Box-Behnken设计试验因素水平表Table 1 Independent factors and the levels used in Box-Behnken experimental design
分析提取液中柠檬苦素含量,结果以mg·g-1FW表示。
1.3.6 柠檬苦素抗氧化活性评价 将1.3.5提取的柠檬苦素乙醇提取液稀释至10、20、30、40、50 μg·L-1,选择代表性的水果酚酸(焦性没食子酸和绿原酸)、类黄酮(芦丁和杨梅黄酮)和花色苷(槲皮素-3-o-芸香苷)[10],同样配置浓度梯度均为10、20、30、40、50 μg·L-1的焦性没食子酸、绿原酸、芦丁、杨梅黄酮、槲皮素-3-o-芸香苷的乙醇溶液,横向比较柠檬苦素与这5种功能性物质在抗氧化活性方面的差异。
DPPH自由基清除率参考Yang等[11]的方法测定,ABTS+自由基清除率参照Schaich等[12]的方法测定,超氧阴离子和羟自由基清除率参照单科开等[13]的方法测定,结果均按自由基清除百分率表示;总还原力参照Oraiza[14]的方法测定,以反应液在600 nm波长处的吸光度值表示还原力水平;亚油酸过氧化抑制率参考Hinneburg等[15]的方法测定,结果以过氧化抑制百分率表示。
1.4 数据处理
采用Design Expert 10.1软件构建回归方程,通过方差分析计算各因素最佳水平,并预测最优柠檬苦素提取量。统计分析中显著水平为P<0.05,极显著水平为P<0.01。
2 结果与分析
2.1 双水相体系的选择
由表2~5可知,4种离子液体双水相体系下,各体系中柠檬苦素分配系数KLimonin均远小于1,说明柠檬苦素主要集中在离子相,在双水相体系下提取难度小;[TMG][Br]/NaH2PO4和[TMG][Cl]/NaH2PO4的KLimonin显著低于[BMG][BF4]/KH2PO4和[PHMG][PF6]/KH2PO4(P<0.05),且1.5 mol·L-1[TMG][Cl]/1.35 mol·L-1NaH2PO4双水相体系的K值最小,分配效率最高,分离效果最好。同时,4种离子液体双水相体系的柠檬苦素萃取率YLimonin值均在较高水平,其中Y值平均值较高的是[TMG][Br]/NaH2PO4和[TMG][Cl]/NaH2PO4体系,说明这2种体系对柠檬苦素的提取效果最好。通过比较表2数据,选择1.5 mol·L-1[TMG][Cl]/1.35 mol·L-1NaH2PO4离子液体双水相体系作为柠檬苦素提取剂,后续试验即优化该双水相萃取体系的最佳操作条件。
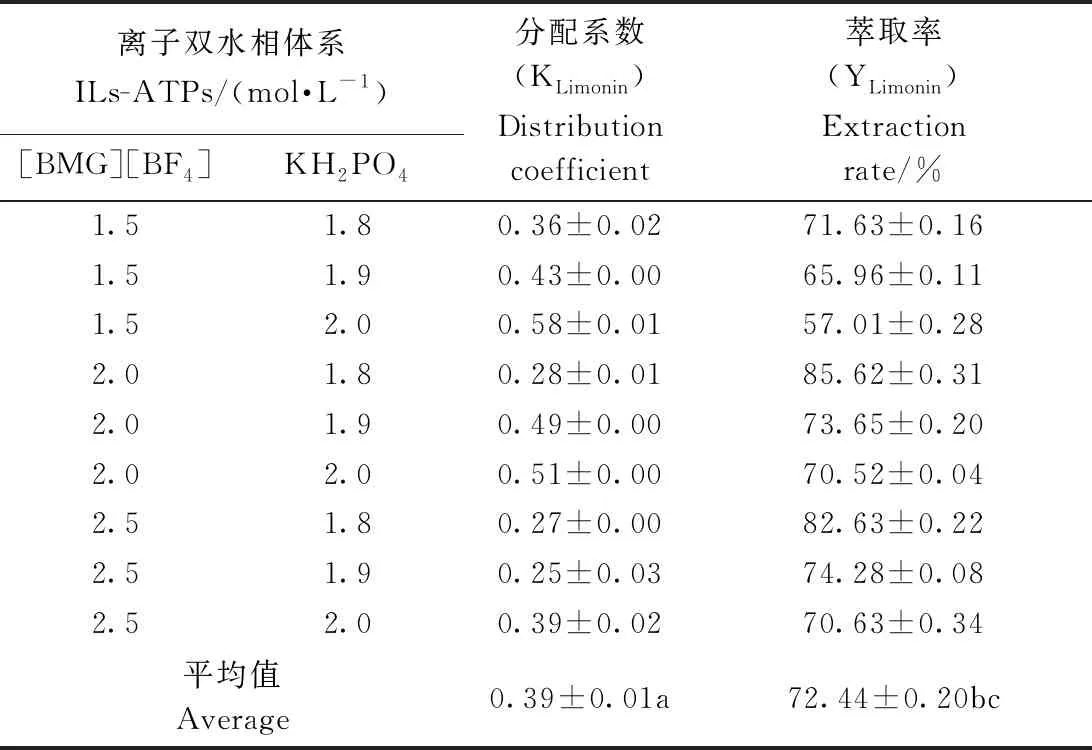
表2 [BMG][BF4]离子液体双水相体系对柠檬籽粒 中柠檬苦素提取效率的影响Table 2 Effects of [BMG][BF4] ionic liquid aqueous two-phase separation systems (ILs-ATPs) on extraction of limonin from lemon seeds

表3 [PHMG][PF6]离子液体双水相体系对 柠檬籽粒中柠檬苦素提取效率的影响Table 3 Effects of [PHMG][PF6] ionic liquid aqueous two-phase separation systems (ILs-ATPs) on extraction of limonin from lemon seeds
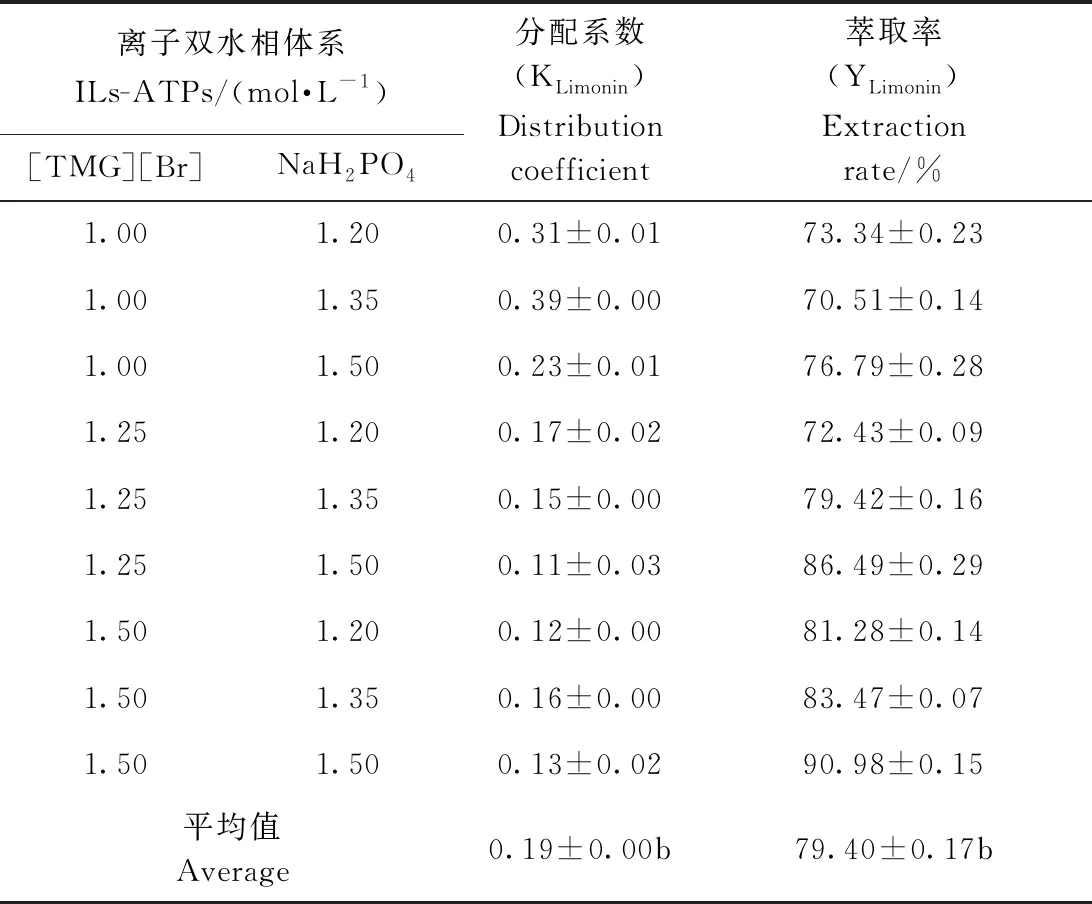
表4 [TMG][Br]离子液体双水相体系对 柠檬籽粒中柠檬苦素提取效率的影响Table 4 Effects of [TMG][Br] ionic liquid aqueous two-phase separation systems (ILs-ATPs) on extraction of limonin from lemon seeds
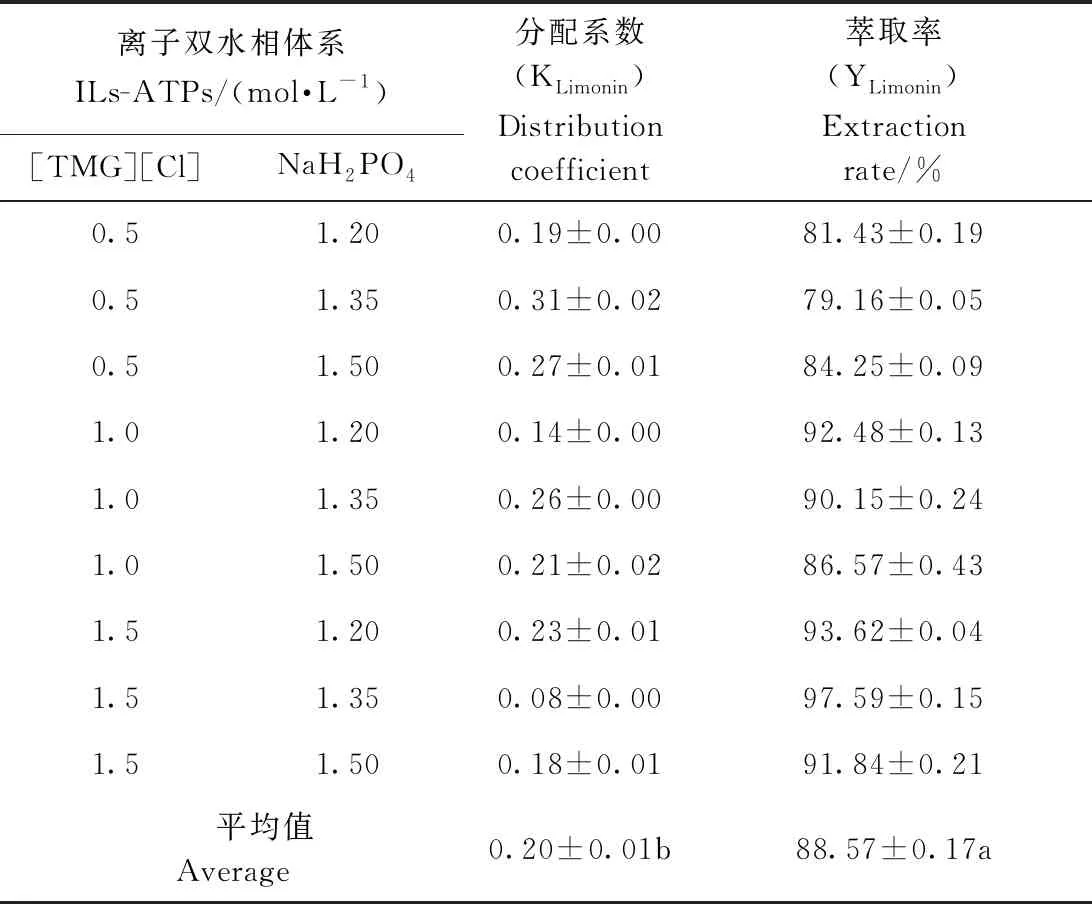
表5 [TMG][Cl]离子液体双水相体系对 柠檬籽粒中柠檬苦素提取效率的影响Table 5 Effects of [TMG][Cl] ionic liquid aqueous two-phase separation systems (ILs-ATPs) on extraction of limonin from lemon seeds
2.2 单因素试验结果
由图1-A可知,当乙醇浓度为50%、液料比为20∶1、提取时间为120 min时,柠檬苦素提取量随提取温度的升高呈现先上升后下降的趋势,在提取温度为70℃时,柠檬苦素提取量出现峰值。同时,当乙醇浓度为50%、液料比为20∶1、提取温度为70℃时,柠檬苦素提取量随提取时间的延长呈现先上升后下降的趋势,在提取时间为90 min时,柠檬苦素提取量达到最大值(图1-B)。当提取温度为70℃、提取时间为90 min、液料比为20∶1时,乙醇浓度为50%~70%时,柠檬苦素提取量较大,其中当乙醇浓度为60%时,提取量最大(图1-C)。当提取温度为70℃、提取时间为90 min、乙醇浓度为60%时,液料比大小与柠檬苦素提取量呈正相关,但液料比大于20∶1时,柠檬苦素提取量上升趋势逐渐变缓,考虑到成本,选择液料比20∶1作为最佳条件(图1-D)。因此,针对[TMG][Cl]/NaH2PO4离子液体相提取体系的单因素试验结果表明,提取温度70℃、提取时间90 min、乙醇浓度60%、液料比20∶1为各参数的最优值,可据此进行下一步整体优化。
2.3 响应面优化试验结果
2.3.1 试验数据和回归模型的建立 根据单因素试验确定的因素中心点和表1的水平设计来优化离子液体双水相提取柠檬苦素的操作参数,优化试验的结果(柠檬苦素提取量)见表6。使用Design Expert 10.1软件,以所得柠檬苦素提取量为响应值(Y),得到柠檬苦素含量关于提取温度(X1)、提取时间(X2)、乙醇浓度(X3)和液料比(X4)的四元二次方程:
Y=a0+ a1X1+ a2X2+ a3X3+ a4X4+ a12X1X2+ a13X1X3+ a14X1X4+ a23X2X3+ a24X2X4+ a34X3X4+ a11X12+ a22X22+ a33X32+ a44X42
(1)

图1 提取温度(A)、提取时间(B)、乙醇浓度(C)和液料比(D)对柠檬籽粒中柠檬苦素提取量的影响Fig.1 Effects of extraction temperature (A), time (B), ethanol concentration (C) and liquid-material ratio (D) on limonin yield from lemon seeds
式中,a0为截距,a1、a2、a3和a4为各因素的一次系数,a11、a22、a33和a44为平方系数,a12、a13、a14、a23、a24和a34为交互作用系数。
将表1中的柠檬苦素提取量实测值和对应的因素水平带入方程(1)进行多元拟合,可解出离子相液体中柠檬苦素提取量对提取温度、提取时间、乙醇浓度和液料比各实际水平值的四元二次回归方程,即
Y=-106.64+2.18X1+0.39X2+0.76X3+0.19X4-12 854.21X1X2+53 624.34X1X3+0.017X1X4-81 542.52X2X3-37 348.33X2X4-0.014X3X4-0.018X12-15 192.44X22-33 251.85X32-80 130.91X42
(2)
通过方程(2)可预测各因素在不同水平组合条件下从离子相液体中萃取出的柠檬苦素含量,其数值同见表6。

因此,以柠檬苦素提取量为响应值的回归方程整体及各主要因素均较显著,方程相关系数高,数据误差较小,此方程可用于对柠檬籽粒中柠檬苦素实际提取量进行预测。
2.3.3 响应面分析 利用Design Expert 10.1软件制作各因素响应曲面和等高线图,结果见图2。等高线图可用于评价各因素间交互作用的强弱,曲面图可确定各因素的最佳水平范围[16]。由图2-A可知,曲面随着提取温度和提取时间的增加,响应值(柠檬苦素提取量)先升高再逐渐降低,当提取温度为65~75℃、提取时间为75~105 min时,柠檬苦素提取量急大;而当提取温度低于62℃或高于78℃时,提取时间高于110 min或低于60 min时,柠檬苦素提取量急剧下降。提取温度和提取时间的曲面图形态平缓,等高线图呈圆形,暗示此两因素的水平交互作用不显著(P=0.898 9), 故在实际生产中可单独设定二者的最优参数。
由图2-B可知,当其他条件不变时,不断增加提取温度和乙醇浓度,柠檬苦素提取量先快速升高后缓慢降低,乙醇浓度在55%~65%范围内,柠檬苦素提取量较高。提取温度和提取时间的曲面图在乙醇浓度方向上陡峭,同时等高线呈椭圆形,表明二者交互作用明显,具有显著性(P=0.035 7)。
随着提取温度和液料比逐渐增加,柠檬苦素提取量响应值先缓慢升高后迅速降低,液料比为20∶1左右时,柠檬苦素提取量有明显峰值。提取温度和液料比的等高线图椭圆形明显,交互作用显著(P=0.014 5)(图2-C)。
图2-D中曲面平缓,暗示提取时间和乙醇浓度两因素对柠檬苦素提取量的影响不显著,且等高线图可进一步确认二者交互作用不显著(P=0.425 4)。其他条件不变,不断增加提取时间和液料比,柠檬苦素提取量先升高后降低,与单因素试验结果一致,且由等高线图可知两者交互作用不显著(P=0.081 1,图3-E)。由图3-F可知,乙醇浓度和液料比相对较低时,增加二者数值,柠檬苦素提取量缓慢增加,而达峰值后降幅有限;等高线呈弯曲状,说明两因素间交互作用显著(P=0.038 1)。

表6 响应面优化试验结果Table 6 Results of optimizing tests by response surface method (RSD)

表7 响应面回归模型的方差分析Table 7 Variance analysis of response surface regression model
2.4 验证试验结果
根据柠檬籽粒中柠檬苦素提取量的多水平试验数据(表6),结合Design Expert软件对回归方程(2)进行优化,发现在提取时间90.74 min、乙醇浓度59.40%、提取温度74.22℃、液料比18.08∶1的条件下,从柠檬籽粒中提取的柠檬苦素最大理论预测提取量为12.126 mg·g-1FW。为检验该模型的可重复性,同时方便实际生产,将柠檬苦素提取工艺调整为提取时间91 min、乙醇浓度60%、提取温度74℃、液料比18∶1。 在此水平下进行验证提取试验,重复3次。验证试验结果显示,提取的柠檬苦素提取量为12.381 mg·g-1FW,较预测值相对误差为+2.11%,差异不显著(P=0.05),证明此四元二次方程模型预测准确度高。
2.5 柠檬苦素抗氧化活性分析
由图3可知,在10~50 μg·L-1浓度范围内,柠檬苦素对各自由基均展现了较强的清除能力并有效抑制了亚油酸的过氧化水平,其总还原力与花色苷类物质相比无显著差异(P>0.05)且处于最高水平;柠檬苦素抗氧化活性与其浓度呈明显正相关。同时,柠檬苦素对亚油酸过氧化的抑制水平显著高于其他抗氧化物质(P<0.05),对ABTS+自由基的清除率也明显高于同水平的焦性没食子酸和绿原酸,然而柠檬苦素对活性氧自由基(超氧阴离子)的清除力显著低于黄酮类和花色苷类化合物(P<0.05)。
3 讨论


图2 试验交互因素影响柠檬苦素提取量的曲面图和等高线图Fig.2 Surface and contour plots of experimental interaction factors affecting limonin yield

图3 不同浓度下柠檬苦素及代表性酚酸、黄酮和花色苷对DPPH(A)、ABTS+(B)、 超氧阴离子(C)、羟自由基(D)清除率,亚油酸过氧化抑制率(E)和总还原力(F)的影响Fig.3 Effects of limonin and representative phenolic acid, flavonoids and anthocyanins on scavenging rates of DPPH (A), ABTS+ (B), superoxide anion (C) and hydroxyl (D) radicals, inhibition rate of linoleic acid peroxidation (E) as well as reducing power (F) at different concentrations
近年来离子液体的双水相体系被证实能高效提取多糖、酚类、维生素及蛋白质等各种功能性物质[17-19]。从机理上看,离子液体饱和蒸气压低,粘度和温度调控范围大,对极性和非极性溶剂均有一定的溶解性,因此通过构建离子液体双水相是一种可充分发挥离子液体高效萃取特性的策略[4]。相较于传统的双水相萃取体系(如聚乙二醇-葡聚糖体系),憎水性弱的离子液体与无机盐构成离子液体双水相体系,操作条件温和,萃取过程稳定,安全性和分离效率高,且对于功能性生物大分子具有较好的萃取选择性和保护作用[20]。本研究中,[BMG][BF4]/KH2PO4、[PHMG][PF6]/KH2PO4、[TMG][Br]/NaH2PO4和[TMG][Cl]/NaH2PO44种胍类离子液体双水相系统能有效地将柠檬苦素从柠檬籽粒初提液中萃取至离子相中,其中以小分子的四甲基胍盐([TMG])为基础构成的离子液体双水相体系相比分子量较大的甲基丁基胍([BMG])和聚六亚甲基胍的六氟磷酸盐([PHMG])的体系分离柠檬苦素效果较好,其原因可能是由于[TMG]与柠檬苦素分子量均较小,二者氢键作用力不易受空间位阻影响,结合程度高。与本研究结果相类似,采用1-乙基咪唑氯盐离子为基础的离子液体双水相体系也对小分子绿原酸有很好的萃取效果[21];[bmim][BF4]也可将金丝桃苷和异槲皮苷等中药提取成分有效浓缩至上相中,达到萃取目的[22]。
本研究发现,在离子液体双水相提取柠檬苦素过程中,提取温度对提取效率影响较大。这主要是由于双水相萃取过程中,在一定pH值(或等电点)条件下,适当提高温度可促进体系熵值的增加以及疏水相互作用力,使带弱电的苦素类物质从NaH2PO4相转移至离子液体相,从而达到进一步提纯的效果[23]。本研究采用乙醇溶液富集萃取离子相中的柠檬苦素,乙醇安全性高、成本低,当乙醇加入离子液体中时,离子液体相中的阴离子可通过氢键结合乙醇,使柠檬苦素在离子相中溶解度下降并逐渐释放至醇相中,这为后续的减压浓缩和进一步提纯提供了基础[24-25]。
柠檬苦素是广泛存在于柑橘属或楝科属植物中的一种三萜类化合物,动物试验研究证实柠檬苦素具有激活谷胱甘肽-S-转移酶(glutathione S- transferase,GST)活性和抑制活性氧自由基过度积累的功能,从而预防正常细胞的癌变[26-27];同时,柠檬苦素也能直接抑制肿瘤细胞增殖,具有极强的抗癌活性[28]。前期有关杨梅[10]和草莓[29]的研究表明,酚酸、黄酮和花色苷类均具有较强抗氧化活性,可有效清除组织内过量自由基,维持活性氧代谢的平衡,因此本研究横向比较了柠檬苦素与典型酚酸、黄酮和花色苷类物质在抗氧化水平方面的差异。结果显示,在10~50 μg·L-1浓度范围内,柠檬苦素均可有效清除DPPH和ABTS+自由基并能减少活性氧自由基的积累,显示了较强的抗氧化活性;同时,相比于酚酸、黄酮和花色苷类物质,柠檬苦素能更显著地抑制亚油酸的过氧化进程,这暗示柠檬苦素具有提升细胞膜中脂肪酸的不饱和程度从而维持膜流动性的作用[30]。
4 结论
本研究建立了[TMG][Cl]/NaH2PO4双水相体系对柠檬籽粒中柠檬苦素提取量的回归预测模型,通过拟合试验得出最佳提取工艺参数为提取时间90.74 min、乙醇浓度59.40%、提取温度74.22℃、液料比18.08∶1,此条件下柠檬苦素提取量12.126 mg·g-1FW, 较单因素提取量有显著提高,说明采用响应面法优化工艺效率高,可操作性好。功能性试验表明,柠檬苦素具有较强抗氧化活性,可有效清除活性氧自由基并抑制不饱和脂肪酸的过氧化,是一种具有开发前景的功能性食品资源。本研究为高效开发柠檬苦素资源提供了可行方案,但相关离子液体的制备较为繁琐,试剂成本也较高,需开发简便易行的试剂回收方法;同时,离子液体双水相体系提取的柠檬苦素提取液中还含有其他苦素类成分(如诺米林),因此相关提取液仍可进一步分离纯化,以获得纯度更高的苦素类单体成分。
