SPE-UPLC-MS/MS测定葡萄酒中的高氯酸盐
2020-12-04王圣仪温昊松杨志伟齐鹏宇张进杰
王圣仪 温昊松 王 飞 杨志伟 齐鹏宇 张进杰 张 昂,*
(1 秦皇岛海关技术中心,河北,秦皇岛 066004; 2河北省葡萄酒质量安全检测重点实验室, 河北 秦皇岛 066004; 3 葡萄酒检测重点实验室,河北,秦皇岛 066004)
高氯酸盐是一种无机环境污染物,能通过母乳影响发育中婴儿神经中枢的正常发育[1],这是由于ClO4-和Ⅰ-结构类似,可以竞争性抑制甲状腺对Ⅰ-的吸收[2]。高氯酸盐常作为氧化剂被广泛应用于军工行业与工业生产[3],其在干旱地区的土壤中检出浓度远高于潮湿地区,因此高氯酸盐易富集在干旱地区的葡萄果实中,进而影响葡萄酒安全[4]。许多国家对高氯酸盐每日的摄入量进行了规定,2014年欧盟食品安全局制定高氯酸盐的每日耐受摄入量为0.3 μg·kg-1[5]。
目前国内外测定高氯酸盐含量的方法主要包括分光光度法、离子色谱-质谱法[6-7]、高效液相色谱-质谱法[8]等,其中针对水、土壤等基质中的检测研究较多[9-10],而对葡萄酒研究较少。Houssain等[11]首次利用离子色谱串联二级质谱技术分析葡萄酒中高氯酸盐含量;李柚等[12]利用离子色谱技术建立了测定红葡萄酒中高氯酸盐的分析方法,但上述方法灵敏度均较低,很难满足进出口食品中的限量检测要求,且离子色谱法多适用于基质简单的样品,对于复杂样品,易受基质干扰而无法实现准确检测。SN/T 4089-2015[13]建立了高氯酸盐测定的液相色谱-串联质谱法,但该标准适用范围未包含葡萄酒,且此方法易对质谱仪造成污染[14]。姚清华等[15]在测定茶叶中高氯酸盐的研究中采用固相萃取(solid phase extraction,SPE)技术去除了提取液中的茶叶色素和大分子类干扰物质;杨志伟等[16]同样采用SPE技术对蜂蜜样品进行前处理,有效减少了样品对仪器的污染。

1 材料与方法
1.1 材料与试剂
21种干红葡萄酒、干白葡萄酒,购自秦皇岛海港区广缘超市;高氯酸钠标准品(NaClO4,纯度>98%)、高氯酸盐18O 标准品(NaCl18O4,纯度>97%),美国Sigma公司;甲酸、甲醇(色谱纯),中国迪马科技公司。
1.2 仪器与设备
Nexera 30A超高效液相色谱仪,日本岛津公司;SCIEX QTRAP 4500三重四极杆质谱仪,美国Applied Biosystems公司;Vortex Genie2T涡旋混匀器,美国Scientific Industries公司;Million-Q IQ 7000超纯水系统,德国Millipore公司;C18色谱柱(150 mm×2.1 mm,3 μm)、Phenyl-Hexyl色谱柱(150 mm×2.1 mm,3 μm)、C18固相萃取柱(500 mg·3 mL-1)、WAX固相萃取柱(60 mg·3 mL-1)、亲水性聚丙烯滤膜(0.20 μm)、尼龙66滤膜(0.22 μm)及聚醚砜滤膜(0.22 μm),美国Waters公司。
1.3 试验方法
1.3.1 溶液配制 分别配制1 mg·mL-1的NaClO4和0.5 mg·mL-1NaCl18O4内标标准储备液,于4℃保存备用,根据试验需要用去离子水逐级稀释标准储备液,配制成适当浓度的工作液。
用含0.1%甲酸的甲醇配制葡萄酒样提取液,其中甲醇∶水=10∶9(v∶v)。
将150 mL乙醇和3 g酒石酸移入1 L容量瓶中,用去离子水定容,得到空白基质液。
1.3.2 色谱柱与滤膜的选择 本试验对C18和Phenyl-Hexyl 2种色谱柱对高氯酸盐的保留效果进行比较,选择保留效果最佳的色谱柱,其中C18色谱柱的填料为十八烷基硅烷键合硅胶,Phenyl-Hexyl色谱柱的填充物为高纯度硅胶。
并对GHP、尼龙66及聚醚砜3种滤膜进行比较,选定对高氯酸盐通过率最高的滤膜,防止杂质污染仪器。
1.3.3 样品预处理 准确移取5.0 mL酒样至25 mL聚乙烯离心管中,加入50 μL内标工作液涡旋混合2~3 min,待净化。取待净化酒样过WAX固相萃取柱(提前用6.0 mL甲醇和6.0 mL水活化),依次用5.0 mL水和5.0 mL甲醇淋洗并抽干,之后用6.0 mL 10%氨水甲醇洗脱,氮气吹干后用1.0 mL定容液(葡萄酒样提取液)复溶,经GHP滤膜过滤后进样。
1.3.4 检测参数 色谱条件:色谱柱:Phenyl-Hexyl色谱柱(150 mm×2.1 mm, 3.5 μm);进样量:5 μL;柱温:30℃;流动相A:5%甲醇溶液(含1%甲酸);流动相B:1%甲酸甲醇溶液,流速:0.2 mL·min-1;洗脱程序:0~2 min 50% B,2~8 min 80% B,8~10 min 50% B,10~12 min 40% B;阀切换:3 min B,8.5 min A。
质谱条件:EI离子源;ESI-电离模式;检测方式:多反应监测(multiple reaction monitoring, MRM);电喷雾电压:4 000 V;雾化气压力:0.5 MPa;气帘气压力:0.35 MPa;辅助气压力:0.7 MPa;辅助气温度:550℃;碰撞室出口电压:13 V;定性离子对、定量离子对、保留时间、去簇电压和碰撞能量见表1。
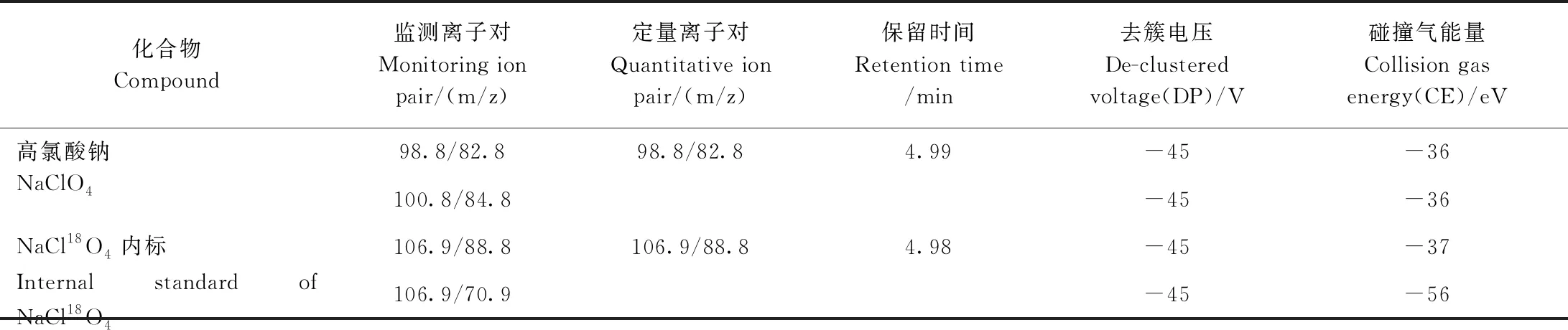
表1 质谱参数Table 1 Parameters of mass spectra
1.4 数据分析
采用SCIEX QTRAP 4500三重四极杆质谱仪自带Analyst 1.5 数据处理系统分析数据,并使用Excel 2016软件制图。
2 结果与分析
2.1 质谱条件的优化
已知自然界中氯元素存在35Cl与37Cl两种同位素状态[22],使得NaClO4在质谱中出现2种质量数不同的质谱图,在1.3.3条件下高氯酸钠及其内标物质的母离子和MS2质谱图。其母离子峰见图1,质荷比为98.8的离子片段为Na35ClO4,质荷比为100.8的离子片段为Na37ClO4,再分别优化相应质谱参数,得MS2图(图2、3)。

图1 母离子质谱图Fig.1 Proton ion mass spectrum

图2 高氯酸盐的MS2质谱图Fig.2 Secondary mass spectrum of perchlorate

图3 内标物的MS2质谱图Fig.3 Secondary mass spectrum of internal standard
2.2 色谱条件的选择
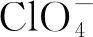
2.3 滤膜的选择
不同材质的滤膜对高氯酸盐吸附程度存在差异[25]。由图6可知,ClO4-在尼龙66滤膜上吸附较强,回收率仅为0.9%,而聚醚砜滤膜的回收率为90%,亲水GHP滤膜的回收率为98%。同时亲水GHP滤膜具有无毒性、耐化学性能优良、强度好等优点,因此后续试验确定选用GHP滤膜。
2.4 前处理方式的选择
为尽可能消除样品中干扰物的影响,将基体和干扰化合物分离。本试验选择C18固相萃取柱[26]和WAX固相萃取柱[27]进行样品前处理并与未过柱进样比较。
由图7可知,未过柱样品色谱图峰型较宽,基线高,受基质影响大(7-A);过C18固相萃取柱与未过柱相比,基质影响小,但无明显差别(7-B);过WAX固相萃取柱的样液色谱图基线低,峰型好,基质影响小(7-C)。且与其他方法相比,WAX固相萃取柱在分离干扰物时可对目标化合物进行富集,增强对待测物的检出能力,这是由于WAX固相萃取柱的填料为混合型弱阴离子交换吸附剂,对含强酸基团的化合物具有高选择性和灵敏度[16]。因此选择WAX固相萃取柱作为前处理的固相萃取柱。

注:A:未过柱; B: C18固相萃取柱; C:WAX固相萃取柱.Note: A: None. B: C18 solid phase extraction column. C: WAX solid phase extraction column.图7 不同固相萃取柱条件下的样品色谱图Fig.7 Sample chromatograms under different solid phase extraction column

图4 过Phenyl-Hexyl色谱柱的样品色谱图Fig.4 Sample chromatogram of Phenyl-Hexyl column

图5 过C18色谱柱的样品色谱图Fig.5 Sample chromatogram of C18 column

图6 3种不同材质滤膜对高氯酸盐的回收率Fig.6 Recovery rate of perchlorate by three different filter membranes
2.5 方法学验证
在上述优化条件下,使用空白基质液配制浓度为1、2、5、10、20 μg·L-1的NaClO4标准溶液和浓度为2.5 μg·L-1的NaCl18O4内标标准工作液平行10次试验,根据5个浓度梯度的空白样品基线噪音值求平均值,根据3倍信噪比计算方法检出限,10倍信噪比计算方法定量限,最终得到方法回收率为94.5%~105%,相对标准偏差(relative standard deviation, RSD)为0.94%~3.17%(表2、3)。
2.6 实际样品检测

表2 方法学验证Table 2 Methodological Validation

表3 葡萄酒中高氯酸盐加标回收率及RSD (n=10)Table 3 Scaling recovery and RSD of Perchlorate in wine (n=10)

表4 葡萄酒样品检测Table 4 Wine sample testing
品高氯酸盐含量小于1 μg·L-1,3组样品高氯酸盐含量在1~15 μg·L-1之间,1组样品含量为16.65 μg·L-1, 超过2009年美国环保署(united states environmental protection agency, US EPA)建议的饮用水中15 μg·L-1高氯酸盐浓度标准[5]。
3 讨论

前人进行样品前处理时对固相萃取柱的选择各异[29],其中使用C18固相萃取柱净化高氯酸盐样品的方法较多[20,28],但C18柱只能去除提取液中的色素和大分子类干扰物质。本研究发现WAX柱在分离干扰物时可对目标化合物进行富集,增强对待测物的检出能力,与杨志伟等[16]使用HPLC-MS检测蜂蜜中高氯酸盐的结果相同,这可能是由于WAX柱的填料为混合型弱阴离子交换吸附剂,对含强酸基团的化合物具有高选择性和灵敏度。而C18柱的填充物是基于键合的反相(二甲基十八碳硅烷)和不规则硅胶(硅胶基)颗粒,这种非极性、未封端的吸附剂提供了与表面硅醇基相关联的额外极性作用,与相应封端的吸附剂相比增强了对碱性化合物的保留,因此WAX柱效果更好。本研究仅对2种固相萃取柱的效果进行了比较,WAX柱是否为最佳净化柱仍需进一步研究。


4 结论
本试验采用UPLC-MS/MS技术建立了测定葡萄酒中高氯酸盐的定性定量分析方法,通过对质谱条件、色谱条件和前处理条件的优化考察,最终得到UPLC-MS/MS方法的检出限为0.15 μg·L-1,定量限为0.5 μg·L-1,加标回收率介于94.5%~105%之间。该检测方法操作简便、灵敏度高、实用性强。经方法学验证和实际样品检测验证本方法可以满足葡萄酒中高氯酸盐的日常监测要求,并应用于日常监测工作。
