低氮胁迫对不同光皮桦基因型苗期生长及生理生化特征的影响
2020-12-04程丽丽林仕雄童再康张俊红
程丽丽 潘 樱 林 艳 林仕雄 童再康 张俊红
(浙江农林大学亚热带森林培育国家重点实验室,浙江 杭州 311300)
氮素是植物生长发育不可或缺的矿质营养元素,在植物生命活动中具有不可替代的作用,是影响植物生产和质量的关键因素[1-2]。氮代谢途径紊乱会对植物生长与形态造成不利影响,显著影响植物根系发育、叶绿素含量及种子产量等[3]。施用氮肥可促进农作物增产,但随着氮肥施用量增加其利用效率逐年降低,同时造成农产品质量下降、生产成本提高和生态环境恶化等问题[4-5]。因此,利用植物自身遗传变异,挖掘植物本身利用养分的潜力,筛选和培育耐低氮、氮高效利用的新品种是解决这些问题的理想途径之一[6]。
光皮桦(Betulaluminifera)为桦木科(Betulaceae)桦木属(Betula)落叶乔木,是我国特有的优良速生用材树种[7]。光皮桦材质优良、用途广、病虫害少,是近年来我国南方山区大力发展的重要用材树种[8]。然而,由于南方山区土壤中可利用氮源较少,缺氮成为影响光皮桦生产的重要因素。研究表明,植物可感知外界逆境胁迫信号,通过自身调节系统在生理和形态上产生响应,以增强在胁迫条件下的生存机会[9-10],且植物不同基因型在矿质营养吸收和利用方面存在显著的遗传差异[11]。目前对植物不同基因型氮素利用差异的研究主要集中于小麦(Triticumaestivum)[1]、玉米(Zeamays)[12]、大麦(Hordeumvulgare)[4]和甘蔗(Saccharumofficinarum)[13]等农作物,关于林木氮生理效率的遗传和育种研究较少。樊瑞怀等[14]研究不同基因型马褂木(Liriodendronchinense)的氮素胁迫响应,将参试家系划分为稳定型高氮效率家系和敏感型低氮效率家系两大类,并结合不同氮素下的生长表现进一步分为生长优良和生长劣势家系。Luo等[15]研究发现速生杨群众杨(Populuspopularis)和慢生杨银腺杨(P.alba×P.glandulosa)在低氮胁迫下根表型和光合作用等响应存在显著差异,速生杨的氮代谢在低氮条件下较慢生杨更敏感。Zhang等[16]研究表明低氮胁迫对青杨(P.cathayana)雌株影响比雄株更大,低氮胁迫下雄株叶绿素含量、氮生理利用效率、谷氨酸脱氢酶和过氧化氢酶活性比雌株更高,且叶绿素超显微结构更完整。
本研究以3个光皮桦基因型为试验材料,通过正常供氮和低氮胁迫分别处理水培光皮桦幼苗,分析不同光皮桦基因型在低氮胁迫下的生长和生理生化指标变化,探索光皮桦适应低氮环境的生理机制,以期为耐低氮胁迫种质的筛选和培育提供科学依据。
1 材料与方法
1.1 供试材料
选用浙江农林大学珍贵树种育种课题组前期筛选的光皮桦G49-3、G50-1和优3三个基因型的组培苗为供试材料。组培苗继代于1/2 MS固体培养基,2月苗龄时移植至基质(泥炭土∶珍珠岩∶蛭石=2∶1∶1),培养30 d后移入水培装置,适应培养30 d。水培条件为:白天25℃,晚上20℃,16 h光/8 h暗,光照强度120 μmol·m-2·s-1。 试验前将试验材料饥饿处理7 d,期间以超纯水培养。
1.2 试验设计
试验在浙江农林大学平山试验基地人工培养室进行。基于前期不同氮浓度的试验及文献[8]选取NO3-浓度。Hoagland营养液配制参照Georgieva[17]的方法,正常供氮组(control,CK)NO3-浓度为15 mmol·L-1; 低氮胁迫组(low nitrogen,LN)NO3-浓度为0.03 mmol·L-1,缺失的K+以浓度为4.97 mmol·L-1KCl补齐,配方参照文献[18]。本试验采用裂区试验设计,氮素处理为主区(A):CK(A1)和LN(A2);基因型为副区(B):G49-3(B1)、G50-1(B2)和优3(B3),均按完全随机区组排列,重复5次。
光皮桦苗处理21 d后于当日上午11时对每个基因型幼苗取样,测定3个基因型植株的株高、叶片和根系表型,叶绿素含量,过氧化物酶(peroxidase,POD)、超氧化物歧化酶(superoxide dismutase,SOD)和硝酸还原酶(nitric reductase,NR)活性等指标。并分别取各基因型的根和叶经液氮速冻后保存于-80℃超低温冰箱,备用。
1.3 测定指标及方法
1.3.1 生物量、叶绿素含量和氮含量测定 将植株从水培装置中取出,从根基部切断,将植株分为地上部和根部,测定株高,并扫描根系。然后分别将地上部和根放入烘箱105℃杀青30 min,再75℃烘干至恒重并记录。叶绿素含量测定采用丙酮-乙醇直接浸渍法[19],于663、645 nm波长处测定吸光度值,代入公式计算(Ca=12.71×A663-2.59×A645,Cb=22.88×A645-4.67×A663,C=8.04×A663+20.29×A645,以mg·g-1表示)。样品经H2SO4-H2O2消煮,利用微量凯氏定氮法[19]测定氮含量。
1.3.2 根系结构 采用平板扫描仪Epson Perfection V700(RZGENT公司,加拿大)以800 dpi分辨率采集根系图像,并利用WinRhizo根系分析系统分析总根长、根系总表面积等根系形态指标。
1.3.3 POD、SOD和NR活性测定 叶片POD和SOD活性分别采用过氧化物酶测定试剂盒(比色法[19])和总超氧化物歧化酶测试盒(羟胺法[19])测定,POD及SOD活性均以U·g-1FW表示。NR活性采用硝酸还原酶测定试剂盒测定,以μg· g-1·h-1FW表示。上述试验所用试剂盒均购自南京建成生物工程研究所。
1.3.4 硝酸盐转运蛋白基因的表达分析 采用CTAB+Trizol法分别提取光皮桦根和叶总RNA,使用PrimeScriptTMRT Reagent Kit[宝生物工程(大连)有限公司]反转录进行cDNA第一链合成。采用StepOne Real-Time PCR system (Applied Biosystem,美国) 进行RT-qPCR,反应体系(10 μL):SYBR premix ExtaqⅡ 5.0 μL、Primer-F 0.4 μL、Primer-R 0.4 μL、cDNA 0.5 μL和ddH2O 3.7 μL。PCR反应程序:95℃预变性30 s;95℃变性5 s,60℃退火20 s,72℃延伸30 s,循环39次;65~95℃作熔解曲线。RT-qPCR所用引物见表1,参考前期光皮桦内参基因筛选结果,选择 large ribosomal subunit 39 (RPL39)作为内参基因(GenBank 登录号: KP245805)[8]。

表1 光皮桦硝酸盐转运蛋白基因引物Table 1 Primers for nitrate transporter genes in B. luminifera
1.3.5 隶属函数的计算方法 耐低氮系数K=低氮处理测定值/对照测定值。耐低氮综合评价采用隶属函数法综合各项指标进行评价[20-21],其计算公式为:


式中,i表示某个基因型;j表示某项指标;Uij表示i基因型j指标的隶属函数值;Xjmin表示各基因型j指标耐低氮系数最小值;Xjmax表示各基因型j指标的耐低氮系数最大值。将各基因型所有性状的隶属函数值进行累加,求其平均值得各基因型的隶属函数值Ui,Ui值越大表示耐低氮能力越强。
1.4 数据处理
应用Microsoft Office Excel 2010对试验数据进行整理,用SPSS18.0软件进行方差分析。
2 结果与分析
2.1 低氮胁迫对不同基因型光皮桦幼苗的表型及叶绿素含量的影响
在CK和LN条件下处理21 d后,3个基因型光皮桦幼苗形态上发生变化。LN各基因型光皮桦幼苗不定根数量明显增多,叶色发黄(图1),尤其嫩叶黄化,叶片较小,呈典型缺氮表型(图2-a)。LN不同基因型光皮桦的叶绿素总量、叶绿素a和叶绿素b含量均显著降低(图 2-b~d),且在不同基因型光皮桦间存在极显著差异。

图1 低氮胁迫处理21 d后3种基因型光皮桦的表型Fig.1 The phenotypes of three genotypes in B. luminifera after 21 days of treatment under LN stress
2.2 低氮胁迫对不同基因型光皮桦幼苗生长的影响
由表2可知,与CK相比,LN各基因型光皮桦的株高、地上部干重、地上氮含量和氮积累量均呈下降趋势,且不同基因型间存在极显著差异,表明低氮胁迫对不同基因型光皮桦生长的抑制程度不同,其中G49-3的株高和地上部干重的降幅达到显著或极显著水平,表明G49-3对低氮更敏感。3种基因型光皮桦地上氮含量和氮积累量下降均达到显著或极显著水平,且均是G49-3降幅最大,G50-1降幅最小,表明G50-1氮含量和氮积累量受低氮胁迫影响较小,表现出较强耐低氮能力,而G49-3对低氮胁迫更敏感。

表2 低氮胁迫下3种基因型光皮桦地上部生长的差异Table 2 Differences in shoot growth of three genotypes in B. luminifera under LN stress
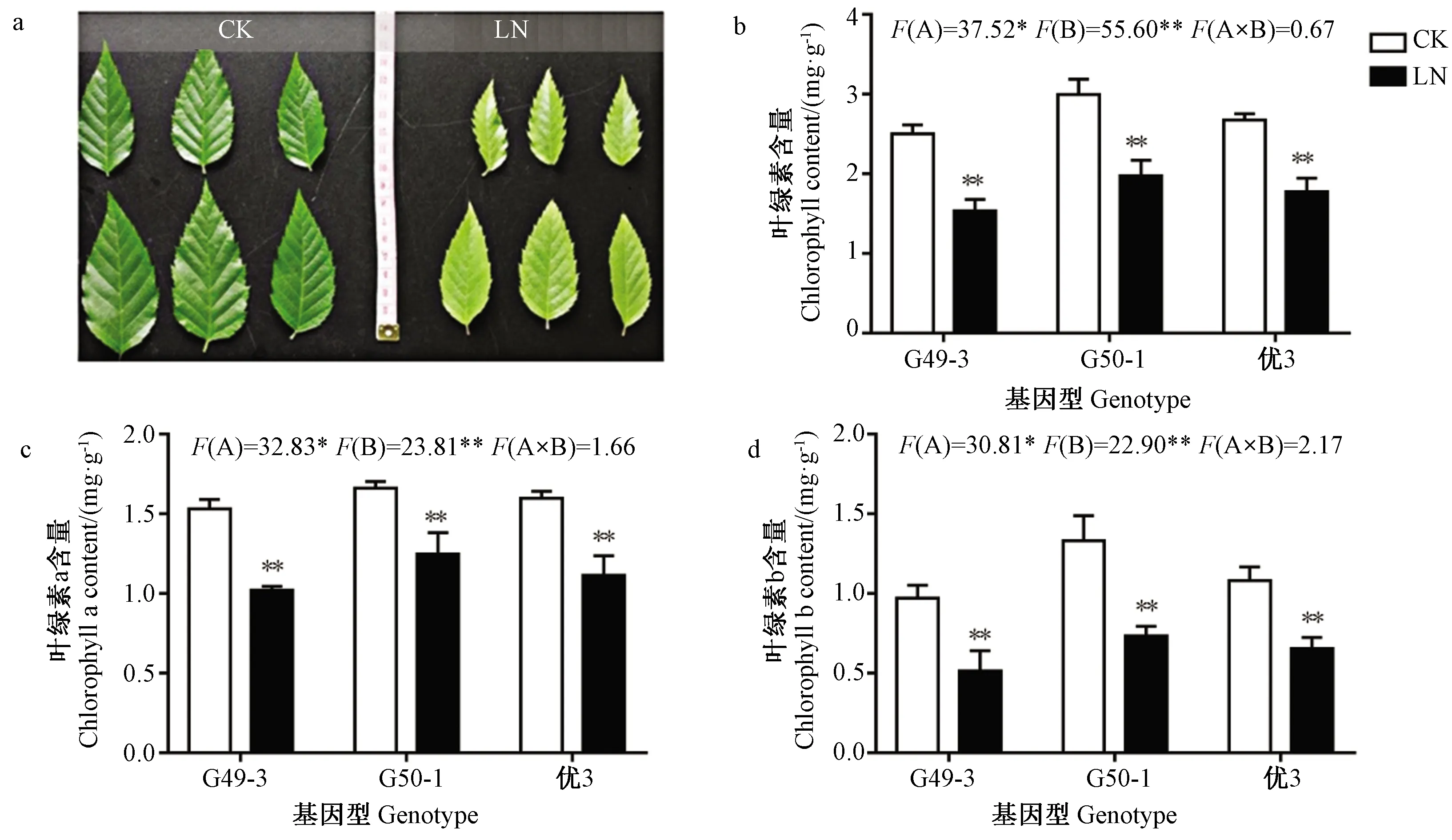
注:a: 光皮桦叶色比较,从顶端向下的第二、第三片叶子。 *表示相对于CK,LN达显著水平(P<0.05),** 表示达极显著水平(P<0.01)。下同。Note: a: Comparison of leaf color in B. luminifera with the second and third leaves from the top. * indicates that LN has a significant level relative to CK(P<0.05), ** indicates a extremely significant level(P<0.01). The same as following.图2 低氮胁迫下三种基因型光皮桦的叶色比较及叶绿素含量分析Fig.2 Comparison of leaf color and chlorophyll content of three genotypes in B. luminifera under LN stress
2.3 低氮胁迫对不同基因型光皮桦幼苗根系的影响
由表3可知,与CK相比,LN处理下3种基因型光皮桦的地下氮含量均呈下降趋势,不同基因型间存在极显著差异;其根干重、根冠比、总根长、根系总表面积和平均直径升高,表明低氮胁迫在一定程度上促进了光皮桦地下部生长。各指标在不同基因型光皮桦间存在显著或极显著差异,但仅G50-1各项指标变化均达到显著或极显著水平,表明G50-1能更好地响应低氮胁迫,进而改变根系形态以摄取更多氮素,表现出更强的耐低氮能力。
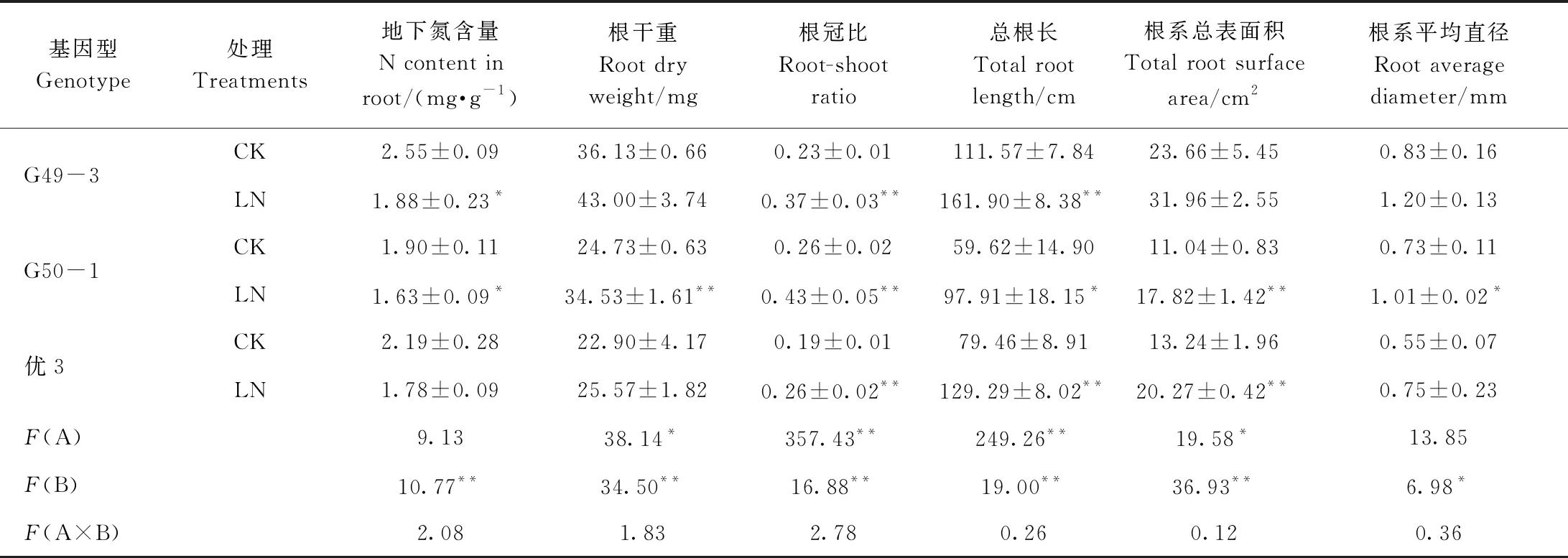
表3 低氮胁迫对3种基因型光皮桦根系的影响Table 3 Effects of LN stress on roots in three genotypes of B. luminifera
2.4 低氮胁迫下光皮桦幼苗保护酶活性的变化
低氮胁迫对不同基因型光皮桦保护酶系统的影响不同(图3),且不同基因型光皮桦间存在极显著差异。LN处理后3种基因型光皮桦POD和SOD活性均降低,其中优3的POD和SOD活性显著降低,G49-3的POD和SOD活性极显著降低。保护酶活性的变化差异说明不同基因型光皮桦响应长时间低氮胁迫时的抵御能力不同,G50-1降幅最低,表明其对低氮胁迫的抵御能力最强。

图3 低氮胁迫下3种基因型光皮桦的POD和SOD活性变化Fig.3 The changes of POD and SOD activity in three genotypes of B. luminifera under LN stress
2.5 低氮胁迫下光皮桦幼苗NR活性的变化
NR是植物氮同化过程中的第一个酶,也是硝酸盐同化过程中的限速酶,其活性强弱与植物体内氮同化能力密切相关,NR活性越强,氮素代谢越旺盛[22]。与CK相比,LN处理下3个光皮桦基因型的NR活性均极显著降低(图4),基因型对光皮桦NR活性的影响存在极显著差异,其中G49-3降幅最大。正常供氮时,G50-1的NR活性不是最高,但在LN条件下降幅最小,活性最高,表明其具有较强的耐低氮能力。

图4 低氮胁迫对3种基因型光皮桦NR活性的影响Fig.4 Effects of LN stress on NR activity in three genotypes of B. luminifera
2.6 低氮胁迫下光皮桦硝酸盐转运蛋白基因的表达分析
低氮处理后叶片中硝酸盐转运蛋白基因NRT1.1和NRT1.2均下调表达(图5-A),但NRT2.1在G49-3中的相对表达量极显著增加。根中表达模式与叶片中不同,NRT1.2在3个基因型光皮桦中均显著下调表达,而NRT2.1极显著上调表达(图5-B),这与NRT转运蛋白主要通过根系吸收转运硝酸盐有密切关系。本试验中,3个基因型光皮桦间NRT2.1表达水平变化存在极显著差异,其中G49-3增幅最大,而优3增幅最小。
2.7 3种基因型光皮桦耐低氮能力的综合评价
光皮桦耐低氮能力受多种因素的综合影响,上述用单一指标来评价3种光皮桦基因型的耐低氮能力存在不一致性。为提高对光皮桦耐低氮能力评价的准确性,运用模糊数学隶属函数法对3个基因型光皮桦的叶绿素、根冠比、总干重、氮积累量、SOD活性、NR活性等17个指标进行综合评价(表5)。基于隶属函数平均值,3个基因型的耐低氮能力强弱依次为G50-1>优3>G49-3。

表4 光皮桦耐低氮能力的综合评价Table 4 Comprehensive evaluation of LN tolerance in B. luminifera

注:A:低氮胁迫下光皮桦叶中NRTs的表达分析;B:低氮胁迫下光皮桦根中NRTs的表达分析。Note: A: Expression analysis of NRTs in B. luminifera leaves under LN stress. B: Expression analysis of NRTs in B. luminifera roots under LN stress.图5 低氮胁迫对3种基因型光皮桦NRTs的表达分析Fig.5 The expression analysis of NRTs in three genotypes of B. luminifera under LN stress
3 讨论
3.1 低氮胁迫下不同基因型光皮桦的生长响应特征
氮是植物生长发育最重要的营养成分,为植物细胞重要的构成元素。缺氮情况下,植物快速响应低氮胁迫,形态和生物量均受影响,但受影响程度存在显著基因型差异[23]。本研究对3种基因型光皮桦在低氮胁迫下生长和生理生化指标进行分析,并结合隶属函数综合评价,结果显示,G50-1 平均隶属函数值(0.73)高于优3(0.44)和G49-3(0.34),表明光皮桦G50-1基因型为耐低氮型品种,而G49-3基因型为低氮敏感型品种。
本试验中,低氮胁迫下光皮桦表型变化明显,植株矮小,叶色发黄。氮素是叶绿素分子的重要组成成分,环境中氮素减少影响叶绿素合成从而使光合作用受阻[24]。3种基因型光皮桦中G49-3的叶绿素含量降幅最大,G50-1降幅最小,即耐低氮基因型光皮桦在低氮环境中仍能保持较高叶绿素含量,表现出较强的耐低氮能力。张楚等[10]研究表明,在低氮条件下苦荞(Fagopyrumtataricum)的株高、叶面积、地上部干重和地上氮含量均显著低于正常组,且耐低氮基因型降幅均小于不耐低氮基因型。本研究中,低氮胁迫影响光皮桦幼苗生长,地上部生长受限而促进根系生长;耐低氮基因型G50-1受低氮胁迫影响较小,其地上部性状指标与不耐低氮基因型相比表现出明显优势,对低氮环境适应性更强。
研究表明,低氮胁迫下植物根吸收的氮虽然先运输到地上部,但是更多同化氮会被分配到根部从而使根冠比增加[1]。本试验中,低氮胁迫下G50-1光皮桦的根冠比增幅最大,这与李强等[24]的“耐低氮基因型玉米根冠比增幅低于氮敏感基因型”研究结果不一致,可能因为光皮桦为多年生林木,根系较一年生农作物更发达,且低氮胁迫同时影响光皮桦地上部和地下部生长。低氮处理后,3种基因型光皮桦的总根长、根系总表面积和平均直径均增加,其中耐低氮基因型G50-1增幅最大。研究表明,当土壤中NO3-有限时,根系形态特征对氮吸收尤为重要[25],这与武永军等[26]在氮亏缺条件下,植物为了尽可能寻找氮源而产生的补偿效应一致,这是植物在低氮条件下采取的最直接应对方式之一。
3.2 低氮胁迫下不同基因型光皮桦的生理响应特征
植物处于逆境时,细胞内活性氧产生与消除间平衡被破坏,植物启动相应防御系统[27]。POD和SOD是植物细胞内清除活性氧的主要抗氧化酶,POD和SOD活性高低可以衡量植物在逆境条件下适应能力的强弱[28]。本研究中,在低氮处理21 d后,3个基因型光皮桦幼苗保护酶活性均降低,其中G50-1下降最少,表明在低氮胁迫下耐低氮基因型能保持较高POD和SOD活性抵抗膜脂过氧化伤害,延缓叶片衰老[29],从而更好地适应低氮环境,这也是耐低氮基因型光皮桦耐低氮胁迫的重要生理机制之一。本试验中保护酶活性变化趋势与李小冬等[30]研究的结果不一致,但与张定一[1]的研究结果相符,可能与植物受胁迫时间长短有关,短时间内低氮胁迫能诱导抗氧化酶系统响应,减轻逆境带来的氧化伤害,但随着处理时间的延长,低氮胁迫对植物造成不可逆伤害,从而导致POD和SOD活性降低。
大多数植物从土壤中吸收的氮素是硝酸盐(NO3-),硝酸盐在参与合成体内含氮有机化合物之前,必须先还原为氨。NR是氮代谢过程中的关键酶[31],能在一定程度上反映植株的营养状况以及硝酸盐同化水平。本试验中,低氮处理后3个基因型光皮桦NR活性均不同程度降低,且耐低氮基因型降幅小于氮敏感基因型。
3.3 低氮胁迫下不同基因型光皮桦的分子响应特征

4 结论
低氮胁迫下光皮桦幼苗生长受到抑制,光皮桦株高、地上部干重、地上氮含量和氮积累量显著降低,但低氮胁迫在一定程度上促进根系生长,表现为根冠比、根系总根长、总表面积和平均直径升高;低氮胁迫使光皮桦幼苗叶绿素含量,POD、SOD和NR活性下降,但高亲和力吸收系统中NRT2.1表达量增加以更好地调节氮代谢适应低氮环境。不同基因型光皮桦对低氮胁迫的响应存在显著差异,耐低氮基因型在低氮环境中能保持较好生长优势,耐低氮能力更强。本研究结果为耐低氮胁迫种质的筛选和培育提供了科学依据,同时表明运用常规遗传改良手段筛选和培育耐低氮、氮高效的光皮桦良种是可行的。
