溶剂效应对络合反应法脱除模拟柴油中氮化物的影响
2020-12-02赖婷婷刘明星汪燮卿
赖婷婷,王 威,刘明星,汪燮卿
(中国石化石油化工科学研究院,北京 100083)
原油中氮质量分数一般在0.05%~0.50%,馏分油中氮元素含量随沸点升高而增加,大部分氮化物分布于重质馏分油中。石油中氮化物组成复杂,主要以碱性氮化物和非碱性氮化物的形式存在,碱性氮化物包括苯胺、吡啶、喹啉、苯并喹啉、吖啶及其衍生物等,非碱性氮化物包括吡咯、吲哚、咔唑及其衍生物等[1-3]。石油产品中的氮化物会影响石油产品的安定性,使油品变色和产生沉淀[4]。石油加工过程中碱性氮化物吸附于催化剂酸性中心,会使催化剂中毒失活[5]。因此,石油脱氮技术的开发研究尤为重要。
目前,加氢脱氮(HDN)技术应用较为广泛,能有效降低石油及其产品氮含量,但该方法需消耗大量氢气,反应条件苛刻,经济成本高。非加氢脱氮方法包括溶剂精制法[6-7]、酸萃取法[8]、吸附法[9-11]、络合法[12]、微波法[13]、微生物法[14-15]等。络合脱氮法基于Lewis酸碱理论,利用能提供孤对电子的碱性氮化物(Lewis碱)与能接受电子的络合剂(Lewis酸)形成配合物,实现沉降分离,从而脱除碱性氮化物。络合脱氮法常选用具有空轨道的过渡金属离子作为络合剂。络合脱氮法具有可操作性强、成本低、选择性高、适用范围广等优势,因此具有广阔的发展前景。
Choi等[16-17]利用CuCl2脱除页岩油中的氮化物,脱除效率可达80%以上,且有较高的油品回收率。张胜等[18]利用TiCl4和CuCl2·H2O络合富集页岩油中的氮化物,结果表明两种金属盐络合可脱去85%以上的碱性氮化物,页岩油馏分沸点越低,金属盐对碱性氮化物的络合效果越好。陈月珠等[19-20]利用两步络合脱氮法富集分离润滑油中的氮化物,在前一种络合剂富集氮化物的基础上,再用CuCl2络合能进一步将氮化物分离成碱性氮化物和非碱性氮化物,提高了碱性氮化物的富集浓度。Qi Jiang等[21]利用微量金属离子与95%(w)乙醇组成的络合剂萃取脱除催化裂化柴油中的氮化物,有效地脱除了其中的碱性氮化物,柴油回收率达到97%以上,并考察了反应条件对氮化物萃取效率的影响。刘淑芝等[22]分别以AlCl3,CuCl2,FeCl3作络合剂,在甲醇溶剂下脱除催化裂化柴油中的碱性氮化物,当溶剂中加入甲酸时,可有效降低络合剂用量。胡震等[23]以FeCl3为络合剂脱除柴油中的碱性氮化物,脱除率可达90%以上。郭文玲等[24]在微波辐射条件下用微量SnCl2和95%乙醇组成的脱氮剂络合脱除柴油中的碱性氮化物,有较高的碱性氮脱除率和油品回收率。徐明等[25]利用自制的脱氮剂进行了页岩油络合脱氮工艺研究,在最佳的工艺条件下,可将页岩油中的碱性氮质量分数从3 775 μgg降至365 μgg。Zhang等[26]利用金属离子与甲醇、乙酸、水混合溶液组成的络合试剂脱除直馏柴油中的碱性氮化物,并探究了络合反应条件对碱性氮化物脱除效率的影响,在最佳络合条件下,能达到90%以上的碱性氮化物脱除率和油品回收率。张伟伟等[27]分别将未脱氮和络合脱氮后的焦化蜡油掺入催化裂化原料,对比考察了催化剂耗量、油浆收率和总液液体收率,结果表明脱氮蜡油可作为良好的催化裂化掺炼原料。周锦等[28-29]进行了焦化蜡油络合脱氮条件优化和中试试验研究,确定了最佳的反应温度和剂油比。Lai Tingting等[30]利用FeCl3络合分离减压蜡油(VGO)及其加氢产品中的碱性氮化物,碱性氮化物脱除率达80%以上。
目前,络合法脱碱性氮化物的报道以方法应用为主,对络合脱氮反应相关影响因素的研究较少,并且主要是优化反应温度和剂油比[31-32],很少考察溶剂的影响。虽然溶剂不直接参与反应,但是溶剂效应在有机反应中的作用不可忽视,对同一种样品,所用溶剂不同,溶质与溶剂间的相互作用也会有所差异。溶剂效应会影响反应平衡、速率甚至是反应机理,是影响反应活性的重要因素[33]。溶剂环境会影响金属-有机骨架材料的Lewis酸强度,即能改变配位金属原子接受电子的能力[34]。本课题以含有链烷烃、环烷烃、芳烃、噻吩类硫化物、非碱性氮化物、碱性氮化物的混合模型化合物来模拟石油组分,采用气相色谱-质谱(GC-MS)方法研究相同金属盐在不同溶剂条件下络合脱除碱性氮化物的效果,分析溶剂效应对络合脱氮反应的影响,旨在为络合法脱除石油中氮化物的应用提供理论支持与数据参考。
1 实 验
1.1 试剂及样品
2,2,4,4,6,8,8-七甲基壬烷(纯度97%)、正十六烷(纯度99%)、正癸基环己烷(纯度98%)、二苯并噻吩(纯度98%)、菲(纯度95%)、吖啶(纯度98%)、咔唑(纯度97%),均购自北京百灵威科技有限公司。二氯甲烷、甲苯、无水乙醇、正己烷,均为分析纯,购自北京精细化学品公司。FeCl3(纯度98%)、ZnCl2(纯度98%)、CuCl2(纯度99%)、PdCl2(纯度99.9%)、Fe2(SO4)3(分析纯)、ZnSO4·H2O(纯度97%)、CuSO4(纯度99%)、NiSO4·6H2O(纯度98%),均购自国药集团化学试剂有限公司。
1.2 仪器及条件
超声仪及条件:KQ-100DE型数控超声波清洗器;超声温度为60 ℃,超声频率为40 kHz,超声强度为100%,超声电功率为100 W。
GC-MS仪及条件:Agilent 7890B型气相色谱仪,配置Agilent 5977型质谱仪,美国Agilent公司产品。色谱柱为HP-5MS(30 m×0.25 mm×0.25 μm),美国Agilent公司产品。进样口温度为250 ℃,进样量为1 μL,分流比为100∶1。色谱柱流速为1 mLmin,升温程序为:初始温度100 ℃,保持2 min,以15 ℃min的速率升温至240 ℃,保持1 min。载气为高纯氦气(He)。质谱离子源为电子轰击电离源(EI),轰击电压为70 eV,离子源温度为230 ℃,质荷比(mz)范围为35~520。
1.3 模型化合物混合溶液的配制
分别称取0.5 g模型化合物2,2,4,4,6,8,8-七甲基壬烷、正十六烷、正癸基环己烷、二苯并噻吩、菲、吖啶、咔唑置于100 mL容量瓶中,加入二氯甲烷,超声使模型化合物充分溶解后定容,得到各模型化合物的质量浓度均为5 000 mgL的混合溶液。
1.4 碱性氮化物的脱除反应
分别移取2.0 mL模型化合物混合溶液于24个10 mL离心管中,编号为1~24,用氮气吹干模型化合物混合液中的二氯甲烷溶剂,分别向编号为1~8的离心管中加入2 mL二氯甲烷,向编号为9~16的离心管中加入2 mL甲苯,向编号为17~24的离心管中加入2 mL乙醇。分别称取8种金属盐作为络合剂加入到模型化合物溶液中,每种金属离子与吖啶物质的量比为6∶1,金属盐在二氯甲烷和甲苯中基本都以沉淀的形式存在,溶解度较低;氯盐在乙醇中溶解性较高,Fe2(SO4)3和NiSO4在乙醇中微溶,CuSO4和ZnSO4在乙醇中不溶[35]。在模型化合物溶液中加入金属盐后出现沉淀,有些是未溶解的固体盐,有些是反应生成的络合物。混合物在60 ℃下超声反应3 h。反应结束后,向溶液中加入3 mL正己烷,以降低络合产物在反应溶液中的溶解度,使络合产物尽量以沉淀的形式存在,而剩余的有机物仍保留在有机相中。在离心机转速为3 000 rmin的条件下离心分离5 min,得到上层有机相澄清液。利用GC-MS分析对比反应前后有机相,考察氮化物脱除情况。
2 结果与讨论
2.1 溶剂效应对Fe2(SO4)3,ZnSO4,CuSO4,NiSO4络合脱除氮化物效果的影响
改变金属盐络合脱除氮化物反应体系中溶剂的种类,考察金属盐在二氯甲烷、甲苯、乙醇体系下络合反应脱除氮化物的效果,其中Fe2(SO4)3,ZnSO4,CuSO4,NiSO4在3种溶剂体系中与氮化物络合反应前后得到的有机相的GC-MS总离子流色谱图(TIC谱图)见图1。在GC-MS的TIC谱图中,如果该络合反应能选择性地脱除碱性氮化物吖啶,则络合反应后的有机相中吖啶的峰会显著变弱,同时其他化合物的色谱峰与络合反应前无明显变化。从图1可以看出:Fe2(SO4)3,ZnSO4,CuSO4,NiSO4与模型化合物在二氯甲烷和甲苯体系反应后TIC谱图中碱性氮化物吖啶的峰与反应前模型化合物TIC谱图中吖啶的峰相比无明显变化,而在乙醇体系反应后TIC谱图中碱性氮化物吖啶的峰基本消失;这4种金属盐在二氯甲烷、甲苯和乙醇体系中反应前后有机相的TIC谱图中其他化合物的峰无明显变化。

图1 Fe2(SO4)3,ZnSO4,CuSO4,NiSO4在不同溶剂体系中络合反应前后有机相TIC图谱1—2,2,4,4,6,8,8-七甲基壬烷; 2—正十六烷; 3—正癸基环己烷; 4—二苯并噻吩; 5—菲; 6—吖啶; 7—咔唑。图2同
总体上看,上述4种硫酸盐在乙醇体系中有机相呈现出的TIC谱图与在二氯甲烷和甲苯体系中有机相呈现的TIC谱图有显著差异,即4种硫酸盐在二氯甲烷、甲苯溶剂体系中对碱性氮化物吖啶没有脱除效果,而在乙醇溶剂体系中,Fe2(SO4)3和CuSO4能有效地脱除碱性氮化物吖啶,ZnSO4和NiSO4也能脱除大部分碱性氮化物吖啶,说明乙醇的溶剂效应会显著影响4种硫酸盐的络合脱除碱性氮化物的效果。这主要是因为乙醇是质子溶剂,有利于金属盐的溶解和金属离子的解离[36-37],使4种硫酸盐的金属以离子的形式游离出来与碱性氮化物发生络合反应。
2.2 溶剂效应对CuCl2,PdCl2,ZnCl2,FeCl3络合脱除氮化物效果的影响

图2 CuCl2,PdCl2,ZnCl2,FeCl3在不同溶剂体系中络合反应前后有机相TIC图谱
CuCl2,PdCl2,ZnCl2,FeCl3在不同溶剂体系络合反应前后的有机相TIC图谱见图2。从图2(a)可以看出,CuCl2在甲苯和乙醇体系比在二氯甲烷体系中对碱性氮化物的脱除效果更好,这可能是由于甲苯中的π电子云与金属离子有较强的相互作用[38-39],有利于金属离子的解离,而乙醇作为一种质子溶剂既能促进金属盐的溶解也有利于金属离子的解离。从图2(b)可以看出,PdCl2在二氯甲烷和甲苯体系中不能选择性脱除碱性氮化物吖啶,而在乙醇体系中,PdCl2对碱性氮化物吖啶有较好的络合脱除效果。也说明质子溶剂有利于PdCl2中Pd2+的解离[40],从而促进络合反应的发生。从图2(c)可以看出,ZnCl2在二氯甲烷、甲苯和乙醇体系中对碱性氮化物吖啶的络合脱除效果一致,在这3种溶剂体系中都能有效地脱除碱性氮化物吖啶,说明溶剂效应对ZnCl2的影响不明显。从图2(d)可以看出,FeCl3在二氯甲烷和甲苯体系中能选择性地脱除碱性氮化物吖啶,但是在乙醇体系中络合反应较为复杂,吖啶的峰仅略有减弱。
总体来看,在二氯甲烷和甲苯溶剂体系中,图2中CuCl2,ZnCl2,FeCl3比图1中4种硫酸盐对碱性氮化物吖啶的络合脱除效果好,这可能是由于硫酸盐的晶格能显著高于氯盐的晶格能[16],二氯甲烷和甲苯较难使硫酸盐克服高晶格能的束缚,金属离子难以游离出来接近碱性氮化物分子,从而影响了硫酸盐的络合脱氮效果。而CuCl2,ZnCl2,FeCl3相对较低的晶格能使得其对溶剂的要求不十分苛刻,即使在二氯甲烷和甲苯中,也能较好地脱除碱性氮化物吖啶。
2.3 FeCl3在乙醇体系进行络合反应的副反应
从图2(d)中FeCl3络合后有机相的TIC谱图可以看出,二苯并噻吩、菲的峰强度减弱,无咔唑的峰,保留时间约12 min处的峰归属为氯代菲(质谱见图3),FeCl3在乙醇体系进行络合反应时伴随着副反应,也说明乙醇体系有利于FeCl3电离,产生了过量的氯离子[41],在室温条件下进行超声反应也很容易发生芳香环上的氯代反应。而络合反应后咔唑峰的消失有可能是咔唑在Fe3+的催化作用下,在乙醇体系中形成了大分子聚合物,滞留在沉淀中[42-44]。咔唑聚合反应示意见图4,这与咔唑在FeCl3水溶液中发生聚合反应现象相似[45]。此外,噻吩类化合物在该体系中也有可能发生氧化偶联反应[46-47]形成聚合物,从而导致二苯并噻吩的峰强度变弱。总之,FeCl3在乙醇体系进行络合反应时发生的副反应过多,并且引入了氯代芳烃这种对后续加工非常不利的副产物,因此在实际应用中应尽量避免使用这一反应体系。
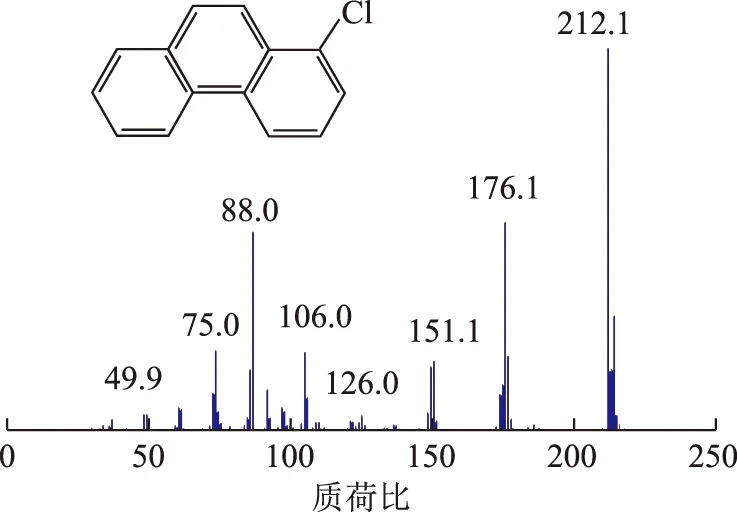
图3 氯代菲的质谱

图4 咔唑的聚合反应
3 结 论
(1)Fe2(SO4)3,ZnSO4,CuSO4,NiSO4在二氯甲烷和甲苯体系中不能有效脱除碱性氮化物,而在乙醇体系中能较好地络合脱除碱性氮化物,即乙醇的溶剂效应会显著影响这几种金属盐络合脱除碱性氮化物的效果,二氯甲烷和甲苯对这几种盐没有表现出溶剂效应。
(2)溶剂对ZnCl2络合脱除碱性氮化物的效果影响不明显,会显著影响CuCl2和PdCl2络合脱除碱性氮化物的效果。CuCl2在甲苯和乙醇体系比在二氯甲烷中脱除碱性氮化物效果好。PdCl2在二氯甲烷和甲苯中均不能与碱性氮化物发生反应,但在乙醇体系则能有效地脱除碱性氮化物。
(3)FeCl3在乙醇体系进行络合反应时有氯代、聚合等较严重的副反应,应尽量避免利用这一反应体系络合脱除碱性氮化物。
