MHS固相萃取-火焰原子吸收法测定食品及水中铅 (II)
2020-12-01吕琳琳兰金铃刁全平吴航贾莲
吕琳琳,兰金铃,刁全平,吴航,贾莲
鞍山师范学院化学与生命科学学院(鞍山 114007)
随着工业生产活动增加,环境污染问题越来越严峻,尤其是重金属污染现象不断加剧。重金属污染主要由采矿、冶炼、印染等人为因素造成[1],这些行业在生产过程中使大量的铅、汞、砷、镉等重金属进入水体、土壤、大气中,引起严重危害。重金属污染具有富集性、不可降解性等特点。即使废水中重金属含量非常低,但是其可在土壤和水体底泥中富集,进而迁移至生长、生活在受污环境中的农作物和鱼类中。人类食用了这些受污染的农作物和鱼类及其制成的食品,重金属就会在人体内(如肝脏等器官内)蓄积,当超过人体所能耐受的限度,会造成中毒。铅、汞、砷、镉是对人体危害最严重的4种重金属,即使含量非常低,也会对人体造成非常大的危害[2]。例如,铅中毒会使人贫血、肾脏损伤、高血压甚至神经机能失调[3],如果在儿童时期即铅中毒,还会严重影响其认知能力和行为能力[4]。
食品及水中铅的分析方法主要有电化学法[5-6]、氢化物-原子荧光光谱法[7-8]、火焰原子吸收法[9]、电感耦合等离子体发射光谱法[10]、电感耦合等离子体质谱法[11]。其中,火焰原子吸收法是应用最普遍的分析方法。但这种方法的主要问题是在分析含量是μg/L级别样品时灵敏度比较低。常用的富集方法有浊点萃取法[12-13]、溶剂萃取法[14]、沉淀法[15]和固相萃取法等。浊点萃取法操作繁琐,而且有机相黏度较大,在测定前需要用水等适合的溶剂稀释,这样就降低了富集倍数[16];溶剂萃取法需要使用大量有机溶剂,富集成本高,而且严重污染环境;沉淀法溶度积较大,使得被测离子溶解损失较多[17]。固相萃取技术作为一种高效的富集方法,是近年来国内外学者研究热点[18-20],吸附剂材料的研制更是研究的重点[21-23]。
试验自制固相萃取吸附剂MHS,提出一种快速富集食品及水中铅(Ⅱ)的固相萃取方法,结合火焰原子吸收光谱仪对食品及水中铅(Ⅱ)含量进行测定。固相萃取吸附剂MHS用于痕量样品中铅的富集尚鲜见报道。
1 材料与方法
1.1 材料与试剂
榛子(产自辽宁岫岩,去仁留壳);邻苯二甲酸氢钾(KHP)、盐酸、氯化钾、六亚甲基四胺、三羟甲基氨基甲烷(Tris)(均为分析纯,国药集团化学试剂有限公司);铅标准溶液(1 000 μ g/mL,国家标准物质研究中心);标准物质GBW 10018(鸡肉)、GBW 10014(白菜)(地质科学院地球物理地球化学勘察研究所);制备MHS用于固相萃取;超纯水;聚四氟乙烯容器、玻璃容器均在10% HNO3中浸泡48 h以上,使用前超纯水重新多次。
缓冲溶液(0.1 mol/L):HCl/KCl缓冲液pH 1.0~2.0;KHP-HCl缓冲溶液pH 2.0~4.0;六亚甲基四胺-HCl缓冲溶液pH 4.0~6.0;Tris-HCl缓冲溶液pH 7.0~8.0。
1.2 仪器与设备
PinAAcle 900F原子吸收分光光度计(Perkin Elmer);上海新科MK-Ⅲ型光纤压力自控密闭微波消解系统;Milli-Q Gradient纯水机;Pb-10 pH计(德国Sartorius)。
1.3 样品
大米、鸡肉、生菜、带鱼、黄豆,购自辽宁鞍山长大供销城;河水采自辽宁鞍山万水河。所有样品用超纯水冲洗干净,大米、生菜、黄豆70 ℃烘干24 h,鸡肉、带鱼110 ℃烘干48 h。烘干后样品粉碎备用。
1.4 固相萃取剂制备
将榛子壳洗净、烘干后用粉碎机粉碎,过筛,得到粒径约0.18 mm榛壳粉HS。称取5 g HS于大烧杯中,加入50 mL 0.1 mol/L NaOH和50 mL 95%乙醇。密闭杯口,在40 ℃水浴中搅拌24 h(150 r/min)。弃去上清液,用大量超纯水洗涤改性后榛壳粉,直至上清液pH近中性,弃去上清液。将得到的NaOH改性榛壳粉于70 ℃恒温干燥箱中烘干24 h,将其命名为SHS。
巯基乙酸40 mL,冰醋酸10 mL和浓硫酸0.2 mL加至烧杯中,冷却后加入5 g SHS,完全浸湿,密闭杯口,80 ℃水浴中搅拌30 min(150 r/min)后,静置浸泡12 h。弃去上清液,大量蒸馏水洗涤改性榛壳粉,至上清液近中性,过滤,70 ℃恒温干燥箱中烘干24 h,得到巯基乙酸改性的榛壳粉,将其命名为MHS。
1.5 固相萃取
装柱:在6 mL固相萃取柱管底部铺上筛板,装入MHS,轻轻振荡,使填料均匀平铺,压好筛板,即得自制固相萃取小柱。
取25 mL 10 μ g/L Pb(Ⅱ) 溶液,用10 mL六亚甲基四胺-HCl缓冲溶液调节溶液pH至5.5。样液流速和洗脱液流速均控制为2.0 mL/min。样液流净后用少量超纯水冲洗固相萃取小柱。然后,用25 mL 3 mol/L HCl冲洗小柱。将洗脱液蒸发浓缩至近干,用0.5 mol/L HNO3溶液定容至2 mL,用火焰原子吸收测定溶液中Pb(Ⅱ) 浓度。
1.6 样品制备
准确称取0.1 g左右样品于聚四氟乙烯烧杯中,加入10 mL浓HNO3和3 mL H2O2,加热至溶液澄清透明,继续加热蒸发至近干。用超纯水定容至25 mL。加入10 mL六亚甲基四胺-HCl缓冲溶液调节溶液pH 5.5。按照1.5小节的中固相萃取过程对样液进行富集,并分析测定。
方法同样适用于各种水样。通过消解、过滤等方式使水样澄清透明,加入缓冲溶液调节至pH 5.5,富集,用火焰原子吸收测定水样中Pb(Ⅱ) 浓度。
2 结果与讨论
2.1 pH的影响
样液的pH是吸附过程中至关重要的因素。考察在pH 1.0~8.0范围内Pb(Ⅱ) 回收率随pH变化情况。试验中所用缓冲溶液为:HCl/KCl缓冲液pH 1.0~2.0;KHP-HCl缓冲溶液pH 2.0~4.0;六亚甲基四胺-HCl缓冲溶液pH 4.0~6.0;Tris-HCl缓冲溶液pH 7.0~8.0。pH大于5.0以后,吸附达到恒定,吸附率达到98%以上。所以,选择pH 5.5作为试验pH。这是因为在低pH范围内,H+同Pb(Ⅱ) 存在竞争吸附关系,阻碍Pb(Ⅱ) 的吸附;随着pH升高,H+浓度降低,Pb(Ⅱ) 的吸附率随之增加。

图1 样液pH对吸附性能的影响(n=3)
2.2 洗脱液的类型、浓度、体积的影响
为将吸附在MHS上的Pb(Ⅱ) 洗脱下来,考察洗脱液的种类及体积对洗脱效果的影响。试验结果见图2和图3。试验表明25 mL 3 mol/L的HCl溶液洗脱效果最好。

图2 不同洗脱液对回收率的影响(样品体积25 mL、pH 5.5、n=3)

图3 3 mol/L HCl洗脱液的体积对回收率的影响(样品体积25 mL、pH 5.5、n=3)
2.3 样液及洗脱液流速对回收率的影响
考察1.0~10.0 mL/min范围内,样液流速及洗脱液流速对回收率的影响,以确定最佳的试验条件。如图4所示。结果表明,样液流速和洗脱液流速2.0 mL/min时,回收率可达99%以上。因此,选择样液和洗脱液的流速2.0 mL/min。

图4 样液及洗脱液流速对回收率的影响(样品体积25 mL、pH 5.5、n=3)
2.4 样液体积的影响
实际样品,尤其是水样中,Pb(Ⅱ) 含量很低。为分析实际水样,需要确定最大能适用的样液体积。在最优的试验条件下,考察体积在25~1 000 mL范围内,Pb(Ⅱ) 含量为10 μg/L的模拟样品溶液回收率的变化情况,结果见图5。样品容量不超过600 mL时,回收率保持不变,在99%以上。此时,富集倍数为300倍(富集倍数=样品溶液600 mL/最终体积2 mL)。
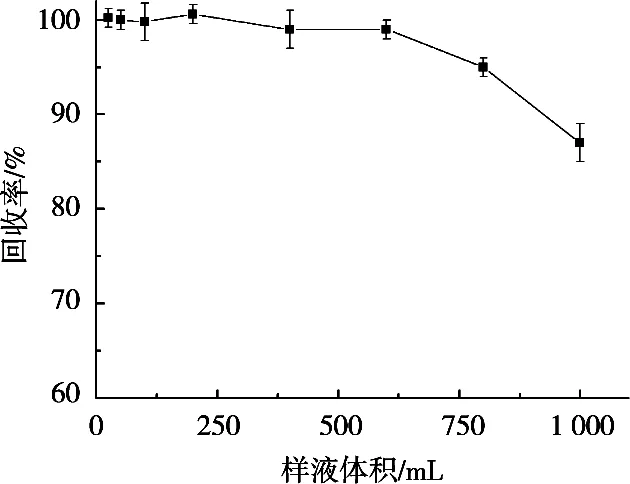
图5 样液体积对回收率的影响(n=3)
2.5 干扰离子
考察食品及水样中普遍存在的阴阳离子对测定的干扰情况,如Na+、K+、Ca2+、Mg2+、Cl-、NO3-、PO43-、Fe3+、Cu2+、Zn2+[24-25]。结果见表1。试验结果表明,样品中常见离子引入的干扰很小,被测离子Pb(Ⅱ) 的回收率均大于95%。因此,可将MHS作为固相萃取剂用于测定食品及水中的Pb(Ⅱ) 。

表1 共存离子对回收率的影响(n=3)
2.6 标准曲线
在试验条件下,分别富集30 mL浓度5,20,50,100,150,200,250和300 μg/L的Pb(Ⅱ) 标准溶液,测定吸光度,绘制标准曲线。其线性范围为5~300 μ g/L,线性方程为A=1.002 1c+0.005 21,线性相关系数为R2=0.999 7。
2.7 方法检出限与精密度
对空白试样在最佳试验条件下连续测定11次,计算方法检出限,该方法检出限为0.22 μg/L。在最佳试验条件下,对10 μg/L的Pb(Ⅱ) 标准溶液平行测定11次,计算得到相对标准偏差,为2.8%。
2.8 样品测定
按照试验方法,对标准品中Pb(Ⅱ) 含量进行测定,结果见表2。试验结果表明,测定值和标准值能很好地吻合,证明该固相萃取方法准确、可靠。

表2 固相萃取法测定标准物质中Pb(n=3)

表3 样品回收率试验(n=3)
按照试验方法对样品中Pb(Ⅱ) 含量进行测定,并进行加标回收试验,结果见表3。试验结果表明,回收率均大于95%,进一步说明该方法准确、可靠。对河水、大米、鸡肉、黄豆、生菜、带鱼的测定结果表明,样品中Pb(Ⅱ) 含量均在国家标准范围内[26-30]。
3 结论
MHS作为一种新型固相萃取剂,具有成本低廉、制备简单等特点,对于Pb(Ⅱ) 的富集效果非常好。采用新型固相萃取剂MHS富集食品及水体中Pb(Ⅱ) ,并利用火焰原子吸收仪器测定其含量,建立分析食品及水中Pb(Ⅱ) 含量的分析方法。方法检出限低、精密度好,对辽宁鞍山地区市售农副产品及河水进行测定的回收为95%~104%。干扰试验表明食品及水中大量存在的离子不干扰测定。方法用于分析食品及水体中Pb(Ⅱ) 含量,操作简单、快速,结果准确、可靠。
