一个基于多羧酸刚性配体的镉配合物的合成、结构及质子传导性研究
2020-11-27初芷同何占宇刘厚亭王素娜
初芷同 何占宇 刘厚亭 卢 静 王素娜
(聊城大学 化学化工学院、山东省化学储能与新型电池技术重点实验室,山东 聊城 252059)
0 引言
质子导体作为质子传输的载体,已被广泛应用于燃料电池、氢气分离、蒸汽电解、传感器和生物传输系统等领域[1-3]. 在过去的几十年里,人们致力于寻找稳定和高传导性的质子导体,发现了Nafion(全氟磺酸聚合物)、陶瓷、碳修饰材料、钙钛矿、金属有机骨架(MOFs)等多种材料具有质子导体的功能,它们表现出不同的质子电导率[4-6]. 在目前所报道的质子导体中,Nafion因其高的质子传导率而得到广泛的应用,但Nafion的热稳定性较差,只能在80 ℃以下才能表现出稳定的高质子传导率. 陶瓷、碳修饰材料等虽然也能表现出良好的质子传导性,但是它们无定形的存在形式使得人们无法准确得知其内在的结构特点,无法确定其质子传导机理. 众所周知,明确材料的结构与质子传导性能间的关系可为开发更高的质子传导新材料提供理论指导,因此质子传导机理是当前科学工作者研究和探索的重点[7,8].多孔晶体材料MOFs的结晶性质使人们能够借助现代技术手段确定其准确的组成结构,这为质子传导机理的研究提供了一个良好的平台. 此外,MOFs材料具有框架可调性、化学稳定性、易与其他材料复合等优点,使其成为质子导体的优良候选材料[9,10].

本文选择同时具有多个亲水性羧酸取代基和氮杂环的刚性有机配体(H3L,图1)与金属Cd(II)在水热条件下得到了一个三维MOFs材料{[Cd3(L)2}n(1),并通过元素分析、红外光谱和单晶X-射线衍射等对其组成和结构进行了表征. 电化学测试结果表明:配合物1在与Nafion复合后,表现出了比空白Nafion更优良的质子传导性.
1 实验部分
1.1 仪器与试剂
Cd(CH3COO)2·2H2O、配体、Nafion溶液、娃哈哈纯净水均为市售试剂,未经处理直接使用.

图1 配体H3L的分子结构图
X-射线单晶衍射分析是在Agilent Gemini-E型 X-射线单晶衍射仪上进行的;X-射线粉末衍射分析是在Bruker D8 粉末衍射仪上进行;元素分析和红外分析分别用元素分析仪Perkin-Elmer 2400 II型和红外光谱仪Nicolet-5700型 (KBr压片,扫描范围400-4000 cm-1)测试;质子传导性能测试采用的是上海辰华的CHI 660-D电化学工作站.
1.2 配合物1 的合成及表征
称取Cd(CH3COO)2·2H2O (10 mg,0.04 mmol)和H3L配体 (3 mg,0.01 mmol)加入到10 mL去离子水中,室温下搅拌30 min. 然后用0.1 mol·dm-3的盐酸溶液调节混合物的pH=3,将混合物转移到15 mL反应釜中,在180 ℃烘箱中加热4 d. 最后,用一天时间缓慢降至室温,得到透明的无色块状晶体. 过滤,晶体用去离子水洗涤三次,室温下自然干燥,产率约为30%(按Cd计算). 元素分析:C28H12N2O12Cd3理论值:C:37.10%, H:1.32%, N:3.09%; 实验值 C:37.31%, H:1.34%, N:3.12%. 红外光谱 (KBr, υ/cm-1):3430 br, m, 1616 s, 1551 s, 1433 s, 1395 s, 1362 s, 1235 m, 1112 w, 1079 w, 912 w, 846 w, 773 m, 735 m, 702 m, 644 w, 539 w.
1.3 配合物1晶体结构的测定
在室温下,选取尺寸为0.23 mm×0.22 mm×0.20 mm的单晶置于Agilent Gemini-E CCD衍射仪上,在室温下,用石墨单色化的Cu Kα辐射为光源(λ=1.54184 Å)进行测定. 化合物的最初结构由SHELXS直接法解出,并利用SHELXL软件包[17,18]对结构内所有非氢原子的坐标和各向异性参数用最小二乘法F2进行精修,所有的氢原子坐标都采用理论计算的加氢方式,并对其进行各向同性精修[19]. 化合物的晶体学数已提交至英国剑桥晶体数据中心(CCDC-1941129),可通过http://www.ccdc.cam.ac.uk下载.
1.4 电化学测试
测试采用三电极体系:工作电极为由掺杂了配合物1的Nafion的复合膜修饰的玻碳电极或纯Nafion薄膜修饰的玻碳电极,参比电极为Ag-AgCl电极,对电极为铂电极. 以市售的娃哈哈纯净水或者pH=5.5的硫酸溶液为电解质溶液. 在扫描前,用恒温夹套将电解质溶液温度升至测定温度,并保持扫描过程中温度恒定.
工作电极的制作:准确称取配合物1的晶体颗粒1 mg加入500 μL水中,球磨10 min后得到颗粒度均一的样品,将其超声分散5 min,得到分散均匀的配合物悬浊液. 将100 μL的Nafion(5%)溶液用400 μL水稀释,得到Nafion稀释液. 取5 μL悬浊液和5 μL Nafion稀释液混合均匀,滴在玻碳电极表面,将此电极在室温下放置1 h,然后置于60 ℃干燥箱中加热1 h,得到以配合物掺杂的Nafion复合膜修饰的玻碳工作电极.
2 结果与讨论
2.1 晶体结构
X-射线单晶结构分析表明,配合物{[Cd3(L)2}n(1)晶体以单斜晶系,P21/c空间群方式堆积. 晶体学独立单元中含有一个L3-配体阴离子和两种Cd(II)阳离子,其中Cd2(II)阳离子的占有率为0.5. 如图2(a)所示,在配合物1中Cd1离子与来自于六个不同L3-配体的六个羧基氧原子(O2A,O2B,O4C,O4D,O6,O6E)配位,形成变形的[CdO6]八面体的几何构型,Cd1位于八面体的配位中心. 其中,四个羧基来自于苯环取代基,两个羧基来自于吡啶环取代基. Cd2离子与来自于两个不同L3-配体的苯环上的三个羧基氧原子(O1F,O2F,O5H),来自第三个L3-配体的吡啶环上的一个羧基氧原子(O3G)以及来自于第四个L3-配体的吡啶氮原子(N1)形成变形的四方锥构型[CdO4N],如图2(b)所示. 配合物中的L3-配体完全被去质子化,其中,苯环上的两个羧基分别采取桥连和螯合桥连的方式连接了4个Cd(II)离子,吡啶环上的羧基桥连了另外两个Cd(II)离子,吡啶氮原子与第七个Cd(II)配位. 所以L3-配体采用的是(κ1-κ1)-(κ1-κ1)-(κ1-κ2)-κ1-μ7七桥连配位模式,如图2(c)所示. 图3(a)所示的来自于六个L3-配体的六个苯环上羧基将三个Cd(II)中心连接形成直线型的三核簇[Cd3(CO2)6]次级结构单元,其中[Cd(1)O6]八面体位于三核簇的中心,与两侧的[Cd(2)O4N]四方锥通过共角的方式连接. L3-配体通过羧基将三核[Cd3(CO2)6]簇次级单元连接形成沿c轴方向延伸的一维链状结构,如图3(b). 同时,[Cd3(CO2)6]簇的两侧分别与另外两个L3-配体的吡啶环上的羧基和氮原子配位. 如此,临近的[Cd3(CO2)6]簇链彼此间通过L3-配体上的吡啶环上的羧基和氮原子连接形成3-D网状结构,如图3(c). 其中,每个Cd3簇被八个L3-配体连接,每个L3-配体与四个Cd3簇作用,其3-D拓扑结构图如图3(d)所示.
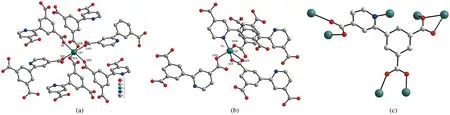
注:对称操作码:A:x,y,z-1; B: -x, -y+2, -z; C: -x,y+0.5, -z-0.5; D:x, -y+1.5,z-0.5; E: -x,-y+2, -z-1; F:-x+1, -y+2, -z; G: -x+1, -y+1.5,z+0.5; H:-x+1, -y+2, -z+1.
图2(a)Cd1离子的配位环境;(b)Cd2离子的配位环境;(c)配体L3-的配位模式
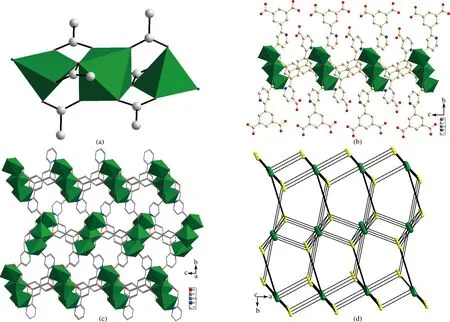
图3 (a)[Cd3(CO2)6]三核簇次级结构单元示意图;(b)通过羧基连接三核簇次级结构单元形成的一维链状图;(c)通过吡啶环连接一维链形成的三维网状图;(d)三维拓扑结构图,黄色球代表有机配体L3-,绿色球代表Cd3簇
2.2 粉末X-射线衍射分析
为了验证配合物(1)的纯度,对它进行了粉末X-射线衍射测试.如图4所示,实验测定的谱图和单晶结构分析模拟的粉末X-射线衍射谱图吻合地很好,证明了配合物(1)是均一的纯相.

图4 配合物1模拟(a)和实验(b)的粉末X-射线衍射图谱
2.3 质子传导性
为了降低配合物1固体颗粒间的晶间电阻,将配合物1 的固态颗粒掺杂在具有良好质子传导性能的有机聚合物Nafion(全氟磺酸薄膜)中,形成复合膜. 在30℃条件下分别测定了配合物1与Nafion形成的复合膜以及空白Nafion修饰的玻碳电极在纯水中的循环伏安行为. 如图5(a)所示,复合膜的循环伏安曲线的峰电流密度与空白Nafion相比有明显增加,表明配合物的掺杂提升了Nafion膜的质子传导行为. 分析配合物1组成结构可推测,由于配合物结构中存在大量的羧基,且所有的羧基都脱去质子并与金属Cd(II),这使得配合物既具有良好的亲水性,也具有一定的亲质子性,与Nafion掺杂后能够提升复合膜的吸水性和结合质子的能力. 配合物中羧基与Nafion中的磺酸基以及吸收的水分子间形成连续的氢键,从而提高复合膜的质子传导性.由图5(b)可以看出,复合膜修饰的玻碳电极的循环伏安峰电流密度随着扫描速率的减小而减小. 峰电流密度与扫速呈直线关系,表明复合膜的质子传导的动力学行为受扩散速率控制. 为了探究温度以及氢离子浓度对于质子电导率的影响,测量了复合膜修饰的玻碳电极分别在中性水和pH=5.5的硫酸溶液中不同温度下的电化学行为和质子传导行为. 如图6所示,电极在中性水中以及硫酸溶液中的氧化峰电流密度随着温度的持续上升逐渐增大,氧化电位逐渐向负电位移动. 且硫酸溶液中的峰电流密度明显高于中性水中的峰电流密度. 说明升高温度、增加酸度皆可以提高H+在复合膜中的传导性.

图5 (a)空白Nafion和复合膜修饰的玻碳电极在纯水中的循环伏安曲线;(b)复合膜修饰的玻碳电极在纯水中不同扫速下的循环伏安曲线
为了研究配合物的质子传导机制,分别对复合膜在纯水中和硫酸溶液中进行了交流阻抗谱学测试. 通过Nyquist图中的容抗弧可知,复合膜在纯水中如图7(a)和硫酸溶液中如图7(c)的电阻率都随温度增加逐渐变小. 复合膜的质子传导率可由公式σ=L/(RS)计算得到[20].其中,σ为质子传导率,L和S分别代表复合膜的厚度(cm)和面积(cm2),R代表复合膜的电阻. 通过计算得出在复合膜在30 ℃和50 ℃时,水中的质子传导率分别为1.07 x 10-4S·cm-1和1.51 x 10-4S·cm-1,而空白Nafion膜的质子传导率在30 ℃和50 ℃时水中电导率分别是7.82 x 10-5S·cm-1、10.6 x 10-5S·cm-1. 由此可见,掺杂了配合物的复合膜的质子传导率明显升高,由此可见配合物的掺杂有利于Nafion膜内外质子的传输. 同理可得到复合膜在pH=5.5的硫酸溶液中,电导率分别为5.22 x 10-4S·cm-1(30 ℃)和7.04 x 10-3S·cm-1(50 ℃),明显高于其在纯水中的电导率. 这表明酸度的增加提高了H+在膜内传输的速度,使材料的质子传导性能提升.

图7 (a)不同温度下,复合膜修饰的玻碳电极在水中的Nyquist图; (b)水中的ln(σT)对1/T的Arrhenius图,红色直线代表最佳线性拟合结果;(c)不同温度下,复合膜修饰的玻碳电极在硫酸溶液中的Nyquist图; (d) 硫酸溶液中的ln(σT)对1/T的Arrhenius图,红色直线代表最佳线性拟合结果
研究表明,质子在固态材料中的传输机制主要有两种形式[21]:一种是Grotthuss跳跃式传导,相邻的质子载体之间通过氢键的断裂与再形成将质子传输,该种模式的传导活化能一般小于0.4 ev;另一种是Vehicular运载式传输,载体带着质子在通道内扩散,传导活化能一般大于0.4 ev. 在人们无法确定质子传输过程的情况下,通常通过质子传导活化能的计算判断材料的质子传导机制. 质子传导活化能与质子传导率之间遵循Arrhenius关系式[22]:σT=Aexp(-Ea/kBT). 其中,T、A、Ea、kB分别代表热力学温度、指前因子、质子传导活化能和Boltzmann常数. 因此以ln(σT)对1/T作图,即可从直线斜率求得复合膜的质子传导活化能. 如图7(c、d)所示,在水中和硫酸溶液中分别测得的不同温度下得到的ln(σT)数值点均能很好落在同一条拟合直线上,即复合膜的质子传导行为很好的遵循Arrhenius关系式. 通过线性拟合结果的斜率计算得到复合膜在水中和硫酸溶液中的质子传导活化能分别是0.15、0.17 eV,二者均小于0.4 eV,为Grotthuss传导.
3 结论
利用含有多个亲水性羧酸基团修饰的刚性有机氮杂环配体与过渡金属Cd在水热条件下成功合成了一个三维网络结构的配位聚合物{[Cd3(L)2}n1. 结构研究表明,配合物1中的三个相邻的Cd(II)通过羧基连接形成三核的Cd3簇,该三核簇被配体进一步连接形成三维配位网络. 对配合物1掺杂的Nafion复合膜进行了循环伏安和交流阻抗谱的测试研究. 结果表明,配合物1的掺杂能够明显提高膜的质子传导性能,且复合膜的质子传导率随温度和酸度的提高而提高.不同温度下的质子传导率的Arrhenius拟合结果表明复合膜的质子传导机理遵循Grotthuss机理.
