壳聚糖催化正丁醛自缩合反应性能
2020-11-24张佳勋胡柏松安华良赵新强王延吉
张佳勋,李 颖,胡柏松,安华良,赵新强,王延吉
(河北工业大学 化工学院,绿色化工与高效节能河北省重点实验室,天津300130)
1 前 言
正丁醛自缩合合成2-乙基-2-己烯醛(辛烯醛)反应是工业生产2-乙基己醇(辛醇)的重要步骤之一。辛醇主要用于生产邻苯二甲酸二辛酯、对苯二甲酸二辛酯、己二酸二辛酯等增塑剂,在溶剂、胶黏剂、石油添加剂等方面也有广泛应用[1-2]。辛醇工业生产采用羰基合成工艺,即丙烯氢甲酰化合成正丁醛、正丁醛自缩合合成辛烯醛、辛烯醛加氢得到辛醇。正丁醛自缩合反应为典型的羟醛缩合反应,其可在酸催化剂、碱催化剂或酸碱两性催化剂作用下进行。目前,工业采用液体碱(氢氧化钠水溶液)催化正丁醛自缩合反应。虽然该工艺可以获得较高的正丁醛转化率和辛烯醛收率,但是存在设备腐蚀、含碱废水排放量大、对环境污染严重等问题。为克服液体碱存在的缺点,开发绿色高效的非均相催化剂成为目前研究的热点。Tsuji等[3]考察了MgO 和CaO对正丁醛自缩合反应的催化性能,发现当催化剂为MgO时,正丁醛转化率为35%,副产物主要为二聚物2-乙基-3-羟基己醛;当用CaO催化该反应时,正丁醛转化率为41%,副产物主要为三聚物(即2-乙基-3-羟基己醛与正丁醛发生季先科交叉酯化反应生成的副产物丁酸-2-乙基-3-羟基己酯)。Hamilton 等[4]以Na/SiO2为催化剂研究正丁醛自缩合反应,在350℃下反应4 h,正丁醛转化率为58.0%,辛烯醛选择性为84.6%。本课题组对KF-γ-Al2O3、Ce-γ-Al2O3和La-γ-Al2O3催化正丁醛自缩合反应进行了研究[5-7]。其中,刘肖红等[5]采用KF-γ-Al2O3催化正丁醛自缩合反应,建立了酸碱协同催化机理,辛烯醛收率和选择性分别可达98.1%和99.1%,但催化剂重复使用性能较差。Xiong 等[6]对Ce-γ-Al2O3催化正丁醛自缩合反应进行了研究,在180℃下反应8 h,辛烯醛收率和选择性分别可达83.1%和88.6%。但当在固定床上进行该反应时,存在因Al2O3水合而导致床层堵塞的问题[8]。上述催化剂的催化活性虽然较好,但其存在反应温度较高或重复使用性能较差等问题。壳聚糖是一种多聚糖,通过甲壳素的碱性脱乙酰作用获得,来源广泛,可生物降解。其分子链上分布着大量─NH2和─OH,可用作催化剂,具有价廉、反应条件温和、催化活性高、选择性好等优点,在缩合、加氢等反应中已有应用。Reddy等[9]采用二甲基亚砜为溶剂,以壳聚糖水凝胶为催化剂催化对硝基苯甲醛与丙酮的羟醛缩合反应,室温下反应18 h,对硝基苯甲醛转化率达100%,β-羟基酮选择性为90%。Sudheesh 等[10]用壳聚糖水凝胶催化庚醛与苯甲醛的缩合反应,160℃下反应8 h,庚醛转化率超过99%,茉莉醛选择性达88%,催化剂可重复使用6次。
本文选用壳聚糖作为正丁醛自缩合反应催化剂,考察了反应条件的影响和壳聚糖的重复使用性能,建立了其回收再利用方法。在此基础上,采用DFT模拟计算了该反应控速步骤的表观活化能,阐明了壳聚糖催化正丁醛自缩合的酸碱协同作用机理。
2 实验部分
2.1 原料与试剂
正丁醛:天津大茂化学试剂厂;邻二甲苯:天津市光复精细化工研究所;氨水:天津市风船化学试剂有限公司;无水乙醇:天津市科密欧化学试剂有限公司;壳聚糖:浙江澳兴生物科技有限公司。除壳聚糖外,以上试剂均为分析纯。市售壳聚糖先用蒸馏水清洗3次,再于100℃下烘干,即可用作催化剂。
2.2 催化剂表征
利用美国NICOLET NEXUS 470 型傅里叶红外光谱仪(FI-IR)分析催化剂表面官能团。分辨率为4 cm-1,扫描速度为0.2 cm.s-1,扫描范围为400~4 000 cm-1。采用KBr 压片法制样。
采用美国TA 公司SDT-2960型热分析仪测定壳聚糖热稳定性。在氮气氛围下进行测定,氮气流速为50 mL.min-1,升温速率为10℃.min-1,测试温度范围为50~500℃。
2.3 催化剂活性评价
正丁醛自缩合反应在100 mL 高压反应釜中进行。典型操作如下:在反应釜中加入30 g正丁醛和1.5 g催化剂,用N2置换釜内空气3次,升温至140℃保持反应8 h,反应结束。待反应液冷却后用气相色谱分析其组成。
2.4 定量分析方法
采用北京北分瑞利分析仪器有限公司生产的SP 2100 型气相色谱仪对产物进行定量分析。以30 mL.min-1的氮气为载气;氢火焰检测器和气化室温度均控制在220℃;KB-1毛细管柱,采用程序升温控制柱温:初温100℃,保持2 min,以10℃.min-1升温至200℃,再保持10 min。以邻二甲苯为内标物,采用内标法进行分析计算。
3 结果与讨论
3.1 壳聚糖的性质和催化性能评价
本文以分子量为30×104的壳聚糖(chitosan,CTS)为催化剂,对其催化正丁醛自缩合反应进行研究。分别对壳聚糖进行了红外光谱和热重分析。图1为壳聚糖样品的红外光谱。红外谱图中各个峰的归属如下:1 078和1 029 cm-1处的吸收峰归属于C─O 键的伸缩振动,1 156 cm-1处的吸收峰归属于C─O─C键的伸缩振动,1 382 cm-1处的吸收峰归属于C─H 键的变形振动,1 599 cm-1处的吸收峰归属于─NH2的变形振动,1 654 cm-1处的吸收峰为C═O键的伸缩振动,2 919 cm-1处的吸收峰为─CH2的伸缩振动,3 444 cm-1处的吸收峰为─NH2的伸缩振动和O─H键伸缩振动。红外光谱分析结果表明壳聚糖表面兼具酸碱两种活性基团,分别为─NH2和─OH。这两种活性基团的存在具备正丁醛自缩合反应所需催化剂的基本特征。

图1 壳聚糖的FT-IR 分析Fig.1 FT-IR spectrum of chitosan sample
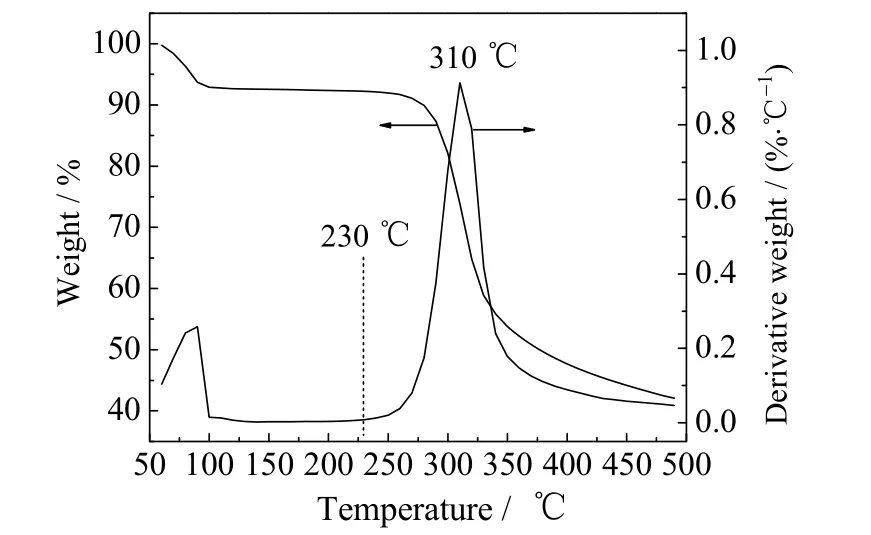
图2 壳聚糖的TG/DTG 曲线Fig.2 TG and DTG curves of chitosan sample
壳聚糖样品的TG 和DTG 曲线如图2所示。从图中可以看出,升温过程中壳聚糖主要有两次失重,分别在60~103℃和230~450℃。第1阶段归属于吸附水分子的脱除,失重量大约为7%。第2阶段质量减少约50%,主要是因为多糖链的分解。失重过程中最大失重速率出现在310℃,为0.9%.℃-1。因此,催化剂的热稳定温度为230℃。文献[9-10]中以壳聚糖催化硝基苯甲醛与丙酮、以及庚醛与苯甲醛的羟醛缩合反应,其结果表明,这2个反应适宜的反应温度分别为80和160℃。参考该结果推测壳聚糖的热稳定温度应该可以满足正丁醛自缩合反应的需要,并初步确定壳聚糖催化正丁醛自缩合的反应条件为:反应温度140℃,反应时间8 h,催化剂用量w= 2.5%。在该条件下进行反应,得到正丁醛的转化率为97.8%,辛烯醛的收率和选择性分别为83.6%和85.5%。为了探索在较低温度下进行壳聚糖催化正丁醛自缩合反应,同时进一步提高反应效果的可能性,采用单因素实验,考察了反应条件的影响。
3.2 反应条件对壳聚糖催化正丁醛自缩合反应的影响
3.2.1催化剂用量
催化剂用量对正丁醛自缩合反应结果影响如表1所示。随催化剂用量增加,正丁醛转化率增加,但辛烯醛收率和选择性均先增大后减小。当催化剂用量少于5%时,增加催化剂用量,相当于增加了活性中心的数量,促进正丁醛自缩合反应的进行,因此正丁醛转化率和辛烯醛收率均逐渐增大。当催化剂用量w= 5% 时,辛烯醛收率和选择性达到最大,分别为88.9%和89.6%。继续增加催化剂用量,正丁醛转化率继续增加,但辛烯醛收率和选择性均下降,这可能是由于过多的活性中心促进了正丁醛与辛烯醛之间的深度缩合。
3.2.2反应温度
考察了反应温度对正丁醛自缩合反应的影响,结果如表2所示。升高反应温度,正丁醛转化率和辛烯醛收率先升高后基本稳定。当反应温度为60℃时,正丁醛转化率和辛烯醛收率均很低;当温度提高到80℃时,正丁醛转化率为96.0%,辛烯醛收率和选择性分别为86.0%和89.6%。而继续提高反应温度,正丁醛转化率和辛烯醛收率只是略有增加。因此,选择80℃作为适宜的反应温度。

表1 催化剂用量对正丁醛自缩合反应的影响Table 1 Effects of catalyst amount on n-butyraldehyde self-condensation

表2 反应温度对正丁醛自缩合反应的影响Table 2 Effects of reaction temperature on n-butyraldehyde self-condensation
3.2.3反应时间
考察了反应时间对正丁醛自缩合反应的影响,结果如表3所示。延长反应时间,正丁醛转化率逐渐增加,辛烯醛收率和选择性先增大后减小。当反应时间为8 h,辛烯醛收率和选择性最大,分别为86.0%和89.6%,此时正丁醛转化率为96.0%。继续延长反应时间,辛烯醛选择性和收率迅速下降,这可能是由于过长的反应时间促进了辛烯醛C─C键断裂产物正己醛与正丁酸的偶联反应、辛烯醛与正丁醛深度缩合等副反应,从而导致辛烯醛选择性下降[11]。因此,选择8 h 作为适宜的反应时间。
综上可见,通过条件实验壳聚糖催化正丁醛自缩合反应温度显著降低,由140降至80℃,并且反应效果还有所提高,辛烯醛收率和选择性分别可达86.0%和89.6%。在此基础上,研究了壳聚糖催化剂的重复使用性能。
3.3 壳聚糖的重复使用性
3.3.1重复使用性能考察
壳聚糖催化剂的回收过程为先用无水乙醇清洗,再于110℃下干燥,其回收率可以达到95%以上。将回收并处理后的壳聚糖用于催化正丁醛自缩合反应,结果如表4所示。循环使用至第3次时,催化活性开始下降。第4次和第5次使用时,催化剂活性迅速降低,主要表现为正丁醛转化率以及辛烯醛收率急剧下降。
3.3.2失活原因分析与再生方法探究
对新鲜及回收催化剂进行了FT-IR 分析,结果如图3所示。新鲜及回收的催化剂中,1 570 cm-1处均出现了─NH2的特征吸收峰。第3次使用的催化剂回收后,在1 689 cm-1处出现了酰胺的谱带(C═O 的伸缩振动),酰基是由副产物中正丁酸的─COOH与活性中心─NH2酰基化反应产生[12]。随着催化剂重复使用次数增加,2 970 cm-1处─CH2的特征吸收峰逐渐增强,说明在反应过程中有机物与催化剂结合在一起[13]。而归属于壳聚糖C─O键、O─H 键和C─H 键的吸收峰均不变。因此,催化剂失活是因为反应体系中正丁酸等物质与氨基结合在一起,使得活性中心─NH2受到破坏。
针对壳聚糖失活原因,先用碱性更强的氨水洗涤回收催化剂以使酰胺水解,重新获得─NH2,再用蒸馏水洗涤催化剂,以排除氨水的影响。氨水处理后的回收壳聚糖重复使用性如表5所示。可以看出,回收催化剂循环使用到第5次时,活性仅略微降低。与表4中新鲜催化剂的活性相比,正丁醛转化率下降5.1%,辛烯醛收率下降3.7%,而辛烯醛选择性基本不变。与只用乙醇洗涤催化剂相比,催化剂的重复使用性明显得到提高。

表3 反应时间对正丁醛自缩合反应的影响Table 3 Effects of reaction timeon n-butyraldehyde self-condensation
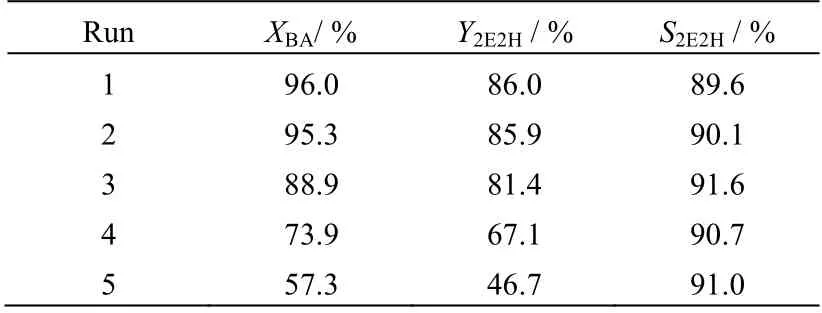
表4 壳聚糖催化剂重复使用性能Table 4 Reusability of chitosan catalysts

图3 新鲜和回收的壳聚糖催化剂红外光谱图Fig.3 FT-IR spectra of fresh and recovered chitosan

表5 回收处理后回收壳聚糖的重复使用性能Table 5 Reusability of recovered chitosan treated with ammonium hydroxide
新鲜催化剂和用氨水或乙醇洗涤处理并使用5次后催化剂的FT-IR 谱图如图4所示。在1 570 cm-1处均出现了─NH2的特征吸收峰,1 654 cm-1均出现了C═O的伸缩振动,而与新鲜及用氨水处理催化剂不同的是:用乙醇洗涤的催化剂在1 689 cm-1处出现了酰胺的谱带(C═O的伸缩振动)。氨水处理的催化剂中未出现酰胺的谱带,说明氨水处理使得酰胺水解,催化剂表面─NH2得以恢复。因此催化剂重复使用性要优于乙醇洗涤的催化剂。
本课题组之前研究的正丁醛自缩合反应催化剂[6-7,14](如Ce-Al2O3、La-Al2O3和TiO2等)虽可达到83%左右的辛烯醛收率,但反应温度高达180℃;部分催化剂[15](如H4SiW12O40/SiO2)可使反应温度降至120℃,但是辛烯醛收率降低(为80.6%),而且该催化剂重复使用性能较差。使用壳聚糖催化正丁醛自缩合反应时,在80℃即可使辛烯醛收率接近90%,较低的活性温度可显著降低能耗,同时回收的壳聚糖经氨水处理即可恢复其催化活性,有很好的应用前景。在此基础上,推测了壳聚糖催化正丁醛自缩合的反应机理,并对其控速步骤进行了量化计算。
3.4 壳聚糖催化正丁醛自缩合反应机理
Shylesh 等[16]研究发现SiO2表面羟基的弱酸性对SiO2负载有机胺催化正丁醛自缩合反应有一定促进作用。作者推测壳聚糖表面的氨基和羟基可能同样具有酸碱协同催化作用,从而使得壳聚糖在正丁醛自缩合反应中表现出较好的催化效果。据此推测壳聚糖催化正丁醛自缩合反应的催化机理,如图5所示。

图4 新鲜和回收壳聚糖催化剂红外光谱图Fig.4 FT-IR spectra of the fresh and recovered chitosan
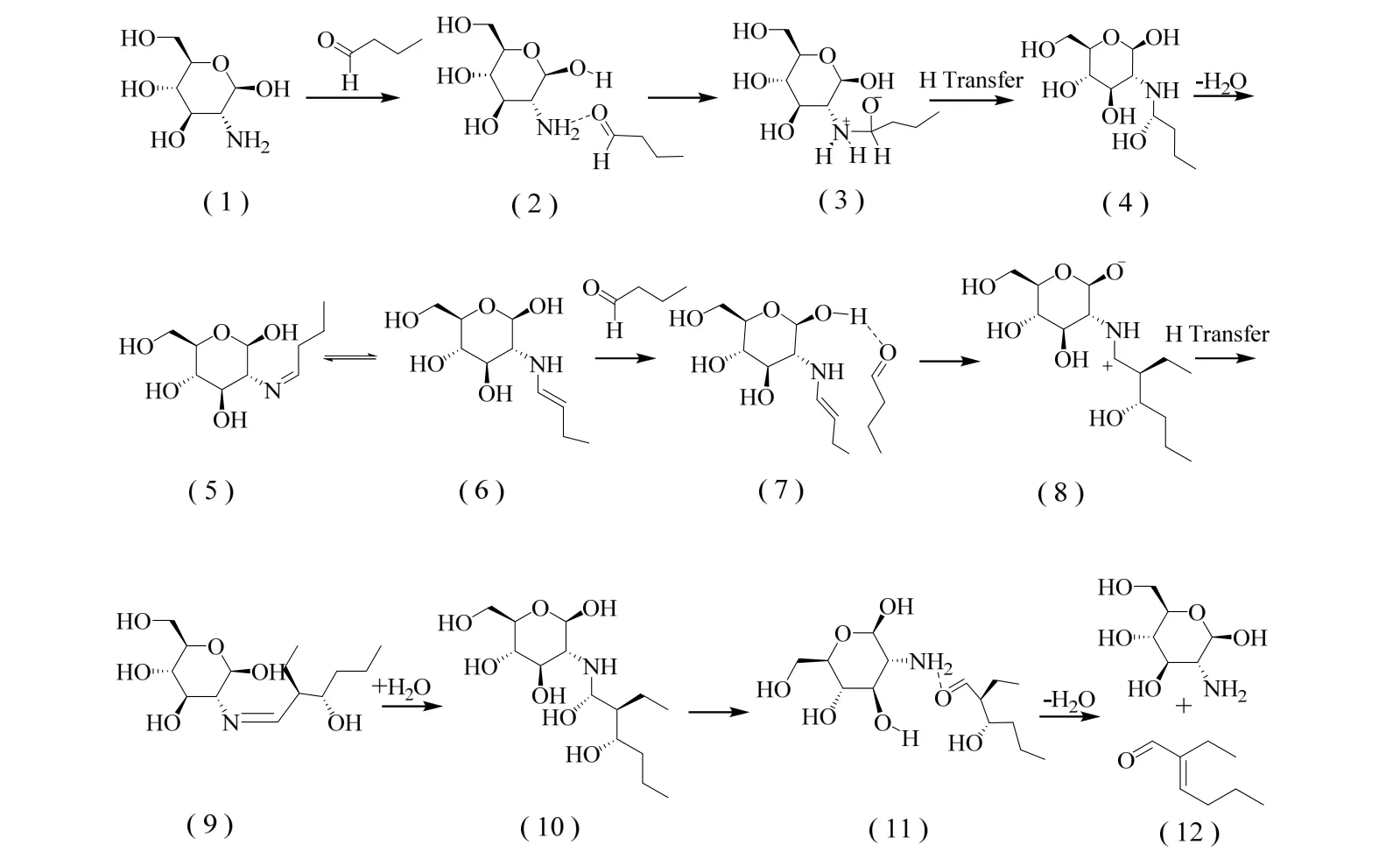
图5 壳聚糖催化正丁醛自缩合反应机理Fig.5 Reaction mechanism of n-butyraldehyde self-condensation catalyzed by chitosan
正丁醛通过其羰基氧与壳聚糖氨基的弱氢键作用吸附在壳聚糖表面,进而正丁醛的羰基碳与壳聚糖氨基上的N 形成C─N 键并发生质子转移生成醇胺物种(4),醇胺物种(4)自身不稳定经分子内脱水生成烯胺和亚胺的互变物种(5)和(6)。与此同时,另一分子正丁醛的羰基氧与壳聚糖表面的羟基发生氢键作用,使得羰基氧被质子化。烯胺物种中的β-C与质子化的羰基发生作用形成新的C─C键,即物种(8),物种(8)经分子内氢转移后形成亚胺物种(9)。水作为亲核试剂进攻亚胺物种(9)中C═N 上的C原子,而后经过氢转移产生处于吸附态的2-乙基-3-羟基己醛(11),2-乙基-3-羟基己醛从壳聚糖催化剂表面脱附使壳聚糖恢复到原来状态,同时2-乙基-3-羟基己醛受热发生分子内脱水生成目标产物辛烯醛。
文献[16-18]研究结果表明,C─C键的形成是正丁醛自缩合合成辛烯醛反应过程的速率控制步骤。Shylesh 等[16]基于密度泛函理论在wB97X-D/6-311++G(3df,3pd)水平上对SiO2负载有机胺催化正丁醛自缩合反应过程进行了模拟计算,得出在70℃下C─C形成步骤的表观活化能垒为85 kJ.mol-1。为了与该催化体系进行比较,本文采用相同的方式对壳聚糖催化正丁醛自缩合反应的C─C键形成步骤进行模拟计算。首先确定以壳聚糖的最稳定结构(如图6所示)作为其理论计算的模型,该模型结构参数的理论计算值与实验测定值相当[19-21]。模型催化剂中的羟基、羟甲基和氨基均位于平伏键的位置,以利于体系处于最稳定的构型。利用交换相关函数基组进行几何优化并通过频率分析确定了各驻点的性质。在每个优化几何结构下计算得到的振动频率用于获得焓和自由能的修正值。在wB97X-D/6-311++G(3df,3pd)能级下进行单点能量计算,得到最终各物种的势能面。结果表明,壳聚糖催化正丁醛自缩合反应过程中,70℃下C─C形成步骤的表观活化能垒为82 kJ.mol-1,低于文献值[16]。说明壳聚糖是一种比SiO2负载有机胺更有利于催化正丁醛自缩合反应的催化剂。具体来讲,壳聚糖表面羟基的H5与正丁醛羰基O4接近至1.866 1Å,形成复合物(7),羟基通过氢键活化了正丁醛的羰基C3,C3所带电荷由+0.418增加至+0.444,使其亲电性增强。C3选择性进攻由另一分子正丁醛与氨基形成亚胺物种上的β-C2(C2上带有-0.341的负电荷,其电荷远低于C1上的-0.024,且C2比C1位阻小),进而形成如图7所示的过渡态结构。可以看出,过渡态中正丁醛与壳聚糖构成9元环结构,此时不仅C2与C3之间逐步靠近至1.688 1Å,而且壳聚糖表面羟基的H5与正丁醛的羰基O4也接近至1.256 0Å。N9-C1-C2 3个原子形成共轭结构,稳定了过渡态结构,降低了过渡态势能面,此时过渡态的虚频为-494.98 cm-1。过渡态释放出44 kJ.mol-1能量后,新的C─C键在C2与C3之间形成,从而得到物种(8)。总之,在整个反应的过程中,催化剂上醇羟基增强了正丁醛羰基碳的亲电性,氨基通过与C1和C2形成共轭结构稳定了反应过渡态,从而促进了反应速率控制步骤的进行。
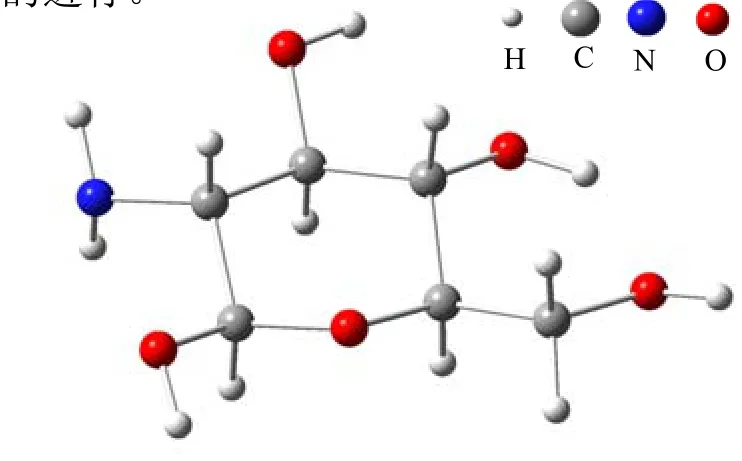
图6 催化剂壳聚糖的计算模型Fig.6 Calculation model for chitosan

图7 C─C键形成过程中的过渡态结构Fig.7 The transition structure during carbon-carbon bond formation processes
4 结 论
壳聚糖对正丁醛自缩合反应具有较好的催化性能,在催化剂用量w= 5%、反应温度80℃和反应时间8 h 时,正丁醛转化率为96.0%,辛烯醛收率和选择性分别为86.0%和89.6%。回收的壳聚糖失活是因为活性组分─NH2受到破坏,使用氨水处理回收的壳聚糖,可保证重复使用5次而活性基本不变。阐明了壳聚糖上的─NH2和─OH 活性位点催化正丁醛自缩合的协同作用机理;壳聚糖催化正丁醛自缩合反应控速步骤C─C键形成的表观活化能垒低于文献中的SiO2负载有机胺催化剂。壳聚糖可以在相对较低的反应温度下实现很高的正丁醛转化率以及辛烯醛收率,而且还具有良好的重复使用性能,是一种优良的正丁醛自缩合反应催化剂。
