不同时机冻融胚胎移植妊娠结局比较
2020-11-21梁利霞刘俊芬范俊梅张志平张秀萍
梁利霞 刘俊芬 范俊梅 张志平 张秀萍
山西省妇幼保健院生殖医学中心,山西太原 030013
在辅助生殖技术中选择性胚胎冷冻技术最初应用于取卵后卵巢过度刺激综合征(ovarian hyperstimulation syndrome,OHSS)风险增加的患者[1],其后应用于胚胎植入前遗传学检查、超促排卵过程中卵泡晚期孕酮升高[2-3]和胚胎-子宫内膜不同步的患者[4],而今全胚冷冻、冻融胚胎移植(frozen-thawed embryo transfer,FET)技术已广泛应用。这一技术的应用可以避免超促排卵过程中高雌激素水平对机体的影响,不仅可以提高妊娠率[5],还可以降低孕产妇和新生儿发病率[6-7]。
然而不孕和接受助孕治疗的患者,特别是体外受精胚胎移植(in vitro fertilization embryo transfer,IVFET)治疗的患者存在严重的心理压力。FET 的应用延长治疗周期的同时,延长了患者焦虑及等待的时间,患者的心理压力相应地增加[8]。FET 作为体外受精治疗中重要的治疗策略和方法,何时可以进行解冻移植,是全胚冷冻后患者最关心的问题之一。本研究旨在分析取卵后第1 个月经周期即开始FET 的妊娠结局与安全性,以探索最早的FET 时机,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2018年1月1日~6月30日于山西省妇幼保健院生殖医学中心行IVF-ET 助孕的患者。本研究经山西省妇幼保健院医学伦理委员会审核批准。纳入标准:①女方年龄≤35 岁;②不孕因素为输卵管因素; ③首次取卵,获卵数≥5 枚,取卵术后OHSS 分级属于无、轻、中度患者[9];④夫妇双方染色体均正常。排除标准:①取卵后OHSS 分级属于重度患者[9];②子宫解剖学异常、子宫肌瘤、子宫内膜异位症、子宫腺肌症;③子宫内膜息肉、子宫内膜炎、宫腔粘连;④感染,合并糖尿病、高血压、甲状腺功能异常、血栓前状态等基础疾病。将符合入组条件的患者根据FET 时机的不同分为两组:A 组(75 例)和B 组(165例)。两组患者的一般资料比较,差异无统计学意义(P>0.05)(表1),具有可比性。
表1 两组患者一般资料的比较(±s)

表1 两组患者一般资料的比较(±s)
A 组B 组t 值P 值75 165 29.10±2.91 29.69±3.41 0.824 0.411 3.61±1.87 3.73±2.28 0.363 0.717 23.61±2.11 23.86±2.02 0.625 0.515组别 例数 年龄(岁) 不孕年限(年) 体重指数(BMI)(kg/m2)
1.2 方法
1.2.1 内膜准备及转化
1.2.1.1 A 组 取卵后第1 个月经周期行FET。患者于取卵术后月经首次来潮第12日返院,经阴道B 超监测子宫内膜厚度,相应地给予雌二醇片(芬吗通,荷兰苏威制药公司,批号:360206),1~4 片/d,分1~3 次口服,连续2~4 d 返院,再次根据内膜厚度调整雌激素用量。
1.2.1.2 B 组 取卵后待卵巢恢复至正常大小行FET。患者于取卵术后第2 次月经来潮第2~3日返院,经阴道B 超检查双侧卵巢内无≥5 mm 不规则无回声,则给予雌二醇片:1 片/次,2 次/d,口服,连续5 d;继而1 片/次,3 次/d,口服,连续3 d。8 d 后返院,根据内膜厚度调整雌激素用量。如月经来潮第2~3日,卵巢内仍有不规则无回声,则推迟1 个月经周期,以此类推。
两组患者均于内膜厚度≥8 mm、血清孕酮(progesterone,P)值<1.5 ng/ml 时,给予内膜转化:黄体酮注射液(浙江仙琚制药股份有限公司,批号:191104)40 mg 肌注,连续5 d。
1.2.2 胚胎移植及移植后黄体支持
两组患者均于内膜转化第6日行FET,每次移植囊胚1~2 枚[10]。囊胚于取卵后第5日,按照Gardner[11]评分体系选择优质囊胚进行玻璃化冷冻。
移植后停用黄体酮注射液,改为雌二醇·地屈孕酮片(芬吗通),2 片/次,2 次/d,口服,连续12 d。
1.3 观察指标
比较两组患者的获卵数、OHSS 分级、内膜准备(包括雌二醇片使用天数、雌二醇片使用剂量、子宫内膜厚度、卵巢体积、移植胚胎数)、妊娠结局。
1.3.1 获卵数
患者行经阴道B 超引导下取卵术,采集得到的全部卵子数。
1.3.2 子宫内膜厚度
FET 子宫内膜准备过程中、转化日及移植当日均行经阴道B 超监测患者子宫内膜厚度(mm)。
1.3.3 卵巢体积
移植当日B 超监测卵巢体积(cm3):长径(cm)×左右径(cm)×前后径(cm)×0.523。
1.3.4 OHSS 分级
根据Golan 分类法[9],OHSS 可以分为3 级,具体如下。轻度OHSS:轻度腹胀、不适,伴或不伴恶心、呕吐及(或)腹泻,卵巢增大,直径5~12 cm;中度OHSS:轻度加超声证实腹腔积液;重度OHSS:中度加临床腹腔积液征及(或)胸腔积液或呼吸困难伴或不伴血容量减少、血液浓缩、血黏度增加、凝血异常、肾灌注减少、肾功能减退。
1.3.5 雌激素使用总量及天数
统计每例患者子宫内膜转化前雌二醇片的使用总量(片)及天数(d)。
1.3.6 妊娠结局
患者移植后12、14 d 测血清β-人绒毛膜促性腺激素(β-human chorionic gonadotrophin,β-HCG)值,如果呈阳性则继续用药。移植后30~35 d 行经阴道B超检查,如妊娠囊中可探查到卵黄囊则确定为临床妊娠。
临床妊娠率=临床妊娠数/移植例数×100%;胚胎种植率=着床胚胎总数/移植胚胎总数×100%; 双胎率=双胎妊娠数/妊娠总数×100%; 早期流产率=早期流产数/妊娠总数×100%;晚期流产率=晚期流产数/妊娠总数×100%;早产率=早产数/妊娠总数×100%;分娩率=分娩例数/妊娠总数×100%。
1.4 统计学方法
采用SPSS 20.0 统计学软件进行数据分析,符合正态分布的计量资料采用均数±标准差(±s)表示,两组间比较采用t 检验,不符合正态分布者转换为正态分布后行统计学分析;计数资料用率表示,组间比较采用χ2检验;等级资料采用秩和检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者获卵数及取卵术后、移植术后OHSS 分级的比较
两组患者的获卵数比较,差异无统计学意义(P>0.05);两组患者取卵术后OHSS 分级比较,差异无统计学意义(P>0.05)(表2);两组患者移植术后均无OHSS发生。
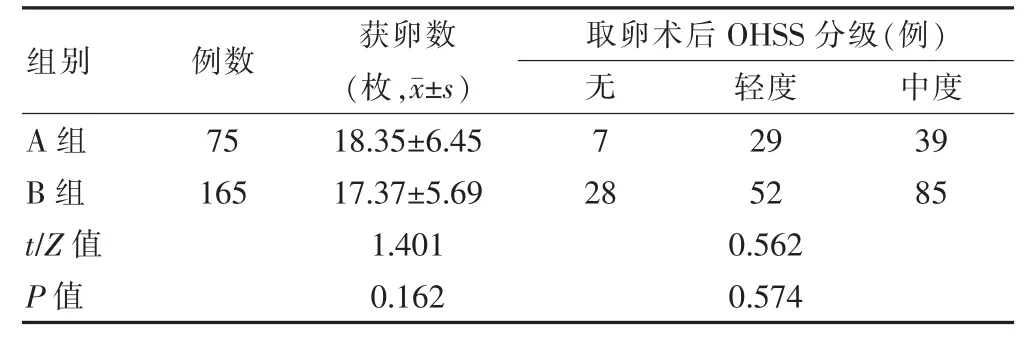
表2 两组患者获卵数及取卵术后OHSS 分级的比较
2.2 两组患者内膜准备的比较
A 组患者的雌二醇片使用天数短于B 组,雌二醇片使用剂量少于B 组,差异有统计学意义(P<0.01);A组患者移植日卵巢体积大于B 组,差异有统计学意义(P<0.01);两组患者移植日子宫内膜厚度、移植胚胎数比较,差异均无统计学意义(P>0.05)(表3)。
表3 两组患者内膜准备的比较(±s)

表3 两组患者内膜准备的比较(±s)
A 组B 组t 值P 值75 165 8.56±2.56 10.44±1.63 6.849<0.01 20.25±8.34 26.14±8.17 5.140<0.01 10.29±1.73 10.26±1.61 0.238 0.812 5.67±0.89 5.02±0.87 6.906<0.01 1.83±0.38 1.94±0.31 0.022 0.982组别 例数 雌二醇片使用天数(d)雌二醇片使用剂量(片)移植日子宫内膜厚度(mm)移植日卵巢体积(cm3)移植胚胎数(个)

表4 两组患者妊娠结局的比较[%(n/N)]
2.3 两组患者妊娠结局的比较
两组患者的临床妊娠率、胚胎种植率、双胎率、早期流产率、晚期流产率、早产率、分娩率比较,差异无统计学意义(P>0.05)(表4)。
3 讨论
3.1 不孕患者的心理压力
在整个IVF 助孕治疗过程中包括治疗前、治疗中、治疗后,患者焦虑及抑郁的发生率分别为67%和86%,其中24%和33%发生在治疗期间[8]。有研究显示,开始IVF 时患者仅在情绪上与正常对照组稍有不同,随着治疗的进行,负面情绪水平会随着不成功的治疗而逐渐升高,并在随后的治疗中持续,直至最终妊娠时负面情绪才消失[12]。故缩短其治疗周期,帮助患者尽快妊娠是符合患者心理需求并帮助其摆脱负面情绪的最佳途径。
全胚冷冻、FET 技术的广泛应用,延长了患者等待及焦虑的时间,而是否需要等到卵巢完全恢复才可以解冻移植?本研究旨在探索一个安全又不影响成功率的最早FET 时机。既往本生殖医学中心FET 的内膜准备均在取卵后2~3 个月,卵巢恢复至超促排卵前水平后开始,由于患者的需要,2018年始部分患者于取卵术后第1 个月经周期进行了FET。本研究回顾性分析了2018年1月1日~6月30日于本生殖医学中心行IVF-ET 助孕患者的FET 情况,分析比较了取卵术后在卵巢未完全恢复的情况下与卵巢恢复后不同的月经周期FET 的妊娠结局,结果显示,其临床妊娠率、胚胎种植率、双胎率、早期流产率、晚期流产率、早产率、分娩率比较,差异均无统计学意义(P>0.05)。提示取卵术后第1 次月经来潮行FET 并不影响胚胎的着床、后期的胚胎发育及妊娠最终结局。
3.2 OHSS 的发生
OHSS 是IVF 治疗常见的医源性并发症之一,早发型主要与补充外源性HCG 相关,通常发生于取卵后9 d 内; 迟发型OHSS 一般发生于取卵10 d 后,与胚胎着床后分泌大量内源性HCG 有关。
全胚冷冻、FET 技术的广泛应用可有效预防早发型OHSS 及迟发性OHSS 对患者的不良影响。本研究中患者均采用全胚冷冻,取卵术后,两组患者的OHSS分级比较,差异无统计学意义(P>0.05);两组解冻移植日卵巢体积比较显示,A 组大于B 组,差异有统计学意义(P<0.01),因A 组卵巢恢复时间短,此结果符合取卵后卵巢的改变。较大的卵巢是否会增加迟发性OHSS 的发生率? 本研究给予A 组患者密切随访,妊娠后均无迟发性OHSS 的发生,故本研究推断取卵术后第1 个月经周期移植是相对安全的,并未增加迟发性OHSS 的发生率。但由于本研究纳入样本量有限,此结论有待于扩大样本量进一步研究。
3.3 内膜准备方式
FET 的内膜准备方式,大致可分为人工周期(hormone replacement therapy,HRT)和自然周期(natural cycles,NCs)两种。
NCs 具有符合自然规律、药物使用少等优势,但存在高达6%的周期取消率[13]。HRT 方法最初应用于卵子捐赠受卵的患者[14],现在已广泛应用于所有FET的患者,其优势在于内膜转化的易操控性,并能有效减少患者的就诊次数,故本研究中两组患者均采用HRT 准备内膜。
既往报道中雌激素的补充,有的研究采用固定量6 mg/d[15],有的模拟NCs 中不断升高的雌激素水平采用不同的方案[16],妊娠结局均较理想。而补充时间,研究发现过短可能会导致流产率升高[17],故如果有必要可以适当延长雌激素的使用时间[18]。
本研究中B 组患者从月经第2~3日开始使用雌二醇片,8 d 后根据患者B 超监测内膜的情况,调整剂量和时间,最终当内膜厚度达到8~14 mm 时转化,采用的方法与既往研究一致[19]。A 组患者月经第12天,阴道B 超检查双侧卵泡无优势卵泡发育,开始使用雌二醇片,内膜转化标准与B 组相同。与B 组相比较,A组雌二醇片的使用剂量减少,使用时间有所缩短,差异有统计学意义(P<0.01),而妊娠结局并无显著差异(P>0.05)。A 组的雌激素内膜补充方式与传统的方式比较,减少了雌激素的使用量,并不影响妊娠结局,为内膜的准备方式提供了新的思路。第1 次月经来潮返院的患者中9 例患者于月经第12日即可观察到优势卵泡(直径>10 mm)发育,即采用NCs 准备内膜,因数量较少,本研究未统计,需进一步研究。
既往研究报道在没有降调的HRT/FET 周期中P值提前升高发生率为1.9%~7.4%[20],而内膜转化日血清P>2.0 ng/ml 可能会导致胚胎与内膜发育不同步,从而降低妊娠率及出生率[21]。本生殖医学中心FET 周期内膜转化日监测血清P 值水平,如P 值≥1.5 ng/ml 取消移植。文献报道血清雌二醇(E2)和黄体生成素(LH) 这两个值并不能预测FET 妊娠结果[22],故此两个值在本研究中未行监测。
3.4 妊娠结局
A 组患者的双胎率低于B 组,但差异无统计学意义(P>0.05),因两组患者胚胎移植数目及种植率均无显著差异(P>0.05),故考虑B 组患者双胎妊娠的增多存在偏倚,需进一步扩大样本量进行研究。B 组患者中5 例发生晚期流产,流产率为6.33%,A 组患者中1例发生晚期流产,流产率为2.56%,B 组晚期流产率高于A组,但差异无统计学意义(P>0.05)。B 组晚期流产患者中4 例、A 组晚期流产患者1 例均为双胎妊娠,流产率的增高考虑与双胎率增高有关,提示双胎妊娠是IVF 妊娠后晚期流产的重要影响因素。
综上所述,取卵术后OHSS 分级属于轻、中度的患者,取卵术后第1 个月经周期即行FET 助孕,不影响患者的妊娠结局。
