肺混合性鳞状细胞腺性乳头状瘤2例临床病理分析并文献复习
2020-11-17孙思柏李世兰
陈 杰 孙思柏 李世兰
肺支气管内实性乳头状瘤(SEPs)为主要发生于成人的罕见良性肿瘤,占所有肺肿瘤的不足0.5%及肺良性肿瘤的约7%[1]。根据乳头表面被覆上皮的不同,主要分为鳞状细胞乳头状瘤、混合性鳞状细胞腺性乳头状瘤(MSCGP)和腺性乳头状瘤,其中以MSCGP最为罕见[1],部分病例可表现为肿瘤性标志物的升高。影像学多表现为支气管腔内或肺实质内的境界清楚的占位性病变,通常以手术切除为主,完整切除的病例长期随访均未见复发及转移。由于此瘤罕见,临床及影像学医师对其缺乏认识,尤其是对于某些伴有继发性改变的病例,常被误判为恶性肿瘤。我们通过搜集本科及文献报道的MSCGP 24例[1-15],分析其临床、影像学及病理形态等特征,旨在加强影像学及病理学医师对此瘤的认识,减少误诊。
1 材料与方法
回顾性分析本医院病理科于2019年诊断的肺MSCGP患者2例,对其临床,病理资料进行复习及总结。所有病例均经罗氏全自动免疫组化染色仪染色,一抗CK、CK7、TTF-1、NapsinA、CEA、p40、CK5/6、SMA及Ki-67均购自福州迈新生物技术有限公司。免疫组化染色中用PBS缓冲液代替一抗作为阴性对照。其中TTF-1、p63、Ki-67均以细胞核出现棕黄色着色为阳性;而CK、CK7、NapsinA、CEA、CK5/6、SMA则以细胞浆出现棕黄色着色为阳性。
2 结 果
2.1 临床及影像学资料 本组共收集MSCGP 24例,包括文献报道病例22例,本院患者2例(1例男性,1例女性,年龄均为64岁)2例均无明显的临床症状,因体检时影像学发现肺占位而就诊,肿瘤直径分别为2.3 cm及1 cm,1例位于支气管腔内,1例位于肺实质,2例患者均无吸烟史。
2.2 病理形态 巨检,病例1为突出于支气管腔内肿物,表现为淡红色息肉样肿物;病例2为发生于肺实质内肿物,肉眼表现为肺实质内形态规则的肿物,与周围肺组织境界清楚,无浸润性生长,切面实性,灰红色,质地中等。镜检:低倍镜下,肿瘤内见乳头状生长结构,内含宽大的纤维血管轴心,部分纤维间质伴有玻璃样变性,纤维轴心的表面被覆鳞状细胞和腺上皮细胞,鳞状上皮细胞多为复层,位于腺上皮下方,胞浆嗜伊红染,通常看不到明显的角化(图1A)。纤维血管轴心被覆腺上皮细胞呈单层或复层,腺上皮细胞立方状至柱状,部分可见纤毛,部分细胞浆嗜伊红色,部分胞浆内含粘液空泡,两种细胞的细胞核形态温和,呈圆形或卵圆形,未见明显异型及核分裂像。
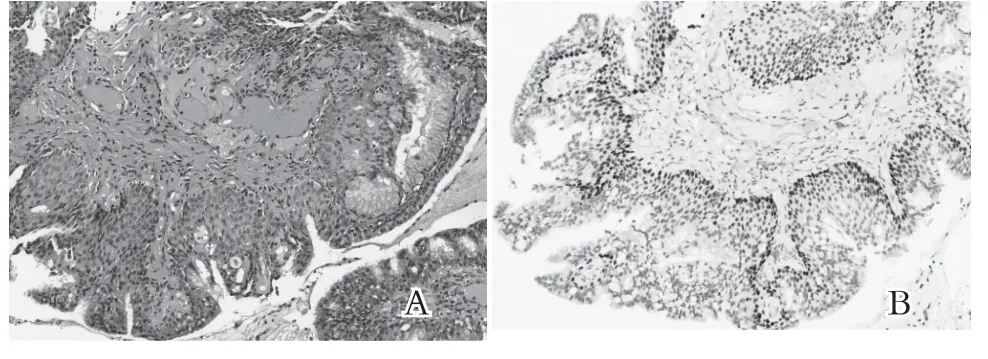
图1 病理形态
2.3 免疫组化结果 基底细胞及鳞状细胞表达p40(图1B)、CK5/6,肿瘤上皮细胞CK7、CEA、TTF-1、NapsinA弥漫阳性表达,纤维血管轴心CD34、SMA阳性表达,Ki-67细胞核增殖指数低<1%。
2.4 治疗与预后 2例患者均行外科手术,病灶完整切除,随访时间分别为6个月及1年,均未出现复发或转移。
3 讨 论
3.1 临床表现 MSCGP为良性病变,文献报道中MSCGP主要发生于相对年长的女性或男性患者,且与吸烟无相关性。作者收集本院诊断及文献报道MSCGP共24例,对其临床及病理等特征进行了分析总结。所有患者平均年龄56.1岁,与文献报道基本一致,但本组中出现2例年轻患者,年龄分别为17岁及18岁,由此可以说明,该肿瘤可以发生于任何年龄阶段,包括青少年。肿瘤多发生于支气管或细支气管内多见。少数病例也可发生于肺实质内。本组24例患者中18例位于支气管腔内,6例位于周围肺实质。MSCGP多无特异性临床表现,部分病例可表现为胸闷、咳嗽、咳痰、咳血等症状。本组24例患者中有临床表现的病例包括10例,主要表现为咳痰、咳血及胸痛。14例患者没有明显临床症状,笔者发现这些伴有症状的患者多数表现为支气管内肿物,且肿瘤直径一般>1 cm。因此推断这可能与肿瘤发生部位及大小相关,当肿物逐渐增大,阻塞支气管腔或细支气管腔,甚至发生炎症时,可引起咳痰、咳血、胸闷、胸痛等反应性症状。
3.2 影像学资料 支气管镜检查,支气管腔内肿物表现为菜花状肿物,肿物基底与支气管壁相连续,但无明显浸润,也无支气管壁僵硬的现象。有时肿瘤也可表现为支气管壁轻度隆起的隐匿性生长方式,支气管镜检查,病变处支气管壁增厚。发生于肺实质内者主要表现为与肺实质境界清楚的类圆形肿物,少数情况下当肿瘤生长于肺边缘近胸膜处时则可以出现胸膜凹陷。另外,一些报道中发现MSCGP在PET/CT检查时会显示出肿瘤的FDG增高(FDG对于生长活跃,且直径>10 mm的肿瘤具有97% 的敏感性和78%的特异性)[3],因此经常导致该肿瘤影像学诊断为恶性。对于支气管壁的微隆起型病变,以及发生于肺实质内,尤其是发生于肺叶边缘导致胸膜凹陷的病例,很容易被误诊为恶性,因此,加强对本病的认识,有助于减少影像及临床的误诊。
3.3 病理学改变 肺实性乳头状瘤为一种罕见的良性病变,巨检,MSCGP大体表现为支气管内灰红色或灰白色菜花样或细乳头样肿物,肿瘤基底与支气管壁相连续。肺组织内病变多与周围肺实质境界清楚,易剥离,切面实性,少见出血及囊性变。镜检,肺MSCGP的主要组织学特点包括:①肿瘤具有宽大的纤维血管轴心,部分可伴有玻璃样变性。②乳头表面被覆鳞状上皮细胞及腺上皮细胞,呈复层或假复层,通常以腺上皮为主,鳞状上皮细胞主要位于腺上皮下方,胞质红染,核轻度异型;腺上皮细胞胞质内可见粘液空泡,细胞均匀一致,核小,圆形。腺上皮内夹杂着纤毛细胞、粘液细胞及杯状细胞,有时可见胞质透明的细胞,但所有细胞均无异型性,或仅有轻度的异型性,无核分裂像,也无坏死。③肿瘤的分枝状间质轴心内可呈炎症改变,有时甚至出现大量淋巴细胞、浆细胞浸润,部分病例周围可见粘液脓性细胞碎屑,可能与肿瘤阻塞支气管及肺泡引发的炎症性改变有关。值得一提的是周围型纤毛腺性乳头状瘤,应给予高度重视。其乳头状结构在肿瘤的周边常不明显,表现为向周围肺泡内延伸,形成类似于沿肺泡壁生长或肺泡内的微乳头结构,肺泡壁有时被破坏形成“粘液湖”样,在快速冷冻切片上与浸润性粘液腺癌极其相似,容易误诊。加强对这些病例的认识,仔细观察细胞的异型性、核分裂像以及寻找纤毛柱状上皮细胞对于减少误诊具有重要意义。
3.4 免疫表型及分子生物学检查 肿瘤中的所有上皮细胞,包括复层或假复层柱状细胞、纤毛细胞、粘液细胞、杯状细胞及基底细胞,均显示CK(pan)弥漫阳性表达;基底细胞和鳞状上皮细胞p40、p63和CK5/6阳性,p40、p63主要表现为细胞核的弥漫阳性,CK5/6则表现为细胞浆的弥漫阳性;CK7、TTF-1表现为腺上皮细胞的弥漫阳性表达,CK7主要表现为细胞浆的弥漫阳性表达,TTF-1则表现为细胞核的弥漫阳性表达。局部纤毛细胞表现为CEA和NapsinA细胞浆弥漫阳性。纤维血管轴心显示SMA等纤维/肌纤维细胞弥漫阳性。本组24例MSCGP中,只有1例出现TTF-1表达缺失,所有肿瘤均显示细胞Ki-67增殖指数低于1%。有报道称鳞状上皮乳头状瘤可发生恶性,并证实其恶变可能与吸烟和HPV感染有关,尤其是HPV16、18和31/33/35的感染相关。此前已有报道在鳞状上皮乳头状瘤中检测到HPV DNA的存在,作者在查阅以往文献报道发现,报道中的少数MSCGP中亦存在p16的表达,并检测到HPV DNA的存在[5],但MSCGP与HPV感染的关系却不甚明朗[5,13]。亦有报道MSCGP存在BRAF基因的改变[5]。当然,基于该肿瘤的病例数甚少的情况,这些还需要进一步的证实,本组收集的24例病变中,所有病例经完整切除后,随访时间3个月~7年,均未见有复发、转移及恶变。
3.5 鉴别诊断 ①原发性/转移性粘液表皮样癌,也可生长于支气管内,主要由粘液样细胞、表皮样细胞和中间细胞组成。粘液样细胞分化成熟时呈杯状或柱状,胞质透明,核在基底部;表皮样细胞类似口腔黏膜的复层鳞状上皮,可见细胞间桥,偶见角化;中间细胞呈立方形,体积较小,大小一致,胞质少,类似上皮的基底细胞,虽与MSCGP相比具有一定的相似性,但粘液表皮样癌肿瘤细胞缺乏一定的极性,且MSCGP中缺乏中间细胞,主要呈乳头状生长。②粘液腺腺瘤:与MSCGP相比,粘液腺腺瘤通常以富含粘液的囊腔或管状结构为主,可在局部形成少量乳头状结构,但不是肿瘤的主要成分。③乳头状腺瘤:乳头状腺瘤一般为实性生长,其发生一般与支气管无关,乳头状结构的表面被覆上皮均为单层立方上皮,并伴有肺泡上皮细胞的分化。④支气管内乳头状鳞癌:该肿瘤一般位于肺门部,呈外生性生长或支气管内生长,是一种特殊类型的肺鳞癌,当仅伴有非常局限的上皮内扩散,伴或不伴有浸润时与MSCGP很难鉴别,但是大多数病例中存在浸润,且鳞状细胞癌可表现角化,有角化珠形成和/或细胞间桥等特征,细胞也有明显的异型性。小的活检标本表现分化良好的乳头状鳞状上皮时诊断尤其应该谨慎。
总之,MSCGP为良性肿瘤,治疗主要以手术切除为主,通过切除可以治愈,是否具有复发及恶变的可能,尚需更多报道进一步证实。对于发生于肺实质的MSCGP,尤其发生于肺叶边缘引起胸膜凹陷的病例,应仔细观察,注意与恶性肿瘤相鉴别。
