漫话丰富多彩的燃料电池
2020-11-17福建
福建 邹 标
燃料电池,指将燃料燃烧的化学能直接转化为电能的装置。燃料电池是高中化学知识中的难点和热点,学生对这类题型缺乏整体认知,没有形成整体的知识网络和思考方法,因此,学生觉得困难重重,得分率较低。本文通过对燃料电池进行较全面的归纳总结,多角度进行拓展、延伸,归纳整理了常见的燃料电池的装置示意图、总反应式、电极反应式、电解质等关联信息。帮助学生建立燃料电池的解题思维模型,从而较好地理解、掌握、应用燃料电池相关原理,有效突破燃料电池的解题瓶颈并期望能培养学生宏观辨识与微观探析、证据推理与模型认知、创新意识等化学核心素养,提升学生化学表征、模型认知、信息处理等核心关键能力。
一、燃料电池简介
根据燃料电池的特点,一般在正极上发生还原反应的物质都是O2,O2得到电子后化合价降低,首先变为O2-,O2-能否存在要看电解质环境。由于电解质溶液的不同,电池中电解质可能为酸、碱或盐,其电极反应也有所不同,下表为四种不同电解质环境中,氧气得电子后生成O2-的存在形式:

电解质环境从电极反应式O2-的存在形式酸性溶液O2+4H++4e- 2H2O碱性溶液O2+2H2O+4e- 4OH-固体电解质(高温下能传导O2-)O2+4e- 2O2-熔融碳酸盐(如:熔融K2CO3)O2+2CO2+4e- 2CO2-3
二、燃料电池分类
1.氧气参与的燃料电池
(1)氢氧燃料电池(包括中性、酸性、碱性、高温氧化物、高温碳酸盐等电解质参与反应的燃料电池)
(2)无机化合物燃料电池(包括N2H4、水煤气、H2S、CO、NO2、NO、SO2等作为燃料的电池)
(3)有机化合物燃料电池(包括烃类、醇类、醛类、苯酚、糖类等作为燃料的电池)
(4)金属空气燃料电池(包括镁-空气、铝-空气、锂-空气、锌-空气、铁-空气、Na-CO2等燃料电池)
(5)微生物燃料电池
2.其他氧化性气体参与的燃料电池
(1)氢氯燃料电池
(2)N2-H2燃料电池
(3)NO-CO燃料电池
3.液体燃料电池
(1)Mg-H2O2
(2)Mg-NaClO
(3)Zn-Br2
(4)NaBH4-H2O2燃料电池
4.固体燃料电池
煤燃料电池等
三、近五年高考化学试题中的燃料电池
在近5年内的高考试题中燃料电池知识点考查了9次(如下表),由于形式新颖,难度较大,致学生得分率较低。

序号年份燃料电池内容12019年全国卷Ⅰ生物燃料电池22019年天津卷锌碘溴液流电池32018年全国卷ⅡNaCO2燃料电池42018年全国卷Ⅲ锂空气电池52018年海南卷镁氧电池62016年全国卷Ⅲ锌空气燃料电池72016年浙江卷金属空气电池82015年全国卷Ⅰ微生物电池92015年江苏卷熔融碳酸盐燃料电池
四、燃料电池的装置示意图与电极反应
有关燃料电池试题的解答是高中化学学习的难点,电极方程式的理解与正确书写更是重难点,下表整理了燃料电池的类别、示意图及电极反应式,通过学习不同燃料电池,帮助学生构建解答燃料电池的思维模型,提升学生的核心素养和解决问题的能力。

类别电池名称装置示意图反应式甲烷燃料电池甲烷酸性燃料电池正极O2+4H++4e- 2H2O负极CH4+2H2O-8e- CO2+8H+总反应CH4+2O2 CO2+2H2O电解质稀硫酸甲烷熔融碳酸盐燃料电池正极O2+4e-+2CO2 2CO2-3负极CH4-8e-+4CO2-3 5CO2+2H2O总反应CH4+2O2 CO2+2H2O电解质熔融K2CO3/Li2CO3甲烷固体氧化物燃料电池正极O2+4e- 2O2-负极CH4+4O2--8e- CO2+2H2O总反应CH4+2O2 CO2+2H2O电解质固体氧化物甲醇燃料电池甲醇空气燃料电池(酸性电解质)正极O2+4H++4e- 2H2O负极CH3OH+H2O-6e- CO2↑+6H+总反应2CH3OH+3O2 2CO2↑+4H2O电解质稀硫酸甲醇空气燃料电池(碱性电解质)正极O2+2H2O+4e- 4OH-负极CH3OH+8OH--6e- CO2-3+6H2O总反应2CH3OH+3O2+4OH- 2CO2-3↑+6H2O电解质KOH溶液氢氧燃料电池聚合物电解质薄膜的燃料电池正极O2+4e-+4H+ 2H2O负极H2-2e- 2H+总反应2H2+O2 2H2O电解质聚合物电解质薄膜碱性氢氧燃料电池正极O2+4e-+2H2O 4OH-负极2H2+4OH--4e- 4H2O总反应2H2+O2 2H2O电解质NaOH
五、典型例题分析
【例1】下面是以熔融K2CO3和Li2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池,装置示意如图,下列说法正确的是
( )

A.用此电池来电解精炼铜,当有0.1 mol电子转移时,则有3.2 g铜溶解
C.该电池使用过程中需补充Li2CO3和K2CO3
【答案】D
【解析】题目提供的是实际生产中真实情景示意图,解答此题需要对电化学有比较深入的理解,需要接受题干所给的信息,提取有用的关键信息,结合所学的知识,才能正确解答。

【例2】(2019·全国卷Ⅰ·12改编)利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是
( )

A.相比现有工业合成氨,该方法条件温和,同时还可提供电能


D.电池工作时质子通过交换膜由负极区向正极区移动
【答案】C
【解析】本题综合考查电化学方面的知识,试题的难度比较大。正确理解电极反应和离子的流动方向是解答问题的关键,属于真实情境问题解答,提供的是陌生的实际电化学装置示意图,考查学生信息理解能力和信息转化能力。

六、建立燃料电池的思维模型
燃料电池的难点是书写电极反应方程式。首先,根据是否有外加电源,判断是电解池还是原电池,若没有电源,就是原电池。其次,根据物质的氧化性和还原性判断正极或负极反应物。氧化性气体或氧化性强的物质(如氧气、氯气、空气、双氧水等为正极反应物),得电子,化合价降低,被还原;还原性可燃气体或还原性物质(如氢气、有机气体、有机物、金属等)为负极反应物,失去电子,化合价升高,被氧化。最后结合提供的电解质,是否与产物发生反应,根据电荷守恒,写出电极反应式。具体思路如下:
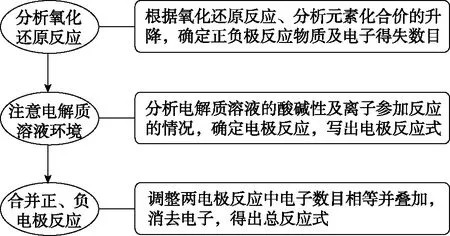
一般情况下,正极反应式的书写比较容易;直接根据总反应式氧化还原反应的规律或题目所给的信息书写;同时,根据电荷守恒,利用总反应式减去正极反应式,得到负极反应式。正确书写电极反应方程式对解决此类电池问题至关重要。
七、试题考查趋势预测与功能价值分析
1.试题的考查趋势预测
通过总结近5年高考试题中的电化学试题,燃料电池类试题是高考的热点和难点。同时,燃料电池与生活、生产紧密联系,新型高效的燃料电池是科技创新的表现。因此,燃料电池特别是新型燃料电池将在今后成为高考试题的高频考点。预计考查的难点问题可能会侧重燃料电池的改进方面,比如“电极材料的改进”“反应原理的改进”“加工工艺的改进”“新材料的应用”“电池效率的提升”等。
2.试题的功能价值分析

