两种圈套器改良牵引法辅助内镜黏膜下剥离术治疗上消化道早癌和黏膜下肿瘤的临床对比研究
2020-11-09刘嵩杨林郭洁刘怡余琼时昭红
刘嵩,杨林,郭洁,刘怡,余琼,时昭红
(武汉市第一医院 消化内科,湖北 武汉430000)
随着内镜技术的不断发展,内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)在消化道早期肿瘤的治疗中应用越来越广泛。特别是在日本和其他亚洲国家,ESD 治疗已成为治疗标准,在没有淋巴结转移风险的早期肿瘤治疗中具有良好的短期和长期疗效[1-2]。但ESD 技术操作难度大,特别易受病变位置、大小和性质(纤维化粘连等)的影响。外科手术过程中,医生能直接牵拉需要解剖的组织,相比之下,内镜医生如果不使用特定的设备和方法,则在ESD 术中无法获得像外科手术那样直接用手辅助牵拉的效果,而术中保持清晰的操作视野至关重要。近年来,有很多关于牵引方法的报道,在上消化道肿瘤ESD 中应用最广泛、报道最多的是线牵引法[3-6],但其局限性在于方向不可变。现有少量报道[7-9]认为,圈套器牵引法具有方向可变性,在胃食管病变和黏膜下肿瘤的ESD 辅助治疗中具有优势。但圈套器的种类繁多,不同粗细的围套器牵拉力也是不一样的,是否在牵引技术的应用上存在差别不得而知。本研究选用两种具有代表性的圈套器,并将牵引方法进行改良,对比分析治疗效果。现报道如下:
1 资料与方法
1.1 一般资料
回顾性分析2017年5月-2019年12月在武汉市第一医院消化内镜中心实施ESD 治疗的患者72 例。其中,食管胃早癌和癌前病变34 例(术前经胃镜、放大染色胃镜、CT和病理诊断确诊)、胃黏膜下肿瘤38 例(术前经胃镜、超声胃镜和CT 确诊)。将72 例患者分为传统ESD方法治疗组(A组,n=24)、粗圈套器圈套牵引组(B 组,n=24)和细圈套器圈套牵引(C 组,n=24)。3 组患者性别、年龄、病灶直径和肿瘤分布部位等一般资料比较,差异均无统计学意义(P>0.05),具有可比性。见表1。所有患者术前均签署知情同意书。手术均由固定的两位有多年ESD操作经验的术者进行。
1.2 观察指标
观察指标包括肿瘤性质、肿瘤部位、病灶直径、手术平均时间、组织夹脱离次数、黏膜下补充注射量、一次完整切除率、术中明显出血和术后迟发性出血等。
1.3 手术器械
治疗胃镜(Olympus GIF-Q260J/Fujifilm EG-580RD)、Olympus NM-200L-0423 注射针、Hook 刀(KD-620LR)、IT刀(KD-611L)、Dual刀(KD-650L)、FD-410LR 止血钳、南京微创ROCC-D-26-195 软组织夹、Olympus SD-211U-25圈套器(单股钢丝钢圈,直径0.3 mm)、ENDO-FLEX NOE342214-C 圈套器(双股钢丝钢圈,直径0.6 mm)、CO2气泵、ERBE VIO 200D电工作站。图套器实物图见图1。
1.4 手术方法
1.4.1 A 组采用传统ESD 技术。操作具体步骤如下:①病灶标记:应用Hook 刀或Dual 刀于病灶边缘3.0 mm 处进行电凝标记,每个标记点间隔约2.0 mm;②黏膜下注射:将1 mL 亚甲蓝、1 mL 肾上腺素和100 mL 生理盐水混合配成溶液,通过内镜注射针在病灶边缘标记点外侧进行多点黏膜下注射,每点各注入2~4 mL,直至病灶充分抬举;③黏膜切开:使用Hook 刀或Dual 刀沿病灶边缘标记点外3.0 mm 处将黏膜切开;④黏膜下层剥离/分离暴露瘤体:用Hook刀或Dual 刀于病灶下的黏膜下层进行剥离,有时可结合IT 刀剥离黏膜下层,直至完整剥离病灶;若为黏膜下肿瘤,黏膜切开暴露瘤体后,用IT 刀沿瘤体外缘剥离,保留瘤体完整很重要,直至完整剥离黏膜下肿瘤;⑤止血和创面处理:术中细小血管出血,可以直接使用Hook 刀、IT 刀或Dual 刀进行电凝;粗大血管或动脉出血,用止血钳电凝止血;剥离后使用止血钳电凝创面的裸露小血管,以预防术后出血;在肌层可疑损伤或缺损处给予软组织夹夹闭;黏膜下肿瘤全层切除,使用尼龙绳钛夹缝合创面;⑥标本回收:使用透明帽吸引或圈套器圈套取出标本,早癌标本行细针固定,所有标本均浸泡于中性甲醛溶液中送病理检查,确定标本性质。
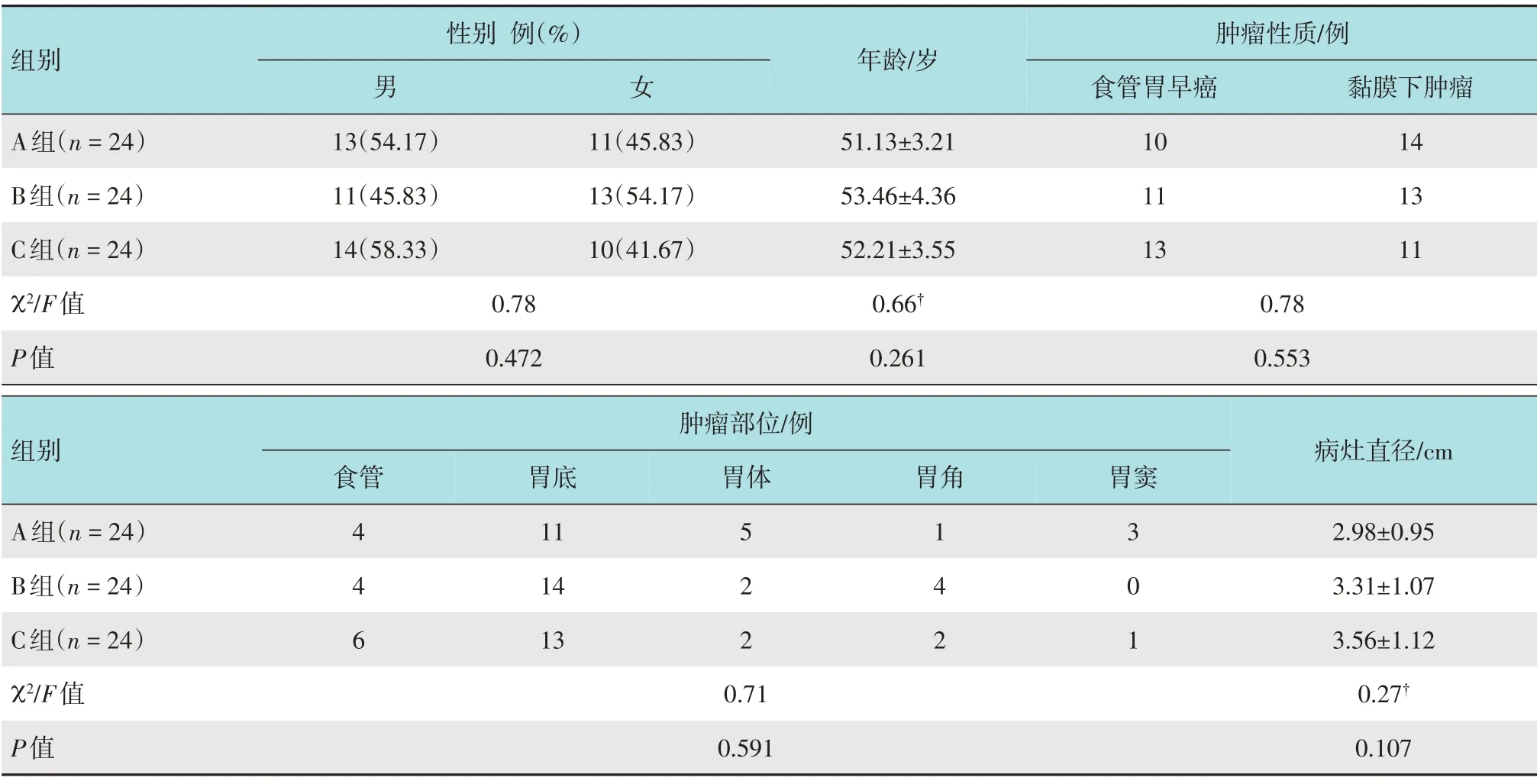
表1 3组患者一般资料比较Table1 Comparison of general data among the three groups
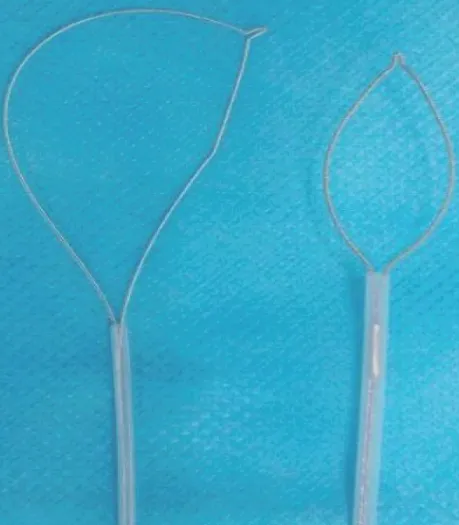
图1 两种圈套器外形Fig.1 Appearance of two types snare
1.4.2 B 组和C 组采用圈套器牵引改良法。B 组使用粗圈套器(ENDO-FLEX NOE342214-C 圈套器:双股钢丝钢圈,直径0.6 mm);C 组使用细圈套器(Olympus SD-211U-25圈套器:单股钢丝钢圈,直径0.3 mm)。在黏膜下层剥离的过程中,出现视野暴露困难和(或)病灶推翻不佳时,可进行牵引,此时退镜,将软组织夹送入活检通道,从内镜前端伸出,打开两侧臂,在镜身外推送圈套器,将电圈挂于组织夹两臂中间后缩小电圈,关闭组织夹,再将组织夹后退回至透明帽,圈套器附在镜身外侧,在直视下由组织夹带着镜身外的圈套器随镜一同进镜,到达病灶处,释放软组织夹,将其连同圈套器电圈一起固定在病变黏膜层上;若为黏膜下肿瘤,组织夹夹在瘤体附近保留的黏膜上。由操作者牵拉体外圈套器套管,可用推或拉来变动牵引方向,充分暴露黏膜下层手术视野,再应用Hook 刀、Dual 刀或IT 刀继续剥离。将病灶完整切除后,可由圈套器将病灶随内镜一同退出,于体外固定。粗细圈套器辅助ESD治疗过程见图2~5。

图2 组织夹固定圈套器收回透明帽Fig.2 Retract transparent cap with tissue clip fixing snare
1.5 术后处理
术后卧床休息3 d,禁食1 或2 d。如术中出现肌层损伤或全层切除,术后放置1根胃肠减压管,观察1 d 若无发热,可于第2 天拔管后开始进流质饮食。给予抑酸、保护胃黏膜和营养支持等治疗,术后预防性抗生素应用不超过3 d。监测生命体征变化,观察有无腹痛和便血等情况。术后6 和12 个月复查胃镜,之后每年复查1 次胃镜,胃早癌患者根据日本“eCura system评分”[10]决定是否追加手术、复查胃镜和腹部CT等。
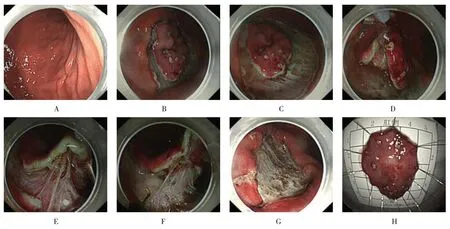
图3 粗圈套器牵引辅助胃体早癌切除的ESD过程Fig.3 Thick snare traction assisted ESD process of early gastric body cancer resection

图4 细圈套器牵引辅助胃角早癌切除的ESD过程Fig.4 Thin snare traction assisted ESD process of early gastric corner cancer resection

图5 细圈套器牵引辅助胃黏膜下肿瘤切除的ESD过程Fig.5 Thin snare traction assisted ESD process of gastric submucosal tumor resection
1.6 统计学方法
采用SPSS 19.0 统计软件分析数据。计量资料以均数±标准差(±s)表示,组间比较行t检验或方差分析;计数资料以例或百分比(%)表示,并采用Pearson χ2检验或Fisher 确切概率法。P<0.05 为差异有统计学意义。
2 结果
2.1 3组患者手术相关指标比较
3 组72 处病灶均完成ESD 切除。A 组手术平均时间为(72.33±26.64) min、B组为(50.58±13.86)min、C 组为(48.58±10.25)min;术中黏膜下补充注射量A 组为(42.58±6.38) mL、B 组为(32.64±3.68)mL、C 组为(20.00±4.51)mL,3 组手术平均时间和黏膜下补充注射量比较,差异有统计学意义(P<0.05)。其中,A组手术平均时间明显长于B 和C 组,差异有统计学意义(P<0.01),B 和C组比较,差异无统计学意义(P>0.05);A组黏膜下补充注射量明显多于C组,两组比较,差异有统计学意义(P<0.05),A 组与B 组比较,差异虽无统计学意义,但B组补充注射量较A组有下降的趋势。A组一次完整切除率为79.16%、B 组为75.00%、C 组为100.00%,C 组明显高于B 组和A 组,差异有统计学意义(P<0.05);B 组固定病灶后组织夹脱离次数为6次、C组为0次,B组明显多于C组,两组比较,差异有统计学意义(P<0.05);B 组和C 组均未发生装置引起的口咽部黏膜损伤。见表2。
2.2 3组患者并发症发生率比较
3组除黏膜下固有肌层肿瘤行全层切除术外,均未发生术中和术后迟发性穿孔。A组发生术中明显出血2 次(8.33%),1 例贲门部早癌和1 例胃体中上部小弯侧早癌均出现动脉搏动性出血,使用止血钳电凝止血;迟发性出血1 次(4.17%),贲门部早癌1 例,表现为术后48 h呕血,再次进镜发现创面一处裸露血管活动性出血,给予止血钳电凝止血。B和C组圈套器牵引组均未发生术中明显出血和迟发性出血。3组术中明显出血和迟发性出血比较,差异均无统计学意义(P>0.05)。见表3。
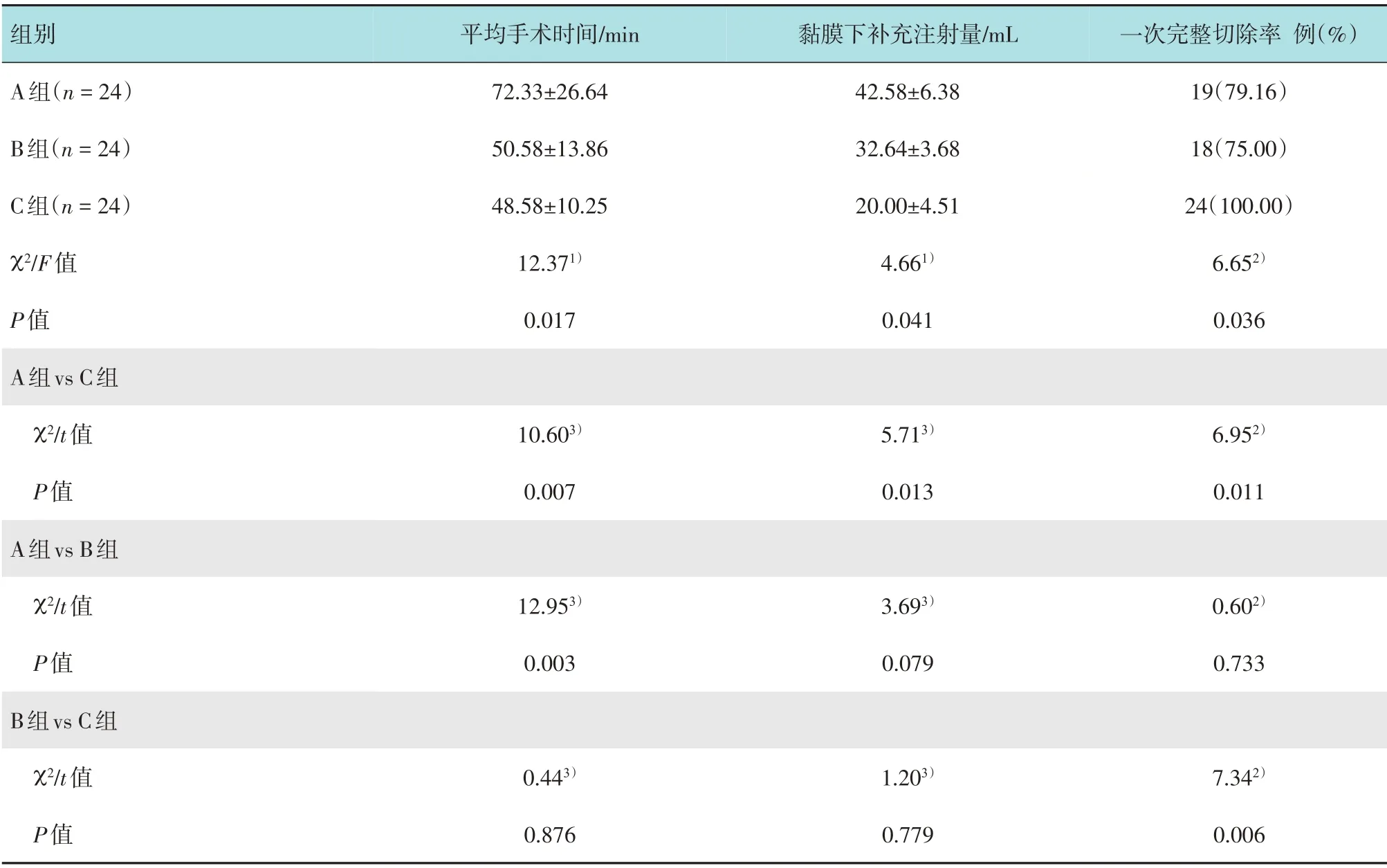
表2 3组患者手术相关指标比较Table2 Comparison of operation related indexes among the three groups

表3 3组患者并发症比较 例(%)Table3 Comparison of complications among the three groups n(%)
3 讨论
3.1 ESD的辅助牵引技术
随着ESD技术广泛地应用于食管、胃黏膜和黏膜下肿瘤,食管和胃腔更大的病变、更难的部位(如贲门、胃底部大弯侧穹窿部、胃底上部前壁、胃体小弯、胃体上部大弯和胃角等)、瘢痕纤维化的病变都可行ESD切除,但对于这些困难ESD,术中不易得到清晰的手术视野。牵引技术的出现,是ESD手术顺利并快速进行和降低并发症风险的关键。理想的牵引能很好地成为内镜医生的第二只手,在外科手术、牵引与切除中独立使用,且牵引的方向和力度随时可控。目前,使用的牵引方法包括双内镜联合、双通道内镜、外抓钳辅助、体外辅助牵引技术、外在磁控和滑轮技术等,都存在各自的不足,实用性不强。橡皮圈内牵引技术在肠道应用较为实用,但对于食管腔狭小和壁薄的患者,多点钛夹使用会影响操作,胃腔宽大使橡皮圈的大小受限,不是每个部位都适用此法。体外线牵引技术特别是牙线牵引技术,由于操作较为方便、材料简单可得,临床应用较广泛,但也存在一些问题,如:牵引方向单一、只能拉不能推、牵引力度过大时可引起钛夹脱落、增加反复进镜次数和延长手术时间等,甚至可能导致病灶组织缺失。而圈套器牵引法解决了牵拉方向不可变的问题。这些技术需要不断优化,才能更好地提高手术治疗效果和缩短操作时间。
3.2 传统圈套器牵引方法的缺点
3.2.1 送入的方式将圈套器外圈收在透明帽外,圈套器套管在镜身外随镜进入:①此方法不在内镜直视下将圈套器送入,同时增加进镜外圈直径,透明帽外圈为钢圈,粗糙不平滑,有损伤口咽部或食管贲门狭窄处黏膜的风险;②进入体内后,松开圈套器送达病变部位操作困难,尤其是倒镜操作的部位。
3.2.2 病灶的牵拉方式①单一圈套器牵拉法:将圈套器圈套在已剥离的一部分病灶上进行牵引,要求剥离足够多的组织才能实现圈套的稳固,且要考虑圈套脱离和病灶组织损伤的可能;②血管夹-圈套器法:钛夹钳夹住病变黏膜,推到需要牵拉的位置,收紧圈套器固定牵拉方向后,释放钛夹,此方法可以保持圈套器和钛夹各自独立,实现多位点牵拉,但需要专门一位助手在牵拉过程中始终收紧圈套器,对于需长时间操作的大病灶或困难病变实践性不强;另外,圈套不紧也会出现脱落,反复圈套增加手术时间;③黏膜下肿瘤的直接钳夹法:对于黏膜下肿瘤的牵拉,钛夹需直接钳夹住肿瘤表面,部分黏膜下肿瘤表面光滑,钛夹不能受力易脱落,是否会造成瘤体破损等尚无定论。
3.3 改良圈套器牵引法的优点
3.3.1 送入的方式使用在活检钳通道内的可反复开闭的组织夹,从镜身头端伸出夹住镜身外的圈套器钢圈,再收回到透明帽内,直视观察下送入到体内。其优点是:①直视观察下送入内镜和圈套器,操作更安全;②未增加透明帽外圈直径和粗糙面,与黏膜的摩擦减小,不会造成黏膜损伤。
3.3.2 圈套器-组织夹固定法①圈套器本身由组织夹钳夹固定送入病灶,即使倒镜也较容易操作;②同时由组织夹钳夹圈套器,再钳夹病灶组织黏膜,圈套器相对不容易脱落;③无需多一名助手操控圈套器,放在一旁即可(牙线法需助手牵拉线,形成牵拉张力)。
3.3.3 牵引方向圈套器牵引的方向可拉可推,适合食管和胃各部位的牵引。
3.3.4 优于常规组本研究中,圈套器牵引组能保持良好的手术视野,明显缩短手术平均时间,细圈套器组还能减少黏膜下补充注射量,明显优于常规ESD术。
3.3.5 可防止肿瘤掉入腹腔在进行固有肌层肿瘤全层切除术时,由于有圈套器的牵拉,不需要更换双腔镜,可以防止肿瘤掉入腹腔。
3.3.6 更易取出肿瘤取出肿瘤变得更容易,用牵拉病灶的圈套器带出即可。
3.3.7 实用性强圈套器和组织夹为ESD手术的基本配置,材料简单易得,实用性强。
3.4 粗细圈套器牵引的优缺点
本研究选择两类具有代表性的圈套器进行对比研究。笔者发现,粗圈套器(双股钢丝)牵引组织夹脱离6 次,其中3 次为食管胃黏膜早癌治疗,在牵引过程中,组织夹连同所夹病变组织部分黏膜一起脱离,病灶组织破损;另3次为胃黏膜下肿瘤治疗,在牵引过程中组织夹连带黏膜下肿瘤附近黏膜一起脱离。分析原因,本研究组织夹脱离在黏膜肿瘤和黏膜下肿瘤中都有发生,例数相同,且发生在不同的部位,所以考虑其脱离与肿瘤性质和肿瘤部位无关。笔者推测,粗圈套器的牵引力过大,从而直接造成牵引黏膜的破损;在胃黏膜下肿瘤中,因牵引力过大,造成黏膜与瘤体的分离,从而影响一次完整切除率,增加术后病理判断难度,而细圈套器组(单股钢丝)则没有发生组织夹脱离。本研究显示,应用细圈套器牵引术,明显减少组织夹脱离次数,防止组织黏膜破损,可以提高一次完整切除率。
综上所述,牵引技术的应用为困难ESD术的顺利进行提供了良好的手术视野。细圈套器牵引力度适中,既可实现牵拉过程中推的力量,也不会出现牵引力过大所致的组织夹脱离和组织破损,再结合改良的牵引方法,优化了圈套器牵引技术,缩短了手术时间。此项技术的材料简单易得,实用性强,在ESD切除上消化道早癌、黏膜下肿瘤中的应用较广泛。但目前研究病例数有限,与其他牵引方法的对比研究还待深入探讨。
