内分泌治疗激素受体阳性乳腺癌的效果及其与ESR1基因位点的关系
2020-11-06顾兵吴旦平张晶晶
顾兵 吴旦平 张晶晶
[摘要] 目的 研究內分泌治疗激素受体阳性乳腺癌的效果及其与雌激素受体1基因(ESR1)单核苷酸多态性位点(rs2077647和rs3798759)的关系。 方法 选择2014年1月—2018年12月于江苏省常熟市第五人民医院收治的86例激素受体阳性乳腺癌患者为研究对象,均接受内分泌治疗,并接受ESR1单核苷酸多态性位点(rs2077647和rs3798759)检测。分析内分泌治疗后短期疗效,并观察其与ESR1单核苷酸多态性位点的关系。 结果 86例患者内分泌治疗后完全缓解、部分缓解、疾病稳定共45例,均归入ETR组;疾病进展41例,归入ETNR组。ETR组rs2077647位点基因型为CC型者占比显著高于ETNR组(P < 0.05),rs3798759位点基因型为TT型者占比显著低于ETNR组(P < 0.05),且基因型为TG型者占比显著高于ETNR组(P < 0.05)。ETR组rs2077647位点等位基因为C者占比显著高于ETNR组(P < 0.05),rs3798759位点等位基因为G者占比显著高于ETNR组(P < 0.05)。ESR1基因多态性是患者内分泌治疗效果的独立影响因素(P < 0.05)。 结论 内分泌治疗激素受体阳性乳腺癌后疗效与ESR1单核苷酸多态性位点(rs2077647和rs3798759)密切相关。
[关键词] 内分泌治疗;激素受体;乳腺癌;雌激素受体1基因
[中图分类号] R737.9 [文献标识码] A [文章编号] 1673-7210(2020)09(b)-0026-04
[Abstract] Objective To study the effect of endocrine therapy on hormone receptor positive breast cancer and its relationship with ESR1 gene locus (rs2077647 and rs3798759). Methods Eighty-six patients with hormone receptor positive breast cancer admitted to the Fifth People′s Hospital of Changshu City in Jiangsu Province from January 2014 to December 2018 were selected as study objects. All patients were treated with endocrine therapy and ESR1 single nucleotide polymorphisms (rs2077647 and rs3798759) were detected. The short-term efficacy of endocrine therapy was analyzed and its relationship with ESR1 single nucleotide polymorphisms was observed. Results Forty five patients of 86 patients with complete remission, partial remission and stable disease after endocrine therapy were included in ETR group, 41 patients with disease progression were classified into ETNR group. The proportion of genotype CC at rs2077647 in ETR group was significantly higher than that in ETNR group (P < 0.05), the proportion of TT genotype of rs3798759 was significantly lower than that of ETNR group (P < 0.05), and the proportion of TG genotype was significantly higher than that of ETNR group (P < 0.05). The proportion of allele C at rs2077647 in ETR group was significantly higher than that in ETNR group (P < 0.05), and the proportion of allele G at rs3798759 was significantly higher than that in ETNR group (P < 0.05). ESR1 gene polymorphism was an independent factor affecting the effect of endocrine therapy (P < 0.05). Conclusion The effect of endocrine therapy on hormone receptor-positive breast cancer is closely related to ESR1 single nucleotide polymorphisms (rs2077647 and rs3798759).
[Key words] Endocrine therapy; Hormone receptor; Breast cancer; Estrogen receptor 1 gene
据报道,近年来乳腺癌发病率呈逐年增长趋势,约75%的患者孕激素受体或雌激素受体呈阳性,而经后续强化辅助内分泌治疗可降低患者复发风险,延长无病生存期与总生存期[1-3]。尤其针对雌激素受体阳性早期乳腺癌患者,行内分泌治疗后可降低50%左右的复发风险[4]。绝大部分雌激素受体阳性乳腺癌患者虽可从内分泌治疗中获益,但治疗过程中会出现内分泌治疗耐药,影响临床疗效[5]。而雌激素受体1基因(ESR1)异常是诱发内分泌治疗耐药常见原因之一[6]。但目前临床多侧重于研究ESR1基因突变与乳腺癌内分泌治疗耐药的相关性,鲜有报道分析内分泌治疗激素受体阳性乳腺癌的效果及其与ESR1单核苷酸多态性位點的关系[7]。因此,本文展开相关研究。
1 资料与方法
1.1 一般资料
选择2014年1月—2018年12月于江苏省常熟市第五人民医院收治的86例激素受体阳性乳腺癌患者为研究对象,年龄18~52岁,平均(42.33±8.16)岁。纳入标准:入院后确诊[8],未发现远处转移;激素受体阳性,孕激素受体或雌激素受体呈阳性;腋窝淋巴结阴性(前哨或腋清);年龄≥18岁,均为绝经前初治患者;临床资料完整。排除标准:严重心、肾等重要脏器功能不全;男性乳腺癌,或转移性、家族性乳腺癌;其他恶性肿瘤;精神障碍、心理障碍病史;对本研究药物过敏者。
1.2 方法
1.2.1 内分泌治疗
口服他莫昔芬(苏州第壹制药,生产批号:100930,规格:10 mg/片),10 mg/次,2次/d,持续治疗12周。
1.2.2 ESR1单核苷酸多态性位点检测方法
1.2.2.1 主要仪器与试剂 主要仪器包括UNOⅡ48型聚合酶链反应(PCR)扩增仪(德国Biometra公司)、7000型荧光定量PCR仪(美国ABI公司)、Je1 Doc 2001型凝胶成像系统(美国Biorad公司)。微量DNA提取试剂盒由杭州新景生物试剂开发有限公司提供(货号:3102050),Tag DNA聚合酶由上海嵘崴达实业有限公司提供(货号:罗氏4738225001),PCR试剂盒由北京百奥莱博科技有限公司提供(货号:YT381-CLI)。
1.2.2.2 检测方法 取全血100 μL,提取DNA后行PCR扩增体系及循环体系设计。反应条件:95℃ 5 min;93℃55 s,58℃ 40 s,72℃ 45 s,持续35个循环;72℃ 10 min。PCR反应体系:总体积25 μL,含Tris-HCl(pH 8.3)10 mmol/L、MgCl2 1.5 mmol/L、KCl 1.5 mmol/L、dNTP 200 mmol/L、上下游引物各15 pmol/L、Taq DNA聚合酶1.0 U和基因组DNA 20~40 ng。行PCR-限制性片段长度多态性基因分型,酶切反应体系20 μL,PCR产物8~17 μL,BSA 0.2 μL,10×Buffer 2.0 μL,限制性内切酶0.7 μL,灭菌双蒸水按照PCR产物量补足体系;37℃恒温箱孵育5 h,琼脂糖凝胶分离,110 V电压电泳40~50 min,行反应产物检测,后将凝胶电泳图像输入凝胶电泳成像系统,鉴定基因型结果。ESR1单核苷酸多态性位点包括rs2077647(基因型TT、CT、CC)和rs3798759(基因型TT、TG、GG),均存在2个等位基因,前者为等位基因T、C,后者为等位基因T、G。
1.3 观察指标
分析内分泌治疗效果并分为内分泌治疗有效(ETR)组和内分泌治疗无效(ETNR)组,观察其疗效与ESR1基因位点的关系。疗效判定参考WTO实体瘤疗效评价标准[9],包括完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD),其中CR、PR、SD均归入ETR组,其余纳入ETNR组。
1.4 统计学方法
采用SPSS 19.0软件处理数据,计数资料以百分率(%)表示,组间比较采用χ2检验或校正χ2检验;等级资料组间比较采用Mann-Whitney U秩和检验;计量资料以均数±标准差(x±s)表示,组间比较采用t检验;多因素logistic回归分析法分析激素受体阳性乳腺癌患者短期内分泌治疗效果的独立影响因素。以P < 0.05为差异有统计学意义。
2 结果
2.1 临床疗效分析
86例患者内分泌治疗后CR 2例,占2.33%;PR 26例,占30.23%;SD 17例,占19.77%,均归入ETR组。PD 41例,占47.67%,归入ETNR组。
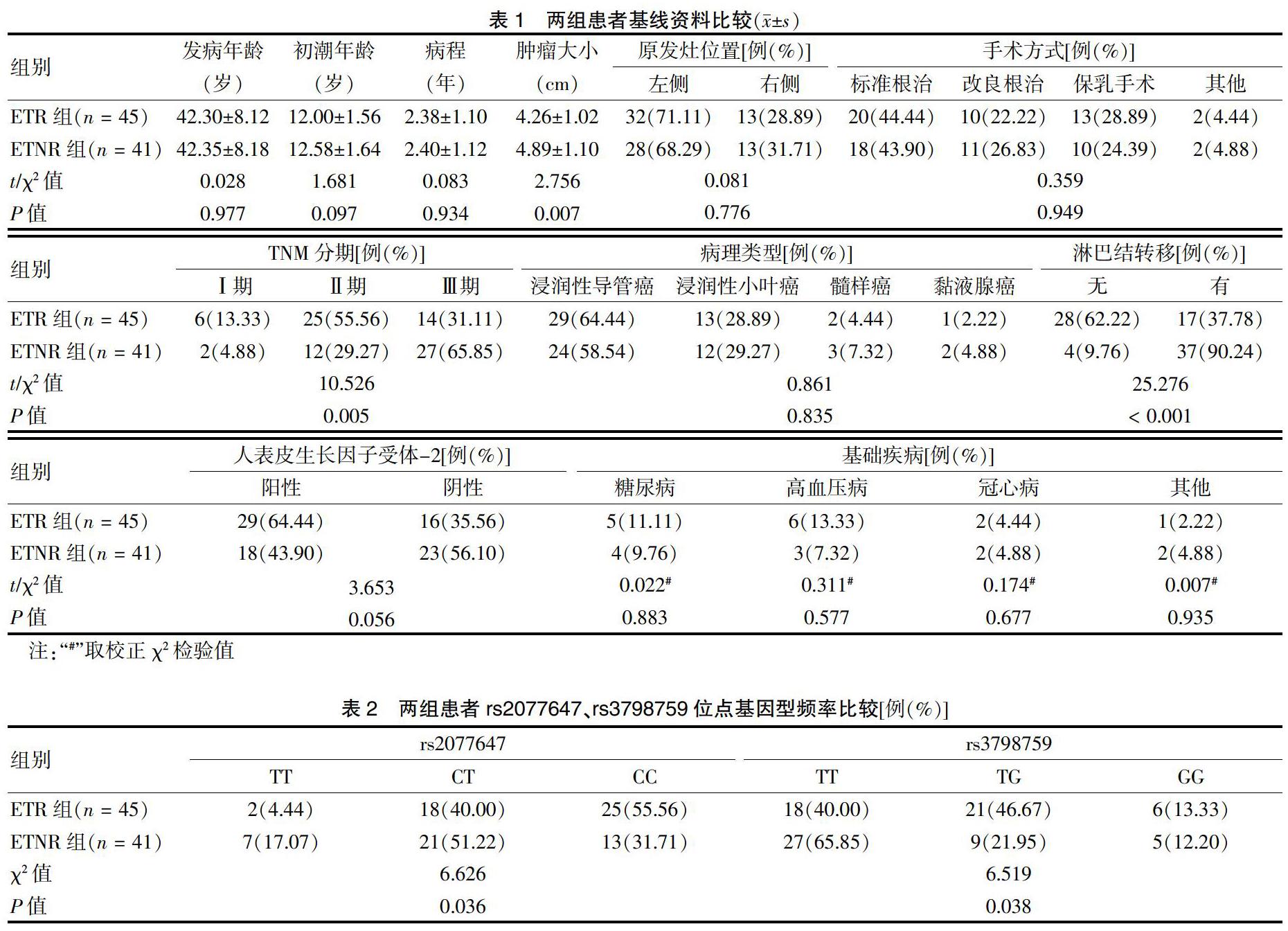
2.2 两组患者基线资料比较
两组肿瘤大小、TNM分期及淋巴结转移比较,差异有统计学意义(P < 0.05)。见表1。
2.3 两组患者ESR1单核苷酸多态性位点检测结果比较
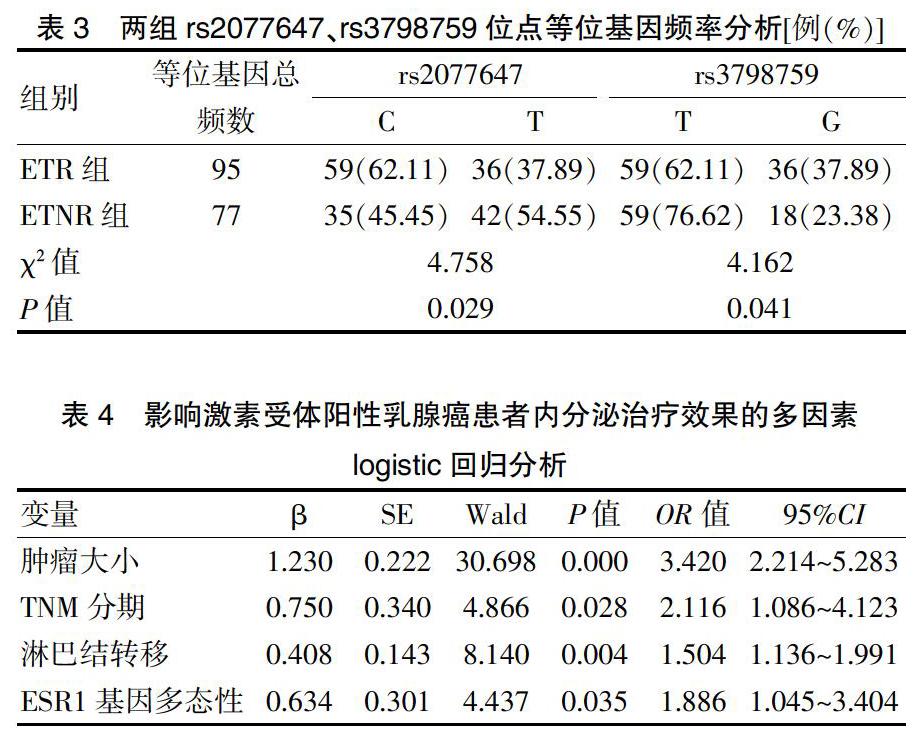
ETR组rs2077647位点基因型为CC型者占比显著高于ETNR组(P < 0.05),rs3798759位点基因型为TT型者占比显著低于ETNR组(P < 0.05),且基因型为TG型者占比显著高于ETNR组(P < 0.05)。ETR组rs2077647位点等位基因为C者占比显著高于ETNR组(P < 0.05),rs3798759位点等位基因为G者占比显著高于ETNR组(P < 0.05)。见表2~3。
2.4 影响激素受体阳性乳腺癌患者内分泌治疗效果的多因素logistic回归分析
以内分泌治疗后短期疗效为因变量,将上述有差异的单因素作为自变量,对各变量进行赋值(肿瘤大小<3.5 cm = 0,≥3.5 cm = 1;TNM分期Ⅰ期=1,Ⅱ期=2,Ⅲ期=3;有淋巴结转移=1,无淋巴结转移=0;ESR1各等位基因不含该等位基因者=0,含该等位基因者=1),纳入多因素logistic回归统计分析。肿瘤大小、TNM分期、淋巴结转移、ESR1基因多态性均为影响患者内分泌治疗效果的独立影响因素(P < 0.05)。见表4。
3 讨论
目前,他莫昔芬被认为是治疗绝经前激素受体阳性乳腺癌的标准一线内分泌治疗方案,主要经自分泌或旁分泌机制干扰肿瘤细胞分泌生长因子及血管生成因子,于乳腺组织中形成雌激素拮抗效应,并与雌激素受体竞争性结合雌激素,经中断与生长停滞及细胞凋亡相关的雌激素,最终实现抗肿瘤目的[10-12]。陈岚等[13]发现,他莫昔芬治疗雌激素受体阳性乳腺癌有效率为32.56%,控制率达51.16%,与本结论(52.33%)相似,证实他莫昔芬治疗该病疗效确切。近年来,已有大量单核苷酸多态性被证实可作为药物反应标记用于临床药物治疗指导,但鲜有报道分析内分泌治疗激素受体阳性乳腺癌的效果及其与ESR1单核苷酸多态性位点的关系[14-15]。
本研究发现,ETR组rs2077647位点基因型为CC型者占比明显高于ETNR组,rs3798759位点基因型为TT型者占比明显低于ETNR组,且基因型为TG型者占比显著高于ETNR组;而ETR组rs2077647位点等位基因为C者占比明显高于ETNR组,rs3798759位点等位基因为G者占比明显高于ETNR组,证实内分泌治疗激素受体阳性乳腺癌后疗效与ESR1单核苷酸多态性位点密切相关。研究发现,乳腺癌他莫昔芬治疗反应与雌激素受体基因点突变、变异、多态性有关[16-18]。Ghali等[19]也认为,rs2077647位点与rs3798759的等位基因及基因型与激素受体阳性乳腺癌内分泌治疗效果相关。rs2077647位点处于外显子l上,本身为同义突变,而rs3798759位点处于3′UTR,两个单核苷酸多态性位点作为遗传标记,按连锁不平衡分析原理,临近区域内可能出现影响内分泌治疗效果的阳性区域,存在内分泌治疗效果相关基因,具体机制尚待今后深入调查。但有报道发现,rs2077647位点与下游rs2234693位点构成的单倍型与乳腺癌内分泌治疗效果无相关性,故认为可向其上游选择遗传标记展开深入分析,但本文未分析此点,有待今后进一步探讨[20]。此外,本研究中发现,ESR1基因多态性亦为影响患者内分泌治疗效果的独立影响因素,进一步证实内分泌治疗激素受体阳性乳腺癌后疗效与ESR1单核苷酸多态性位点有关。
综上,ESR1单核苷酸多态性位点(rs2077647和rs3798759)与激素受体阳性乳腺癌激素受体阳性乳腺癌疗效有关,但本文选取病例数偏少,结果可能存在偏倚,故今后需深入研究。
[参考文献]
[1] 唐金海.乳腺癌70年[J].中国肿瘤外科杂志,2019,11(3):153-154.
[2] 杨海波,高晋南,宋宛芝.单纯乳腺癌与乳腺癌合并甲状腺癌患者临床病理特征分析[J].中华肿瘤杂志,2019,41(8):624-627.
[3] 马辰,王振宇,华建芬,等.老年女性乳腺癌新辅助内分泌治疗的临床进展[J].国际老年医学杂志,2019,40(2):120-123.
[4] 李田宏,郭放,谢晓冬.2018年ASCO年会CDK4/6抑制剂联合内分泌治疗晚期乳腺癌最新进展解读[J].中华内分泌外科杂志,2019,13(2):159-161.
[5] 武星星,王伏生,胡耀峰,等.乳腺癌内分泌治疗耐药相关信号通路的研究进展[J].癌症进展,2019,17(12):1380-1384.
[6] 赵爽,陈双双,于正洪.ESR1基因改变在乳腺癌内分泌治疗耐药中的研究进展[J].临床肿瘤学杂志,2016,21(10):947-951.
[7] 朱琳,杨顺娥.乳腺癌雌激素受体相关基因研究进展[J].现代肿瘤医学,2015,23(8):1135-1138.
[8] 中国抗癌协会乳腺癌专业委员会.中国抗癌协会乳腺癌诊治指南与规范(2007版)[J].中国癌症杂志,2009,19(6):410-428.
[9] 中国华人民共和国卫生部.中国常见恶性肿瘤诊治规范[M].北京:北京医科大学、中国协和医科大学联合出版社,1991:25-29.
[10] 朱蔼瑜,许宇媚,许晶,等.雄激素受体对雌激素受体阳性乳腺癌细胞增殖的抑制作用[J].医学研究生学报,2016,29(4):354-358.
[11] 杨帏,李苏,邓颖斐,等.中国人群CYP2D6基因多态性及其与激素受体阳性早期乳腺癌他莫昔芬代谢的关系[J].实用医学杂志,2018,34(12):1995-1999.
[12] 李英彬,郭茜,包文华,等.他莫昔芬对乳腺癌SK-BR-3细胞侵袭能力的影响及其机制[J].中华内分泌外科杂志,2019,13(5):368-371.
[13] 陈岚,陈巍,李硕果.贞芪扶正胶囊联合他莫昔芬治疗雌激素受体阳性乳腺癌的临床研究[J].现代药物与临床,2018,33(5):1172-1175.
[14] 丁佩剑,金秀菊,孙宝信.人类单核苷酸多态性研究进展[J].临床和实验医学杂志,2016,15(12):1235-1238.
[15] 高啟龙,张新峰,耿良,等.UGT2B4基因RS1826690单核苷酸多态性对乳腺癌新辅助化疗病理完全缓解的影响[J].中华医学杂志,2018,98(16):1242-1245.
[16] 叶长生,姚广裕.检测循环肿瘤DNA中ESR1突变在晚期乳腺癌治疗中的价值[J].循证医学,2016,16(3):143-144.
[17] 李娟,李萍萍,刘洁,等.抑癌基因LKB1与乳腺癌他莫昔芬耐药性之间的关系[J].现代肿瘤医学,2018,26(20):3184-3189.
[18] 王炜,项晶晶,周虹,等.乳腺黏液癌HER2基因表达特征分析[J].中华病理学杂志,2015,44(4):278-279.
[19] Ghali RM,Al-Mutawa MA,Al-Ansari AK,et al. Differential association of ESR1 and ESR2 gene variants with the risk of breast cancer and associated features:a case-control study [J]. Gene,2018,651(1):194-199.
[20] 殷玉莲,张卫红,周悦,等.ERα基因单核苷酸多态性与乳腺癌应用芳香化酶抑制剂引发骨丢失的相关性研究[J].实用肿瘤学杂志,2018,32(1):14-18.
(收稿日期:2020-02-25)
