取代硫脲衍生物的抗菌活性研究进展
2020-11-04张解和
张解和,孟 歌
(1.皖南医学院,安徽 芜湖 241002;2.复旦大学化学系,上海 200433)
在生物活性的研究领域,作为一类广谱有机化合物,硫脲类衍生物已受到了越来越多药学家的广泛关注[1].研究表明,硫脲类化合物具有良好的生物活性,包括抗细菌,抗真菌,抗肿瘤,抗寄生虫,抗疟疾,抗病毒,抗艾滋病和抗单纯疱疹病。
抗细菌或者抗真菌药物是通过抑制细胞壁的生物合成、影响细菌胞浆通透性、抑制细菌核酸和蛋白质的合成来达到抑制细菌生长或者杀灭细菌的作用。长期使用单一抗生素,极可能使细菌产生耐药性,而不能产生有效的抗菌活性。因此,寻找高效、有效的抑菌药物依然成为人们研究的热点。在此,我们通过阅读大量文献,总结不同取代基的硫脲衍生物的抗菌活性。
1 烷基/芳基/杂环-N-取代硫脲衍生物
1.1 单取代硫脲衍生物
根据硫脲NH取代的官能团的特性,可以分为苯环单取代衍生物和杂环单取代衍生物,在抗菌活性方面都有广泛的研究。
1.1.1 苯基取代硫脲衍生物
2012年,P.Umadevi合成了新型的抗菌活性的硫脲衍生物。化合物1-3金黄色葡萄球菌、枯草芽孢杆菌、沙门杆菌、志贺氏菌都与氨苄西林有相当的抗菌活性,实验表明氨苄西林对沙门杆菌、志贺氏菌并没有作用。因此,该类化合物有望成为新一类有效抗菌剂[2]。
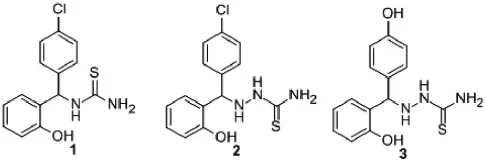
图1 苯基单取代抗菌硫脲衍生物的结构
1.1.2 酰胺取代硫脲衍生物
酰胺单取代的硫脲衍生物,不仅有抗细菌的活性,也具有很好的抗真菌活性。Abdul Jamalabdul Nasser合成化合物4a-4b,4a对金黄色葡萄球菌、肺炎双球菌、大肠杆菌、铜绿假单胞菌的抑菌圈的半径与环丙沙星小,具有更高的抗菌活性,而4b与环丙沙星抗菌活性相似,但是其对铜绿假单胞菌没有明显作用。改变吡啶4位相连的苯环上取代基的结构得到的不同衍生物4a,不如由于4a的3位和5位具有酰胺的结构,4位有对氯苯的结构密切相关[3]。
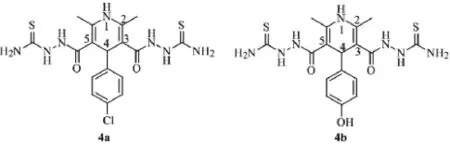
图2 抗菌杂环单取代硫脲衍生物的结构
1.2 双取代硫脲衍生物
这类化合物的结构复杂多变,生物活性也比较广泛,不仅能够抑制各种细菌色生长,还能杀灭真菌。
1.2.1 双苯基取代硫脲衍生物
含甲基、甲氧基、三氟甲基取代的苯基,取代硫脲NH所得化合物,具有极高的抗菌活性。Vandana M.Kamble[4]发现了5a对革兰氏阳性菌和革兰氏阴性菌都有很好抗菌活性MIC=20μg/mL,与环丙沙星相当。但是,其没有抗炎活性,相反5b只有一个-CF3,其抗炎活性远高于5a(含两个-CF3)。还发现了,苯环F取代的硫脲衍生物也具有很好的抗革兰氏阳性、阴性菌活性,6a、6b苯环上分别在2位和4位取代,抑菌活性前者与后者相当,但是抗炎活性相差很大。含有CF3的6c也具有很高的抗菌活性[5]。
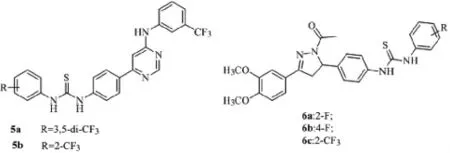
图3 抗菌双苯基取代硫脲衍生物的结构
1.2.2 苯基、杂环取代硫脲衍生物
Annunziata Soriente根据已上市药物利奈唑胺的结构特征,依据生物电子等排体原理,将利奈唑胺甲酰胺部分修饰得到硫脲结构,得到了其类似物7,它对金黄色葡萄球菌ATCC 29213的抑菌活性MIC=2μg/mL,与利奈唑胺相似,并且其对耐利奈唑胺的菌株ATCC43300具有很好的抗菌活性,该化合物引起了人们高度的重视,抗菌机制正在研究中[6]。

图4 利奈唑胺类似物的结构
2 酰基硫脲衍生物
当苯或杂环甲酮结构取代硫脲的NH所得产物也具有一定的抑菌活性,部分化合物还具有抗真菌活性。
2.1 苯甲酰基硫脲衍生物
磺胺类药物常用于细菌性感染疾病的治疗。Sumera Zaib发现了一类磺酰胺类硫脲衍生物,8a-c对大肠杆菌、枯草芽孢杆菌、金黄色葡萄球菌和弗氏志贺菌的抗菌活性MIC都在0.15-0.32μg/mL之间,8b抑菌活性是环丙沙星的1-4倍。8c更能抑制多种真菌 A.niger、A.flavus、A.pterus和W.rot生长的作用,抑制活性略小于特比萘芬。该类化合物苯环上卤素、硝基等吸电子基的引入有助于其抗菌活性,而脂肪链烃增加了其抗真菌活性[7]。
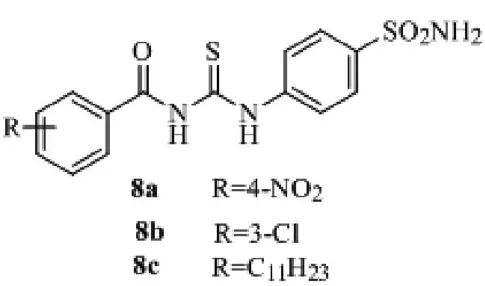
图5 苯甲酰硫脲衍生物的结构
2.2 杂环甲酰基硫脲衍生物
杂环类酰基硫脲主要有五元杂环吡唑和呋喃类,不同杂环酰基硫脲的抑菌活性也各不相同。Alexandru V.Missir发现了一类吡唑酰基硫脲的衍生物9a-9m,这些化合物对枯草芽孢杆菌、金黄色葡萄球菌等菌种抑制活性很弱,抑制活性MIC几乎都超过1000μg/mL,只有 9d和9f在250-1000μg/mL。这可能与酰胺结构跟生物体内各种重要的阳离子结核,形成复合物的难易程度有关。该类化合物酰基相连大体积的烷基部分R,不利于酰胺与生物氨基酸残基形成氢键,阻止了生物复合物的形成[8]。之后,I.V.Kulakov[9]接着对酰基硫脲结构进行了优化,将大脂肪烃结构换为哌啶环,含氮杂环也有含氧呋喃环代替,结果发现9n对常见细菌细胞株有良好的抑制活性MIC在12-18μg/mL,超过庆大霉素MIC在23-25μg/mL。
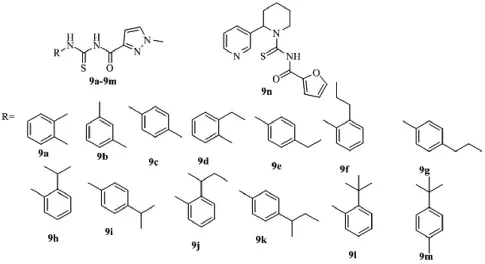
图6 杂环酰硫脲衍生物的结构
3.缩氨基硫脲衍生物
2013年,Pawar RP由杂环甲醛和不同取代的苯甲醛与硫脲缩合得到一类对称的硫脲衍生物10a-10d。它们对大肠杆菌、伤寒沙门菌、金黄色葡萄球菌的抑菌圈大小各不相同。10b对上述细菌的抑制活性最强,100 μg/mL下,其抑菌圈为20mm左右,与青霉素相近。同时,该系列所有化合物的抗真菌活性也不尽相同,10a、10c、10d对曲霉A还不能表现抑制作用,10b上述所有菌株都有明显的抑制活性[10]。
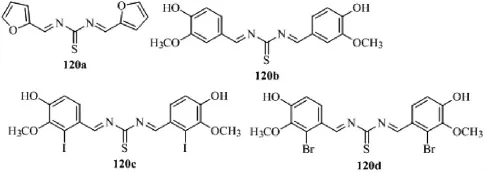
图7 抗菌缩氨基硫脲衍生物的结构
4.硫脲构建杂环衍生物
由于硫脲的化学性质活泼,常用于构建多种杂环,例如五元含氮杂环、六元嘧啶等,这些杂环硫脲衍生物也表现出不同的抗菌活性。
4.1 五元杂环内硫脲衍生物
Iraj Nikokar在2013年合成了咪唑类硫脲衍生物11a-d,但是这类化合物具有很低的抑菌活性,与阳性对照的庆大霉素要弱很多[11]。化合物12a-b是由硫脲合成的三氮唑衍生物,具有很高的生物活性。对炭疽菌和灰霉菌的抑制活在0.3μM、3.0μM、30μM 可达到 90%,与阳性对照药克菌丹相当。
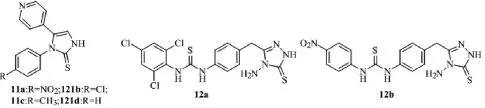
图8 抗菌五元杂环硫脲衍生物的结构
4.2 六元杂环内硫脲衍生物
Mahesh P.Davadra[12]发现了一个嘧啶类硫脲衍生物13,其对革兰氏阳性菌、阴性菌,真菌的白假丝酵母菌都有极高的抑制活性。抗革兰氏阳性和阴性菌活性MIC=62.5μg/mL高于安比西林,抗真菌活性略低于灰黄霉素。后来人们又发现该类嘧啶并吡喃的化合物具有更广泛、更强的抑菌活性,14不论是对革兰氏阳性菌、阴性菌,还是抗真菌活性都很高,比灰黄霉素高出1-2倍。
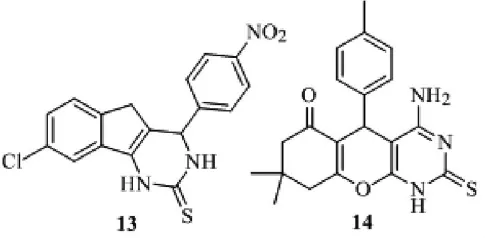
图9 抗菌六元杂环硫脲衍生物的结构
5.氨基硫脲金属配合物
氨基硫脲及其衍生物能与适合的金属(第一过渡系金属离子,锌、铜、镍、镉)形成金属配合物,配合物不仅有广泛的抗肿瘤活性,近些年来,人们发现硫脲金属配合物能够破换DNA分子的氢键结构,使之断裂而抑制细菌生长,逐渐用于抗菌活性的研究。P.R.Chetana[13]用硫脲衍生物与CuCl形成的配合物15a和15b相同浓度条件下,对革兰氏阳性菌、革兰氏阴性菌抑制活性,比硫脲单体具有活性更高。15a和15b对革兰氏阳性、阴性菌的抑菌圈分别是单体的两倍和三倍。这是因为,15b对细菌体内核酸分子具有更高的清除活性。
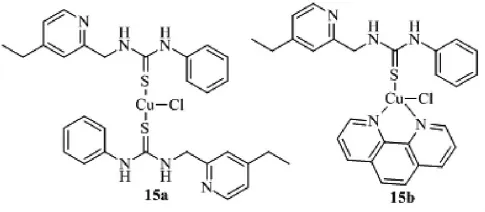
图10 抗菌硫脲金属配合物的结构
随着耐药细菌多样性的出现,发展新型且有效的抗菌药物来降低感染率是迫在眉睫的需求[14]。综上,不同基团取代的硫脲衍生物对结核杆菌、革兰氏阳性菌和革兰氏阴性菌都具有很好的抑制活性。
