水热-二元催化乙醇法分离麦草组分及结构解析
2020-11-04修慧娟李静宇李金宝黎金桂谢竺航
修慧娟 李静宇 李金宝 冯 盼 黎金桂 赵 欣 谢竺航
(陕西科技大学轻工科学与工程学院,轻化工程国家级实验教学示范中心,陕西省造纸技术及特种纸品开发重点实验室,陕西西安,710021)
木质纤维素生物质是地球陆生生态系统中最普遍的低成本、可再生生物质原料,但其中89%木质纤维尚未被充分利用[1],其主要技术瓶颈之一就是缺乏清洁、高效、低成本的组分分离技术。水热法[2-4]和乙醇法[5-7]因其溶剂可回收利用而被广泛关注,但这两种分离方法都仅对单一组分半纤维素或木质素的分离效果较好;如果采用水热-乙醇联用的分离方法,在水热处理段分离半纤维素,乙醇处理段分离木质素,有望实现半纤维素、木质素及纤维素的高效分离。
已有的研究表明,水热-乙醇法对半纤维素的分离效果非常好,但是水热处理段使木质素发生形态和结构上的变化,导致了乙醇处理过程中木质素的分离效果极差[8]。前期研究发现加入催化剂可以提高乙醇处理段对木质素的脱除效率[9]。因此,本课题采用水热-二元催化乙醇法对麦草纤维素、木质素、半纤维素进行分级分离,主要研究了该工艺方法对这3种组分的分离效果,以及半纤维素和木质素分离物的化学结构。
1 实 验
1.1 原料及药品
麦草,水分10%,取自陕西某地,粉碎后筛取40~60 目组分备用[10-11];质量分数95%乙醇、质量分数30%过氧化氢、氢氧化钠均为分析纯,购自天津市大茂化学试剂厂。麦草原料的组分含量按照国家标准进行检测,结果如表1所示。
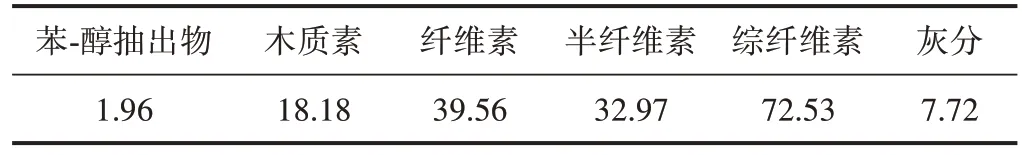
表1 麦草全组分含量 %
1.2 实验仪器设备
PARR-5500 轻便型台式反应釜,美国Parr 公司;W201 恒温水浴锅,上海申生科技有限公司;SHBIII 循环水式多用真空泵,巩义市予华仪器有限责任公司;DHG-9030A 电热鼓风干燥箱,上海一恒科学仪器有限公司;BS210S 分析天平,北京赛多利斯天平有限公司;DL-1 万用电炉,北京中兴伟业仪器有限公司;SX-4-10马弗炉,天津泰斯特仪器有限公司;ICS 5000 高效阴离子色谱仪,德国Dionex 公司;VERTEX70 傅里叶变换红外光谱仪,德国Bruker 公司;FD-1A-50 冷冻干燥机,北京博医康实验仪器有限公司;RE-52AA 旋转蒸发仪,上海亚荣生化仪器厂;TG16-WS 台式高速离心机,湖南湘仪实验室仪器开发有限公司;AVIII 400 MHz 核磁共振波谱仪,德国Bruker公司。
1.3 水热法提取半纤维素
称取一定量麦草与水按总固液比为1∶24(g∶mL)均匀混合,置于高压反应釜中,升温速率为7℃∕min,升温至180℃,保温40 min。过滤分离,得到固相产物和水解液。用H2SO4调节水解液pH 值至2,离心分离上清液,再经旋转蒸发仪蒸发浓缩至一定体积,加入乙醇溶剂沉淀[12],过滤分离沉淀物,并冷冻干燥得到半纤维素分离物。
1.4 二元催化乙醇法提取木质素
将水热固相产物与质量分数50%乙醇溶液混合,在质量分数3% H2O2和质量分数3% NaOH 二元催化下,按总固液比为1∶16(g∶mL),置于高压反应釜中,升温速率为7℃∕min,升温至190℃,保温90 min,过滤分离固相产物,并用55%乙醇溶液和去离子水洗涤,干燥得到粗纤维素;液相产物通过稀释沉淀法[13]分离出木质素,过滤干燥后得到木质素分离物。水热-乙醇法不添加催化剂,其余步骤与上述相同。
1.5 分析与表征
1.5.1 粗纤维素得率、木质素与半纤维素脱除率和提取率的计算
粗纤维素得率、木质素与半纤维素脱除率和提取率分别按式(1)~式(5)计算。

式中,m1为粗纤维素质量,g;m2为原料质量,g;m3为粗纤维素中木质素质量,g;m4为原料中的木质素质量,g;m5为木质素分离物质量,g;m6为粗纤维素中的半纤维素质量,g;m7为原料中的半纤维素质量,g;m8为半纤维素分离物质量,g。
1.5.2 水解液中半纤维素含量的测定
取1 mL 水解液稀释适宜倍数,再经0.22 μm 针孔过滤器过滤后,采用高效阴离子色谱仪,以Dionex CarboPacTM PA200(3 mm × 250 mm)为分析柱,以CarboPacTM PA200(3 mm × 50 mm) 为保护柱,柱温 30℃,取样 25 μL,淋洗液分别为 100 mmol∕L NaOH、500 mmol∕L NaOAc溶液和蒸馏水,以0.3 mL∕min的流速梯度淋洗,测定水解液中低聚木糖(DP=2~6)及半纤维素单糖(如木糖、葡萄糖、阿拉伯糖、半乳糖、鼠李糖、岩藻糖)的含量[14]。
1.5.3 红外光谱测试
将木质素分离物以及半纤维素分离物研成粉末,与KBr 压片。由傅里叶变换红外光谱仪(FT-IR)测量其红外光谱[15]。测试参数为:扫描次数10 次、波数范围500~4000 cm-1、分辨率0.5 cm-1。
1.5.4 核磁共振波谱测试
分别将50 mg 和100 mg 半纤维素分离物溶解在1 mL的D2O 中,采用核磁共振波谱仪(NMR) 对其进行1H NMR 和13C NMR 测定。测定的参数为:采样时间1.36 s,驰豫时间1.89 s,分别扫描128和5000 次[16]。将60 mg木质素分离物溶解在0.5 mL 的DMSO-d6 中,采用核磁共振波谱仪对其进行1H NMR 测定[17]。测定的参数为:采样时间2 s,弛豫时间3 s,扫描512次。
2 结果与讨论
2.1 水热法对半纤维素的分离效果
水热处理对半纤维素的分离效果如图1 所示。由图1 可知,经水热处理后,半纤维素的脱除率为81.8%,其中,醇沉法得到半纤维素聚糖为38.1%,水解液中未沉淀出来的低聚木糖以及单糖的含量为28.0%,各种低聚木糖以及单糖的含量如表2 所示,其中戊糖含量为 2.89 g∕L,高于己糖含量 0.96 g∕L;低聚木糖(包含木二糖、木三糖、木四糖、木五糖和木六糖)含量为1.78 g∕L;己糖主要是甘露糖,含量为0.66 g∕L;残留在固相产物的半纤维素是18.2%,在水热过程中转化为其他组分损失的半纤维素占15.7%。
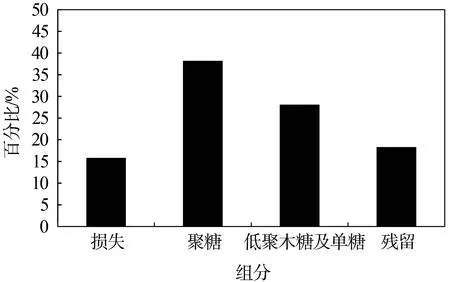
图1 水热法对半纤维素的分离效果
2.2 水热-二元催化乙醇法对麦草组分的分离效果
水热-二元催化乙醇法对麦草3 种主要组分分离效果如图2所示。从图2中可以看出,水热-二元催化乙醇法对半纤维素的脱除率为91.5%,木质素的脱除率为85.6%,粗纤维素得率为40.7%。相比水热处理,水热处理后再经二元催化乙醇处理段,只有9.7个百分点的半纤维素进一步被脱除,因此可以得出,半纤维素主要在第一步水热段中大量脱除。但是与水热-乙醇法相比,水热-二元催化乙醇法对木质素的脱除率有明显的提高,脱除率从56.1%增加至85.6%,提高了52.6%,表明了二元催化乙醇段对木质素的脱除效果更好;其中稀释沉淀法木质素提取率为55.5%。同时二元催化乙醇段对纤维素的降解也较少,粗纤维素得率仅从43.3%降低到40.7%,因此,水热-二元催化乙醇法可以满足水热段分离半纤维素和二元催化乙醇段分离木质素,从而实现麦草3种主要组分的高效分离。
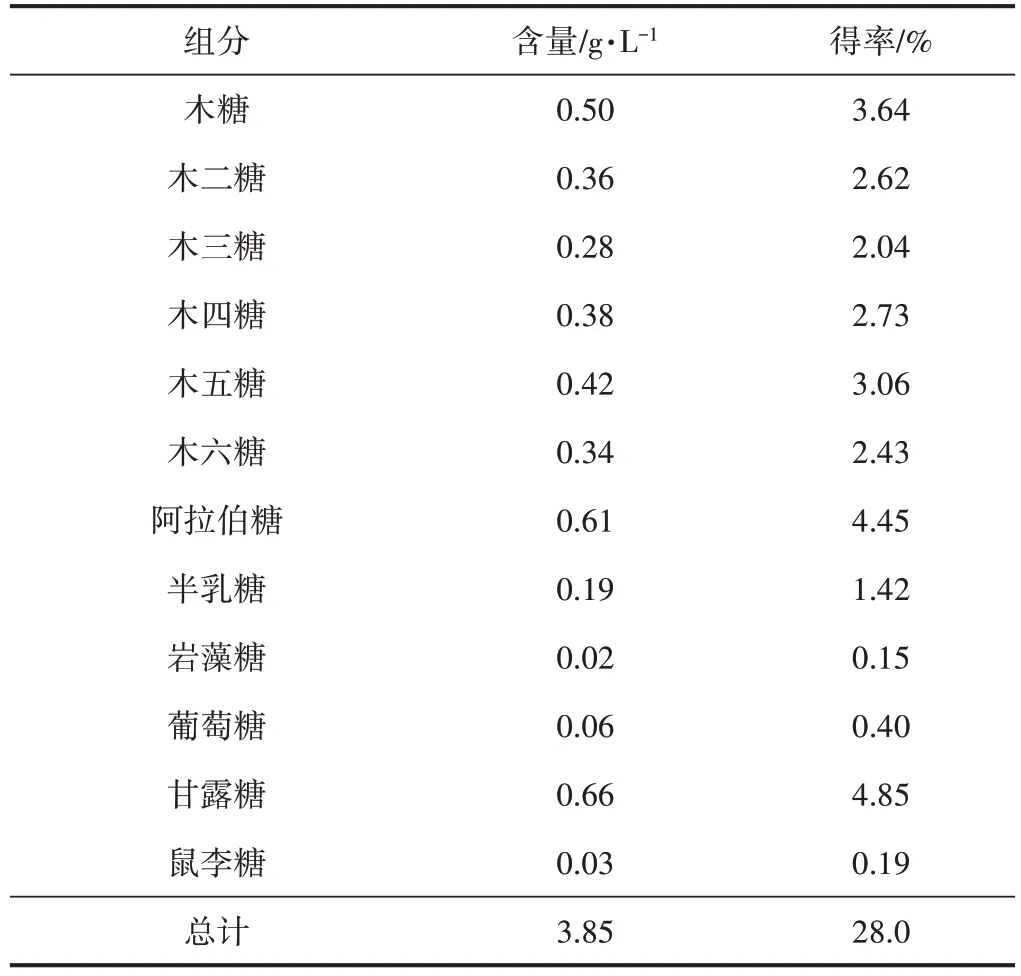
表2 水解液中半纤维素各组分含量和得率
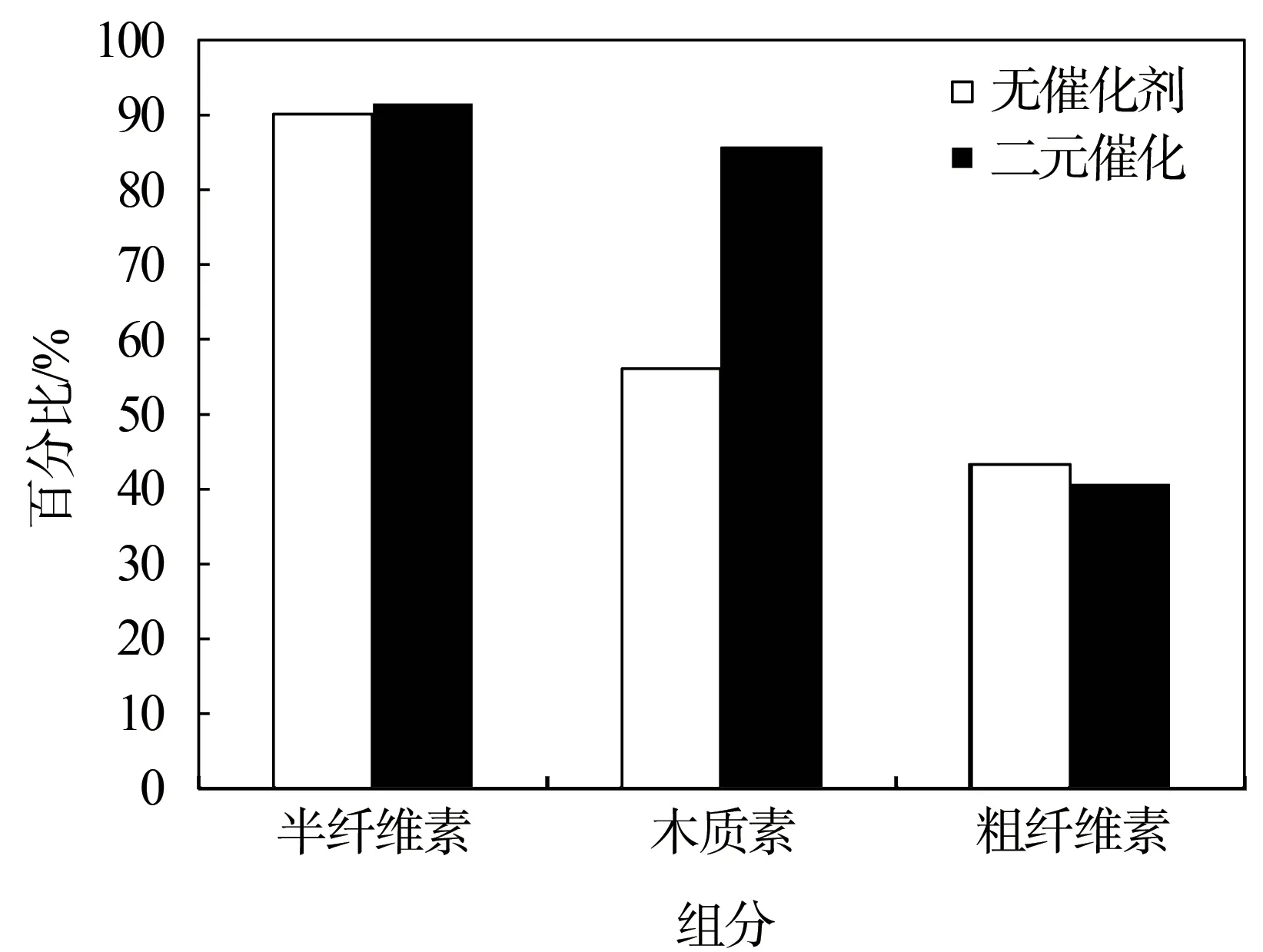
图2 水热-二元催化乙醇法与水热-乙醇法对麦草3种主要组分的分离效果
2.3 半纤维素分离物的FT-IR分析
半纤维素分离物的FT-IR 谱图如图3 所示,从图3 可以看出,3303 cm-1处的吸收峰为羧基和羟基中的O—H 特征峰,2903 cm-1为C—H 的非对称伸缩振动吸收峰,1734 cm-1处的吸收峰归属于半纤维素中的乙酰基[18],说明水热法提取的半纤维素中依然还有部分没有脱落的乙酰基;1596、1514、1426 cm-1处为糖醛酸的吸收峰。半纤维素的特征吸收峰主要集中在800~1400 cm-1范围之内,1377 cm-1和 1251 cm-1处来源于半纤维素中—OH 和C—O 的弯曲振动,894 cm-1处的吸收峰表明糖单元之间的连接是β-糖苷键,1048 cm-1处吸收峰归属于1,4-β-聚木糖中的 C—O、C—C 伸缩振动和 C—OH 弯曲振动[19]。1163 cm-1和987 cm-1处的吸收峰代表了阿拉伯糖基的特征峰[20]。
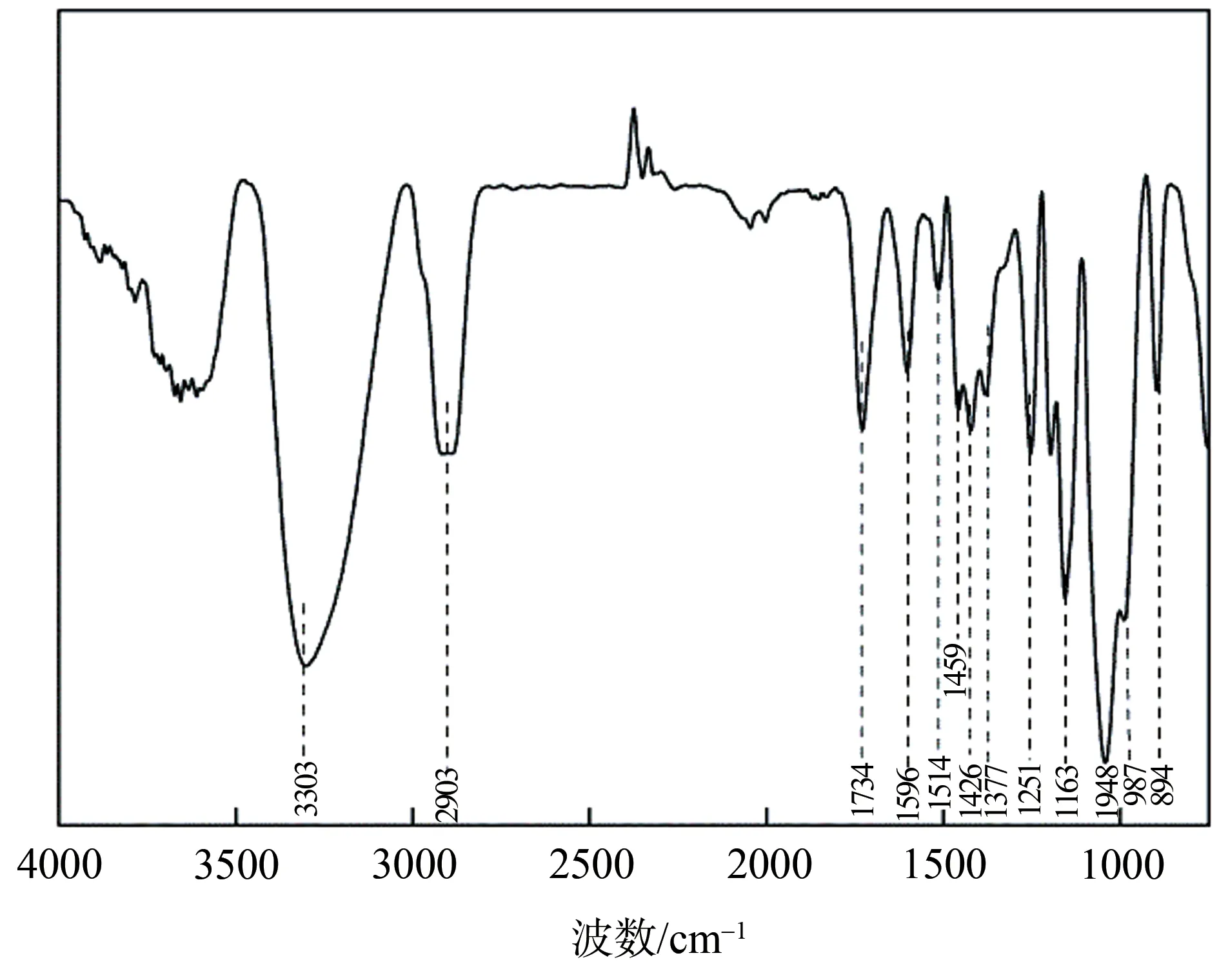
图3 半纤维素分离物的FT-IR谱图
2.4 半纤维素分离物的NMR分析
2.4.11H NMR 分析
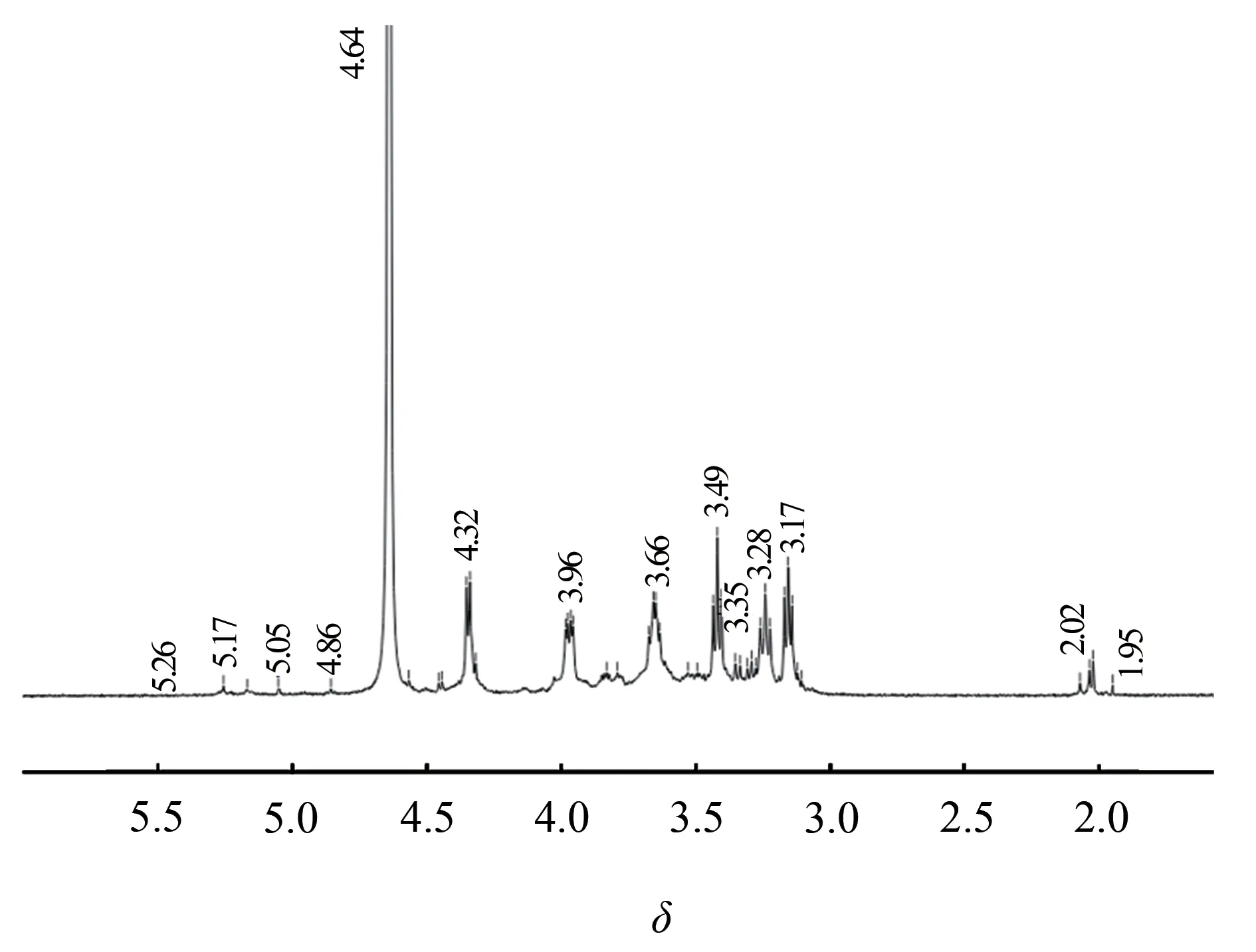
图4 半纤维素分离物的1H NMR谱图
采用NMR 进一步研究半纤维素分离物的结构,其1H NMR 谱图如图4所示。从图4可知,δ为5.26和4.64处分别归属于α-L-呋喃式阿拉伯糖基和1,4-β-D-吡喃式木糖-2-O-(4-O-甲基-α-D-吡喃式葡萄糖醛酸基),δ为 4.3~4.9 来源于β-异头氢[21],表明了木糖单元之间以β-糖苷键连接,与FT-IR 谱图中894 cm-1处所代表的结构信息吻合。δ为4.32、3.96、3.66、3.49、3.35、3.17处的峰分别归属于1,4-β-D-吡喃式木糖结构单元上的H-1、H-5e、H-4、H-3、H-5a、H-2[22],说明了半纤维素的主链为吡喃木糖,而侧链为α-L-呋喃式阿拉伯糖基、4-O-甲基-α-D-吡喃式葡萄糖醛酸基和乙酰基。
2.4.213C NMR 分析
半纤维素分离物的13C NMR 谱图如图5 所示。从图5 可知,δ为 101.6、76.3、73.4、72.1、62.8 处分别为1,4-β-D-吡喃式木糖结构单元上的C-1、C-4、C-3、C-2、C-5[23-24]。4-O-甲基-α-D-吡喃式葡萄糖醛酸基、α-L-呋喃式阿拉伯糖基和乙酰基等侧链基上的C信号比较弱,其原因可能是,在麦草半纤维素聚阿拉伯糖-4-O-甲基葡萄糖醛酸木糖中,每26 个D-木糖基分别含有1 个4-O-甲基葡萄糖醛酸基支链,2 个L-阿拉伯糖基支链,以及1 个木糖基支链[25],说明水热法提取半纤维素仍然可以保留其中的4-O-甲基葡萄糖醛酸和乙酰基,综合FT-IR 和NMR 的结果可知,水热法提取的麦草半纤维素分离物的结构主要为:D-吡喃式木糖以1,4-β-糖苷键连接形成主链,4-O-甲基-α-D-吡喃式葡萄糖醛酸基、阿拉伯糖基以及乙酰基形成侧链。
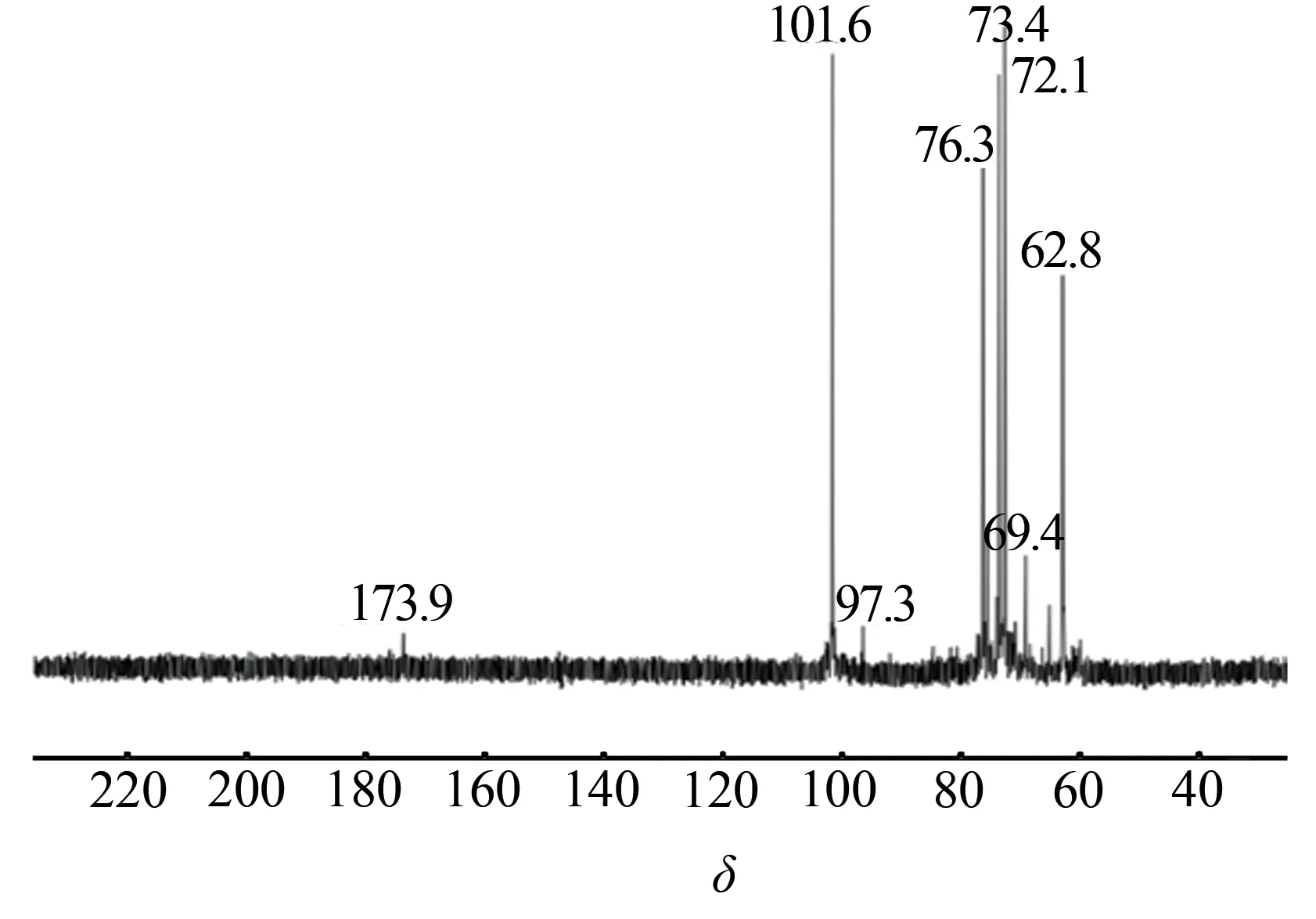
图5 半纤维素分离物的13C NMR谱图
2.5 木质素分离物的FT-IR分析
木质素分离物的FT-IR 谱图如图6 所示。从图6可以看出,在3359 cm-1处有1 个宽的吸收峰频带为O—H 伸缩振动,2922 cm-1和2880 cm-1分别是甲基和亚甲基中C—H 键的对称伸缩振动和不对称伸缩振动,1596、1503 和1426 cm-1处的吸收峰归属于木质素的苯环,1325 cm-1处S 型木质素结构单元和缩合的G 型木质素结构单元、1262 cm-1处G 型木质素结构单元的C=O 伸缩振动和1215 cm-1处G 型木质素结构单元的C—C和C—O伸缩振动分别代表了不同类型木质素的结构单元,1124 cm-1处的峰代表了S 型木质素上C—H 键的变形振动,1032 cm-1处的峰代表了G 型木质素上C—H 键的变形振动,915 cm-1为G 型木质素芳香环的C—H 面外弯曲振动,839 cm-1处为S—H 型木质素芳香环的C—H面外弯曲振动[26-29];1124 cm-1(S型木质素)处吸收峰的强度高于1032 cm-1(G 型木质素)处吸收峰,说明水热-二元催化乙醇法提取的木质素中S型木质素含量多于G型木质素。
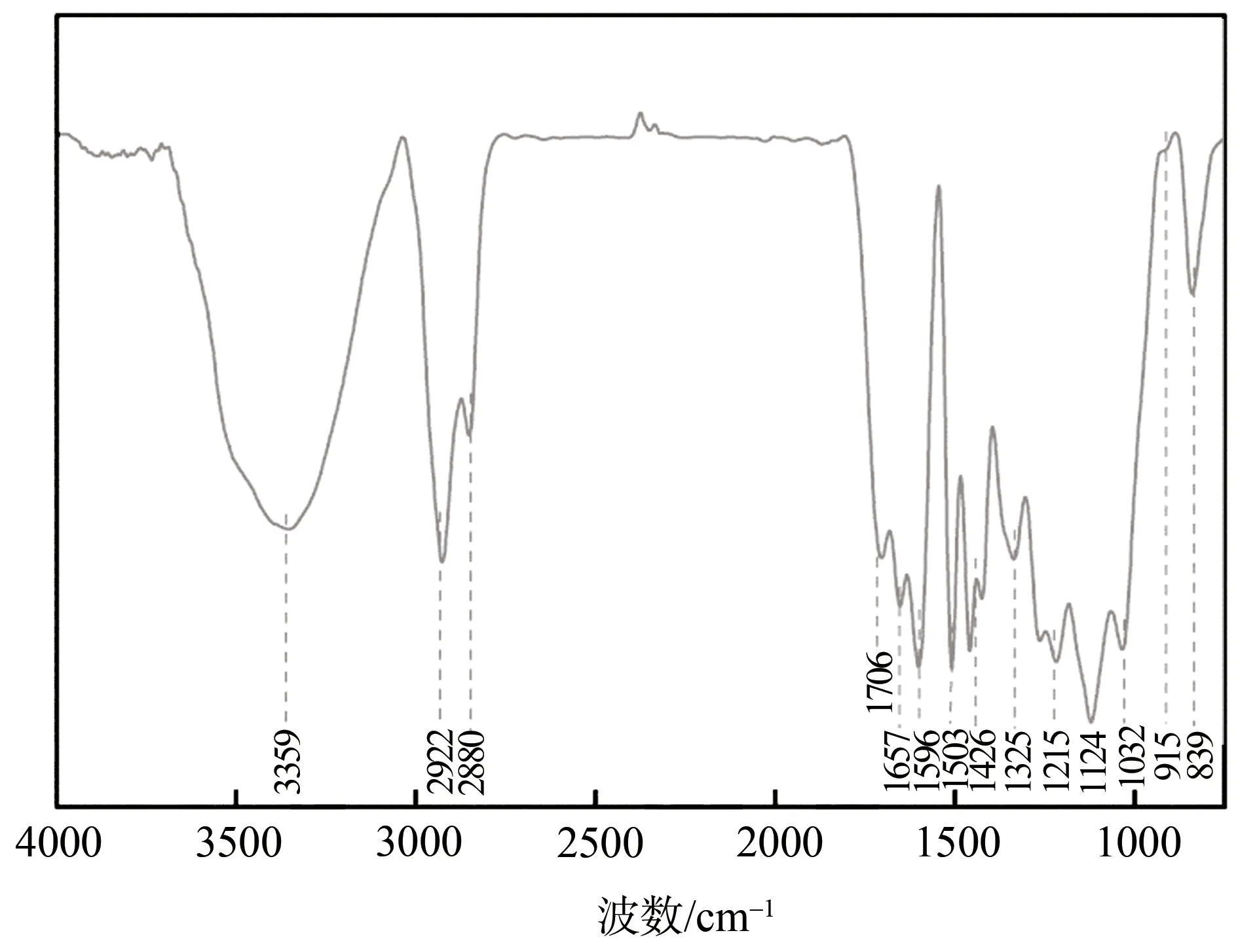
图6 木质素分离物的FT-IR谱图
2.6 木质素分离物的1H NMR 分析
木质素分离物的1H NMR谱图如图7 所示。从图7可知,δ为 6.7、7.4 和 7.8 处分别为 S 型木素、G 型木素和H 型木素结构单元上的质子,同样,代表S 型木质素的信号更强,与FT-IR 的分析结果吻合;另外,δ为5.4 处归属于β-5结构中的Hα,δ为4.9处归属于β-O-4 结构中的 Hα,δ为 4.1 处属于β-O-4 结构中的Hγ,δ为 3.7处归属于甲氧基中的质子,δ为 2.5 和δ为2.7分别归属于β-5和β-β结构中的Hβ,δ为0.8和δ为1.2归属于高遮蔽效应的脂肪族质子[30],表明水热-二元催化乙醇法提取的木质素结构较为完整。
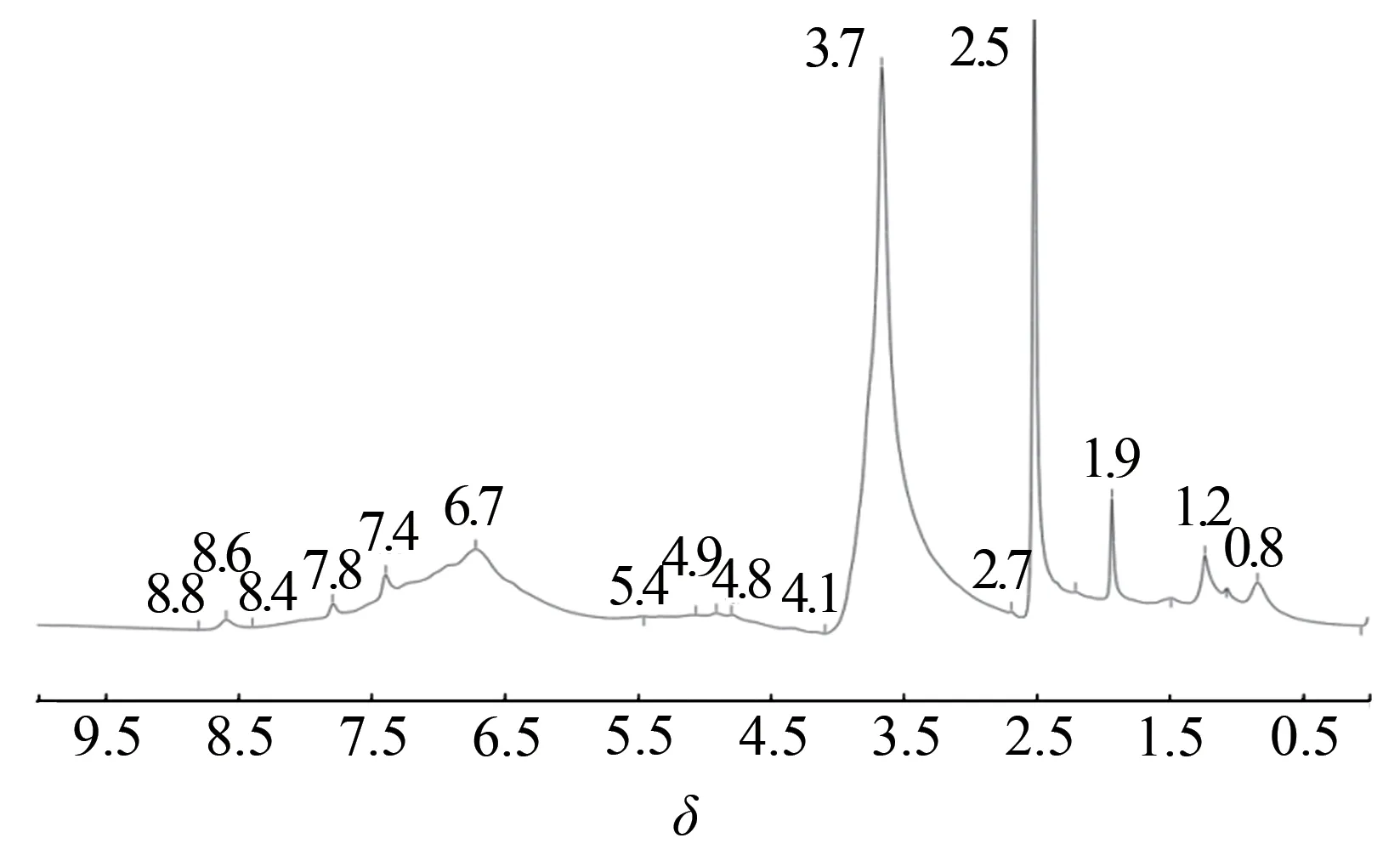
图7 木质素分离物的1H NMR谱图
3 结 论
本课题研究了水热-二元催化乙醇法对麦草纤维素、半纤维素和木质素组分的分离效果,并对半纤维素分离物和木质素分离物的化学结构进行了表征。
3.1 水热-二元催化乙醇法可以实现麦草组分的高效分离,对半纤维素的脱除率为91.5%,醇沉法半纤维素提取率为38.1%;稀释沉淀法木质素提取率为55.5%,木质素的脱除率为85.6%,相比水热-乙醇法,木质素脱除率提高了52.6%,粗纤维素的得率为40.7%;另外,半纤维素主要由第一步水热法脱除,且水热法处理后半纤维素的4种存在形式分别为:醇沉法得到半纤维素聚糖38.1%,水解液中未沉淀出来的低聚木糖以及单糖的含量28.0%,残留在固相产物的半纤维素18.2%;转化为其他组分损失的半纤维素15.7%。
3.2 采用水热-二元催化乙醇法高效分离得到的半纤维素聚糖的主链由D-吡喃式木糖以(1,4)-β-糖苷键连接形成,支链为4-O-甲基-α-D-吡喃式葡萄糖醛酸基、α-L-呋喃式阿拉伯糖基和乙酰基。木质素分离物结构较完整,且木质素分离物中S 型木质素含量多于G 型木质素。
