阴极铜生产中电解液As、Te、Bi杂质脱除的作用
2020-11-04宋元湖
宋元湖
(江西铜业贵溪冶炼厂,江西 鹰潭 335424)
在铜的冶炼和精炼过程中,很难电解液中存在的杂质全部去除[1]。因此,阴极铜需要进行电精炼以满足在大多数应用领域中的纯度要求。电解期间精炼铜,其中包含的一些阳极杂质很难溶解到电解质中并积累金属离子,这些杂质通常包括:As、Te、Bi。由于As、Te、Bi的标准还原电位非常接近铜,因此这些杂质易于在阴极。本文通过提纯电解液的实验使其浓度始终低于规定值,致力于阴极铜质量达到理想水平。到目前为止,大多数的铜精炼厂仍然每天使用电解沉积法处理电解质,但这种常规方法有很多缺点,例如:废弃材料难以处理,能源消耗量大,容易形成有毒气体[2]。在阴极铜电解精炼过程中,一部分杂质As、Te、Bi从阴极溶解会自发沉淀,从电解液到阴极粘液或残留物铜。在未完全了解杂质脱除原理之前,人们普遍认为砷酸盐形成了砷(V),Sb(III)和Bi(III)离子产生可用于去除这些杂质。虽然砷酸盐的形成很好地解释杂质从电解液中去除砷,在一个偶然的实验中发现As,Te、Bi之间发生沉淀反应即使在铜电解液中不存在Sb(III)离子也是如此。显然,这种现象不能充分解决由砷酸盐或砷酸盐锑酸盐解释。为此,本文提出阴极铜生产中电解液As、Te、Bi杂质脱除的作用研究。
1 实验
首先做好As(III)、Te(V)和B(iIII)的储备工作,选取As2O3的样品在加热过程中快速搅拌的条件下溶于水,得到As(III)储备溶液。在Bi2O3的样品中加入浓硫酸,加热并搅拌制备B(iIII)储备溶液,As(V)库存通过将过氧化氢添加到搅拌下的As(III)储备溶液中。而后将Te2O3样品溶解在浓缩液中,用水稀释,然后氧化用过氧化氢获得Te(V)原料解,加入少量盐酸促进Te2O3溶解。过量的H2O2通过将溶液煮沸约30分钟自行分解。本次实验中元素的总含量由原子吸收光谱法测定,实验中使用的电解液包含以下基本成分包括:44−46 g/LCu2+,180−185g/LH2S O4,以及As,Te和Bi杂质[3]。在合成电解质中As和Bi的含量、初始浓度为列于表1中。
结合表1信息,通过将电解液加热到65°C以300 r / min搅拌4 h,以纯化的电解质作为过滤收集沉淀物的结构表征,以杂质去除量为根据,确定沉淀物的组成[4]。可以通过化学方法以及能量色散光谱法,利用透射电子显微镜以及扫描电镜微观的观察FTIR光谱。
2 结果和讨论
2.1 As、Te、Bi杂质脱除的作用
以电解质As、Te、Bi杂质脱除的纯化实验为根据,进行As、Te、Bi的去除量计算。得出As、Te、Bi杂质脱除的具体作用,如图1所示。

图1 As、Te、Bi杂质脱除的具体作用
通过图1可知,As、Te、Bi沉淀反应仅在初始Te(V)离子浓度时发生,可达到0.8 g / L。砷,锑和铋的去除量随着初始Te(V)浓度的增加而增加,并且随着Te(V)的进一步增加保持几乎恒定,离子浓度超过1.2g/L-1后。去除As和Bi的比率分别达到76.83%和79.2%,在Te(V)离子浓度为1.2g/L时。净化时间延长以获得更高的杂质去除率。发现As的去除率,Te和Bi分别达到15.26%,88.61%和91.01%,相同条件下搅拌16小时后。根据这个结果表明,延长净化时间可以提高净化效率。显然,Te(V)离子对杂质脱除具有明显的影响。在来自电解液的As、Te和Bi杂质脱除中相似的结果是,从Te(III)到铜电解液中的Te(V)可以提高百分比。铜中溶解的杂质As,Te和Bi起初为阴极,然后通过杂质沉积到阴极粘液增加。沉淀结构表征为:进行鉴定As、Te的去除机理具有一致性,而Bi(V)离子在去除过程中会产生Bi杂质。与此同时,为了比较和澄清As、Te、Bi杂质结构,可以从Larox过滤器中获得的工业过滤器残渣。
2.2 As、Te、Bi杂质沉淀物结构表征
根据杂质沉淀物的SEM图像以及EDS模式,确定含有10 g·L-1As的合成电解液中形成沉淀物结构表征。沉淀物由块状颗粒组成,块状颗粒的尺寸分布不同,范围从几十微米到几分微米不等,其长度达到100 nm,这些颗粒会聚在一起形成大块的不规则块。1.2 g·L-1Sb(V)以及0.5 g·L-1Bi的沉淀物呈许多不规则块状,尺寸为1000-200μm,主要由As、Te、Bi组成。沉淀物可以迅速沉积在电解液底部,由于容器的底部尺寸较大,必须加速从中去除沉淀物。将含有确切成分的沉淀物与工业过滤器残留物的分离,得到合成沉淀物和工业成分滤渣。合成沉淀物和工业成分滤渣具体信息,如表2所示。
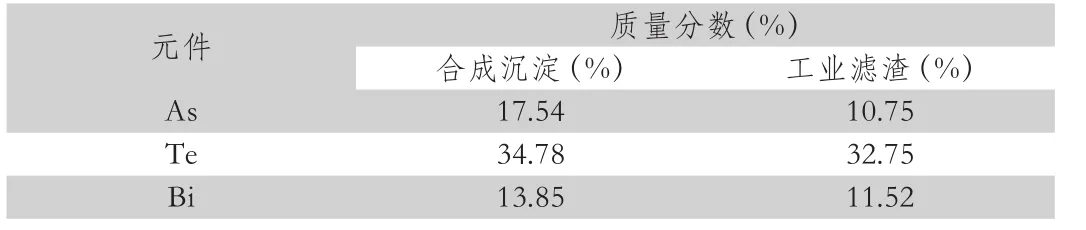
表2 合成沉淀物和工业成分滤渣
从表2中可以看出,在合成沉淀物中As,Te和Bi的含量为66.94%,表明As,Te和Bi是关键元素。因此,可得摩尔比为:n(As):n(Sb):n(Bi),换算后大约为3.5:4.0:1合成沉淀。As和Bi的含量在工业过滤器的残留物接近于那些合成沉淀,而Te的含量却很高。沉淀物和工业过滤器残留物内容之间的差异可能是由于所含初始As(10 g / L)的浓度在合成电解质中较高。此外,存在Sb(III),Pb,Sn,Zn以及Fe元素,虽然不是存在于合成电解质中,也可能导致工业过滤器残留。在此基础上,绘制电子衍射图,再进行TEM观察从而得到有关沉淀物结构的更多信息,如表3所示。
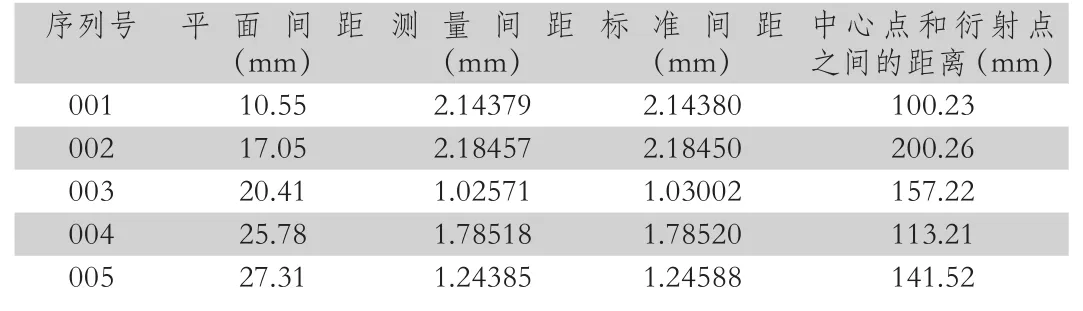
表3 As、Te、Bi杂质沉淀物晶体与AsTeO4相比间距
通过表3可知,As、Te、Bi杂质沉淀物的测量间距分别接近于标准间距。因此,可以推断结晶中还包括BiTeO4。As、Te、Bi杂质沉淀物晶体与BiTeO4相比间距,如表4所示。
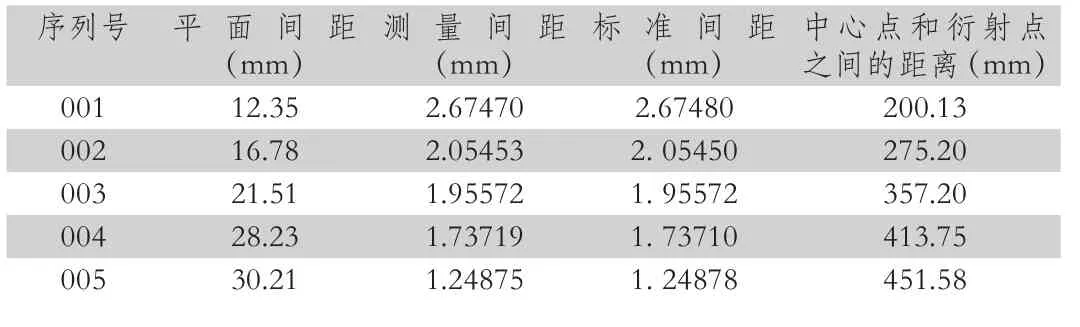
表4 As、Te、Bi杂质沉淀物晶体与相比间距
通过表4可知,与 相比间距的TEM结果也进一步证实了合成沉淀物中含有AsTeO4,与XRD结果一致。
2.3 机理分析
通过结构分析表明沉淀为BiTeO4以及AsTeO4,发现存在As(III),Te(V)和B(iIII)以AsO +的形式存在。因此,在以下过程中可能发生以下反应,电解液净化:
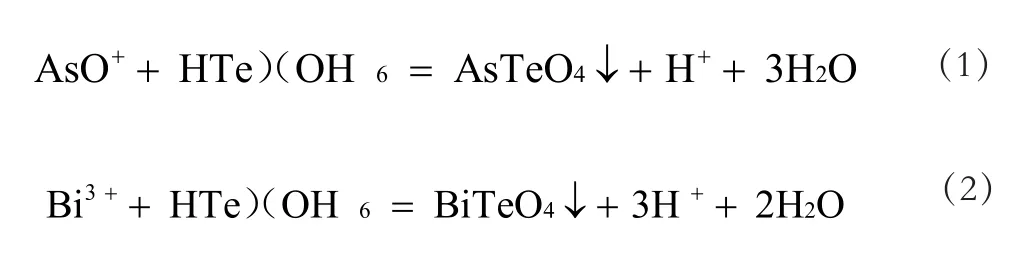
根据化学表达式(1)、(2)所示,沉淀物中的混合物形成并沉积在去除As、Te和Bi杂质的铜电解液中。
根据以上结果,Te(V)可以结合与As(III)或B(iIII)离子形成AsTeO4和BiTeO4。锑酸盐的形成导致砷,锑和铋杂质的浓度下降在电解质中。因此,主要的贡献Te(V)离子可去除As,Te和Bi杂质,归因于铜中锑的形成电解质。当Te(V)离子浓度太低(0.4g/L-1)时, Te和Bi元素以自由离子的形式存在,离子溶解度常数Ksp小于AsTeO4和BiTeO4。因此,没有电解液中的沉淀As、Te和Bi不能从电解质中去除。随着Te(V)离子浓度增加,形成基于等式的锑(4)-(6)被加速并且沉积的杂质As、Te和Bi的百分比进入沉淀物增加,导致增加杂质去除量。当Te(V)浓度超过1.2 g / L,锑酸盐的形成是饱和的,因此去除了As、Te和Bi保持几乎恒定。为了证明Te(V)离子在杂质脱除中的作用,纯化实验为通过添加1.2 g / L Te(V)离子进行铜电解液。在纯化实验之前,在电解液中添加适量的还原剂将As(V)离子调整为As(III)离子。搅拌后4 h发现As、Te和Bi的浓度从12.584、0.934和0.608 g / L降至10.637,分别为0.344和0.252 g / L。结果进一步确认通过Te(V)离子可以去除As,Te和Bi杂质。
结语
通过研究表明As、Te和Bi杂质可通过以下方法去除:Te(V)离子和As以及Bi的去除率达到76.83%,并且分别在合成电解质中包含10 g / L-1的As,1.2 g/L-1的Te(V)和0.5g/L-1的Bi(III),在65℃下搅拌4小时。沉淀物主要由As、Te,Bi组成,在合成铜中形成电解质,呈大小不规则的块状50-200μm的块状颗粒。主要特征带沉淀物的FTIR光谱为:As-O-As;As-O
- Te;Te -O-Bi;Te -O- Te和Bi-O-Bi。沉淀物由微晶组成包括:以及。Te(V)的主要作用离子在去除As,Te和Bi杂质时,可以归因于阴极铜中的锑酸盐形成的电解质,从而提高阴极铜精炼质量。
