实验室间乳酸脱氢酶项目的一致性分析*
2020-11-03孙丽丽赵鸿梅
高 昕,孙丽丽,曲 波,赵鸿梅
(中国医科大学人民医院暨辽宁省人民医院检验科,辽宁沈阳 110016)
2018年1月,原国家卫生和计划生育委员会和国家中医药管理局共同发布了《关于印发进一步改善医疗服务行动计划(2018-2020年)的通知:国卫医发〔2017〕73号》,要求医疗机构建立检验结果互认制度,各地实现医学检验等专业医疗质量控制全覆盖,医疗机构通过省级、市级等相关专业医疗质量控制合格的,在相应级别行政区域内检验结果实行互认[1]。为此,本课题组参考美国临床医院标准化委员会(NCCLS)的EP9-A2文件的要求[2],对辽宁省内6家通过ISO15189认可的三级甲等医院乳酸脱氢酶(LDH)项目进行方法学比对和一致性评价,为实现不同实验室间检验结果的互认提供依据。
1 资料与方法
1.1一般资料 按照EP9-A2文件的要求[2],收集20例新鲜血清标本,分别编号1~20。以1 200×g 离心10 min,保证无乳糜、黄疸和溶血标本,浓度覆盖检测范围,并满足各实验室的可报告范围。每例标本分装成6份,每份至少300 μL,分装后放置-20 ℃的冰箱中密封、冷冻保存。
室内质控数据来源于上海昆涞生物技术有限公司提供的两个浓度水平的质控品(Lot:376B8C9/376DFDA)。
每日常规标本检测之前进行质控品的检测,质控在控后方可进行常规标本检测。检测日统一发放比对标本,用保温箱冷藏运输,各实验室得到标本后充分平衡至室温,待标本完全融化后上下颠倒混匀10次,每份标本重复检测3次,检测顺序为1~20、20~1、1~20,尽快完成标本的检测。
1.2仪器与试剂 各实验室的仪器均按照中国合格评定国家认可委员会《内部校准要求:CNAS-CL01-G004》的相关规定进行校准[3],且最近一次外部校准的时间均在一年之内,2018年3次原国家卫生和计划生育委员会室间质评LDH项目均满分,检测方法均为速率法(L-P),报告单位均为U/L。各实验室的检测系统信息见表1。

表1 各实验室检测系统信息
1.3方法 按EP9-A2文件要求进行方法间离群值检查[1]。然后将6家实验室的检测结果(Y)分别与组内均值(X)进行线性回归分析。通过回归方程计算出相关系数r2、斜率b、截距a及线性回归方程Y=bX+a。r2≥0.95,说明分布范围合适[4-6],将医学决定水平处浓度(Xc)代入线性回归方程,计算Y与X之间的绝对偏差(AD)=Y-Xc,相对偏差(RD)=(AD/X)×100%。以文献[7-8]确定允许总误差(TEA)。依据CNAS-CL38确定比对试验的可接受标准为小于1/2TEA[9]。

2 结 果
2.1线性回归分析结果 结果显示,各实验室的r2均为0.999 3~0.999 8,说明各实验室的相关性良好,见表2。
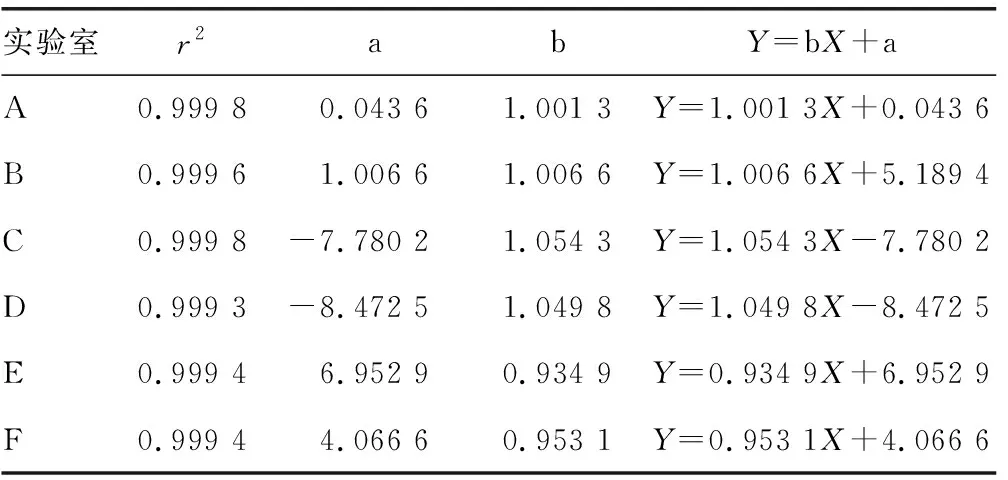
表2 各实验室的r2和线性回归方程
2.2各实验室检测系统间的一致性评价 将LDH的两个医学决定水平1(浓度值300 U/L)和医学决定水平2(浓度值500 U/L)分别代入线性回归方程,以RD小于1/2TEA(5.5)作为判断标准,各实验室的RD均为0.14%~5.12%,比对通过,见表3。

表3 各实验室检测系统间一致性评价
2.3室内质控数据的SDI和CVR分析 统计各实验室的室内质控数据,CV为1.22%~4.17%,SDI绝对值为0.01~1.30,CVR为0.5~1.7,各实验室的室内质控的准确度和精密度良好,见表4,根据SDI和CVR值绘制Youden图,见图1。

表4 各实验室室内质控数据分析

图1 室内质控Youden图
3 讨 论
随着检验医学的飞速发展,临床诊疗技术的不断进步,人们越来越关注检验结果的可靠性和可比性,尤其是实现不同医院检验结果的互认是目前检验行业的热点和难点。目前,各厂家生化分析仪检测LDH主要采用速率法[10],虽然检测方法相同,但由于检测系统的差异,溯源的参考物质来源不同[11],导致检测结果存在一定的差异,需要对各实验室的检测结果进行一致性评价[12]。
本研究采用以各实验室检测结果的均值作为X,检测结果作为Y进行回归分析,r2均大于0.95,说明X的取值范围合适,回归方程的斜率和截距可靠[4-6]。CNAS-CL38指出,比对试验的可接受标准不低于国家标准、行业标准或地方法规的要求;定期比对试验中,根据回归方程计算在医学水平处的RD应小于1/2TEA[9],以SDI和CVR值评价准确度和精密度情况[13]。将不同LDH的医学决定水平代入线性回归方程,各实验室RD均在0.14%~5.12%,均满足TEA的要求,所有实验室的RD均小于1/2TEA,而A、B、D 3个实验室的RD小于1/3TEA,说明这3个实验室的检测结果具有高度一致性。各实验室的室内质控CV在1.22%~4.17%,A实验室的CV小于1/2TEA,B实验室的CV小于1/3TEA(3.67%),其他实验室的CV小于1/4TEA(2.75%);各实验室的SDI绝对值在0.01~1.30,只有D实验室的低水平SDI绝对值为1.30,其他实验室的SDI绝对值均小于1;各实验室的CVR值在0.5~1.7,A、B实验室的CVR在1~2,E实验室高水平的CVR为1.04,其他实验室的CVR均小于1。说明各实验室LDH的室内质控的离散程度、精密度和准确度均较好。通过上述比对试验和室内质控数据两种方法评价6家实验室的LDH检验结果是一致的,辽宁省内6家三级甲等医院实验室的LDH比对结果通过。
实验室分别采用4个厂家的仪器和试剂进行LDH的比对试验,其中A和B实验室采用同一厂家的仪器、原装试剂和校准品,C和D实验室采用同一厂家的仪器、原装试剂和校准品,而E和F实验室采用与其他医院均不相同的仪器、非配套试剂和校准品,其中F实验室的仪器启用时间最久约为11年,E实验室为9年,C实验室为7年,其他实验室的仪器启用时间均在5年之内。所有仪器均按照ISO15189认可的要求进行操作、校准、维护和保养,最近一次外部校准的时间均在一年之内,此6家实验室LDH项目的精密度、正确度、线性、可报告范围和生物参考区间等性能验证符合要求,且2018年3次原国家卫生和计划生育委员会室间质评LDH项目的结果均满分,检测方法和报告单位均相同,是比对试验的必要保证。但本次评估的影响因素较多,各实验室分别采用4个厂家的仪器和试剂,E和F实验室采用非配套的试剂和校准品,其仪器与其他医院均不相同且启用时间较久可能是影响标本比对偏差较大的原因;同时,存在质控品的基质效应问题[14],各实验室的质控数据点不一,质控数据个数不充分是影响室内质控数据分析的主要原因。
医学实验室通过ISO15189的认可是以国际标准规范进行实验室质量管理,旨在提高在同行业中的学术地位和水平,提高医疗市场的竞争力和美誉度,同时也是实现检验结果互认的质量保障。检验结果的互认不仅是检验科的工作,因为检验质量贯穿检验前、中、后整个检验过程,规范全面的质量管理体系是开展检验结果互认的重要基础,需要临床各个部门的医护人员的支持和配合,检验结果的互认也不是一蹴而就的,需要逐渐探索。检验结果互认对于减轻患者负担,加快流程,减少医保支出均具有重要的意义。
本研究仅仅是生化项目比对方案的初步探索,课题组将继续定期进行标本比对,以及进行长期连续的室内质控动态监测,保证充足的实验数据,提高研究的可靠性。目前,使用不同的检测系统(一个检验项目所涉及的仪器、试剂、校准品、质控品、检验程序、校准计划和保养计划的实施等组合)对同一生化指标进行检测,其灵敏度、准确性等存在差异,导致不同检测系统检测的结果可能存在差异[15-16],需要对各项目的检测结果进行一致性评估。未来,课题组将以LDH为例,逐步完成其他生化项目的比对。
综上所述,辽宁省内6家通过ISO15189认可的全国三级甲等医院,其医学实验室的LDH检测结果具有可比性,此项目可以实现6家实验室间的检验结果的互认。
(致谢:感谢中国医科大学附属第一医院、中国医科大学附属盛京医院、辽宁中医药大学附属第一医院、辽宁中医药大学附属第二医院、中国人民解放军北部战区总医院和平院区对本研究的大力支持,各单位提供仪器设备并协助完成本研究。在此,给予诚挚的谢意。)
