锂离子电池无序结构正极材料的研究进展
2020-11-03孔继周
孔继周, 陈 瑶, 徐 朋, 周 飞
(南京航空航天大学 机电学院, 江苏 南京 210001)
为了真正贯彻落实全面可持续战略,太阳能、潮汐能、风能等清洁可再生能源的商业化应用迫在眉睫,在有效利用这些新能源的过程中,能源的储存和转化是关键[1].在储存这些间歇性新能源的众多手段中,锂离子电池具备质量轻、体积小、能量密度大、循环稳定性优异、自放电小、无记忆效应和绿色无污染等优点,得到了科研工作者的广泛青睐[2-3].在锂离子电池中,正极材料的低能量密度是限制其发展的主要因素,对电池的电化学性能和安全性有着重要影响,且化学储能电站、电动汽车(EV)等对锂离子电池的能量密度要求越来越高,因此研发高能量密度的正极材料成为研究者的工作重点.
传统的锂离子电池正极材料大体可分为5类: ① 层状钴酸锂(LiCoO2),比容量较高,合成工艺简单,但钴资源短缺且价格昂贵,毒性较大且会污染环境; ② 尖晶石锰酸锂(LiMn2O4),安全性好,价格低廉,但在充放电过程中不稳定,Jahn-Teller效应以及锰的溶解会使电池容量迅速衰减; ③ 尖晶石镍酸锂(LiNiO2),原材料价格低廉,来源广泛,但制备困难,热稳定性差,存在较大的安全隐患; ④ 橄榄石磷酸铁锂(LiFePO4),放电平台平稳,环境友好且资源丰富,但其堆积密度和体积能量密度较低,大电流充放电下的性能差; ⑤ 三元材料(如NCM和NCA),能量密度高,低温性能好,但容易发生阳离子混排,影响充放电性能.
除了上述传统的5种正极材料外,L. SEBASTIAN等[4]于2003年第1次研究发现无序结构的Li2MTiO4(M 代表 Mn,Fe,Co,Ni)材料可作为锂离子电池的正极材料,该体系材料的结构稳定性好,理论容量高,但其循环稳定性差,容量衰减特别迅速.此后,无序正极材料的研究便陷入了较长的瓶颈期.J. LEE等[3]、A. URBAN等[5]在2014年制备出Li1.211Mo0.467Cr0.3O2(LMCO),发现经过几个循环后,材料的结构便从有序结构向无序结构转变,并提出0-TM和1-TM这2种Li+扩散通道,DFT计算结果显示,1-TM通道的势垒较高,而0-TM的势垒低,表明Li+在0-TM通道的扩散阻力小.尽管0-TM通道使用频率远小于1-TM通道,但只要引入足够的Li量,0-TM通道就可以在无序结构中更活跃.虽然无序正极材料在充电/放电过程中电极动力学反应速率较慢[6-7],但不可否认的是,无序结构材料的提出为锂离子正极材料的发展提供了一个新的研究方向.故笔者对Ti基和Nb基的无序正极材料的制备方法及其电化学性能进行总结和分析.
1 Li-M-Ti-O系正极材料
1.1 Li-Mn-Ti-O 氧化物
L. SEBASTIAN等[4]采用了固相烧结法,以Li2CO3,MnC2O4·2H2O和TiO2为原材料在900 ℃保温3 d制备得到了Li2MnTiO4,同时为防止Mn2+被氧化成Mn3+,整个烧结过程在Ar气氛中进行.基于上述研究,ZHANG X. Y.等[8]采用溶胶-凝胶法制备了不同锂量的Li2+xMn1-x/2TiO4无序正极材料(x分别为0,0.2,0.4).研究发现:在30 mA·g-1的电流密度下,Li2MnTiO4极化现象严重,放电容量仅为112.2 mA·h·g-1,而Li2.4Mn0.8TiO4容量高达187.5 mA·h·g-1;且随着电流密度增至60 mA·g-1,容量差距更加明显,这说明过量的Li可在无序的锂-过渡金属氧化物正极材料中打开渗透网络,提高Li+的扩散率.但试验数据表明,Li2+xMn1-x/2TiO4(x分别为0,0.2,0.4)材料的容量衰减较为迅速,20 个循环后的容量保持率分别为66.6%,65.9%和59.9%,之所以发生这种显著的容量衰减,极有可能是因为Li+在脱嵌过程中,材料的结构发生了不可逆的变化.
A. KITAJOU等[9]在Li2+xMn1-x/2TiO4材料的基础上改变了Li-Mn-Ti-O氧化物的组分,采用固相烧结法在Ar气环境下,以Li2CO3,MnO和TiO2为原材料制备得到Li2+2xMn1-xTi1-xO4(0≤x≤0.3).研究发现:在0≤x≤0.2范围下,随着Li含量的增加,Li2+2xMn1-xTi1-xO4的比容量也在增加(见表1[9]),但Li含量过多(x=0.3)时,材料容量反而呈现下降趋势.在7.5 mA·g-1的电流密度下,Li2.4Mn0.8Ti0.8-O4放电容量超过220 mA·h·g-1,在15个循环后其容量保持率同样令人满意.这是由于过量的锂激发了无序岩盐材料中的1-TM Li+扩散通道的活性,提高了Li+的迁移率,从而提升了材料的容量,这个结果与J. LEE等[3]预测的一致.
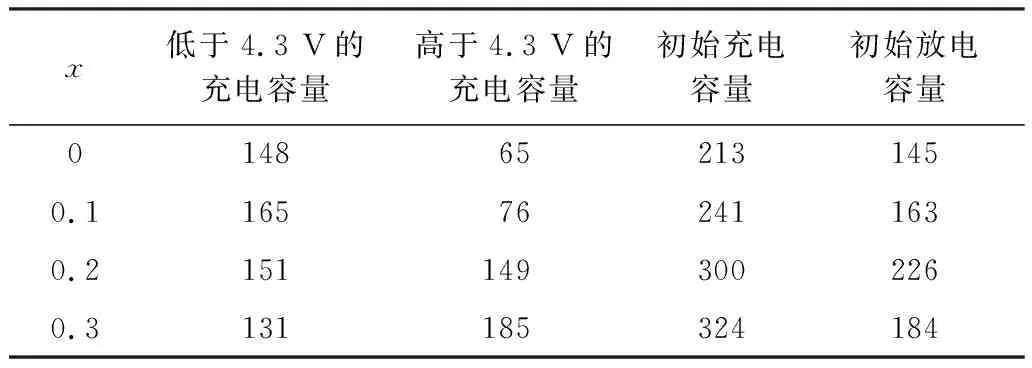
表1 Li2+2xMn1-xTi1-xO4首次充放电容量 mA·h·g-1
1.2 Li-Ni-Ti-O氧化物
与Li2MnTiO4相比,Li2NiTiO4可以在相对较低的温度下合成[4].S. R. S. PRABAHARAN等[10]用羧酸-硝酸盐在低于300 ℃的温度下制备得到了纳米颗粒的Li2NiTiO4.在145 mA·g-1的电流密度下,材料的首次充电容量高达180 mA·h·g-1,但放电容量却只有96 mA·h·g-1.研究指出,Li2NiTiO4材料的首次充放电容量损失过大有可能归因于以下几点: ① 无序岩盐相结构的正极材料中的阳离子分布不均匀; ② 高氧化电位下非水电解质的部分分解; ③ 充电过程中氧气的损失.
由于Li2NiTiO4的循环稳定性差,可以通过掺杂金属或非金属离子来提高电子和离子的电导率,稳定材料的晶体结构,从而提高材料的电化学性能.Y. KAWANO等[11]以TEOS为Si源制备了Si掺杂的Li2NiSi0.1Ti0.9O4,研究发现:在Li2NiSi0.1Ti0.9O4的横截面中Si颗粒分散均匀,且少量的Si掺杂可以有效地降低材料的结晶度.在0.32 mA·g-1的电流密度下,Li2NiTiO4和Li2NiSi0.1Ti0.9O4的放电容量分别为153.4,145.5 mA·h·g-1,但经20个循环后,Li2NiSi0.1Ti0.9O4的放电容量可以保持在75.6 mA·h·g-1,但Li2NiTiO4却衰减至57.1 mA·h·g-1,证明Si掺杂可以提高Li2NiTiO4的循环性能.
WANG Y. M.等[12]采用熔盐法,通过添加助溶剂NaCl-KCl降低烧结温度,制备得到了平均粒径约为10 μm的Li2NiTiO4材料,并用乙炔黑包覆Li2NiTiO4材料来改善材料的导电性.研究发现在14.5 mA·g-1电流密度下,Li2NiTiO4/C纳米复合材料初始充电容量高达203 mA·h·g-1,经50次循环后,在室温和50 ℃下的容量保持率分别为86%和83%.Li2NiTiO4/C在循环期间具有较好的电化学可逆性和结构稳定性,这是因为小粒径的材料颗粒可以减少Li+扩散长度从而改善离子电导率,且包覆在Li2NiTiO4材料表面的碳可以提升正极材料的电导率,并可以促进电极反应.
1.3 Li-Fe-Ti-O氧化物
M. KÜZMA等[13-14]基于柠檬酸盐前体的方法制备得到Li2FeTiO4/C,研究表明相比包覆一层导电碳涂层,材料颗粒粒径(10~20 nm)的减小对Li2FeTiO4提高容量更为重要,且Li2FeTiO4/C的循环性能在60 ℃下比在室温下更优秀.X射线衍射(X-ray diffraction,XRD)分析结果表明:在Li2FeTiO4岩盐结构中,Li+的交换遵循固溶机制,且这种结构变化并不完全可逆,在完全氧化期间晶胞体积的收缩仅为1.4%,确保了材料良好的结构稳定性.
YANG M.等[15]通过溶胶-凝胶法制备得到粒径为20~50 nm的Li2FeTiO4/石墨烯,发现石墨烯作为导电基质可以限制纳米颗粒的聚集.在10 mA·g-1的电流密度下,Li2FeTiO4/石墨烯复合正极材料的首次放电容量高达218.8 mA·h·g-1,50次循环后的容量保持率仅为81%(176.9 mA·h·g-1).首次放电过程中的容量损失可能是由于Li2FeTiO4的结构发生了变化,而初始几个循环中的容量衰减和库仑效率低可能是因为结构变化的不可逆性以及Li2FeTiO4/石墨烯电极表面形成了固体电解质界面(SEI)膜.
1.4 其他氧化物
YANG M.等[16]用溶胶-凝胶法制备Li2CoTiO4材料,并对其进行了碳包覆改性.Li2CoTiO4第1次可逆放电容量为102.3 mA·h·g-1,极化情况严重,传输反应电阻较高,但Li2CoTiO4/C的首次放电容量为144.3 mA·h·g-1,明显优于Li2CoTiO4.同时,岩盐型结构的Li2CoTiO4和Li2CoTiO4/C在几个初始循环后也表现出优异的循环稳定性,循环70次后的容量保持率分别为85.3%和75.1%,但在电流密度为160 mA·g-1时,Li2CoTiO4/C可以正常充放电,而Li2CoTiO4的容量几乎为0.
R. DOMINKO等[17]采用溶胶-凝胶法制备了Li2-xVTiO4/C.柠檬酸的降解使残余碳的多孔复合物包覆Li2-xVTiO4,提高了电子电导率.研究发现:相比于2.0~4.2 V和2.0~4.4 V,Li2-xVTiO4/C在1.0~4.4 V的电压窗口的放电容量最高,为300 mA·h·g-1,经20次循环后,容量保持率为86%,库伦效率在95%以上.但在这样较宽的电压窗口下测试,充放电曲线之间的极化情况非常严重.
S. L. GLAZIER等[18]利用Li2CO3,Fe2O3和TiO2通过固相烧结法制备了Li(1+x)Ti2xFe(1-3x)O2(0≤x≤0.33)材料.研究发现:烧结温度和Li含量对材料的电化学性能影响并不符合线性关系,当烧结温度为700 ℃,x=0.18时,材料的最大放电容量为190 mA·h·g-1;当烧结温度为800 ℃,x=0.21时,材料的最大放电容量为235 mA·h·g-1;当烧结温度为800 ℃,x=0.19,0.21,0.28时,Li(1+x)Ti2xFe(1-3x)O2材料在充放电过程中,Fe3+/Fe4+的氧化还原反应受到抑制,但其实际容量却比预期分别高了37%,48%,27%,容量的增加是由于O2-/O-参与了电荷补偿过程,且0-TM通道提供了更多位点,令Li+脱嵌可逆度更高.
CHEN R. Y.等[19]通过溶胶-凝胶法在Ar气氛围下烧结制备了一系列的Li2FeVyTi1-yO4(y=0,0.2,0.5),XRD分析表明该系列材料均为阳离子无序立方岩盐结构.研究发现:在7 mA·g-1的电流密度下,Li2FeVyTi1-yO4的可逆比容量高达250 mA·h·g-1,循环性能优异.CHEN R. Y.等[19]用57Fe穆斯堡尔光谱去探测八面体FeO6位点中Fe离子的价态分布,证明Li2FeV0.5Ti0.5O4材料充电时的比容量主要来源于Fe2+/Fe3+和V3+/V4+以及在电压为1.5~1.8 V时次要的Ti4+/Ti3+氧化,而放电过程的容量则源于V4+/V3+和Fe3+/Fe2+的还原,且V的引入明显抑制了放电过程中电压滞后的现象.
2 Li-Nb-M-O系正极材料
N. YABUUCHI等[20]等将Li3NbO4基氧化物作为高密度能量的正极材料应用于锂离子电池中.对于该xLi3NbO4-(1-x)LiMO2体系,大多数采用高温固相合成法.先选定组元并确定x的值,然后将多种组元以上的粉末在低熔组元的熔点以下温度进行高温烧结.尽管其晶体结构被归类为阳离子无序的岩盐型结构,但在渗透网络中,锂离子可以快速地进行脱/嵌,且不牺牲动力学性能.
2.1 Li-Nb-Mn-O氧化物
WANG R.等[21]采用固相烧结法制备,通过将一定比例的Li2CO3,Mn2O3和Nb2O5混合球磨后压片,再置于Ar气氛围下以1 000 ℃温度烧结12 h制备出粒径小于100 nm的Li1.25Nb0.25Mn0.5O2无序正极材料.研究发现:在10 mA·g-1的电流密度下,Li1.25Nb0.25Mn0.5O2在55 ℃和室温下首次充电比容量均高于300 mA·h·g-1,放电比容量分别为287,197 mA·h·g-1,这种差异可能是较高温度有助于提高Li+在该材料中的扩散率导致.在充放电过程中,Mn和O共同参与了电荷的可逆转移过程.
KAN W. H.等[22]采用熔盐法制备了单晶正极材料Li1.3Nb0.3Mn0.4O2并对工艺参数进行了详细的探究,发现当助熔剂和TM前驱体之间的摩尔比为2.5~5.0时,将Li2CO3,Mn2O3,Nb2O5和助熔剂KCl球磨后烧结可以得到形貌均匀、颗粒度良好的单晶Li1.3Nb0.3Mn0.4O2正极材料,且在950 ℃时反应12 h制备出的材料循环性能和倍率性能最佳.在电流密度为25 mA·g-1时,Li1.3Nb0.3Mn0.4O2首次充放电容量分别为330,290 mA·h·g-1,库伦效率为88%.但随着循环次数的增加,放电比容量也在减小,经27次循环后放电容量降至160 mA·h·g-1,容量损失接近45%.
2.2 Li-Nb-V-O氧化物
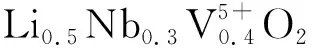
M. NAKAJIMA等[25]采用固相烧结法制备出Li1.25Nb0.25V0.5O2,并将Li1.25Nb0.25V0.5O2材料与乙炔黑混合球磨以此减小颗粒的尺寸并提高导电性能.在10 mA·g-1电流密度下,Li1.25Nb0.25V0.5O2材料具有250 mA·h·g-1的可逆容量,同时,研究发现热处理可以极大地增加样品的电极性能,热处理前的样品在2 000 mA·g-1下仅可提供20 mA·h·g-1的放电容量,而热处理后的HT-800材料(在Ar氛围下800 ℃烧结1 h)却可以提供150 mA·h·g-1.以上研究表明:热处理不仅可以改变Nb和V离子的分布使其变得更加均匀,还可以提高颗粒的电导率,降低电极的阻抗.
2.3 Li-Nb-Mo-O氧化物
S. HOSHINO等[26]采用高温固相法合成材料Li9/7Nb2/7Mo3/7O2,当烧结温度为 1 000 ℃时,产物依然为LiMoO2和Li3NbO4的混合相.经过研究发现:Li9/7Nb2/7Mo3/7O2为亚稳定相,通过高温固相法无法制备纯相的亚稳定材料.高能球磨法利用磨球的转动或振动,对原材料进行强烈的撞击、研磨和搅拌,从而改变材料的组织和性能,达到细化晶粒、提高材料粉末的活性,改善颗粒分布均匀性的目的,是获得亚稳相材料的一种常见方法.因此,S. HOSHINO等[26]利用高能球磨法合成亚稳相Li9/7Nb2/7Mo3/7-O2.XRD分析结果显示LiMoO2和Li3NbO4在15°~37°的对应衍射峰消失,并在38°,42°和63°出现了典型阳离子无序岩盐结构的峰,表明LiMoO2和Li3-NbO4的混合物经磨球发生反应转变为阳离子无序的岩盐结构.球磨后的Li9/7Nb2/7Mo3/7O2在10 mA·g-1电流密度下可提供150 mA·h·g-1的放电容量,而乙炔黑包覆后的Li9/7Nb2/7Mo3/7O2的可逆容量则高达280 mA·h·g-1,这表明乙炔黑可以提高Li9/7Nb2/7Mo3/7O2的电子电导率,从而提升容量.
2.4 Li-Nb-Cr-O氧化物
采用常规的高温固相烧结法未能得到亚稳相Li1.3Nb0.3Cr0.4O2,WANG W. W.等[27]将Li3NbO4和LiCrO2置于充满Ar气的罐中进行高速球磨,得到纯相的Li1.3Nb0.3Cr0.4O2.研究发现:尽管Li1.3Nb0.3-Cr0.4O2的初始充/放电容量高,达到368/362 mA·h·g-1,但其循环性能特别不理想,容量衰减迅速,因此提出了通过恒定容量模式充电去改善Li1.3-Nb0.3Cr0.4O2的循环特性,即每5个充放电循环后容量增加50 mA·h·g-1,从最初的充电容量从100 mA·h·g-1逐步增加到250 mA·h·g-1.与恒定电流充放电模式相比,恒定容量充电模式明显对Li1.3Nb0.3Cr0.4O2循环性能有显著改善,经60次循环后,正极材料的容量依旧保持约250 mA·h·g-1.
3 结 论
主要总结了2大类无序结构正极材料(Li-M-Ti-O和Li-Nb-M-O)的制备方法和电化学性能.目前这2种系列材料的合成方法大多采用固相烧结法、熔盐法、溶胶-凝胶法以及高能球磨法等,但合成正极材料的电化学性能有待提升.后期通过导电剂(如乙炔黑)的包覆、热处理或减少材料粒径等方法,提高无序正极材料的电子电导率,缩减Li+在充放电过程中的扩散长度,从而提高无序正极材料的电化学性能.Li-M-Ti-O和Li-Nb-M-O系列无序正极材料的理论容量大,相比之下,Li-Nb-M-O系列的正极材料结构稳定性较好,该无序正极材料在低电流密度下充放电容量高,其循环性能也较为优异,且在充放电过程中存在电荷补偿机制,带负电的氧化物离子以及过渡金属氧化物可以同时被氧化,这一点与传统的正极材料不同.尽管目前已经有大量有关无序正极材料的文献,但其充放电机理仍然存在争议,需要进一步的研究和商榷.
近几年,无序正极材料吸引了科研人员的关注,经过大量的研究发现,该类材料仍然存在着较多的问题.在上述文献中,发现无序正极材料在循环过程中容量保持率一般,长时间循环后容量损失严重,且无序结构的正极材料倍率性能差,大倍率充放电过程中容量低,并存在严重的极化现象.针对这一问题,离子掺杂、表面包覆以及采用电解液添加剂等常规措施可以有效改善其电化学性能,除此之外,由于传统的有序正极材料一般采用恒定电流充放电模式,但该充放电模式是否适合无序正极材料,是否可以通过改变充放电模式来提高无序正极材料的电化学性能,这一点值得我们关注和研究.尽管无序正极材料有很多缺点,但其理论容量非常大,电化学性能还有很大的提升空间,且它的提出也为锂离子电池正极材料的发展提供了一个崭新的方向.为了将无序正极材料投入锂离子市场并实现成熟的商业化生产,必须解决其循环稳定性差的问题,并优化其工艺,降低生产成本,这一过程需要广大科研工作者共同努力.
