电针对功能性消化不良肝郁脾虚模型大鼠十二指肠TLR4、NF-κB p65的影响❋
2020-10-31张红星荣培晶侯理伟李少源王俊英张金铃张紫璇王艺霏何家恺
王 丹,张红星△,荣培晶,侯理伟,李少源,王 瑜,王俊英,张金铃,赵 斌,国 笑,张 悦,张紫璇,王艺霏,何家恺
(1. 湖北中医药大学,武汉 430061; 2. 中国中医科学院,北京 100700)
功能性消化不良(functional dyspepsia,FD)属于功能性胃肠病范畴,主要表现为上腹痛或灼烧,餐后早饱、腹胀等,且并无引起这些症状的具体疾病,消化系统也无任何器质性病变[1-2]。目前,FD的发病机制尚处于探索阶段,主要认为可能与脑肠轴、脑肠肽、HP(Helicobacter Pylori,幽门螺杆菌)感染、胃肠动力障碍、内脏高敏感性、肠道菌群失调、心理及精神因素、轻度炎症等相关[3]。有研究发现[4],十二指肠的轻度炎症能引起局部感觉、运动障碍,从而导致腹胀、腹痛。Toll样受体(TLRs)和NF-κB (Nuclear factor κB,核转录因子κB)可激发细胞信号,启动炎症反应[5-6]。在哺乳动物细胞膜上发现了10余种TLRs模式识别受体,其中TLR4在炎症组织中表达最多,如溃疡性结肠炎。动物实验研究发现[7],当抑制NF-κB p65表达时,可显著降低炎症因子水平,因此NF-κB p65在炎症反应中发挥重要作用。本实验检测十二指肠TLR4(Toll-like receptors 4,Toll样受体4)、NF-κB p65表达情况及血清IL-6(Interleukin 6,白介素-6)、TNF-α(Tumor Necrosis Factor α,肿瘤坏死因子α)水平,探究电针治疗FD的新靶点及FD的发病机制。
1 材料与方法
1.1 实验动物
选用SPF级雄性SD大鼠30只,体质量(200±20)g,购自三峡大学实验动物中心,许可证号SCXK(鄂)2017-0012。经湖北中医药大学实验动物福利委员会许可饲养于SPF动物房,室温22 ℃~25 ℃,相对湿度50%~70%,每笼5只,适应性喂养1周后开始试验。喂养期间自由饮水、摄食。本实验已通过湖北中医药大学实验动物伦理委员会审查。
1.2 主要试剂与仪器
TLR4抗体(Santa Cruz公司,批号Sc-293072),NF-κB p65抗体(武汉三鹰,批号10745-1-ap)。甘油醛-3-磷酸脱氢酶(GAPDH);兔多抗(杭州贤至,批号AB-P-R 001);HRP标记羊抗小鼠二抗(武汉博士德,BA1051);HRP标记羊抗兔二抗(武汉博士德,BA1054);水合氯醛(上海国药集团公司,批号40935760)。
华佗牌0.35×25 mm(1寸)无菌针灸针(苏州医疗用品厂有限公司);HANS-200 A型韩式穴位神经刺激仪(南京济生医疗科技有限公司); 垂直电泳槽(北京六一仪器厂,型号:DYCZ-24DN);电转仪(北京六一仪器厂,型号:DYCZ-40);离心机(湖南湘仪实验室仪器开发有限公司,型号:HI650);酶标仪(Thermo,型号:mμLISKANMK3);自制大鼠鼠衣及悬挂大鼠装置。
1.3 实验动物分组及造模
将30只SD大鼠按随机数字表法分为空白对照组、模型组、电针组各10只。模型组及电针组大鼠参考多因素干预法[8]加以适当改良制备FD肝郁脾虚模型。冰生理盐水灌胃:配制0.9% NaCl溶液,置于冰箱中冰冻至-4 ℃,每次灌胃2 mL,每日1次;夹尾法刺激:用长尾夹包裹纱布以免损伤大鼠尾部,夹在大鼠尾部后2/3处,以不破皮为度, 令其暴怒并激怒全笼大鼠,表现为大鼠均站立,双上肢打斗,每天1次(刺激间隔不少于6 h),每次30 min,隔日禁食,饮水正常。以上三法按顺序同时实施,造模20 d。每日21时称大鼠体质量并登记,记录所有大鼠每日食物等质量。
造模成功标志:大鼠体质量进行性减轻;活跃程度从时常笼中自发打斗至喜成堆蜷缩,敲打笼子仍不动弹,抓捕反应迟钝;情绪由稍有声响就易怒烦躁转变为持续噪音刺激或是喂食仍无特别反应,情绪异常低落;鼠毛从白净顺滑至凌乱、倒张、发黄,大鼠粪便从深棕色、干燥、质硬、无臭、长条圆柱状进展成棕黄色、湿润、质软、微臭、短条圆柱状,最后成为黄绿色稀便,可见未消化的颗粒饲料奇臭。经模型评价,模型组及电针组20只大鼠造模均成功,在造模期间空白组大鼠给予安静环境隔离,不予任何处置。
1.4 电针刺激
造模结束后第2天开始对电针组进行电针干预。给电针组大鼠穿上定制的鼠衣后悬挂于自制悬挂架上。参照《实验针灸学》[9]选取“足三里”穴,即大鼠的“后三里”穴。再选取“太冲”穴酒精局部消毒后,采用0.35×25 mm(1寸)针灸针分别直刺深度约12.5 mm(约0.5寸)、5 mm(约0.2寸)。将双侧“后三里”穴接韩氏穴位神经刺激仪连续波,频率2 Hz,强度1 mA,双侧“太冲”穴静留针,每次治疗时间30 min,每日治疗1次(9AM~11AM),治疗14 d。空白组和模型组在治疗期间给予电针组同样的穿鼠衣及悬吊,不予其他任何处置,在安静环境中隔离。在电针组最后1次治疗结束,将各组大鼠称重并禁食24 h后取材。
1.5 ELISA(Enzyme Linked Immunosorbent Assay,酶联免疫吸附剂检测)测定血清IL-6、TNF-α水平
治疗结束后各组大鼠均禁食24 h后取材,用20%乌拉坦4 mL/kg腹腔注射麻醉后,给予腹主动脉采血,3000 r/min离心15 min,取上清液后置于干净EP管。根据酶联免疫吸附试剂盒说明书,按步骤检测大鼠血清IL-6、TNF-α水平,操作步骤严格按照说明书进行。
1.6 WB(Western blot,免疫印迹法)检测十二指肠TLR4、NF-κB p65蛋白表达
取少量十二指肠碎组织加入0.3 mL裂解液匀浆后裂解,随后于4 ℃下12000 r/min离心5 min,取上清液,提取总蛋白之后用DG-3022 A酶标仪测定蛋白浓度。随后将提取的蛋白上清与5ⅹ蛋白上样缓冲液进行沸水浴中10 min,使蛋白变性。配置5%浓缩胶、12%分离胶后开始电泳、转模、免疫印迹显色等步骤检测后得到灰度条带,用Image J软件对蛋白条带灰度值进行测定。
1.7 统计学方法

2 结果
2.1 各组大鼠血清IL-6、TNF-α水平比较
表1示,与空白对照组比较, 模型组及电针组大鼠血清IL-6均升高,模型组TNF-α水平升高,差异有统计学意义 (P<0.05),但电针组TNF-α水平较空白组比较差异无统计学意义(P>0.05),与模型组比较, 电针组大鼠血清IL-6、TNF-α均下降,差异有统计学意义(P<0.05),提示电针能明显降低肝郁脾虚FD模型大鼠血清IL-6、TNF-α的含量。

表1 各组大鼠IL-6、TNF-α水平比较
2.2 各组大鼠十二指肠TLR4、NF-κB p65表达比较
图1示,与空白对照组比较,模型组大鼠十二指肠TLR4、NF-κB p65表达显著增多(P<0.05)。与模型组比较,电针组大鼠十二指肠TLR4、NF-κB p65表达明显降低(P<0.05)。
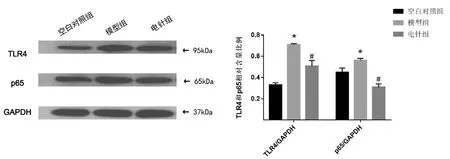
注:与空白组比较:*P<0.05;与模型组比较:#P<0.05图1
3 讨论
FD虽然并不是致命的急性疾病,但其极度影响患者的生活质量,加重社会医疗负担。据调查[10],在全世界范围内,20%的人群受FD困扰。因此,FD的病因病机研究一直是热点。罗马Ⅳ标准提出,低度炎症、肠道菌群改变等可能与FD发病有关[10]。研究表明,功能性胃肠病患者均存在低度黏膜炎症和免疫细胞活化,且与肠黏膜屏障损伤及肠神经异常敏感有关[11-12]。
TLRs位于细胞膜上,是一种模式识别受体(pattern recognition receptor,PRR)。TLRs能激活免疫应答,是防御外来毒物的第一层屏障,也是目前应用于抗炎症治疗的重要靶点[13-14]。研究表明,TLRs可通过激活下游信号通路产生大量炎症因子,诱导疾病的发生[15]。大鼠胃肠黏膜上存在TLR4,正常状态下TLR4表达量极少,当机体处于炎症状态时,TLR4表达增多。研究发现,TLR4激活可使树突状细胞等免疫细胞相继活化,分泌大量促炎细胞因子如IL-6、TNF-α等,导致组织炎症损伤[16]。NF-κB是一种重要的参与炎症介导的核转录因子,p65 是NF-κB的5个亚单位之一。在静息状态下与抑制性蛋白(Inhibitor kappaB, IκB)结合,存在于细胞质中;当受到内源性或外源性刺激,NF-κB中脱离IκB入核与DNA结合,参与相应蛋白合成,调控炎症免疫反应。NF-κB的下游促炎因子如TNF-α和IL-6,可在其被激活后迅速增多并加剧炎症反应[17]。因此,NF-κB p65可反映炎症严重程度,也可用来评价疗效[18]。
中医并无FD命名,根据该病的相关症状,其属于“痞满”“胃脘痛”范畴。中医疗法治疗FD疗效显著,已经越来越受广大医生及患者的认可,如电针、穴位敷贴、耳穴贴压、拔罐等[19]。临床研究表明[20],电针治疗FD患者后可显著缓解上腹痛、早饱等不适。动物实验中,电针可改善FD大鼠稀便、毛发干枯凌乱[21]、增强胃肠动力[22-23]、减轻局部炎症及免疫反应[24]等,因此电针治疗FD疗效肯定。本实验模型大鼠为肝郁脾虚证,选取太冲穴可疏理肝气,调畅气机;足三里穴可补中气、调理气机、帮助运化, 疏通胃肠,两穴合用共奏补虚泻实、疏肝健脾之功。实验数据显示,电针治疗后大鼠十二指肠TLR4、NF-κB p65蛋白表达显著降低,且IL-6、TNF-α也较模型组降低。提示电针减轻FD大鼠炎症反应,可能通过降低TLR4、NF-κB p65表达实现。因此,本研究结果验证了FD病因可能与消化道低度炎症有关,而TLR4、NF-κB p65二者之间可能存在某种关系,减轻炎症因子(IL-6, TNF-α)的合成,但二者之间的信号沟通关系需要进一步研究。
