华蟾素胶囊联合化疗治疗晚期结直肠癌的系统评价与Meta分析❋
2020-10-31马银杰何生奇
金 金,马银杰,何生奇
(中国中医科学院望京医院,北京 100102)
结直肠癌是消化系统常见的恶性肿瘤之一,已严重威胁到人类健康及生命安全。据国际癌症研究中心最新报道,2018年全球结直肠癌新发病例180万例,死亡88.1万例,已成为世界范围内癌症第二大死亡原因[1]。约有25%的结直肠癌患者发现时已为晚期,另有25%~50%的患者在确诊后仍发生转移进入晚期阶段[2]。目前临床常用的晚期结直肠癌一线化疗方案为奥沙利铂+卡培他滨(XELOX)方案和奥沙利铂+亚叶酸钙+氟尿嘧啶(FOLFOX)方案[3]。化疗可在一定程度上缓解疾病进展,延长患者生存期,但伴随化疗出现的毒副反应,严重影响部分患者的生活质量[4],加上长期使用化疗药物易使患者产生耐药性,进而导致肿瘤复发和转移[5]。近年来,随着现代肿瘤治疗观的转变,中医药在晚期结直肠癌的综合治疗中地位日益突出[6-8]。华蟾素为中药制剂蟾皮的阴干提取物, 具有清热解毒、消肿、止痛等作用[9]。现代药理学研究表明,华蟾素可通过抑制肿瘤细胞增殖及其血管生成、诱导肿瘤细胞凋亡、增强机体免疫功能等多种途径发挥抗肿瘤活性作用[10]。在我国一些省份,华蟾素已成为治疗肝癌和非小细胞肺癌的重要辅助治疗药物[11],且在结直肠癌中的疗效也越来越受到临床医生的重视。但尚无循证医学依据证实华蟾素治疗中晚期结直肠癌的有效性与安全性。本文旨在对华蟾素治疗中晚期结直肠癌的RCTs进行严谨的Meta分析,以期为临床运用提供指导。
1 资料与方法
1.1 纳入标准
研究类型为RCTs,语种仅限中英文。研究对象符合中国临床肿瘤学会颁布的2019年版《结直肠癌诊疗指南》标准,经细胞学、病理学或影像学等诊断为结直肠癌患者。干预措施:试验组为华蟾素胶囊联合化疗药物,对照组单用化疗药物。至少观察下列1项结局指标,如近期疗效有效率,标准参照世界卫生组织(world health organization, WHO)疗效评价标准或实体瘤疗效评价标准(response evaluation criteria in solid tumors, RECIST),有效率为完全缓解(complete response, CR)与部分缓解(partial response, PR)的发生率;生活质量稳定率标准参照卡氏(karnofsky performance status, KPS)评分标准,KPS评分较治疗前增加10分以上为改善,增加或减少均未超过10分为稳定,降低10分以上为减退。稳定率为KPS评分为改善与稳定的发生率;疼痛缓解率标准参照数字评分法(numerical rating scale, NRS),疼痛缓解率为CR+PR的发生率;不良反应包括白细胞毒性、胃肠道不良反应、肝功能异常及手足麻木发生率。
1.2 排除标准
无法获取全文者;数据存在严重错误者;重复发表或数据重复的研究(前者保留第一篇,后者保留数据最全的1篇);结局指标中的KPS评分采用连续性变量数据者。
1.3 检索策略
计算机检索中文数据库CNKI、WanFang、CBM、VIP,英文数据库检索Medline、Cochrane Library、Web of Science,检索时间均为该数据库建库至2019年10月。
中文检索词采用“华蟾素胶囊”“福欣甘”“结直肠癌”“大肠癌”,英文检索词采用“cinobufacini capsule” “huachansu” “fuxingan” “colorectal neoplasms” “colorectal cancer”。
以CNKI和PubMed为例,CNKI检索策略为#1 华蟾素胶囊;#2 福欣甘;#3 #10R#2;#4 结直肠癌;#5 大肠癌;#6 #4OR#5;#7 #3AND#6。Pubmed检索策略为#1 cinobufacini capsule; #2 huchansu; #3 fuxingan; #4 #1OR#2OR#3; #5 colorectal neoplasms; #6 colorectal cancer;#7 #5OR#6; #8 #4AND#7。
1.4 评价方法
1.4.1 文献筛选 2名研究者根据纳入和排除标准独立筛选文献,并相互核对结果,如遇分歧讨论解决。首先采用Note Express软件进行文献管理和查重,将获得的文献通过阅读标题、摘要进行初筛,排除明显不符合纳入标准的文献;其次进一步查找、阅读全文进行复筛,最终确定纳入文献。
1.4.2 文献数据提取 将确定纳入的文献按照自行设计的资料提取表进行资料提取,内容包括纳入研究的一般资料,其中包括作者、发表时间;纳入研究的特征包括样本量、研究例数、干预措施、对照措施、疗程、疗效指标等,如有必要对有缺失的相关数据与原作者联系。
1.4.3 方法学质量评价 2名研究者将纳入的文献依据《Cochrane评价手册》[12]中关于RCTs的偏倚风险评估工具进行质量评价,包括纳入研究的随机方案、盲法的实施、试验数据的完整性、选择性报告研究结果和其他偏倚做出低偏倚风险、高偏倚风险或不清楚的评价,当意见不一致时由第三者核查或讨论解决,直到达成共识。
1.5 统计学方法
采用Cochrane协作网提供的RevMan 5.3软件进行统计分析,计数资料采用RR为疗效分析统计量,并以其95%CI表示,P≤0.05为差异有统计学意义。试验间异质性采用χ2检验,若P>0.1,I2≤50%时采用固定效应模型进行Meta分析,若P≤0.1,I2>50%时则采用随机效应模型,若各研究结果间异质性过大采用描述性分析。本项研究根据实体瘤疗效评价标准的不同进行亚组分析,若结局指标所纳入的文献≥10篇采用倒漏斗图分析是否存在发表偏倚。
2 结果
2.1 文献检索结果
图1示,初步筛选出相关文献116篇,经逐层筛选后最终纳入9篇文献。
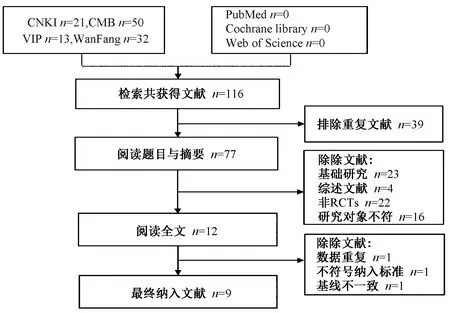
图1 文献检索流程
2.2 纳入文献的基本特征
表1示,共纳入9项[13-21]研究,包括658例晚期结直肠癌患者,所有试验均在国内进行。纳入研究的最小样本量为35例,最大为157例。所有研究试验组均为华蟾素胶囊联合化疗药物,对照组则为各化疗药物。其中2项[15, 21]研究化疗采用XELOX方案,6项[13-14, 16, 18-20]研究采用FOLFOX方案,1项[17]研究采用FOLFOX类方案(奥沙利铂+替吉奥),用药疗程从2周期到4周期不等。所有研究均采用近期有效率为疗效评价指标,其余指标包括生活质量评分、疼痛缓解率、不良反应等。

表1 纳入研究基本特征比较
2.3 纳入研究的质量评价
表2示,纳入的9项研究均未提及研究方案及样本量估算,其中3项[13, 16-17]研究报告了恰当的随机分配方法,2项[14, 20]研究依据治疗方式分组,其余研究仅提及进行了随机分组,但均未说明具体做法,仅有1项[17]研究进行了随机分配方案隐藏。所有研究均未报告盲法的实施及是否存在病例脱落和失访现象。

表2 纳入文献质量评价表
2.4 疗效分析
2.4.1 近期疗效有效率 WHO疗效评定标准:表3示,纳入的研究中有5项[13, 15, 18, 20-21]研究采用世界卫生组织(WHO)实体瘤疗效评定标准进行评价。异质性检验结果显示,各研究间无统计学异质性(P=0.63,I2=0%),故采用固定效应模型进行Meta分析。结果显示,华蟾素胶囊联合化疗药疗效优于单纯使用化疗药[RR=1.32,95%CI=(1.03,1.69),P=0.03]。RECIST标准:表3示,共有4项[14, 16-17, 19]研究采用RECIST标准进行评价。异质性检验结果显示,各研究间无统计学异质性(P=0.70,I2=0%),故采用固定效应模型进行Meta分析。结果显示,与对照组比较,华蟾素联合化疗对抑制肿瘤生长疗效显著[RR=1.32,95%CI=(1.10,1.59),P=0.003]。

表3 华蟾素胶囊联合化疗治疗晚期结直肠癌不同疗效评价标准Meta分析结果
2.4.2 生活质量稳定率
表4示,共有8项[13, 15-21]研究报道了患者生活质量变化状况。经异质性检验,各研究间无统计学异质性(P=0.98,I2=0%),故采用固定效应模型进行Meta分析。结果显示,与对照组比较,华蟾素胶囊联合化疗可显著提高患者生活质量[RR=1.71,95%CI=(1.35,2.16),P≤0.00001]。
2.4.3 疼痛缓解率 表4示,共有3项[15, 17, 19]研究对患者癌性疼痛缓解程度进行了评价。异质性检验结果显示,各研究间无统计学异质性(P=1.00,I2=0%),故采用固定效应模型进行Meta分析。结果显示,与对照组比较,华蟾素联合化疗可显著缓解患者疼痛[RR=4.09,95%CI=(1.97,8.51),P=0.0002]。

表4 华蟾素胶囊联合化疗治疗晚期结直肠癌结局指标Meta分析结果
2.4.4 不良反应 表5示,白细胞毒性共有8项[13-16, 18-21]研究报告了白细胞变化情况。经异质性检验,各研究间无统计学异质性(P=0.50,I2=0%),故采用固定效应模型进行Meta分析。结果显示,与对照组比较,华蟾素联合化疗可降低白细胞毒性[RR=0.32,95%CI=(0.22,0.47),P<0.00001]。胃肠道不良反应:共有5项[14-15, 17-19]研究报告了发生胃肠道不良反应的病例数。异质性检验结果显示,各研究间统计学异质性较小(P=0.17,I2=38%),故采用固定效应模型。Meta分析结果显示,与对照比较,华蟾素联合化疗可减少胃肠道不良反应的发生[RR=0.83,95%CI=(0.70,0.99),P=0.04]。肝功能损害:共有2项[15, 21]研究报告了肝功能损害的病例数。经异质性检验结果显示,两研究间统计学异质性较小(P=0.19,I2=42%),采用固定效应模型进行Meta分析。结果显示,与对照组比较,华蟾素胶囊联合化疗可减少肝功能损害的发生[RR=0.39,95%CI=(0.18,0.87),P=0.04]。手足麻木:共有4项[15, 18-19, 21]研究报告了手足麻木发生情况。异质性检验结果显示,各研究间无统计学异质性(P=1.00,I2=0%),故采用固定效应模型进行Meta分析。结果显示,与对照组比较,华蟾素联合化疗可减少手足麻木的发生[RR=0.72,95%CI=(0.58,0.91),P=0.005]。
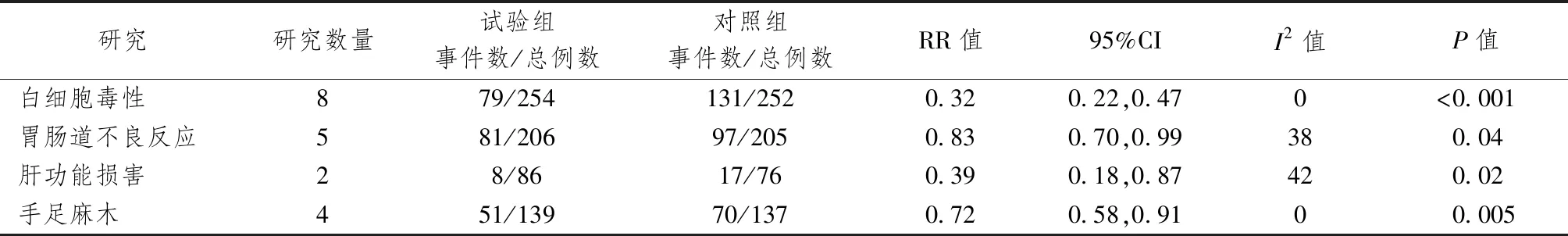
表5 华蟾素胶囊联合化疗治疗晚期结直肠癌不良反应Meta分析结果
3 讨论
随着人口老龄化进程的加快和人们生活方式的转变,结直肠癌发病率呈上升趋势,现已成为第三大最常见的男性癌症和第二大最常见的女性癌症,是世界范围内第二大癌症死亡原因[22]。由于该病早期症状不明显,多数患者发现时已进入晚期,失去了手术治疗机会[23]。化疗是晚期及复发转移性结直肠癌的主要治疗手段,可延长患者生存期且相对经济简便[24]。然而化疗药物在杀伤肿瘤细胞的同时也可杀伤正常细胞而造成胃肠道反应、骨髓抑制等严重的副反应,部分患者耐受性差,最终迫使其终止治疗[25]。因此,如何在保证抗癌疗效的同时降低化疗药物的毒副反应,成为迫切需要解决的问题[17]。中医药是中华民族几千年来对生命、健康和疾病认识及实践经验的积累,在恶性肿瘤的治疗中发挥着不可替代的作用[26]。多项研究表明,中药联合放化疗、靶向药物治疗等可显著改善患者生存质量、减轻化疗毒副反应等[27]。华蟾素作为我国自行研制和开发的二类新药,其成分中的脂蟾毒配基、蟾毒灵、华蟾酥毒基等具有明显的抗肿瘤活性作用[28]。有文献总结,华蟾素可通过增强巨噬细胞的吞噬功能,抑制肿瘤细胞DNA和RNA的合成,诱导肿瘤组织细胞凋亡,影响细胞中癌基因的表达,抗肿瘤组织血管的生成等多种途径抑制肿瘤生长,提高患者生活质量[29]。
尽管多项研究表明,华蟾素胶囊联合化疗可用于治疗晚期结直肠癌,但其疗效和副作用尚存有争议。本文通过对严格筛选出的9项相关研究进行Meta分析,结果表明,华蟾素胶囊联合化疗在近期疾病有效率、生活质量稳定率、疼痛缓解率上均高于单纯使用化疗药,且在白细胞毒性、胃肠道不良反应、肝功能异常、手足反应的发生率低于对照组,表明华蟾素胶囊联合化疗治疗晚期结直肠癌是有效安全的。此外,尽管干预措施不完全相同,有研究采用FOLFOX化疗方案,也有研究采用XELOX方案,但已有数据表明,XELOX方案与FOLFOX方案在肿瘤控制率、近期有效率、疾病进展时间等方面疗效相当,差异无统计学意义[30]。
评价干预措施的疗效及安全性需要高质量的方法学辅助,方法学质量低下的试验在一定程度上会放大试验的真实结果[ 31-33]。然而本次研究纳入的文献方法学质量相对较低,具体表现如下:随机化是将研究对象随机分配到各组,包括随机序列的产生和实施两大要素,理想的结果是研究对象不知道该序列[34]。然而多数研究仅提及随机二字,并未报道具体实施方案,仅有1项研究提及随机分配方案的隐藏,其余研究均未进行报道。因此,无法对随机分组的充分性作出判断。盲法是指研究对象和(或)研究者或评估者不明确干预措施的分配,在临床试验中可控制多个阶段的偏倚,是一个重要且独特的方面[35]。本项研究所纳入的试验均未提及盲法,故纳入的研究可能存在一定偏倚。由于临床试验尤其受试对象为肿瘤化疗患者,会不可避免地出现受试者的退出和失访,而完整的报告退出和失访例数并进行意向性分析是对研究质量的重要保证[33]。而纳入的9项研究均未报道受试者退出和(或)失访情况,故在一定程度上可能会影响对结果证据强度的评价。
由于本次研究纳入的文献数量较少,故存在一定的局限性。如纳入的研究均为中文文献,可能遗漏以往其他语种发表的文献,故可能存在着一定语言偏倚,影响本次结果的外推性。由于未纳入未检索到的灰色文献,故本研究存在一定的发表偏倚。各研究运用化疗药物疗程各不相同,虽有对照组作为比较,但疗程的不同可能会影响疗效的判定和对结论的分析。本次研究纳入研究均为小样本、单中心进行,故存在一定的临床异质性。
综上所述,本研究通过对9项随机对照试验进行分析,认为华蟾素胶囊联合化疗治疗晚期结直肠癌是有效、安全的,可在提高近期有效率、生活质量评分及疼痛缓解率的同时,降低白细胞减少率、胃肠道反应、肝功能损害及手足麻木等不良反应的发生。但本次研究仅为初步评价,尚需大样本、多中心、高质量的随机对照试验进行验证。
