王不留行炮制前后的UPLC指纹图谱比较及刺桐碱和王不留行黄酮苷的含量测定
2020-10-30曹斯琼吴文平罗宇琴马瑞瑞潘礼业李国卫陈向东
曹斯琼 吴文平 罗宇琴 马瑞瑞 潘礼业 李国卫 陈向东

摘 要 目的:比較王不留行炮制(清炒)前后的指纹图谱差异,并测定其炒制前后刺桐碱、王不留行黄酮苷的含量。方法:采用超高效液相色谱(UPLC)法,色谱柱为YMC Trait C18,流动相为乙腈-水(梯度洗脱),流速为0.35 mL/min,检测波长为219 nm,柱温为35 ℃,进样量为1 μL。以王不留行黄酮苷为参照,绘制王不留行生品及其炮制品(各17批,编号分别为S1~S17、CS18~CS34)的指纹图谱;采用《中药色谱指纹图谱相似度评价系统(2012版)》进行相似度评价及共有峰指认;采用SPSS 20.0软件进行聚类分析、主成分分析和因子分析。采用上述UPLC法测定王不留行生品及其炮制品中刺桐碱、王不留行黄酮苷的含量。结果:17批王不留行生品及其炮制品的UPLC指纹图谱中均有共有峰5个,相似度均大于0.99;共指认了刺桐碱和王不留行黄酮苷等2个共有峰。聚类分析结果显示,S1~S17聚为一类,CS18~CS34聚为一类;主成分分析及因子分析结果显示,第1主成分的方差贡献率为76.418%,刺桐碱、王不留行黄酮苷在第1主成分上有较高载荷(特征值分别为0.976、0.966)。刺桐碱、王不留行黄酮苷检测质量浓度的线性范围分别为6.437~321.832、7.729~386.437 μg/mL(r均大于0.999);检测限、定量限分别为0.085、0.284 ng(生品)和0.739、2.465 ng(炮制品);精密度、重复性、稳定性(12 h)、耐用性试验的RSD均小于3%(n=6或n=5);平均加样回收率分别为96.42%(RSD=0.85%,n=6)、99.13%(RSD=1.74%,n=6)。两种成分的含量分别为0.11%~0.20%、0.42%~0.63%(生品)和0.08%~0.11%、0.34%~0.50%(炮制品)。结论:成功建立了王不留行生品及其炮制品的UPLC指纹图谱。王不留行炒制前后的化学成分虽一致性较好,但炒制后刺桐碱、王不留行黄酮苷的含量均有所降低。
关键词 王不留行;炮制;超高效液相色谱法;指纹图谱;刺桐碱;王不留行黄酮苷;聚类分析;主成分分析
ABSTRACT OBJECTIVE: Compare the fingerprint difference of Vaccariae Semen before and after processed (stir-fried), and to determine the contents of erythrine and vaccarin before and after stir-fried. METHODS: UPLC method was adopted. The determination was performed on YMC Trait C18 column with mobile phase consisted of acetonitrile-water (gradient elution) at the flow rate of 0.35 mL/min. The detection wavelength was set at 219 nm, and the column temperature was 35 ℃. The sample size was 1 μL. Using vaccarin as reference, the fingerprints of Vaccariae Semen crude product and its processed product (each of 17 batches, S1-S17, CS18-CS34) were drawn. The similarity evaluation and common peak identification were carried out by Similarity Evaluation System of TCM Chromatographic Fingerprint (2012 edition); cluster analysis, principle component analysis (PCA) and factor analysis were performed by using SPSS 20.0 software. The contents of erythrine and vaccarin in Vaccariae Semen crude product and its processed product were determined by UPLC. RESULTS: There were 5 common peaks in UPLC fingerprints of 17 batches of Vaccariae Semen crude product and its processed product. The similarities were all higher than 0.99. Among them, 2 common peaks were identified, i.e. erythrine, vaccarin. Results of cluster analysis showed that S1-S17 were clustered into one category and CS18-CS34 were clustered into one category. Results of PCA and factor analysis showed that variance contribution rate of the first principle component was 76.418%; erythrine and vaccarin had higher loading on the first principal component (eigenvalues were 0.976 and 0.966, respectively). The linear ranges of above 2 components were 6.437-321.832 μg/mL and 7.729-386.437 μg/mL,respectively (r>0.999). The limits of detection and quantitation were 0.085,0.284 ng (crude product) and 0.739, 2.465 ng (processed product), respectively. RSDs of precision,reproducibility, stability (12 h) and durability tests were all lower than 3%(n=6 or n=5). Average recoveries were 96.42% (RSD=0.85%, n=6) and 99.13% (RSD=1.74%, n=6). The contents of the two components were 0.11%-0.20%, 0.42%-0.63%(crude product)and 0.08%-0.11%, 0.34%-0.50%(processed product). CONCLUSIONS: UPLC fingerprint of Vaccariae Semen crude product and its processed product are established successfully. Although the chemical constituents in Vaccariae Semen are consistent before and after stir-fried, the contents of erythrine and vaccarin are all decreased after stir-fried.
KEYWORDS Vaccariae Semen; Processing; UPLC; Fingerprint; Erythrine; Vaccarin; Cluster analysis; Principal component analysis
王不留行为石竹科植物麦蓝菜Vaccaria segetalis (Neck.) Garcke的干燥成熟种子,具有活血化瘀、下乳消肿、利尿通淋之功效[1]。该药味苦、性平,归肝、胃经,可用于治疗乳腺癌、产后缺乳、泌尿系统疾病等[2]。据文献报道,该药的主要化学成分包括黄酮苷类、生物碱类、三萜皂苷类、环肽类和脂肪油类等[3-5]。其中,黄酮苷类成分是王不留行催乳的有效成分,具有促进乳汁分泌的作用[6];而且,该类成分还能保护血管内皮细胞,促进内皮细胞增殖[7-8];此外,王不留行中的刺桐碱具有抗炎、增强免疫和抗肝损伤的作用[9]。
中药自古有“逢子必炒”的说法,种子类中药炒制后,种皮爆裂,质地酥脆,有利于有效成分溶出,也有助于生物利用度的提高[10-11]。2015年版《中国药典》(一部)收载的王不留行的炮制方法为清炒法[1]。据文献研究报道,王不留行炮制前后脂溶性成分含量及浸出物含量有明显差异[12];炮制对王不留行中环肽A、B、E含量的影响较小[13],但炮制后其黄酮苷的含量大幅度下降,而异牡荆素-2″-O-阿拉伯糖苷的含量却大幅上升[14-15]。指纹图谱作为一种体现中药化学成分整体特征的质量评价方法,对药材的全面控制具有重要作用。本研究通过建立王不留行生品及其炮制品的超高效液相色谱(UPLC)指纹图谱,应用化学模式识别方法比较两者的差异性,并测定两者中刺桐碱和王不留行黄酮苷的含量,以期为王不留行生品及其炮制品的质量控制及综合评价提供参考。
1 材料
1.1 仪器
H-Class型UPLC仪(美国Waters公司);XP26型百万分之一分析天平、ME204E型万分之一分析天平(瑞士Mettler Toledo公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 药品与试剂
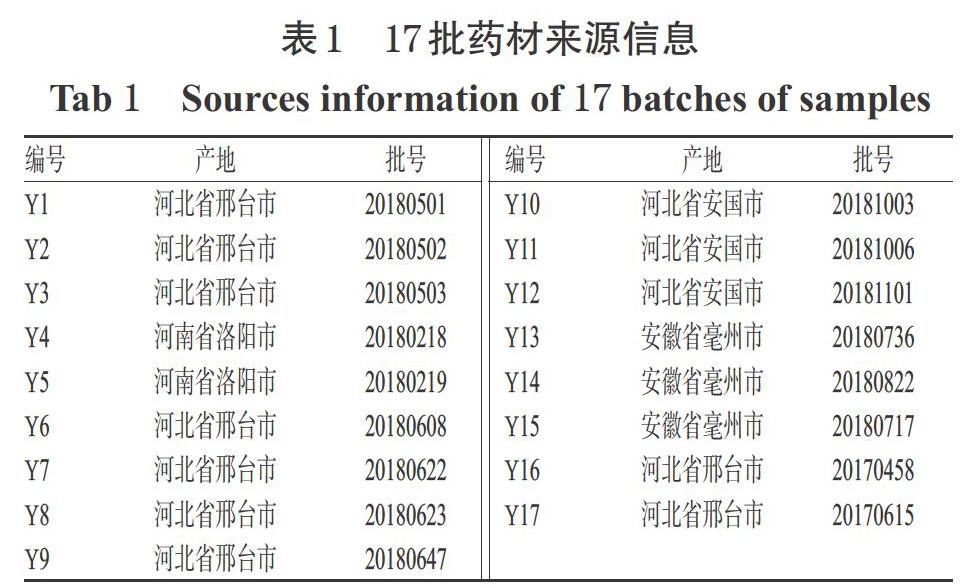
王不留行黄酮苷对照品(中国食品药品检定研究院,批号:111853-201704,纯度:99.7%);刺桐碱对照品(上海源叶生物科技有限公司,批号:P26N6F6550,纯度:98.0%);乙腈为色谱纯,其余试剂均为分析纯,水为超纯水。17批王不留行药材购自河北、河南、安徽,经广东一方制药有限公司魏梅主任中药师鉴定,均为石竹科植物麦蓝菜V. segetalis (Neck.) Garcke的干燥成熟种子。17批药材来源信息见表1。
2 方法与结果
2.1 样品炮制
取王不留行药材,按2015年版《中国药典》(一部)王不留行项下“王不留行”炮制方法[1],除去杂质,得王不留行生品饮片(编号:S1~S17);按“炒王不留行”炮制方法,取净王不留行,照“清炒法”炒至大多爆开白花,得炒王不留行饮片(编号:CS18~CS34)。
2.2 混合对照品溶液制备
精密称取刺桐碱对照品3.344 mg、王不留行黄酮苷对照品3.011 mg,加甲醇制成每1 mL含刺桐碱32.771 μg、王不留行黄酮苷30.020 μg的混合对照品溶液。
2.3 供试品溶液制备
取饮片样品,粉粹,过三号筛,取粉末约1 g,精密称定,置具塞锥形瓶中,精密加入75%乙醇25 mL,称定质量,超声(功率:250 W,频率:40 kHz)处理30 min,静置至室温,再称定质量,用75%乙醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.4 色谱条件
色谱柱:YMC Trait C18(100 mm×2.1 mm,1.9 μm);流动相:乙腈(A)-水(B),梯度洗脱(0~5.5 min,10%A→15%A;5.5~11 min,15%A→30%A;11~16.5 min,30%A→70% A);流速:0.35 mL/min;柱温:35 ℃;检测波长:219 nm;进样量:1 μL。
2.5 UPLC指纹图谱的建立
2.5.1 精密度试验 取“2.3”项下同一供试品溶液(编号:S3)適量,按“2.4”项下色谱条件连续进样测定6次,记录色谱图。以王不留行黄酮苷峰为参照,计算各共有峰的相对保留时间和相对峰面积。结果,各共有峰相对保留时间和相对峰面积的RSD均小于1.0%(n=6),表明本方法精密度良好。
2.5.2 稳定性试验 取“2.3”项下同一供试品溶液(编号:S3)适量,分别于室温下放置0、2、4、6、12 h时按“2.4”项下色谱条件进样测定,记录色谱图。以王不留行黄酮苷峰为参照,计算各共有峰的相对保留时间和相对峰面积。结果,各共有峰相对保留时间和相对峰面积的RSD均小于3.0%(n=5),表明供试品溶液于室温下放置12 h内稳定性良好。
2.5.3 重复性试验 取饮片样品(编号:S3)粉碎,过三号筛,取粉末适量,共6份,分别按“2.3”项下方法制备供试品溶液,再按“2.4”项下色谱条件进样测定,记录色谱图。以王不留行黄酮苷峰为参照,计算各共有峰的相对保留时间和相对峰面积。结果,各共有峰相对保留时间和相对峰面积的RSD均小于1.0%(n=6),表明本方法重复性良好。
2.6 UPLC指纹图谱的生成及相似度评价
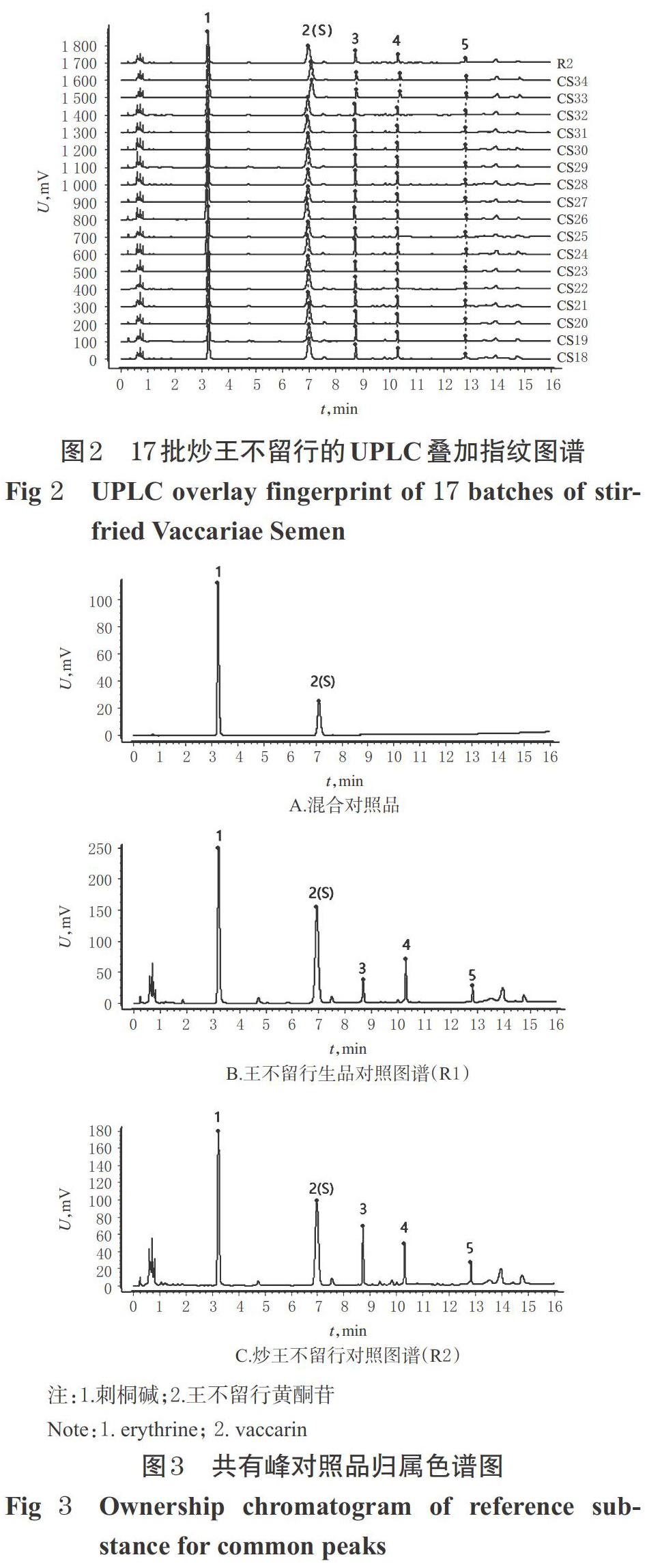
分别取17批王不留行生品饮片和17批炒王不留行饮片,按“2.3”项下方法制备供试品溶液,再按“2.4”项下色谱条件进样测定,记录色谱图。将图谱导入《中药色谱指纹图谱相似度评价系统(2012版)》,分别以S1、CS18样品的指纹图谱为参照图谱,以2号峰为参照峰(S峰)进行保留时间校正并进行全峰匹配,生成叠加指纹图谱,采用平均数法生成共有模式图(对照特征图谱为R1、R2),详见图1、图2。
由图1、图2可见,各共有峰较稳定,具有指纹图谱特征性,可初步认定为王不留行生品与其炮制品的指标成分群。王不留行生品和炒王不留行的UPLC叠加指纹图谱中,分别有共有峰5个;通过与混合对照品溶液进行比对,指认了其中2个成分,即1号色谱峰为刺桐碱峰,2号色谱峰为王不留行黄酮苷峰。因王不留行黄酮苷峰分离效果好、出峰稳定且保留时间适中,故以其保留时间和峰面积作为参照(S)。共有峰对照品归属色谱图见图3。
以共有模式作为对照图谱,将17批王不留行和17批炒王不留行分别进行相似度评价。结果,所有批次样品的相似度均大于0.99,表明王不留行生品与其炮制品的化学成分一致性较好,详见表2。
2.7 指纹图谱的化学计量学分析
2.7.1 聚类分析 以各共有峰的峰面积为原始数据,运用SPSS 20.0软件,采用组间平均数联结法,以夹角余弦作为样品相似度的距离公式,对17批王不留行生品和炒王不留行进行系统聚类。结果,S1~S17王不留行生品样品聚为一类,CS18~CS34炒王不留行样品聚为一类,提示清炒这一炮制方法对王不留行的化学成分含量有一定的影响,详见图4。
2.7.2 主成分分析及因子分析 以各共有峰的峰面积为原始数据,利用SPSS 20.0软件对17批王不留行生品和17批炒王不留行指纹图谱所得的5个共有峰进行主成分分析,得到相关矩阵的特征值及其方差贡献率,详见表3;得到初始因子载荷矩阵,详见表4。提取表3中特征值>1的成分(主成分),仅第1成分符合要求,计算得其方差贡献率为76.418%,表明该主成分代表了王不留行生品和炒王不留行中5个成分76.418%的信息量,具有很好的代表性。由表4可知,峰1和峰2在第1主成分上有较高载荷,峰1(刺桐碱)的特征值为0.976,峰2(王不留行黄酮苷)的特征值为0.966,说明第1主成分主要反映了刺酮碱和王不留行黄酮苷的信息,是用以区分王不留行生品和炒王不留行的重要因素。第1主成分可代表王不留行与炒王不留行指纹图谱的大部分信息,主成分分析结果基本显示出了不同批次王不留行样品之间的相似度和差异性。按方差贡献率计算各样品第1主成分得分,结果显示,王不留行生品得分较炒王不留行高,第1主成分可作为区分两种样品的指标,详见表5。根据主成分分析结果绘制散点图,详见图5。由图5可知,本试验中的样品可以分为2类,即王不留行生品(S1~S17)为一类,炒王不留行(CS18~CS34)为一类。
2.8 刺桐碱和王不留行黄酮苷的含量测定
由“2.7”项下可知,峰1和峰2对区分王不留行生品和炒王不留行的指纹图谱起着决定性作用,故本研究采用UPLC法对刺桐碱和王不留行黄酮苷2种成分的含量进行测定。
2.8.1 色谱条件 同“2.4”项下色谱条件。
2.8.2 系统适用性试验 取“2.2”项下混合对照品溶液、“2.3”项下供试品溶液和阴性对照溶液(75%乙醇)各适量,按“2.8.1”项下色谱条件进样测定,记录色谱图。结果,刺桐碱峰和王不留行黄酮苷峰的分离度均大于1.5、理论板数均大于6 000,阴性对照不干扰测定,详见图6。
2.8.3 线性关系考察精密称取刺桐碱对照品、王不留行黄酮苷对照品各适量,加甲醇制成每1 mL含刺桐碱321.832 μg、王不留行黄酮苷386.437 μg的混合对照品溶液。分别取该溶液1 mL,分置于1、2、5、10、25、50 mL量瓶中,加甲醇稀释至刻度,摇匀,得系列线性工作溶液。分别精密吸取上述线性工作溶液1 μL,按“2.8.1”项下色谱条件进样测定,记录峰面积。以各待测成分质量浓度(x,μg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,得回归方程,详见表6。
2.8.4 定量限、检测限考察 分别精密吸取“2.2”项下混合对照品溶液适量,加甲醇倍比稀释后按“2.8.1”项下色谱条件进样测定,分别以信噪比10 ∶ 1、3 ∶ 1计算定量限、检测限,结果见表6。
2.8.5 精密度试验 取“2.2”项下混合对照品溶液适量,按“2.8.1”项下色谱条件进样测定6次,记录峰面积。结果,刺桐碱和王不留行黄酮苷峰面积的RSD分别为0.16%、0.45%(n=6),表明仪器精密度良好。
2.8.6 重复性试验 取王不留行样品(编号:S3)适量,共6份,分别按“2.3”项下方法制备供试品溶液,按“2.8.1”項下色谱条件进样测定,并按标准曲线法计算样品中2种成分的含量。结果,刺桐碱、王不留行黄酮苷的平均含量分别为0.13%、0.52%,RSD分别为1.35%、1.78%(n=6),表明该方法重复性良好。
2.8.7 稳定性试验 取“2.8.6”项下供试品溶液(编号:S3)适量,分别于室温下放置0、2、4、6、12 h时按“2.8.1”项下色谱条件进样测定,记录峰面积。结果,刺桐碱、王不留行黄酮苷峰面积的RSD分别为0.53%、0.52%(n=5),表明供试品溶液于室温下放置12 h内稳定性良好。
2.8.8 加样回收率试验 取王不留行生品(编号:S3)共6份,每份约0.5 g,精密称定,分别加入一定量的刺桐碱、王不留行黄酮苷对照品,按“2.3”项下方法制备供试品溶液,再按“2.8.1”项下色谱条件进样测定,记录峰面积并计算加样回收率。结果表明该方法准确度良好,详见表7。
2.8.9 耐用性试验 取王不留行生品(编号:S3)适量,按“2.3”项下方法制备供试品溶液,按“2.8.1”项下色谱条件以不同流速(0.30、0.35、0.40 mL/min)、不同柱温(30、35、40 ℃)、不同色谱柱[Waters BEH C18(100 mm×2.1 mm,1.7 μm)、YMC C18(100 mm×2.1 mm,1.9 μm)、Agilent SB C18(100 mm×2.1 mm,1.8 μm)]进样测定,记录峰面积并按标准曲线法计算样品中2种成分的含量。结果,刺桐碱、王不留行黄酮苷含量的RSD均小于3%(n=3),表明该方法能够满足试验要求,耐用性良好。
2.8.10 样品含量测定 取17批王不留行生品和17批炒王不留行各适量,分别按“2.3”项下方法制备供试品溶液,按“2.8.1”项下色谱条件进样测定,记录峰面积并按标准曲线法计算刺桐碱和王不留行黄酮苷的含量,结果见表8。由表8可知,王不留行生品中刺桐碱和王不留行黄酮苷的含量均比炒王不留行高,说明这2种成分在炮制后出现明显下降,与周国洪等[14]的研究结果一致。
3 讨论
本研究分别考察了不同色谱柱、流动相系统、检测波长等色谱条件,经比较发现YMC Trait C18色谱柱(100 mm×2.1 mm,1.9 μm)、乙腈-水(梯度洗脱)和检测波长为219 nm的分离效果较好、峰形更佳,故确定其为最终的色谱条件。
王不留行生品长于消痈肿;炒制后走散力较强,长于活血通经、下乳、通淋[16]。王不留行炮制前后功效的差异,说明炮制后王不留行所含化学成分发生了改变。中药炮制后的变化主要体现在成分含量及成分种类的变化上,仅通过单一成分王不留行黄酮苷的含量作为指标性成分来控制王不留行炒制前后的质量有一定局限性。为此,本研究建立了鉴别、评价王不留行生品和炒王不留行的UPLC指纹图谱,其相似度评价结果显示,17批王不留行生品及相应的炮制品饮片的指纹图谱的相似度均大于0.99,说明王不留行经炮制后其化学成分并未发生质的变化。通过聚类分析可以将王不留行生品和炒王不留行分为2类;在主成分分析中,可知色谱峰1(刺桐碱)和峰2(王不留行黄酮苷)是区分王不留行生品和炒王不留行的主成分,故对这2种成分进行含量测定,结果发现王不留行炮制后其化学成分发生了量的变化。从王不留行炮制前后的指纹图谱并未发现有新成分产生,但是从峰面积结果发现,炮制后色谱峰1、2、4、5的峰面积均有一定幅度的减少,而色谱峰3的峰面积有所增加。由于色谱峰3、4、5均未能够指认,色谱峰3与其余各峰之间是否存在转化关系,则需要进一步对该色谱峰進行指认。此外,王不留行炮制前后化学成分的变化对药理作用的影响尚需进一步开展药效学实验,对二者药效作用的差异进行研究,以更好指导临床合理用药。
综上所述,本研究建立了王不留行生品及其炮制品的UPLC指纹图谱,该方法稳定、简便、快速,结合相似度评价、聚类分析与主成分分析,可用于王不留行生品及其炮制品的质量评价。
参考文献
[ 1 ] 国家药典委员会.中华人民共和国药典:一部[S]. 2015年版.北京:中国医药科技出版社,2015:54-55.
[ 2 ] 汪晶晶,任红立,武洪志,等.中药王不留行的化学成分及药理作用研究进展[J].黑龙江畜牧兽医,2017(4上):101-103.
[ 3 ] 魏薇.中药王不留行的研究进展[J].中国医药指南,2014,12(16):87-88.
[ 4 ] 孟贺,陈玉平,秦文杰,等. HPLC 测定王不留行中王不留行黄酮苷的含量[J].中国中药杂志,2010,35(16):2072-2074.
[ 5 ] 周国洪.王不留行化学成分及炮制对其影响研究[D].北京:中国中医科学院中医研究所,2016.
[ 6 ] 秦君,李庆章,高学军.王不留行主要成分对小鼠乳腺上皮细胞增殖及β-酪蛋白表达的影响[J].中国农业科学,2008,41(8):2442-2447.
[ 7 ] 谢凤珊,冯磊,马丽萍,等.王不留行黄酮苷对过氧化氢和高糖诱导损伤的人脐静脉内皮细胞的保护作用[J].天然产物研究与开发,2014,26(7):1009-1013.
[ 8 ] 王旭,候豹,蔡维维,等.王不留行黄酮苷的分离纯化及对细胞增殖活性的影响[J].天然产物研究与开发,2017,29(2):316-321.
[ 9 ] 蔡维维,侯豹,陈旭红,等.王不留行中刺桐碱的分离鉴定及抗炎活性研究[J].天然产物研究与开发,2018,30(4):616-620.
[10] 张亚丽,王东青.果实种子类药物炮制浅见[J].辽宁中医药大学学报,2009,11(6):216.
[11] 郭建民.“逢子必炒”之探索[J].贵阳中医学院学报,1994,16(3):59-60.
[12] 李翠芹,任钧.王不留行生品与炮制品脂溶性成分的GC-MS分析[J].中成药,2009,31(1):79-81.
[13] 周国洪,唐力英,寇真真,等.炮制对王不留行中王不留行环肽A,B,E含量的影响[J].中国实验方剂学杂志,2016,22(4):29-31.
[14] 周国洪,唐力英,寇真真,等.炮制对王不留行中刺桐碱及黄酮苷类成分含量及溶出率的影响[J].中国实验方剂学杂志,2016,22(22):18-21.
[15] 阴钺玲,薛睿,孙兆林. UPLC法测定炮制前后王不留行中Vaccarin含量[J].亚太传统医药,2015,11(20):20-21.
[16] 龚千锋.中药炮制学[M].北京:中国中医药出版社,2003:101.
(收稿日期:2020-05-14 修回日期:2020-07-02)
(编辑:胡晓霖)
