甲酸分离辐照稻草中纤维素、木质素和木糖的工艺
2020-10-30武小芬徐远芳王克勤
武小芬 齐 慧 陈 亮 张 勇 徐远芳 邓 明 王克勤
(湖南省农业科学院 湖南省核农学与航天育种研究所 长沙410125)
我国是农业大国,农作物秸秆产量巨大,2016 年可收集农作物秸秆约8.24 亿吨,其中玉米秆、稻草和小麦秆产量位列前三,分别占总量的41.29%、23.23%和18.36%[1]。随着禁烧力度加强,农作物秸秆利用水平持续提高,2016 年综合利用率达81.68%,肥料化、饲料化和基料化利用率分别为47.20%、17.99%和11.79%,原料化和燃料化利用率仅为2.47%和2.23%[2-3]。因此,目前秸秆利用方式还是以农用产品为主,而秸秆木质纤维素含量丰富,可开发多种高品位生物燃料和化学品,提高其附加值。
稻草中纤维素、半纤维素和木质素含量分别为 33.8%~39.4%、 18.6%~26.3% 和 11.8%~28.5%[4-8],将这3种组分高效分离并改性利用,可大幅提高稻草利用率和经济价值。目前,稻草中木质纤维素的分离方法有化学法[9]、蒸汽爆破法[10]、离子液体法[11]和有机溶剂法[12-13]等。张保平等[9]采用质量分数72%的硫酸分离稻草中的木质素,室温下反应2 h,木质素产率为9.23%。Jiang等[11]采用离子液体(1-烯丙基-3-甲基咪唑盐酸盐)分离稻草纤维素,稻草经2.5 MPa蒸汽爆破处理25 min 后,采用离子液体分离的稻草纤维素中酸不溶性木质素含量低于0.9%。黄丽君等[12]采用助剂G 与1,4-丁二醇的混合体系,以浓硫酸和乙酸为催化剂,160 ℃下保温1 h,木质素得率为16.02%。Krishania 等[14]采用硝酸、氢氧化钠和次氯酸钠依次水解以及H3PO4分步沉淀分离稻草组分,100 g 稻草可制备13.8 g 结晶木糖,同时纤维素、木质素和二氧化硅的回收率分别为26.01%、6.21%和10.11%。这些方法存在化学法试剂用量大,溶剂不易回收;离子液体价格贵;高沸醇分离温度高等问题,均不利于稻草木质纤维素的高效分离。
甲酸是一种价格低廉、沸点较低(100.8 ℃)的有机酸,它通过断裂木质素β-O-4 键和降解半纤维素使其溶解,从而保留纤维素,实现三者的分离。甲酸分离法可在常压较低温度下进行,溶剂可回收循环利用[15-16]。朱盛伟等[17]采用甲酸分离缅甸黄花梨木质纤维素(88%甲酸,110 ℃,2 h),纤维素得率为89.56%,木质素纯度为90%。武小芬等[18]采用辐照结合甲酸分离玉米芯纤维素、木质素和木糖,发现辐照处理有利于提高甲酸分离木质纤维素的效果。因此,本文系统研究吸收剂量、反应温度、反应时间对甲酸分离稻草纤维素、木质素和木糖的影响,确定辐照协同甲酸分离稻草木质纤维素的最佳工艺,为稻草全组分的高效利用提供参考。
1 材料与方法
1.1 原料与试剂
稻草收割于湖南省农业科学院水稻研究所,晒干后装入编织袋中,储存于阴凉干燥环境中备用。甲酸(质量分数88%)、硫酸(质量分数98%)为分析纯,购自国药集团上海化学试剂有限公司;葡萄糖、木糖纯度大于99%,购于美国Sigma 公司;试验用水为去离子水。
1.2 仪器
60Co 辐照装置(源强3.03×1016Bq,湖南省核农学与航天育种研究所);恒速搅拌器(JJ-6,江苏金仪仪器科技有限公司);电热恒温水浴锅(DZKW-s-4,北京市永光明医疗仪器有限公司);立式压力蒸汽灭菌锅(YXQ-50SII,上海博讯实业有限公司医疗设备厂);旋转蒸发仪(RE-2000B,上海亚荣生化仪器厂);紫外分光光度计(BlueStar A,北京莱伯泰科仪器股份有限公司);高效液相色谱(UltiMate 3000,美国赛默飞世尔科技有限公司);纯水系统(Eco-S15,上海和泰仪器有限公司)。
1.3 辐照处理及粉碎
将稻草装入金属辐照箱中,于室温下进行动态辐照处理,吸收剂量分别为200 kGy、400 kGy、600 kGy、800 kGy,0 kGy 为未经辐照处理的对照组。处理后样品粉碎,收集通过0.425 mm 筛网的粉末,装入自封袋中备用。
1.4 组分分析
水溶性组分的测定:称取2.0 g 样品于三角瓶中,加入60 mL蒸馏水,50 ℃水浴反应2 h、搅拌转速130 r/min,反应结束后抽滤,滤渣用少量蒸馏水冲洗3次,105 ℃烘干至恒重,即为滤渣绝干质量。合并滤液和冲洗液,定容至100 mL,分析水溶性组分中葡萄糖、木糖、葡聚糖和木聚糖含量,水溶性组分含量计算见式(1)。

水溶性组分中葡萄糖和木糖含量的测定:取1 mL定容后的滤液,过0.45 μm滤膜后,采用高效液相色谱法(HPLC)测定葡萄糖和木糖含量,色谱柱Aminex HPX-87H(300 mm×7.8 mm),柱温55 ℃;流动相为0.005 mol/L 的硫酸,流速0.6 mL/min;示差折光检测器,温度45 ℃[18]。
水溶性组分中葡聚糖和木聚糖含量的测定:量取7 mL 定容后的滤液,加入0.25 mL 72%的硫酸,121 ℃反应60 min,冷却后稀释至合适倍数,HPLC测定葡萄糖和木糖含量。
纤维素、半纤维素和木质素含量测定:参照国际可再生能源实验室的标准分析方法(LAP,NREL)[19]。
1.5 甲酸分离辐照处理后稻草纤维素、木质素和木糖
稻草纤维素、木质素和木糖提取率和纯度计算见式(2)~(6)。

称取10.0 g稻草粉置于250 mL直三口烧瓶中,按固液比1∶10 加入88%甲酸溶液100 mL,80~100 ℃水浴反应2~4 h,搅拌转速200 r/min。反应结束后抽滤,获得滤液1和滤渣1,用100 mL 88%的甲酸溶液冲洗滤渣1,再用去离子水冲洗至中性,于60 ℃烘干,即为稻草纤维素。合并滤液1和甲酸冲洗液,60 ℃减压浓缩至近干,加入7 倍体积的去离子水析出木质素,抽滤,获得滤液2和滤渣2,滤渣2 用去离子水洗至中性后60 ℃烘干,即为稻草木质素。滤液2,减压浓缩去除甲酸,定容至200 mL,即为稻草木糖。纤维素、木质素纯度测定参照两步硫酸水解法进行[19]。
1.6 数据处理
数 据 用-x±s 表 示,采 用Excel 2016 和Origin 2019软件进行数据图像处理。采用SAS 8.1进行显著性分析,p<0.05 时认为数据之间存在统计学差异。
2 结果与分析
2.1 辐照处理对稻草组成成分的影响
由表1 辐照处理对稻草组分含量的影响可知,随着吸收剂量的升高,稻草水溶性组分增加,纤维素和木聚糖含量降低,木质素含量降低但变化不显著;水溶性组分中葡萄糖和木糖含量增加,但总量均低于0.14%;水溶性葡聚糖和木聚糖含量分别从0.68%和3.00%(0 kGy)升高至4.68%和8.32%(800 kGy)。由于γ 射线辐照降解属于无规裂解,样品分子量越大,受射线作用的概率越高,因此,分子量较高的纤维素和半纤维素容易受到射线攻击,降解成低聚糖,而低聚糖进一步降解为单糖的概率相对较低[20-21]。所以,辐照处理后稻草水溶性组分中低聚糖含量显著增加,而单糖含量总体较低。

表1 辐照处理对稻草组分含量的影响Table 1 Effect of irradiation on the content of rice straw components (%)
2.2 吸收剂量对甲酸分离稻草纤维素、木质素和木糖的影响
图1为吸收剂量对甲酸分离稻草纤维素、木质素和木糖的影响。由图1(a)可知,随着吸收剂量的升高,纤维素提取率先增加后降低,200 kGy时达到最大值85.51%,而200~400 kGy 差异不显著;木质素提取率也呈先增后减趋势,600 kGy时达到最大值49.15%,400~800 kGy范围内差异不显著。由于高剂量辐照后稻草纤维素和木质素含量降低、且结构破坏严重[22],使得甲酸分离时部分纤维素和木质素发生降解,从而导致纤维素和木质素提取率随吸收剂量的升高而降低。木糖提取率随吸收剂量的升高呈增加趋势,800 kGy时达到最大值78.44%,由于辐照处理对木聚糖的降解显著,同时甲酸有利于木聚糖水解为木糖[17];由图1(b)可知,400 kGy剂量辐照处理后的稻草经甲酸分离的纤维素和木质素纯度最高,分别为57.12%和78.06%,纤维素纯度在200~600 kGy 无显著差异,木质素纯度在400~800 kGy 无显著差异。因此,从分离效果和辐照成本综合考虑,选择400 kGy剂量辐照处理的稻草进行后续试验。

图1 吸收剂量对甲酸分离稻草纤维素、木质素和木糖的提取率(a)和纯度(b)的影响a,b,c,同一系列不同字母表示存在显著差异(p<0.05)(甲酸质量分数88%,温度90 ℃,时间3 h)Fig.1 Effects of absorbed dose on extraction rate(a)and purity(b)of cellulose,lignin,and xylose in rice straw a,b,c,there are significant differences in the same series with different letters(p<0.05)(formic acid mass fraction of 88%,temperature of 90 ℃,and reaction time of 3 h)
2.3 反应温度对甲酸分离稻草纤维素、木质素和木糖的影响
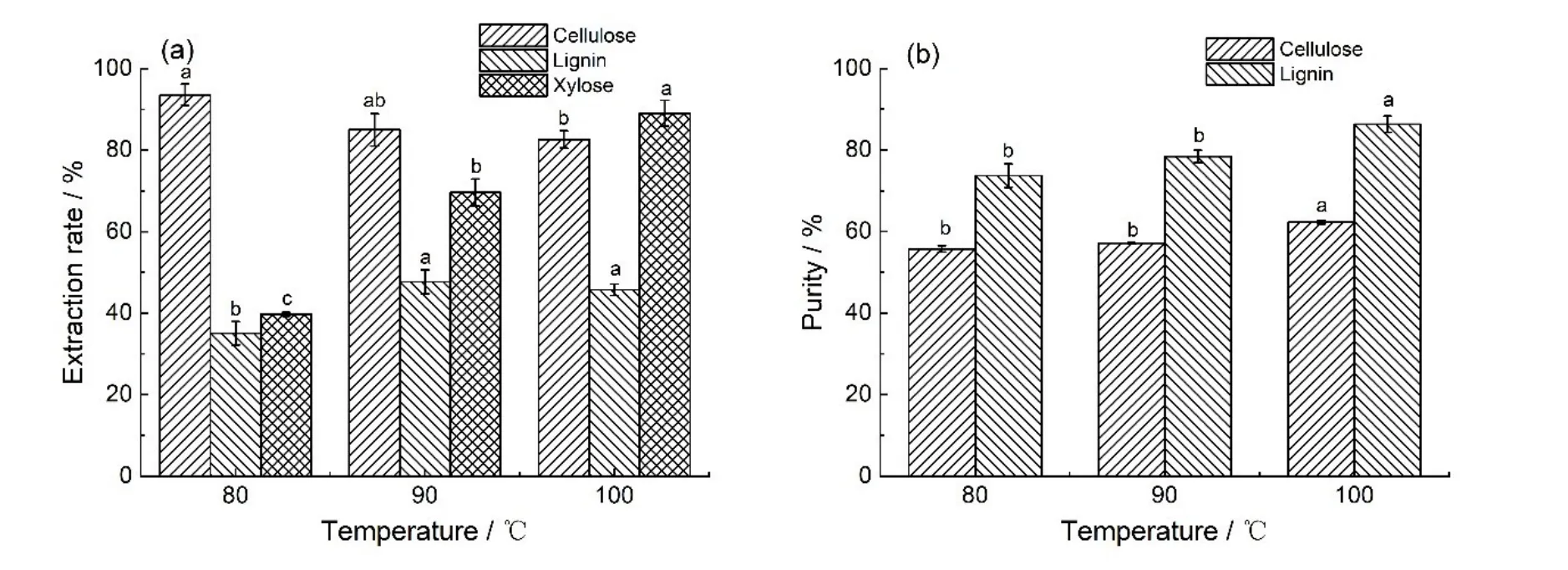
图2 反应温度对甲酸分离稻草纤维素、木质素和木糖的提取率(a)和纯度(b)的影响a,b,c,同一系列不同字母表示存在显著差异(p<0.05)(吸收剂量400 kGy,甲酸质量分数88%,反应时间3 h)Fig.2 Effects of temperature on extraction rate(a)and purity(b)of cellulose,lignin and xylose in rice straw a,b,c,there are significant differences in the same series with different letters(p<0.05)(absorbed dose of 400 kGy,formic acid mass fraction of 88%,and reaction time of 3 h)
以400 kGy剂量辐照处理的稻草为材料,研究温度对甲酸分离稻草纤维素、木质素和木糖的影响,结果如图2所示。由图2(a)可知,随着反应温度的升高,纤维素提取率降低,80 ℃提取率最高为93.59%;木质素提取率先升高后降低,90 ℃达到最大值47.68%,当温度从90 ℃升高至100 ℃,纤维素和木质素提取率变化不显著。木糖的提取率随温度的升高显著增加,提取温度为100 ℃时达到最大值89.02%,因为高温下纤维素和半纤维素水解反应更易进行,所以100 ℃分离会导致纤维素提取率降低和木糖提取率升高[23]。由图2(b)可知,随着温度的升高,纤维素和木质素的纯度均提高,100 ℃时达到最大值,分别为62.30%和86.35%。因此,对于400 kGy 剂量辐照处理的稻草,甲酸分离纤维素、木质素和木糖的最佳温度为100 ℃。
2.4 反应时间对甲酸分离稻草纤维素、木质素和木糖的影响
图3 为不同反应时间对甲酸分离400 kGy 剂量辐照处理稻草中纤维素、木质素和木糖的影响。
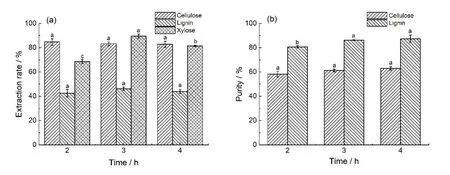
图3 反应时间对甲酸分离稻草纤维素、木质素和木糖的提取率(a)和纯度(b)的影响a,b,c,同一系列不同字母表示存在显著差异(p<0.05)(吸收剂量400 kGy,甲酸质量分数88%,反应温度100 ℃)Fig.3 Effects of temperature on extraction rate(a)and purity(b)of cellulose,lignin and xylose in rice straw a,b,c,there are significant differences in the same series with different letters(p<0.05)(absorbed dose of 400 kGy,formic acid mass fraction of 88%,and reaction temperature of 100 ℃)
由图3(a)可知,随反应时间延长,纤维素提取率下降,但无显著差异;木质素和木糖提取率先升高后降低,反应3 h均达到最大值,分别为46.18%和89.52%。图3(b)显示,随反应时间的延长,纤维素和木质素纯度均升高,但当时间从3 h延长至4 h,纤维素和木质素的纯度增加不显著。在甲酸分离木质纤维素组分过程中,增加反应时间有利于木质素充分溶解于甲酸溶液,半纤维素降解为木糖,但反应时间过长,会造成木质素和木糖的降解,纤维素水解成葡萄糖的含量升高[24]。因此,3 h 为甲酸分离经400 kGy 剂量辐照处理稻草纤维素、木质素和木糖的最佳反应时间。
2.5 甲酸分离的稻草纤维素、木质素和木糖的组成和结构分析
400 kGy 剂量辐照处理的稻草,经88%的甲酸,100 ℃条件下反应3 h,分离获得稻草纤维素、木质素和木糖样品。稻草纤维素中纤维素纯度为61.26%,木聚糖、木质素和灰分含量分别为2.01%、3.20%和19.90%;稻草木质素中木质素纯度为86.19%,其中纤维素、木聚糖和灰分含量分别为1.66%、0.81%和3.36%。分离获得的木糖组分中木糖浓度为7.04 g/L,此外,纤维二糖、葡萄糖和阿拉伯糖浓度分别为0.16 g/L、0.07 g/L 和0.77 g/L。
甲酸分离获得的稻草纤维素和木质素傅里变换叶红外光谱(FTIR)如图4 所示。由图4 可知,3 338 cm-1为-OH伸缩振动,1 714 cm-1为非共轭C=O伸缩振动。1 618 cm-1、1 513 cm-1、1 424 cm-1为芳香环骨架振动,1 315 cm-1、1 260cm-1、1 176 cm-1分别为紫丁香基(S)、愈创木基(G)和对羟基苯基(H)特征吸收峰[18,25],说明分离获得的稻草木质素为GSH型木质素。
稻草甲酸纤维素FTIR(图4)中,3 361 cm-1为-OH伸缩振动,1 717 cm-1为非共轭C=O伸缩振动,1 429 cm-1、1 373 cm-1、1 319 cm-1分别为纤维素-CH2对称弯曲振动、-CH2弯曲振动、C-H对称弯曲振动,而1 160 cm-1、1 103 cm-1、1 068 cm-1分别为纤维素C-O-C不对称伸缩振动、C-O伸缩振动、C=O伸缩振动,899 cm-1为β-1,4-糖苷键特征峰[18,26]。甲酸分离获得的稻草纤维素和木质素均有非共轭羰基伸缩振动吸收峰,可能是因为甲酸分离过程中稻草纤维素和木质素发生了甲酰化修饰[17]。

图4 甲酸分离稻草纤维素、木质素FTIR光谱Fig.4 FTIR spectra of rice straw cellulose and lignin separated by formic acid
3 结论
辐照处理能破坏稻草木质纤维素结构,纤维素、木聚糖和木质素发生降解生成水溶性组分。88%甲酸协同辐照分离稻草纤维素、木质素和木糖的最佳工艺为吸收剂量400 kGy,反应温度100 ℃,反应时间3 h。分离获得的纤维素、木质素和木糖的提取率分别为83.22%、46.18% 和89.52%;纤维素和木质素的纯度分别为61.26%和86.19%。经甲酸分离获得的稻草纤维素和木质素均发生了甲酰化修饰。
