CNTs/TiO2复合材料的制备及光催化性能研究
2020-10-27秦艳利赵鹏羽王雨晴孙博慧
秦艳利,杨 艳,赵鹏羽,王雨晴,孙博慧
(1.沈阳理工大学 理学院,沈阳 110159;2.中国科学院金属研究所 沈阳材料科学国家实验室,沈阳 110016)
水资源严重匮乏、水污染严重是全球性的难题。工业生产等造成的有机废水可谓是水污染的主要原因之一,因此有效的降解有机污染废水相当重要。便捷低廉的新型光催化技术可以对有机废水深度净化,被认为是最有前景的水污染处理方法之一。
1967年,光催化技术由富士岛和本田首次发现,其可以将光能转化为化学能[1]。这种技术利用太阳光驱动一系列化学反应,在反应过程中可产生高氧化性的羟基自由基,能降解大部分有机污染物,不会产生二次污染,可回收再利用、耗能低、反应速度快等优点,受到越来越多的关注。常见的半导体光催化剂有TiO2[2]、ZnO[3]、CdS[4]、WO3[5]、Fe2O3等。其中TiO2相比WO3、Fe2O3等许多半导体材料有更高的光催化活性;比ZnO、CdS等光照吸收更稳定,不易产生光辐射[6]。但TiO2较宽的禁带使其只对紫外光有响应,限制了其在可见光范围的应用;且其光生电子空穴寿命短,复合较快,也影响了光催化效率,因此必须对其改性[7-8]。
碳材料具有的高导电性、大比表面积、高化学稳定性等优点,将其与TiO2复合有利于降低TiO2的光生载流子复合几率,提高其量子效率,并可增强对有机污染物的吸附,进而提高TiO2光催化效率[9-12]。碳纳米管(CNTs)这种独特的碳材料,除拥有这些性能外,还具有大长径比、一维管腔等独特的内在结构,因此表现出特殊的金属或半导体性。将CNTs和TiO2复合,可以将两者的优势结合起来,有效的改善TiO2的光催化效率。目前,CNTs/TiO2已在储氢、光催化、生物传感等领域展开应用研究。吴俊明等[13]用溶胶凝-胶法和低温水热法合成了TiO2/CNTs复合催化剂,研究了不同制备工艺对催化剂活性的影响。Y.Yao等[14]合成的CNTs与TiO2复合的纳米材料,在紫外光下降解苯酚的速率为纯TiO2的2.6倍。Wang等[15]提出当以多壁碳纳米管(MWCNTs)为催化剂的载体时,提高了TiO2反应的比表面积,且TiO2和MWCNTs之间的相互接触具有光化学协同作用。这些研究表明CNTs和TiO2复合可有效提高TiO2在紫外光下的光催化活性,但关于复合材料最佳制备工艺和光催化机理有待于进一步深入研究。
将CNTs 和TiO2复合制备CNTs/TiO2的方法很多,如机械混合[16]、溶胶-凝胶法[14]、化学气相沉积沉积[17]、电子溅射[18]等。溶胶-凝胶法具有定量化准确、方便的优点,但也存在TiO2在CNTs表面分布不均和焙烧过程中TiO2容易团聚的问题[15,19]。进一步分析和研究溶胶-凝胶法制备CNTs/TiO2的工艺参数,得到最佳催化活性的CNTs/TiO2复合物是必要的。本文以钛酸四丁酯为前驱物,利用溶胶-凝胶法制备不同TiO2含量的CNTs/TiO2复合光催化材料,以甲基橙为目标降解物,研究CNTs/TiO2复合材料的光催化效果,并分析CNTs与TiO2协同增强机理。
1 实验
1.1 试剂
实验主要试剂见表1所示。

表1 实验中的主要原料
1.2 样品制备
1.2.1 TiO2溶胶的制备
以钛酸四丁酯为前驱物,无水乙醇为溶剂,乙酰丙酮为螯合剂,硝酸为抑制剂,制备TiO2溶胶(1mol/L)。具体步骤为:取100g无水乙醇加入180g 用硝酸调节的PH=3的去离子水配成混合溶液A;将340.3g钛酸四丁酯和71g乙酰丙酮在快速搅拌下缓慢加入200g无水乙醇中,形成混合溶液B;然后在快速搅拌下将A溶液用滴定管缓慢加入B溶液中,得到均匀透明的溶胶;最后无水乙醇将溶胶体积补充到1L,即获得1mol/L的TiO2溶胶。获得的溶胶静止陈化24h待用。
1.2.2 CNTs/ TiO2复合材料的制备
取1g CNTs,1.5g 3-磺丙基十四烷基二甲甜菜碱加入400mL去离子水,强力超声4h,离心30min;取离心后CNTs上层悬浮液两份各100mL,分别加入12.5mL 和25mL TiO2溶胶(1mol/L),搅拌后120℃下干燥;然后在真空炉中350℃烧2h,取样品适量测定其结晶温度,继续将样品在真空下以结晶温度烧2h,得到CNTs/ TiO2粉末。样品记为C1、C2。
1.3 分析与表征
通过X射线衍射法(XRD)对样品的物相结构进行标定,设备为德国布鲁克X射线衍射仪;以CuKα射线作为X射线放射源,扫描范围为10~80°(2θ)。用场发射电子显微镜(SUPRA 55 SAPPHIRE)分析样品的微观形貌和结构特征。采用差示扫描量热法(differential scanning calorimetry,DSC)分析材料的结晶温度。
1.4 光催化降解实验
通过监测在距离烧杯上方25cm的紫外光照射(500W 高压汞灯)下,用甲基橙(MO)进行光催化降解实验。将制备好的光催化剂(50mg)分散在装有100mL MO水溶液(10mg/L)的玻璃容器中。在光照射之前,将悬浮液在黑暗中磁力搅拌30min,以实现光催化剂和MO之间的吸附-解吸平衡。然后,在照射期间每10min取4mL悬浮液并离心5min,离心机转速10000rpm。然后取去除了悬浮颗粒的上清液,用紫外-可见分光光度计测定MO的残余浓度。
2 结果和讨论
2.1 物相与结构分析
差示扫描量热法(DSC)是在程序控制温度下,测量样品和参比物的功率差与温度关系的一种技术。利用此分析方法可得到样品的多种热力学和动力学参数。图1为CNTs/TiO2复合材料的DSC曲线。
由图1可知,在样品的DSC曲线上大约450℃出现了一个入热峰,该峰为锐钛矿型TiO2结晶转变峰;在150℃左右出现一个强的吸热峰,表明150℃时样品开始结晶,初始晶型为锐钛矿型;450℃以后开始由锐钛矿型转变为金红石型。
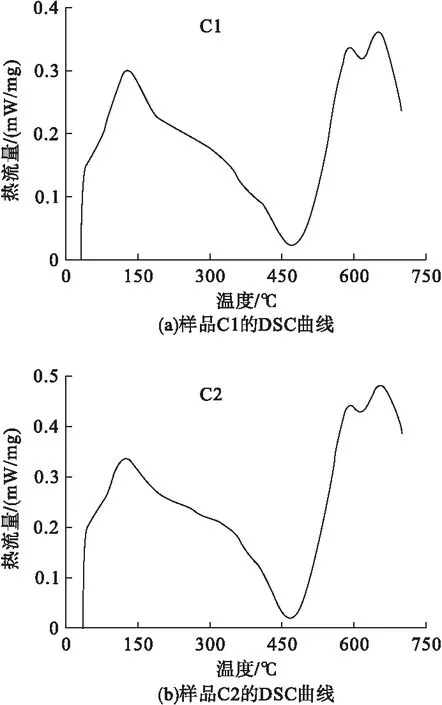
图1 CNTs/TiO2复合材料的DSC曲线
TiO2有金红石、锐钛矿、板钛矿三种晶型,其中板钛矿是自然存在相,合成相当困难,金红石和锐钛矿型较易合成。一般而言,锐钛矿型比金红石型的光催化活性好,催化效果更好。因此,选择450℃为样品的煅烧温度,对前期处理过的样品进行进一步的真空煅烧。
图2是样品的XRD衍射图。

图2 CNTs及CNTs/TiO2复合材料的XRD图
由图2可知,在样品C1和C2的XRD图谱中明显看出锐钛矿TiO2的衍射峰,对应于(101)、(004)、(200)、(105)、(211)、(204)、(116)、(220)和(215)晶面(JCPDS file No.21-1272),无其他杂质峰。表明TiO2结晶度良好,且CNTs的复合未明显改变TiO2的晶相。C2相比于C1各个衍射峰的强度增强,表明与CNTs结合的TiO2的含量增多。未在样品C1、C2的XRD图中观察到CNTs的衍射峰;分析原因,一方面可能是CNTs在2θ=26°处的特征衍射峰被锐钛相TiO2的2θ=25.4°的特征峰掩盖,CNTs的2θ=43.4°的特征衍射峰太弱,另一方面由于CNTs的含量低,其衍射强度低,未被仪器检测到。
拉曼光谱是研究纳米复合材料的晶体结构和表面缺陷的一个有效工具。图3是CNTs/TiO2复合材料的拉曼光谱。

图3 CNTs及CNTs/TiO2复合材料的拉曼光谱
由图3可知,样品C1和C2在144cm-1处有显著的峰,对应于锐钛矿TiO2的衍射峰,其中样品C2在394cm-1、513cm-1、637cm-1也分别存在锐钛矿TiO2的特征峰,再一次表明制备的样品中的TiO2均为锐钛矿型,与XRD的结果一致。另外,在所有样品中CNTs具有明显的D峰(1354cm-1)和G峰(1587cm-1)。D峰表现的是CNTs的结构缺陷,是由sp3杂化碳原子结构中C-C键的振动引起的;G峰是吸收峰,是sp2杂化碳原子结构中C-C键的振动引起的;D峰和G峰的峰强比表示CNTs微观结构的石墨化程度[20]。经计算,C1和C2的D峰和G峰的峰强比无明显差异(分别为1.02和1.01),表明两者的石墨化程度相当。
2.2 形貌分析
图4为复合前的CNTs(图4a)和复合后样品的宏观图(图4b和图4c)。
从图4可看出,当加入TiO2溶胶的量增多时,样品表面发生变化,由黑色明显变为灰色,说明有白色的TiO2生成。对其进行SEM表征,结果如图5所示。

图4 CNTs及CNTs/TiO2复合材料的宏观图

图5 CNTs及CNTs/TiO2复合材料的SEM图
由图5b、图5c可知,样品C1在低倍下表现为块状,将其在高倍下放大,发现不均匀的块体是由CNTs和TiO2团聚组成,其中有部分CNTs和TiO2的聚合物裸露在表面上,未观察到明显的颗粒状的TiO2。由图5d、图5e可知,样品C2中存在大量的球状TiO2颗粒,说明适当增加TiO2溶胶加入量时,减少了样品的团聚。TiO2和CNTs的质量百分比是影响CNTs/TiO2复合材料的重要因素之一。
2.3 光催化活性分析
样品C1和C2的吸收光谱如图6所示。
从图6中可以看出,由于复合材料C1和C2的光催化降解作用,在464nm处的MO吸收峰的强度随着时间推移逐渐降低,表明甲基橙分子逐渐被催化剂降解。

图6 样品C1和C2降解MO水溶液的吸收光谱图
在紫外-可见吸收光谱中,吸收峰的强度和溶液的浓度成线性关系。因此可根据朗伯-比尔定律计算复合材料的光催化降解效率R(%)[20]。
式中:A是每个照射时间的MO浓度;A0表示初始时MO的起始浓度。由此可得到其光催化降解曲线图,如图7所示。

图7 CNTs/TiO2复合材料的降解图
由图7可知,在暗处理时,样品C1、C2均表现出较强的吸附性能,其中C1的吸附性能更好,可能与CNTs占比较多有关。比较发现,C2比C1表现出更大的光催化效率,具有更优异的光催化性能。在紫外灯照射30min后,C1和C2的甲基橙的降解率分别约为85%和96%,相比于文献[13-15]对纯TiO2光降解率的研究,光催化效率有明显提高。这归因于CNTs和TiO2存在的相互协同作用,CNTs良好的导电性使光生电子空穴对的复合减少以及延长了电子空穴对寿命;另一方面,其大的比表面积提供了更多的反应活性位点,增加了TiO2对紫外光的利用率[21-25]。
3 结论
利用溶胶-凝胶法制备了不同TiO2百分比的CNTs/ TiO2复合光催化剂C1、C2,在紫外灯照射下对其进行了光催化降解实验,结果表明CNTs/ TiO2复合材料具有优异的光催化效果:(1)CNTs/ TiO2制备时的最佳煅烧温度为450℃,在此温度下制备的样品中TiO2为锐钛矿型;(2)适当增加TiO2溶胶的加入量时,减少了样品的团聚,有利于光催化效果的提升;(3)C2(96%)比C1(85%)表现出更高的光催化效率,TiO2和CNTs的质量百分比是影响光催化效果的重要因素。
