基于AGEs/RAGE/NF-κB通路探讨老年性骨质疏松症发病机制
2020-10-26孙菁朱媛媛郭海英沈沐瑶李佳洋
孙菁 朱媛媛 郭海英 沈沐瑶 李佳洋
南京中医药大学第二临床医学院,江苏 南京 210023
骨质疏松症(osteoporosis,OP)是一种慢性、全身性疾病,随着骨矿物含量的减少而增加骨折风险,并直接导致日常生活能力(ADL)和生活质量(QOL)降低[1]。随着人口老龄化程度的不断加剧,到2016年中国老年人骨质疏松症患病率为36%,骨质疏松及其伴随的疼痛与骨折高风险已成为我国面临的重要公共卫生问题[2]。预计至2050年,我国骨质疏松性骨折患病人数将达599万,相应的医疗支出高达1 745亿元[3]。 其中老年性骨质疏症(senile osteoporosis,SOP)是世界范围内常见的老年慢性疾病,衰老是SOP无法避免的高危因素,其发病率随着年龄增长呈现显著上升趋势[4]。
现阶段,SOP的机制研究主要从常规骨代谢信号通路、机械应力、细胞因子以及非编码RNA等方面考虑。近年来体内糖基化终末产物(advanced glycation end products,AGEs)与阿尔茨海默症、动脉粥样硬化性疾病、帕金森病之间的相关性已经得到证实[5],AGEs在衰老退行性疾病的发病机制中起着重要作用,但其与老年性骨质疏松症发病的关系尚不明确且具体作用机制不祥。最新研究发现,AGEs的堆积能激活核因子kappa B(NF-κB)信号通路并诱发氧化应激炎性反应(oxidative stress,OS),被认为是导致衰老相关的组织退化的一种潜在机制。本文旨在根据已知的AGEs与其受体RAGE的最新研究进展,基于NF-κB通路探讨SOP的可能发病机制。
1 AGEs及受体RAGE的概述
高级糖基化终产物是由还原糖的羰基以及蛋白质、脂类或核酸中的游离氨基之间的非酶促反应形成的一组异构化合物,以棕色、荧光和聚合倾向为特征[6]。AGEs种类繁多,大体包括内源性(自身体内合成)和外源性(饮食或吸烟摄入)。其中内源性AGEs的形成是自然新陈代谢的结果,是一个不可避免的过程,但高水平的AGEs累积在组织和循环中具有一定的致病性[7-8]。AGEs容易被存在于不同细胞类型上的AGEs受体(RAGE)特异性识别,目前已知的具有不同特性和质量的AGEs结合蛋白包括AGE-R1、AGE-R2、AGE-R3、Scr-II、CD 36和RAGE[9]。其中RAGE作为研究最多的晚期糖基化终产物受体,是细胞对AGEs负荷反应的主要上游调节因子。哺乳动物中表达的RAGE是一种多配体受体,属于免疫球蛋白超家族(Ig)的45kDa跨膜受体,具有高电荷的细胞质结构域,也可用作细胞粘附分子,在大多数组织中的基础表达较低[10]。 RAGE与AGEs之间的相互作用主要引起促炎反应,慢性低级、无菌性炎症随着AGEs增长而增加,可导致线粒体功能障碍或细胞衰老,成为衰老的潜在重要促成因素[11]。
2 AGEs/RAGE对骨质的影响
AGEs长期以来被认为是促进宿主细胞死亡和器官损伤的强毒性分子,有研究[12]表明AGEs能抑制MSCs的增殖,诱导细胞凋亡,阻止同源分化为脂肪组织、软骨和骨,提示AGEs在肌肉骨骼疾病的发病机制中起着有害的作用。据报道[13],经AGEs修饰的胶原能促进细胞内活性氧的释放,干扰成骨细胞与基质的粘附,抑制成骨细胞的分化和增殖。AGEs可以破坏骨基质蛋白的结构完整性,I型胶原蛋白占骨基质的85%,是骨中最丰富的蛋白质,寿命长,易受AGEs变化的影响,骨蛋白的糖基化能同时影响骨重塑过程、破骨细胞骨吸收、成骨细胞骨形成的生长过程[11]。研究[14]结果表明,经AGEs介导的交联蛋白溶解度降低,导致骨组织的生物力学性能改变,如胶原硬度的增加,非钙化胶原基质在骨中的变性随AGEs的增加而增加,这类骨胶原变性与非酶胶原交联有关,与骨的强度和韧性有关。AGEs导致ALP活性和I型胶原蛋白水平降低,成骨特异性基因和蛋白质[Runx2、Osterix、ALP、骨桥蛋白(OPN)、I型胶原蛋白和骨钙素(OCN)]表达下调,骨形成减少[15]。
3 AGEs/RAGE/NF-κB诱发骨质疏松的可能机制
3.1 衰老致体内AGEs堆积激活NF-κB诱发OS
衰老是SOP无法避免的高危因素,导致体内自由基氧化加快,同时体内的还原剂、抗氧化酶等抗氧化剂含量不足,不能限制AGEs的前体水平,内源性AGEs不能通过细胞外蛋白水解和AGER 1介导的细胞内摄取和降解,导致AGEs在体内堆积,引发机体蛋白质和葡萄糖非酶糖基化(nonenzymatic glycosylation,NEG),这种与能量代谢有关的生物化学不良反应诱发OS,是SOP的重要发病机制[16-18]。在衰老等因素刺激下,AGEs形成加快。当体内AGES堆积的时候,RAGE会随之上调,导致OS和炎症增加。
AGEs与受体RAGE结合可激活多种细胞内信号级联,如Janus激酶/信号转导和转录激活因子(JAK/STAT),p38丝裂原活化蛋白激酶(P38MAPK)、细胞外信号调节蛋白激酶1和2(ERK 1/2)与c-jun N端激酶(JNK)可激活转录因子NF-κB,随后转录一系列涉及不同生物系统的基因,导致细胞因子、生长因子和粘附分子的表达增加,如白细胞介素1(IL-1)、白细胞介素6(IL-6)和肿瘤坏死因子(TNF-α),并进一步激活NF-κB信号转导通路[8, 12],使炎症或促炎信号持续存在。此外,AGEs-RAGE相互作用还通过烟酰胺腺嘌呤磷酸二核苷酸(NADPH)氧化酶途径刺激活性氧(ROS)的生成,促进OS等炎性反应。当ROS水平升高时,AGEs/ROS的恶性循环促进更多脂质和葡萄糖的氧化,加速体内AGEs的形成[19],激活更多NF-κB,进一步加速OS发生[20-21],由此形成AGEs-Ros-OS-AGEs的恶性循环。见图1。
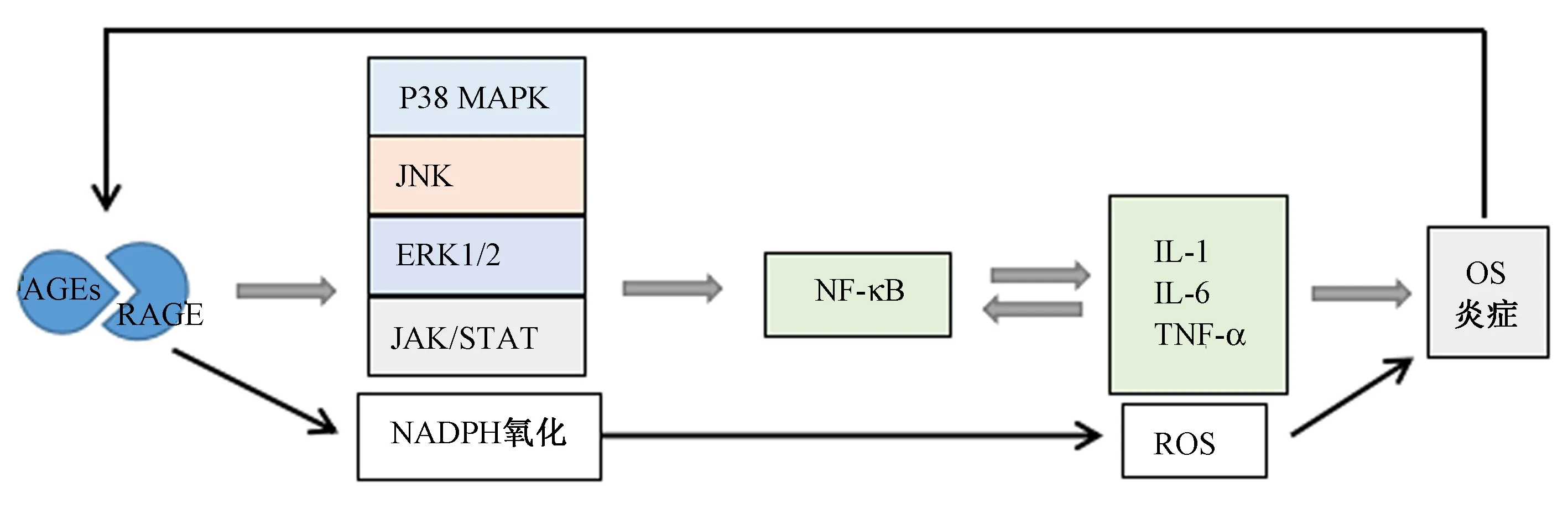
图1 AGEs/RAGE激活NF-κB信号转导通路Fig.1 AGEs/RAGE activates NF-κB signal transduction pathway
3.2 NF-κB通路促进破骨细胞生成
核因子κB受体活化因子(receptor activator of NF-κB,RANK)是核因子κB受体活化因子配体(RANKL)的受体,RANKL与破骨细胞表面的RANK结合,激活破骨细胞(osteoclast,OC)、破骨前体细胞内的核因子kappa B(NF-κB)信号通路,肿瘤坏死因子受体相关因子(TNF receptor-associated receptor,TRAFs)会迅速结合RANK胞质区,当RANK与TRAF6结合后,激活NF-κB诱导激酶,并进一步磷酸化IκB激酶(IKKβ),IKKβ可将IκBα磷酸化,使其发生聚泛素化并被 26S 蛋白酶体降解,该过程伴随着 p65/p50二聚体向核内转移,导致破骨细胞转录因子激活,如活化T细胞核因子(nuclear factor of activated T-cells,cytoplasmic 1,NFATc1),该因子与其他转录因子相互作用后,可诱导抗酒石酸酸性磷酸酶(TRAP)、组织蛋白酶K(cathepsin K,CatK)等破骨细胞特异性基因的表达,导致破骨细胞大量分化并促进其成熟[22-25]。破骨细胞沿骨表面移动,且不断聚集以扩大吸收陷窝,直至骨吸收完成。
正常情况下NF-κB位于胞质中并与其抑制蛋白IκB紧密结合,当细胞受到OS炎性因子等因素刺激时,被激活的NF-κB数量增加,NF-κB可从胞质转移到胞核中,激活NF-κB信号转导通路,促进破骨细胞的形成与活化[26],令骨吸收增加。见图2。
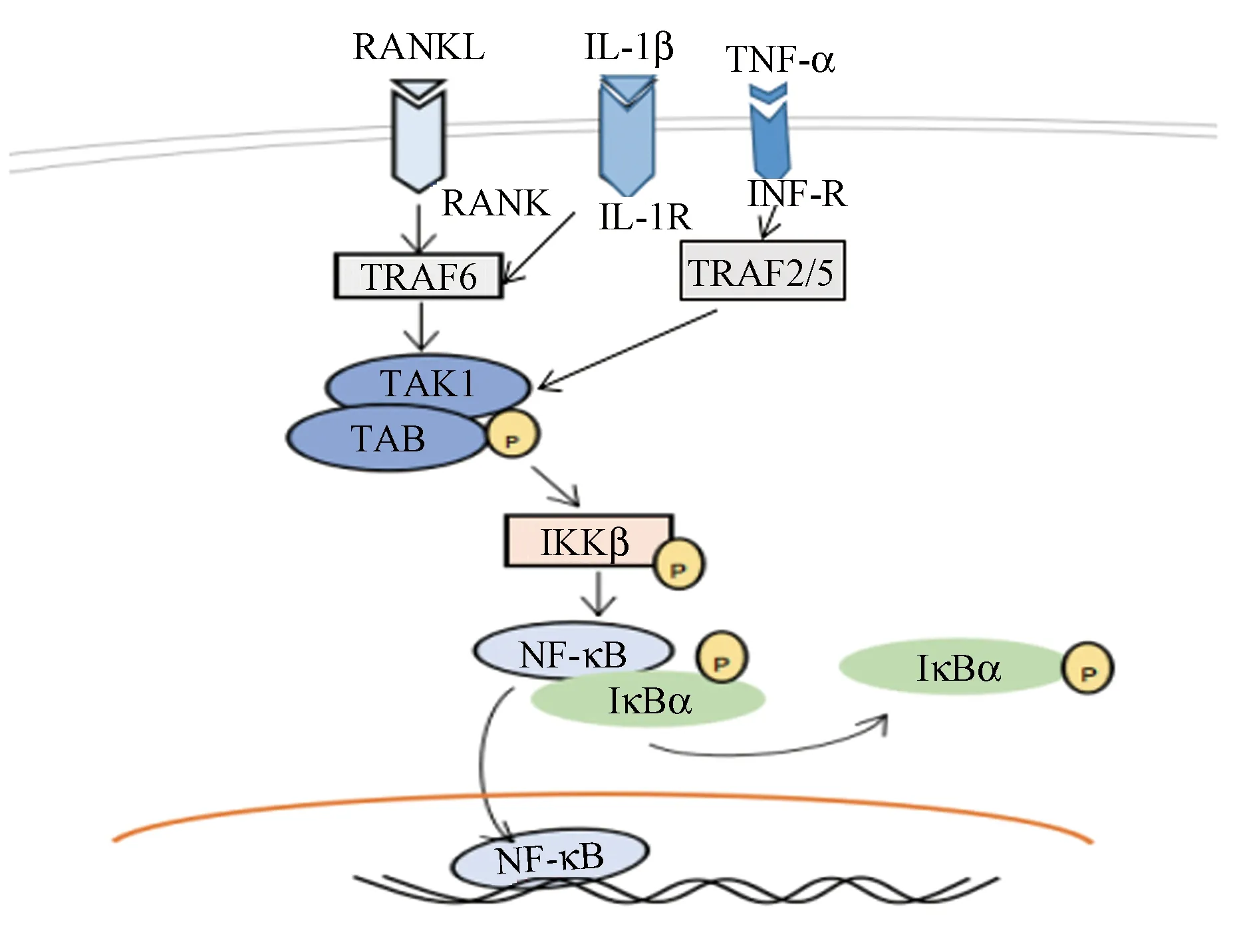
图2 NF-κB信号转导通路Fig.2 NF-κB signal transduction pathway
3.3 NF-κB通路调控破骨细胞自噬
NF-κB信号通路作为破骨细胞形成的主要通路,同时也是细胞自噬的关键通路。自噬是细胞的一种自我消化行为,是真核细胞吞噬自身细胞质蛋白或细胞器的主要代谢过程,以满足细胞新陈代谢和更新细胞器的需求[27]。NF-κB在复杂的细胞因子网络中起着中心调节作用,在细胞增殖、分化、凋亡和自噬中扮演重要角色。哺乳动物NF-κB家族成员分别为p50/p105(NF-κB1)、p52/p100(NF-κB2)、c-Rel、RecB、p65(RecA)[26]。研究[25]表明自噬在一系列退行性疾病中至关重要,自噬相关蛋白参与了破骨细胞的分化、形成过程,对维持骨骼强度,预防骨质疏松的发生发挥着至关重要的作用。也有研究[28]发现TNF-α激活NF-κB可以抑制细胞自噬,而抑制NF-κB活性则明显改善受阻细胞的自噬水平,但两者间具体的关系尚无明确的定论,有待进一步探索。
研究[29-31]表明,一般情况下当机体衰老时,细胞自噬水平下降,破骨细胞活性降低,骨吸收被抑制;但在氧化应激条件下,ROS在线粒体中大量蓄积,引起线粒体膜脂质过氧化,导致线粒体功能异常,进而激活自噬;自噬激活又可通过降解过氧化氢酶(抗氧化剂)反过来增加细胞内ROS水平,最终形成自噬-ROS的恶性循环,进一步加剧机体氧化应激炎性反应,破骨细胞需要通过自噬以适应氧化应激环境,所以破骨细胞在OS状态下始终维持高水平的自噬。体外细胞实验[32]发现,破骨细胞自噬被抑制后,NFATc1、TRAP、CatK 等破骨细胞特异性基因的表达也显著降低,提示自噬能诱导破骨细胞的分化和形成,作为一种保护性机制维持其在氧化应激状态下的细胞功能,促进骨吸收。
故在衰老状态下,虽从理论上讲自噬应减弱,在一定程度上可以抑制破骨细胞自噬,抑制骨吸收,但同时,成骨细胞的自噬也受到抑制,成骨亦减少。另外在衰老情况下,AGEs与RAGE结合促进机体氧化应激反应,并进一步促进细胞自噬,促进骨吸收;亦可通过激活NF-κB通路,促进骨吸收。骨吸收程度远大于骨形成,引发骨质疏松。见图3。
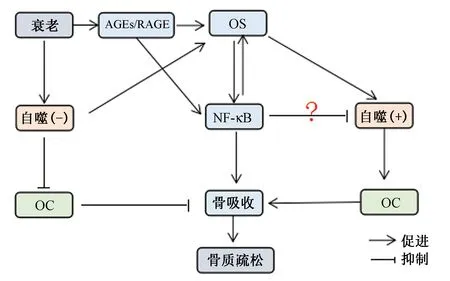
图3 老年性骨质疏松的可能发病机制图Fig.3 Possible pathogenesis of senile osteoporosis
4 小结
衰老后体内AGEs的堆积及其经肾脏自然清除率的降低为SOP自然发病的根本原因,AGEs进一步与其受体RAGE反应诱发的氧化应激反应可作为SOP发病的催化剂,而NF-κB信号通路则是SOP发生的关键通路,能从多个方面促进破骨细胞的分化及形成,促进骨吸收。首先,在自然条件下,RANKL/RANK/NF-κB是破骨细胞形成的经典通路,NF-κB活性增加,促进破骨细胞形成,则能进一步促进骨吸收;其次,NF-κB不仅仅作为促进破骨细胞形成的必要通路,同时也是炎症因子的转导通路,体内AGEs与RAGE结合可经过多途径激活NF-κB,NF-κB活性增强,体内炎症因子亦增多,促进机体的炎性反应与衰老,形成恶性循环;另外,NF-κB可以通过调节破骨细胞自噬,促进破骨细胞更新换代,加速骨吸收。
综上所述,本文基于现有的文献资料分析了自然衰老情况下老年性骨质疏松症的可能发生机制,但目前只是理论研究,后续有必要开展一系列实验来证实该作用机制,比如从抗氧化应激角度或抑制NF-κB活性的角度来治疗老年性骨质疏松症。
