贝伐珠单抗联合紫杉醇、卡铂治疗复发性卵巢癌的疗效及对血清糖类抗原125、人附睾蛋白4 水平的影响
2020-10-17李丽华宋俊莉杨幸繁
李丽华,宋俊莉,杨幸繁
许昌市妇幼保健院妇科,河南 许昌4610000
卵巢癌是女性常见的恶性肿瘤,由于早期病情隐匿,大多数患者确诊时已处于中晚期,较高的发病率、病死率成为威胁女性健康的主要原因[1]。研究显示,卵巢癌的治疗手段包括手术、化疗、放疗、免疫生物治疗等,但受早期诊断局限性、化疗药物反应性的影响,根治效果不佳;早期卵巢癌的复发率为19%,而晚期卵巢癌患者的5 年复发率高达70%;对于复发性卵巢癌,二线化疗方案效果不明显,靶向药物成为其治疗的研究热点[2]。贝伐珠单抗是靶向性治疗中抗血管生成的代表性药物,主要通过阻断血管内皮生长因子(vascular endothelial growth factor,VEGF)与其受体结合而发挥作用[3]。研究显示,贝伐珠单抗联合化疗能够使卵巢癌患者在中位无进展生存时间(progression-free survival,PFS)明显获益,但在中位总生存时间(overall survival,OS)上的优势尚不显著[4]。早期监测、病情评估对明显改善复发性卵巢癌患者的预后具有重要意义。血清糖类抗原125(carbohydrate antigen 125,CA125)、人附睾蛋白4(human epididymis protein 4,HE4)是临床常用的肿瘤标志物,二者联合检测可作为卵巢癌的理想监测指标[5-6]。本研究对贝伐珠单抗联合紫杉醇、卡铂治疗复发性卵巢癌的疗效及对血清CA125、HE4 水平的影响进行探讨,旨在为提高复发性卵巢癌的临床治疗效果及改善预后提供理论依据,现报道如下。
1 资料与方法
1.1 一般资料
选取2014 年1 月至2017 年3 月许昌市妇幼保健院收治的复发性卵巢癌患者。纳入标准:①年龄在30 岁以上;②经组织病理学检查确诊为卵巢癌,且于化疗或肿瘤细胞减灭术后经评估疾病缓解,但停药6 个月及以上复查显示卵巢癌复发;③存在至少1 个可测病灶,且为首次复发;④卡氏功能状态(Karnofsky performance status,KPS)评分≥80 分;⑤采取紫杉醇+卡铂(PC)方案或贝伐珠单抗联合PC 方案治疗;⑥临床资料完整。排除标准:①既往有单抗药物治疗史;②合并其他恶性肿瘤;③伴有严重的心、肝、肾功能障碍;④对治疗药物过敏;⑤妊娠或哺乳期女性。根据纳入和排除标准,本研究共纳入100 例复发性卵巢癌患者,并根据治疗方案的不同分为观察组(n=53,采取贝伐珠单抗联合PC 方案治疗)和对照组(n=47,采取单纯的PC 方案治疗)。两组患者的年龄、KPS 评分、病理类型等一般资料比较,差异均无统计学意义(P﹥0.05)(表1),具有可比性。
1.2 方法
对照组采取PC 方案治疗,其中,紫杉醇135~175 mg/m2,第1 天,静脉滴注3 h 以上;卡铂AUC5,第2 天,静脉滴注1 h 以上。使用紫杉醇前需进行常规预处理,且做好紫杉醇超敏反应的紧急抢救措施。3 周为1 个治疗周期,连续治疗6 个周期。
观察组在对照组的基础上联合使用贝伐珠单抗10 mg/kg+100 ml 0.9%氯化钠溶液静脉滴注1 h,首次滴注时间为1.5 h,于PC 方案治疗后滴注。3周为1 个周期,共治疗6 个周期。
两组患者于治疗前后均给予常规防过敏、止吐、保护胃黏膜、保肝、维持水电解质平衡等对症治疗,以预防不良反应。每个周期结束后至下一个周期开始前,复查计算机断层扫描(CT)以检测病灶情况。
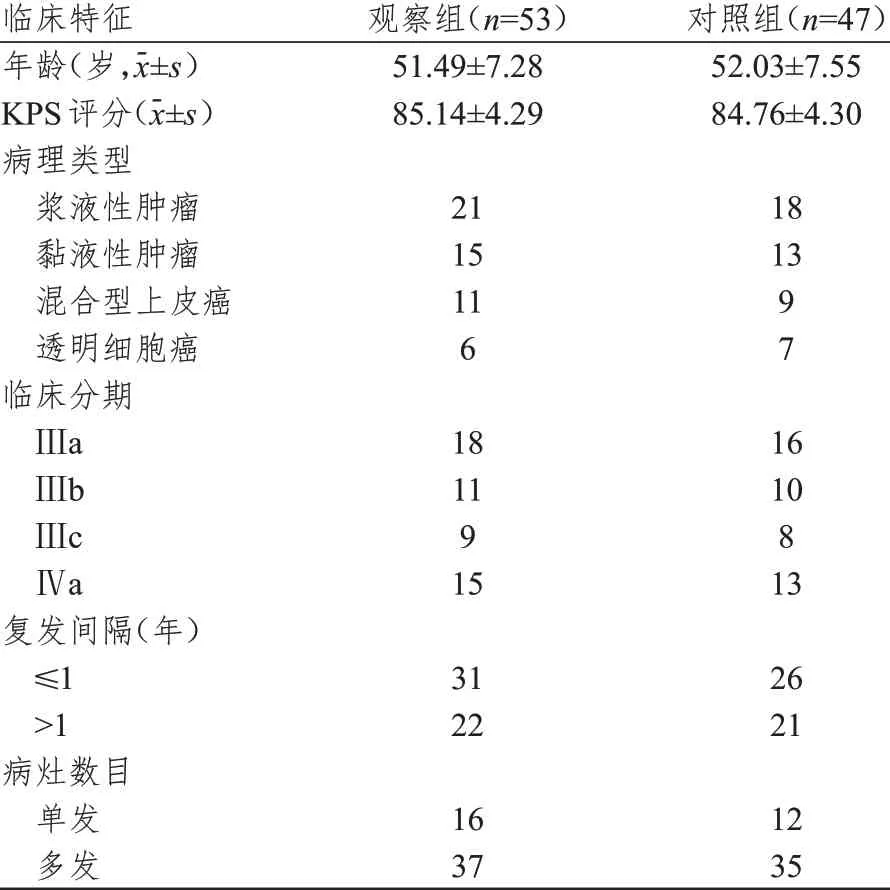
表1 两组患者的临床特征
1.3 观察指标和评估标准
参照实体瘤疗效评价标准[7]评估近期疗效:完全缓解(CR),肿瘤病灶消失且未发现新病灶;部分缓解(PR),肿瘤最大径缩小>30%;疾病稳定(SD),肿瘤最大径缩小﹤30%或增大﹤20%;疾病进展(PD),肿瘤最大径增大超过20%或出现新病灶。客观有效率(objective response rate,ORR)=(完全缓解+部分缓解)例数/总例数×100%;疾病控制率(disease control rate,DCR)=(完全缓解+部分缓解+疾病稳定)例数/总例数×100%。
血清CA125、HE4 水平:于治疗前、治疗后1周内采集患者清晨空腹静脉血5 ml,离心分离后于-80 ℃保存备用。采用罗氏Cobase 601 全自动电化学发光免疫分析仪检测血清CA125、HE4 含量,严格按照说明书步骤进行操作。
分析从化疗之日起3 年内的随访资料(无失访),计算中位OS 和中位PFS。根据世界卫生组织(WHO)制定的抗癌药物常见毒副反应分级评价标准[7]评价不良反应,包括高血压、血小板减少、恶心呕吐、肝功能不全、肾功能不全等。
1.4 统计学分析
采用SPSS 22.0 软件对数据进行统计分析。计量资料以均数±标准差(±s)表示,组间比较采用独立样本t 检验;计数资料以例数和率(%)表示,组间比较采用χ2检验;等级资料的比较采用秩和检验;采用Kaplan-Meier 法绘制生存曲线,组间比较采用Log-rank 检验。以P﹤0.05 为差异有统计学意义。
2 结果
2.1 近期疗效的比较
观察组患者的ORR、DCR分别为67.92%(36/53)、84.90%(45/53),均高于对照组的46.81%(22/47)、63.83%(30/47),差异均有统计学意义(χ2=4.560、5.901,P﹤0.05)。(表2)
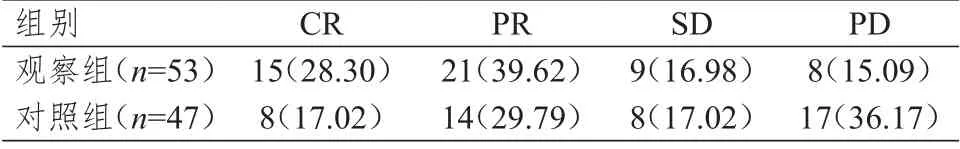
表2 两组患者的近期疗效[n(%)]*
2.2 血清CA125、HE4 水平的比较
治疗前,两组患者的血清CA125、HE4 水平比较,差异均无统计学意义(P﹥0.05);治疗后,两组患者的血清CA125、HE4 水平均低于本组治疗前,差异均有统计学意义(P﹤0.05)。治疗后,观察组者的血清CA125、HE4 水平均明显低于对照组,差异均有统计学意义(t=18.032、10.307,P﹤0.01)。(表3)
表3 两组患者治疗前后的血清CA125、HE4 水平(±s)

表3 两组患者治疗前后的血清CA125、HE4 水平(±s)
指标CA125(U/ml)HE4(pmol/L)时间治疗前治疗后治疗前治疗后观察组(n=53)685.74±56.11 45.20±4.35 280.45±30.78 51.33±7.26对照组(n=47)692.05±57.49 62.26±5.11 282.51±29.86 67.15±8.09
2.3 生存情况的比较
观察组患者的中位PFS、OS 分别为17.64、20.19 个月,分别长于对照组患者的11.23、14.28 个月,差异均有统计学意义(χ2=4.423,5.801,P ﹤0.05)。(图1、图2)
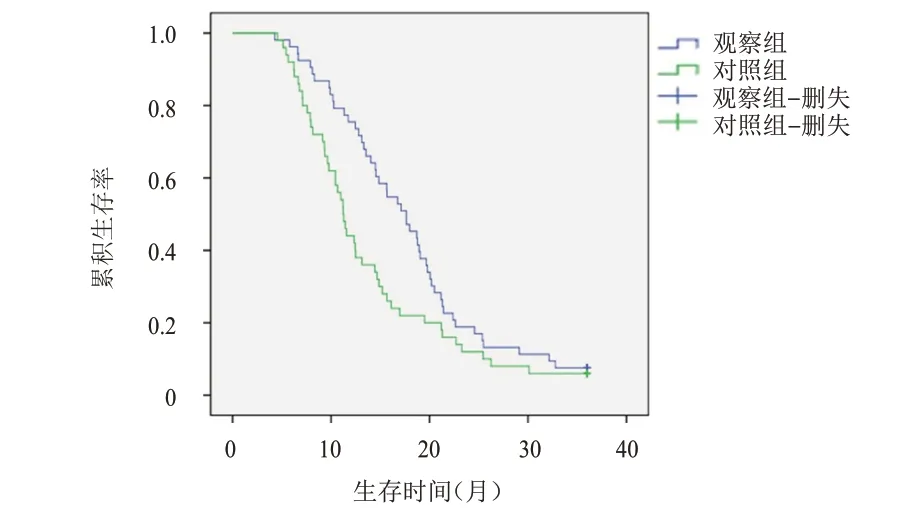
图1 观察组(n=53)和对照组(n=47)复发性卵巢癌患者的无进展生存曲线
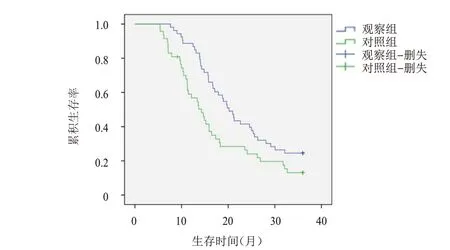
图2 观察组(n=53)和对照组(n=47)复发性卵巢癌患者的总生存曲线
2.4 不良反应发生情况的比较
两组患者发生了不同程度的不良反应,不良反应主要包括高血压、恶心呕吐、血小板减少、肝功能不全、肾功能不全,且主要为1~2 级不良反应,患者均可耐受。两组患者各不良反应的发生情况比较,差异均无统计学意义(P﹥0.05)。(表4)

表4 两组患者的不良反应发生情况
3 讨论
与发达国家相比,发展中国家女性卵巢癌的发病率逐年升高,而且向年轻化发展,卵巢癌及乳腺癌家族史是卵巢癌发生的最大危险因素[8]。研究表明,经规范化治疗后,仍有部分卵巢癌患者面临疾病进展的风险,尤其是晚期卵巢癌患者在2~5 年内出现PD 的风险更高[9]。因此,经规范化治疗后,动态监测患者的血清肿瘤标志物水平,指导临床及早调整治疗方案,改善患者预后,延长生存期,是复发性卵巢癌的主要治疗目标。
手术联合化疗是对于初治的卵巢癌患者的主要治疗方案,但部分患者尤其是晚期卵巢癌患者仍会出现肿瘤复发的情况。对于复发性卵巢癌患者,由于手术治疗的意义不大,因此,主要采取化疗、靶向性治疗等综合治疗。贝伐珠单抗是2004年美国食品药物管理局(Food and Drug Administration,FDA)批准的第一个用于治疗转移性结肠癌的抗肿瘤血管生成药物,属于重组人源化抗VEGF的单克隆抗体,不仅可通过阻断VEGF 与其受体结合来抑制肿瘤的生长,还能使畸形的肿瘤血管重塑,提高肿瘤细胞摄取药物的机会,从而降低肿瘤转移的发生风险。目前,贝伐珠单抗不仅用于治疗肾细胞癌、非小细胞癌,在卵巢癌中的应用还取得了较大进展[10-11]。
CA125 是位于染色体19p13.2 区域的基因,正常情况下人体血清中的CA125 水平较低,当发生癌变后,CA125 水平急剧升高,被广泛应用于与良恶性卵巢肿瘤的鉴别[12]。相关研究发现,CA125 在胸腹膜、输卵管、结肠等组织中也有表达,而且妊娠期女性血清中CA125水平也会相应升高,其单独检测卵巢癌的特异度较差,具有一定的局限性[13]。因此,临床一般联合其他肿瘤标志物共同检测或评估卵巢癌。HE4 基因位于染色体20q12213.1 上,是乳清酸四硫化物核心蛋白家族成员,除了在男性睾丸、前列腺中表达外,在女性生殖系统、气管、甲状腺、乳腺中也有表达[14]。Stiekema 等[15]研究发现,HE4 在卵巢癌、胃癌中呈过表达,并进一步从基因学方面研究发现,HE4 可能参与卵巢癌细胞的增殖、转移、侵袭。HE4 的分子量小,较易分泌进入血液,血清HE4 水平的监测对于卵巢癌的早期诊断和治疗具有重要意义。
本研究结果显示,观察组患者的ORR、DCR 均高于对照组,表明贝伐珠单抗联合PC 方案治疗复发性卵巢癌疗效显著,与其他相关研究结果[16]一致。贝伐珠单抗联合紫杉醇治疗难治性或铂敏感复发性卵巢癌的疗效显著,原因可能是贝伐珠单抗增强了紫杉醇、卡铂的抗血管生成的作用,同时通过重塑肿瘤血管提高了化疗药物的利用率,从而增强了抗肿瘤效果。研究发现,病理类型与复发性卵巢癌的预后无关[17]。荟萃分析结果显示,抗血管生成制剂可延长Ⅲ/Ⅳ期复发性卵巢癌患者的生存时间,病理类型、临床分期对治疗结局无影响[18]。本研究发现,治疗后,观察组者的血清CA125、HE4水平均明显低于对照组(P ﹤0.01),提示血清CA125、HE4 水平可作为复发性卵巢癌患者临床治疗效果的反映指标。贾素娟等[19]指出,单一的血清CA125 或HE4 对卵巢癌术后复发的诊断价值无明显差异,但二者联合应用可提高诊断的灵敏度,而且结合影像学检查的诊断价值更高。
本研究通过绘制生存曲线发现,观察组患者的中位PFS、OS 均长于对照组,提示贝伐珠单抗联合PC 方案可改善复发性卵巢癌患者的预后。既往研究结果亦显示,贝伐珠单抗联合化疗可明显改善复发性卵巢癌患者的主要终点OS 及次要终点PFS[20-21]。本研究中,两组患者发生了不同程度的不良反应,主要为1~2 级不良反应,但均可耐受,且两组患者各不良反应的发生情况差异不明显,说明贝伐珠单抗并不会增加不良反应,安全性较高,与既往研究结果[22]相同。
综上所述,贝伐珠单抗联合PC 方案可提高复发性卵巢癌患者的近期疗效,改善患者的远期生存情况,且不会增加不良反应;血清CA125、HE4 水平可作为患者预后预测的重要指标。
