非洲猪瘟病毒P30蛋白单克隆抗体的制备与应用
2020-10-17郝丽影王彦伟孙玉洁曹红梅逄文强李向东邓均华田克恭
郝丽影,王彦伟,孙玉洁,曹红梅,黄 甜,逄文强,李向东,邓均华,田克恭,
(1.洛阳普泰生物技术有限公司,河南 洛阳 471000;2.国家兽用药品工程技术研究中心,河南 洛阳 471000)
非洲猪瘟(African swine fever, ASF)是由非洲猪瘟病毒(African swine fever virus, ASFV)引起的猪的一种急性、烈性、传染性疾病。自2018年8月3日我国确诊首例发生于辽宁省沈阳市沈北新区的疫情以来,ASF迅速在我国各省市蔓延[1-4],给我国养猪业造成了巨大的损失,并严重威胁着世界养猪业的发展。
ASF尚无有效的疫苗,防控主要依靠严格的生物安全措施。敏感、准确的诊断试剂可为该病的防控提供可靠的工具。P30、P54、P72、PK205R蛋白均为目前ASFV诊断试剂研究的热点蛋白[5-10]。其中P30蛋白是ASFV的主要结构蛋白,且在病毒感染早期大量表达和分泌,是优良的早期检测靶标[11]。已有研究将P30蛋白应用于ASFV抗体的血清学检测,但将其单克隆抗体应用于胶体金检测试纸条的研究鲜有报道[12-15]。为此,利用原核系统表达重组P30蛋白并制备单克隆抗体,以期建立基于P30蛋白单克隆抗体的胶体金免疫层析检测法,旨在为ASFV的早期诊断提供参考。
1 材料和方法
1.1 材料
1.1.1 基因、质粒及感受态细胞 ASFVP30基因、pET28a质粒均由苏州金唯智生物科技有限公司合成、提供;大肠杆菌BL21(DE3)感受态细胞购自天根生化科技(北京)有限公司。
1.1.2 供试细胞与病毒 SP2/0细胞由洛阳普泰生物技术有限公司保存;猪瘟病毒(SFV)C株、猪繁殖与呼吸综合征病毒(PRRSV)JXA1-R株、猪伪狂犬病毒(PRV)Bartha-K61株、猪圆环病毒2型(PCV2)HH3株均由国家兽用药品工程技术研究中心提供。
1.1.3 供试动物 SPF级BALB/c小鼠购自北京维通利华实验动物技术有限公司。
1.1.4 主要试剂 ASFV阳性血清、ASFV抗原板、ASFV抗原等均购自欧洲非洲猪瘟参考实验室[Centro de Investigación en Sanidad Animal(CISA-INIA), Madrid, Spain];Ni2+亲和层析填料购自美国GE Healthcare公司;HRP标记的羊抗猪IgG、羊抗鼠IgG均购自Thermo公司;HAT混合盐、HT混合盐、弗氏完全佐剂、弗氏不完全佐剂等均购自Sigma公司;小鼠单抗Ig类/亚类/亚型鉴定用ELISA试剂盒购自洛阳佰奥通试验材料中心。
1.2 方法
1.2.1 重组表达质粒pET28a-P30的构建 根据GenBank中ASFVP30基因序列(GenBank: MH766894.1),进行大肠杆菌密码子优化,将优化后的基因送苏州金唯智生物科技有限公司进行全序列合成,5′和3′端分别引入酶切位点NdeⅠ和XhoⅠ,并连接到pET28a质粒上。将合成的质粒转化大肠杆菌BL21(DE3)感受态细胞,挑取单菌落后提取质粒进行双酶切鉴定,鉴定正确的质粒即为pET28a-P30。
1.2.2 重组P30蛋白的表达 将pET28a-P30质粒转化大肠杆菌BL21(DE3)感受态细胞,挑取单菌落至LB培养基中培养过夜。取2 mL培养过夜的菌种接种至200 mL含卡那霉素的LB液体培养基,于37 ℃、220 r/min振荡培养。当菌液OD600值达到0.8~1.0时,加入终浓度为0.5 mmol/L的IPTG溶液于28 ℃诱导培养12 h。收集菌体,用高压匀质机破碎,取样通过SDS-PAGE检测目的蛋白表达情况。
1.2.3 重组P30蛋白的纯化与Western blot鉴定 在菌体破碎上清液中加入0.01 mol/L咪唑后经0.45 μm过滤器过滤。取滤液采用Ni2+亲和层析法进行纯化。收集纯化产物进行SDS-PAGE电泳检测,通过光谱扫描分析目的蛋白的纯度,并利用Western blot鉴定其与ASFV阳性血清的反应性。
1.2.4 间接ELISA方法的建立 将P30蛋白稀释至0.1 μg/mL,混匀后加入酶标板,100 μL/孔,于2~8 ℃静置16~24 h;弃去板中液体,加入封闭液,200 μL/孔,于37 ℃封闭2 h;洗板,加入稀释后的样品,100 μL/孔,同时设置加PBS(0.01 mol/L,pH值7.4,下同)的孔为阴性对照,置37 ℃温育60 min;洗板,加入稀释至工作浓度的二抗,100 μL/孔,置37 ℃温育45 min;洗板,依次加显色剂A、B液,各50 μL/孔,振荡混匀后置37 ℃避光温育15 min,加入终止液,50 μL/孔,振荡混匀。设定酶标仪波长于450 nm处,测定各孔OD值。阴性对照OD值<0.2时试验成立,S/N(样品OD值/阴性对照OD值)≥2.1者,判为阳性;S/N(样品OD值/阴性对照OD值)<2.1者,判为阴性。
1.2.5 小鼠免疫 按照200 μL/只(含40 μg的重组P30蛋白)的量皮下多点免疫4~6周龄雌性BALB/c小鼠。首次免疫使用弗氏完全佐剂,后续免疫使用弗氏不完全佐剂。免疫间隔时间为7 d。于3次免疫后采集小鼠血清,用间接ELISA方法检测血清抗体效价。选择抗体效价高的小鼠进行细胞融合,于融合前3 d腹腔注射重组P30蛋白80 μg。
1.2.6 杂交瘤细胞株的建立
1.2.6.1 细胞融合 无菌分离免疫小鼠的脾细胞,将其与1.0×107~1.5×107个SP2/0细胞混合后,按照常规方法进行细胞融合。将融合后的细胞滴加至铺有饲养细胞的96孔细胞板,于37 ℃、5% CO2条件下静置培养。
1.2.6.2 杂交瘤细胞的筛选及亚克隆 当细胞长至孔底面积1/2~1/3时,取上清用1.2.4中所述间接ELISA方法检测。选择OD值高的孔采用有限稀释法进行亚克隆。反复进行杂交瘤细胞的筛选及亚克隆,直至单克隆孔的细胞上清检测阳性率为100%。
1.2.6.3 单克隆抗体的生产及效价测定 取BALB/c小鼠腹腔注射液体石蜡,0.5 mL/只。10 d后腹腔注射杂交瘤细胞,25万个细胞/只。待小鼠腹部明显膨大后抽取腹水,10 000 r/min离心10 min取上清,系列稀释后用1.2.4中所述间接ELISA方法检测,检测结果为阳性的孔对应的最高稀释度为腹水的抗体效价。
1.2.7 单克隆抗体的鉴定
1.2.7.1 亚类鉴定 用小鼠单抗Ig类/亚类/亚型鉴定用ELISA试剂盒对单克隆抗体进行亚类鉴定,操作按说明书进行。
1.2.7.2 与ASFV的反应性鉴定 用ASFV抗原板按照常规间接免疫荧光法(Indirect immunofluorescence assay,IFA)对单克隆抗体进行检测,以加PBS的孔作为阴性对照。
1.2.7.3 特异性鉴定 用猪瘟病毒C株、猪繁殖与呼吸综合征病毒JXA1-R株、猪伪狂犬病病毒Bartha-K61株、猪圆环病毒2型HH3株制备的抗原板,分别按照常规IFA方法对单克隆抗体进行检测,分别设置加病毒阳性血清、PBS的孔作为阳、阴性对照。
1.2.8 胶体金免疫层析检测法的建立 用柠檬酸三钠还原法制备胶体金溶液,并标记纯化后的重组P30蛋白单克隆抗体制备胶体金标记垫。用另一纯化后的P30蛋白单克隆抗体包被检测线,用羊抗鼠IgG包被对照线,组装成胶体金检测试纸条。用试纸条检测梯度稀释的ASFV抗原以及阴性样品,优化配对抗体。选择检测灵敏度最高且背景清晰的抗体制备胶体金检测试纸条,再进一步对胶体金标记抗体制备的pH值、标记量、检测线包被的单克隆抗体浓度进行优化,获得最优工艺。
1.2.9 胶体金免疫层析检测法的初步评价 选择世界动物卫生组织(OIE)推荐的ASFV PCR方法检测阴性的猪脾、肺、肾、肝、淋巴结、扁桃体组织研磨液以及血清、抗凝全血共8份样品作为阴性样品,并在阴性样品中按照1∶50比例添加ASFV抗原,制备8份阳性样品。按照最优工艺建立的方法,对样品进行检测。
2 结果与分析
2.1 重组表达质粒pET28a-P30的构建
质粒双酶切后电泳检测,可见约600 bp的目的片段和约5 000 bp的pET28a载体片段(图1),表明重组表达质粒pET28a-P30构建正确。
2.2 重组P30蛋白的表达
SDS-PAGE鉴定结果(图2)表明,菌种在IPTG诱导后可表达出重组P30蛋白,且表达的重组蛋白主要存在于上清中,大小约30 ku,与预期结果一致。

M:蛋白质Marker;1:未诱导全菌;2:诱导后菌体裂解液;3:诱导后菌体裂解液上清
2.3 重组P30蛋白的纯化与Western blot鉴定
采用Ni2+亲和层析法纯化上清中的可溶性重组P30蛋白。SDS-PAGE鉴定及光谱扫描结果表明,纯化后目的蛋白纯度约为83%(图3A)。Western blot结果显示,重组P30蛋白与ASFV阳性血清反应可见特异性的阳性反应条带(图3B)。表明重组P30蛋白具有良好的反应性。

M:蛋白质Marker;1:纯化的重组P30蛋白
2.4 P30蛋白免疫小鼠血清ELISA效价测定
利用P30蛋白免疫5只BALB/c小鼠,3免后小鼠血清的ELISA效价最高为1∶256 000。
2.5 杂交瘤细胞的筛选及亚克隆
将杂交瘤细胞上清用间接ELISA方法筛选,选择OD值高的阳性细胞进行亚克隆,经3~5次亚克隆获得10株稳定分泌P30蛋白单克隆抗体的杂交瘤细胞株,分别命名为4F7、2H4、1B11、1D4、5H3、4A7、4B10、2C8、3C11、2G1。
2.6 P30蛋白单克隆抗体的生产及效价测定
制备了10株分泌P30蛋白单克隆抗体的杂交瘤细胞株的小鼠腹水,经间接ELISA方法检测,10株腹水的ELISA效价均高于1∶40 000。
2.7 P30蛋白单克隆抗体的鉴定
2.7.1 亚类鉴定 10株P30蛋白单克隆抗体的重链亚类为IgG1、IgG2b、IgG2a,轻链亚类均为Kappa(表1)。
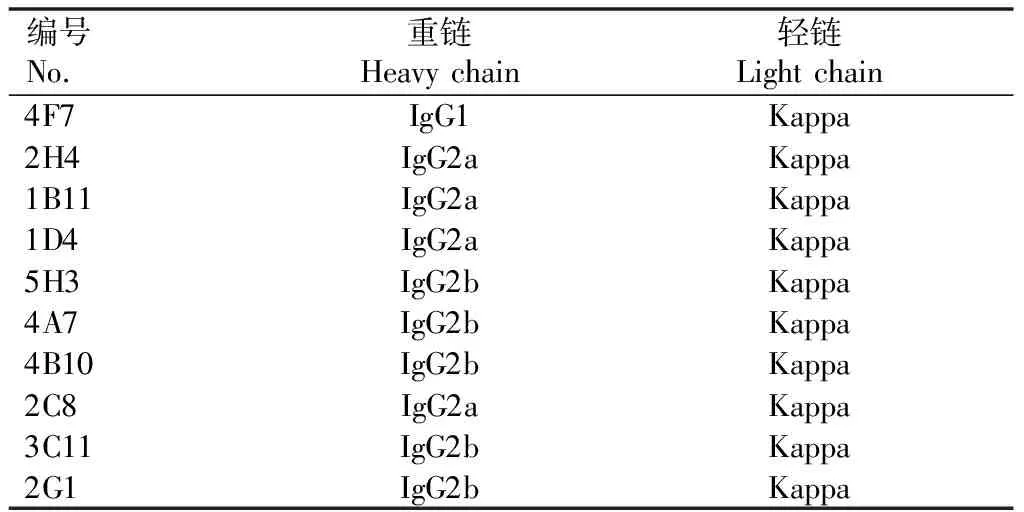
表1 P30蛋白单克隆抗体亚类鉴定结果
2.7.2 与ASFV的反应性鉴定 IFA结果显示,10株P30蛋白单克隆抗体与ASFV反应后均可见明显的荧光,而阴性对照无可见荧光。表明10株P30蛋白单克隆抗体均可与ASFV反应(图4)。
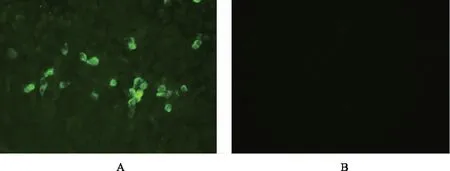
A:单克隆抗体4F7与ASFV的反应;B:阴性对照
2.7.3 特异性鉴定 IFA结果显示,除阳性对照外,P30蛋白单克隆抗体与所有病毒反应后均无可见荧光(图5),表明所有P30蛋白单克隆抗体与猪瘟病毒C株、猪繁殖与呼吸综合征病毒JXA1-R株、猪伪狂犬病病毒Bartha-K61株、猪圆环病毒2型HH3株均不反应,特异性良好。

A:阳性对照;B:阴性对照;C:单克隆抗体4F7
2.8 ASFV胶体金免疫层析检测法的建立
经各项条件优化,确定胶体金免疫层析检测法的最优工艺为P30蛋白单克隆抗体1B11按照1.5 mg/mL的量包被,单克隆抗体4F7在pH值8.0、质量浓度为18 μg/mL条件下制备胶体金标记抗体。该工艺下制备的试纸条检测ASFV抗原的灵敏度最高,1∶100倍稀释检测仍为阳性。
用该方法检测8份阳性样品,检测结果均为阳性,8份阴性样品均为阴性,表明该方法可用于ASFV的检测。
3 结论与讨论
ASF的临床症状与猪瘟等猪常见病易混淆,其诊断需从流行病学、临床症状、病理变化、病原检测等方面综合分析,确诊主要依据实验室检测结果。随着国内ASF疫情的发展,临床检测对诊断方法的需求更加具体化。研制满足不同应用场景需求的多样化的诊断试剂,将为ASFV病毒疫情的监测及控制提供重要的支持。而单克隆抗体的制备,将为其免疫学诊断试剂的研发提供重要的生物原料。
P30蛋白由CP204L基因编码,为ASFV的内膜蛋白,是病毒重要的结构蛋白之一。有研究表明,在病毒感染2~4 h即有P30蛋白的表达,且可持续整个感染周期[16-17]。P30蛋白参与病毒内化,在病毒入侵宿主细胞的过程中起重要作用,具有良好的免疫原性,可引起机体产生高水平的抗体反应,于感染后8 d即可检测到抗体,是一种理想的血清学诊断和免疫学检测抗原[18-22]。
大肠杆菌表达系统遗传背景清晰、目的基因表达量高且表达周期短,是一种蛋白质表达的重要工具。前人利用大肠杆菌表达系统表达ASFV P30蛋白,经验证表达的重组蛋白具有良好的免疫原性和反应性[18]。本研究利用大肠杆菌表达系统成功表达了可溶性的重组P30蛋白,用ASFV阳性血清进行Western blot鉴定,发现表达的重组蛋白有良好的反应原性。用纯化的重组P30蛋白免疫小鼠,间接ELISA方法检测小鼠血清效价最高为1∶256 000,表明该蛋白有良好的免疫原性。
PETROVAN等[11]的研究表明,P30蛋白单克隆抗体与ASFV有很好的反应性,利用IFA方法可以识别病毒,利用免疫组织化学方法可以检测感染猪组织中P30蛋白的表达,这些结果均表明,P30蛋白单克隆抗体可作为ASFV检测的重要工具。本研究制备的10株P30蛋白单克隆抗体,IFA检测显示均可与ASFV反应。利用2株P30蛋白单克隆抗体进行了ASFV胶体金免疫层析检测法的建立,初步评价可用于ASFV的抗原检测。以上结果表明,获得的P30蛋白单克隆抗体可为ASFV的免疫学诊断技术开发提供重要的生物原料,同时也可为ASFV P30蛋白的基础研究提供支持。
