2型糖尿病患者合并肾脏疾病的临床病理及预后
2020-10-12李灿明叶增纯饶嘉玲娄探奇
李 明,李灿明,叶增纯,饶嘉玲,彭 晖,娄探奇
(中山大学附属第三医院肾内科,广东广州 510630)
糖尿病性肾病(diabetic nephropathy,DN)是糖尿病的严重并发症,也是世界范围内终末期肾病(end stage renal disease,ESRD)的主要原因[1-2],在中国导致ESRD 的病因中,糖尿病肾病占了约16.4%[3]。临床上诊断糖尿病肾病主要根据糖尿病病程、肾脏损害的临床表现如蛋白尿以及是否合并糖尿病视网膜病变等。然而,越来越多肾脏病理资料证实,糖尿病患者合并的肾脏损害中非糖尿肾病(non diabetic renal disease,NDRD)所占比例并不低(17%~85%)[4-17]。NDRD可以单独出现,也可以叠加在DN 上。诊断糖尿病患者的NDRD非常重要,因为这些疾病的治疗和预后完全不同。本研究采用回顾性队列研究的方法,分析本中心2005-2014 年行肾穿刺活检的2 型糖尿病患者的临床、病理资料,并对其进行了后续的随访,观察预后的情况,旨在为临床诊断及治疗决策提供依据。
1 材料与方法
1.1 研究对象
纳入标准:自2005 年1 月至2014 年12 月在中山大学附属第三医院肾内科确诊为2 型糖尿病及合并肾脏疾病,年龄>18 岁,且接受过肾脏穿刺活检术,临床与病理资料完整的患者。肾脏疾病定义为临床上出现持续尿检异常[(24 h 尿蛋白定量>0.5 g 和(或)伴有血尿)]和(或)Scr 升高。排除标准:排除1 型糖尿病及肾脏活检时已开始接受肾脏替代治疗者。本研究最初共纳入124例患者,其中有4 名患者同时合并DN 和NDRD(合并IgA肾病2 例,膜性肾病1 例,间质性肾炎1 例),因该组患者数太少在统计时未将其纳入。本研究获得中山大学附属第三医院伦理委员会批准,所有患者均已签署知情同意书。
1.2 方 法
按肾脏病理检查结果将入选的2 型糖尿病合并肾脏病变的患者分为:DN 组(57 例);NDRD 组(63 例)。DN 组患者肾组织病理表现为糖尿病肾小球病改变,病理组织按RPS 分型方案进行评估[18],主要依据肾小球分型:Ⅰ型:肾小球基底膜(glomerular basement membrane,GBM)增厚;Ⅱa 型:轻度系膜增生;Ⅱb 型:重度系膜增生;Ⅲ型:结节硬化;Ⅳ型:晚期糖尿病肾小球硬化。回顾性收集患者的基线及随诊临床或病理资料。临床指标包括:性别、年龄、体质量指数(BMI)、DM 病程、血压、血肌酐(Scr)、估算肾小球滤过率(eGFR,根据EPI 公式计算)、空腹静脉血浆葡萄糖(FPG)、糖化血红蛋白(HbA1c)、血清白蛋白(Alb)、血清尿酸(UA)、血清总胆固醇(TC)、血清三酰甘油(TG)、血红蛋白(Hb)、尿白蛋白肌酐比(ACR)、糖尿病视网膜病变(DR),由眼科医师使用直接或间接检眼镜行眼底检查和荧光素眼底血管造影检查确定。肾脏活检组织标本经B 超引导下经皮肾穿刺活检取得,行光镜、免疫荧光、电镜等检查。
1.3 随访及观察终点
随访截止日期为2018 年12 月31 日。观察终点为接受维持性肾脏替代治疗(包含血液透析和腹膜透析)或进入ESRD,并记录患者的全因死亡事件。随访截止时间为:达肾脏终点事件、失访,或截至2018 年12 月31 日的最后1 次随访。
1.4 统计方法
采用SPSS 19.0 软件进行统计分析。所有数据在统计分析前行正态分布检验,连续性资料符合正态分布资料采用表示,两组比较采用独立样本t检验,多组比较采用方差分析;连续性资料不符合正态分布资料采用中位数和四分位数,即P50(P25~P75)表示,两组间及多组间比较采用非参数检验;计数资料用构成比表示,两组及多组比较采用卡方检验。使用Kaplan-Meier 曲线及Cox 回归分析2 型糖尿病合并肾损害患者发生ESRD 的风险。所有检验均为双侧检验,P<0.05 视为差异有统计学意义。
2 结果
2.1 基线资料比较
本研究共120 例患者,男性74 例(61.7%),年龄(50.9±11.2)岁,糖尿病病程(92.8±41.3)月,血肌酐(181.7±155.1)μmol/L。DN、NDRD 组患者性别、年龄间的差异无统计学意义。与NDRD 组相比,DN组患者的糖尿病病程较长(Z=-4.802,P<0.01);DM 病程>5 年患者的比例也较高(χ2=13.324,P<0.01);肾穿前eGFR水平较低,且合并eGFR<60 mL/min 患者的比例较高(χ2=9.720,P<0.01);合并贫血(χ2=18.982)、糖尿病周围神经病变(χ2=15.447)、DR(χ2=45.551)、PDR(χ2=10.545)的比例明显高于NDRD 组(P<0.01)。两组组间Scr、血清白蛋白、尿蛋白量及合并血尿的患者比例的差异无统计学意义。按照尿蛋白量与eGFR 分组后分析发现,DN组eGFR<60 mL·min-1·(1.73 m2)-1且尿蛋白>3.5 g/24 h 患者的比例高于NDRD 组(χ2=8.993,P<0.01)。DN组患者收缩压水平显著高于NDRD组(t=-2.661,P<0.01),但舒张压水平两组之间没有显著差异。另外,两组组间糖化血红蛋白、空腹血糖、总胆固醇、低密度脂蛋白的差异无统计学意义(表1)。
2.2 2 型糖尿病患者合并肾脏疾病的病理改变
120 例患者中,DN 组患者57 例,病理表现均为糖尿病肾小球病改变,依据2010 年RPS 肾小球分型,未发现Ⅰ型患者,Ⅱa、Ⅱb、Ⅲ、Ⅳ型患者分别有9 例(15.8%)、9 例(15.8%)、24 例(43.8%)、15 例(24.6%)。NDRD 组患者63 例,其肾脏病理改变最常见类型是膜性肾病(18 例,28.6%),其次是IgA 肾病(15 例,23.8%)和狼疮肾炎(8 例,12.7%),后面依次为微小病变(4 例,6.3%),系膜增生性肾小球肾炎(3 例,4.8%),高血压肾病(3例,4.8%),局灶节段性肾小球硬化(3例,4.8%),膜增生性肾小球肾炎(3 例,4.8%),间质性肾炎(3 例,4.8%),乙肝相关性肾炎(1 例,1.6%),ANCA相关性肾炎(1 例,1.6%),脂性肾病(1 例,1.6%)。
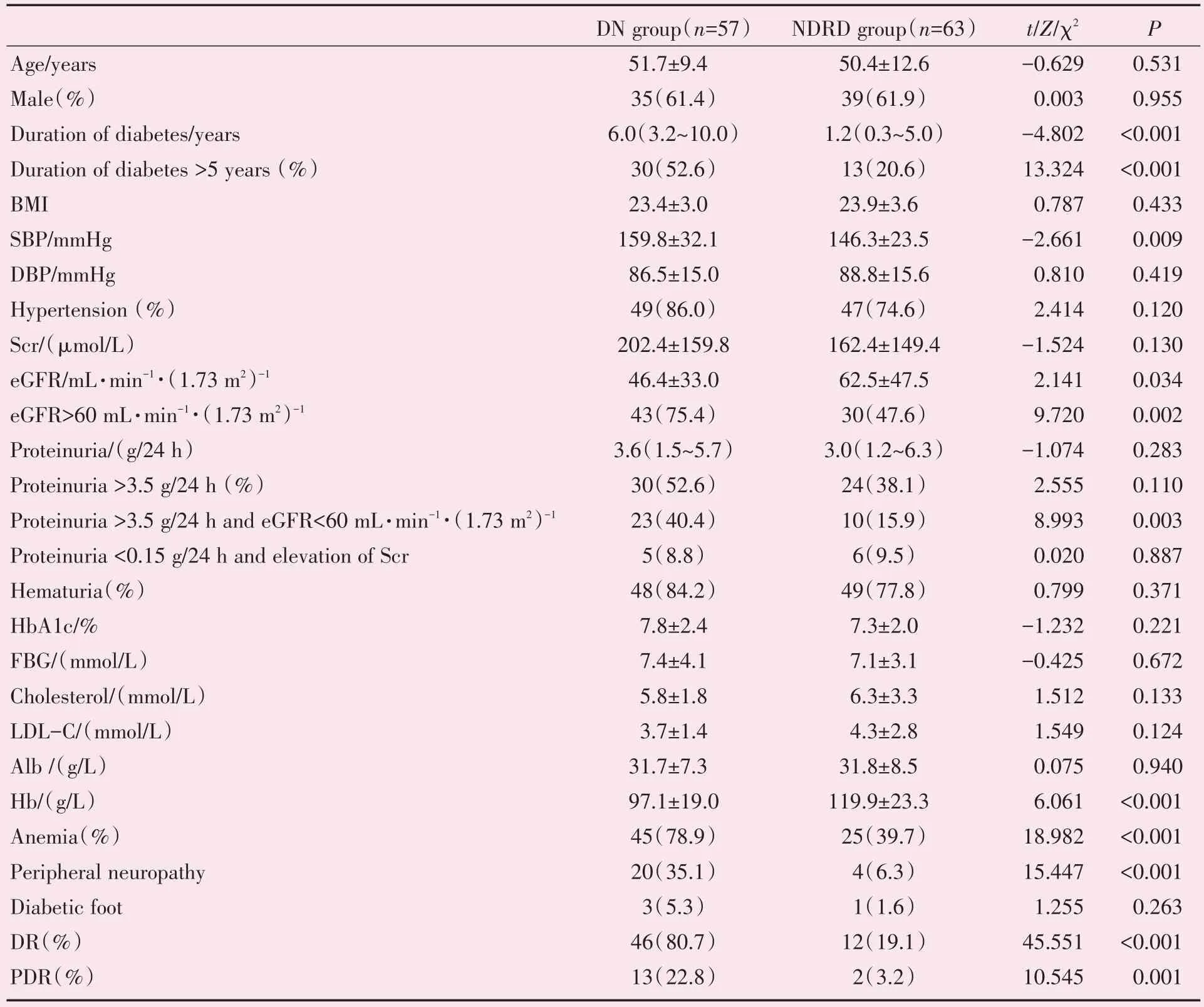
表1 DN 组和NDRD 组患者的基线临床特征Table 1 Baseline clinical features of patients in the DN group and NDRD group
2.3 2 型糖尿病患者合并糖尿病肾病的预测因素
为进一步从临床资料来鉴别糖尿病肾病和非糖尿病肾病,我们对DN 和NDRD 两组患者进行了多因素logistic 回归分析,将有统计学意义的变量(糖尿病病程、糖尿病病程>5 年、SBP、eGFR,eG⁃FR<60 mL·min-1·(1.73 m2)-1、HGB、合并糖尿病视网膜病变、合并糖尿病周围神经病变、合并PDR等)纳入多因素Logistic 逐步回归方程,结果发现,只有合并糖尿病视网膜病变(OR 12.354,95%CI 4.690~32.541,Wald χ2=25.882,P=0.000),及血红蛋白水平(OR 0.960,95%CI 0.938~0.984,Wald χ2=11.103,P=0.001)是预测DN 的独立危险因素。考虑到糖尿病视网膜病变在诊断糖尿病肾病中有重要的提示意义,我们继续考察了其对DN 诊断的敏感度和特异度,利用四格表法计算得到DR 诊断DN 灵敏度为80.7%,特异度为81.0%。
2.4 随访情况
本研究随访中位时间为34.3(11.8~61.3)月。其中DN 组平均随访时间为(30.3±25.9)月,NDRD组平均随访时间为(49.7±31.4)月,两组间有统计学差异(P<0.01)。120 例患者在本院随访至少一次。至随访结束,发生肾脏终点事件48 例(40.0%),其中DN 组29 例(50.9%),NDRD 组19 例(30.2%)。DN 组全因死亡6 例(10.5%),NDRD 组全因死亡4 例(6.3%),死亡原因包括慢性肾衰竭、慢性心力衰竭急性加重、肺部感染。Kaplan-Meier 生存分析显示,DN组累积生存率为33.1%,NDRD组为65.6%。DN 组肾脏生存中位时间为48.6 个月,1 年、5 年肾脏生存率分别为81%、41%,而NDRD 组1 年、5 年肾脏生存率分别为95%、84%。NDRD 组的肾脏存活率显著高于DN 组(Log Rank χ2=17.85,P<0.001;图1)。多因素COX 回归分析结果显示,与2 型糖尿病合并NDRD 患者比较,DN 患者进入ESRD 的HR=3.81,95%CI 1.61~9.01,P=0.002(表2)。
3 讨论
2 型糖尿病合并慢性肾脏病(CKD)患者肾脏病理改变有很大的异质性。合并糖尿病的肾脏病患者有可能为糖尿病肾病、非糖尿病肾脏疾病或两者并存。而糖尿病肾病依据病理的轻重,也存在着不同的分型,目前比较广泛接受的是2010 年RPS 分型方案。受种族和地域的影响,不同地区NDRD 检出率和主要病理改变各不相同。美国哥伦比亚大学医学中心肾病实验室对620 例糖尿病合并肾脏损害患者进行研究分析,结果发现局灶节段性肾小球硬化(FSGS)在NDRD 中的比例最高,该研究主要研究对象为白人及美国黑人(86.5%),亚裔仅占15 例(4.4%)[19]。但印度的资料则显示以AIN为主[6]。来自中国内地和亚洲等地的多项研究均发现NDRD 中病理改变类型的首位为IgA 肾病[7-8,15],其次为膜性肾病。但刘健等[17]报道NDRD中局灶节段硬化性肾炎(41.7%)最多,与国内其他报道有所差别。本研究120 例患者中,NDRD检出率为52.5%(63/120),其主要病理改变类型为膜性肾病,其次是IgA 肾病,与徐静等报道的结果相似[4,10-11]。由于本研究中的中老年男性患者比例较高,而膜性肾病是中老年患者原发性肾病综合征最常见的病理类型,这可能是本研究中膜性肾病在NDRD 中较IgA 肾病比例更高的原因之一。
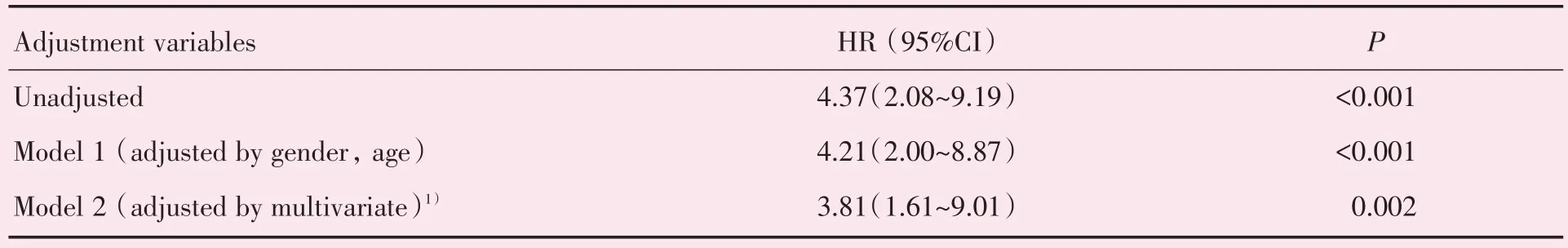
表2 DN 患者与NDRD 患者进入ESRD 的风险比较(Cox 回归分析)Table 2 The risk of ESRD in T2DM patients with DN compared with T2DM patients with NDRD(Cox regression analysis)
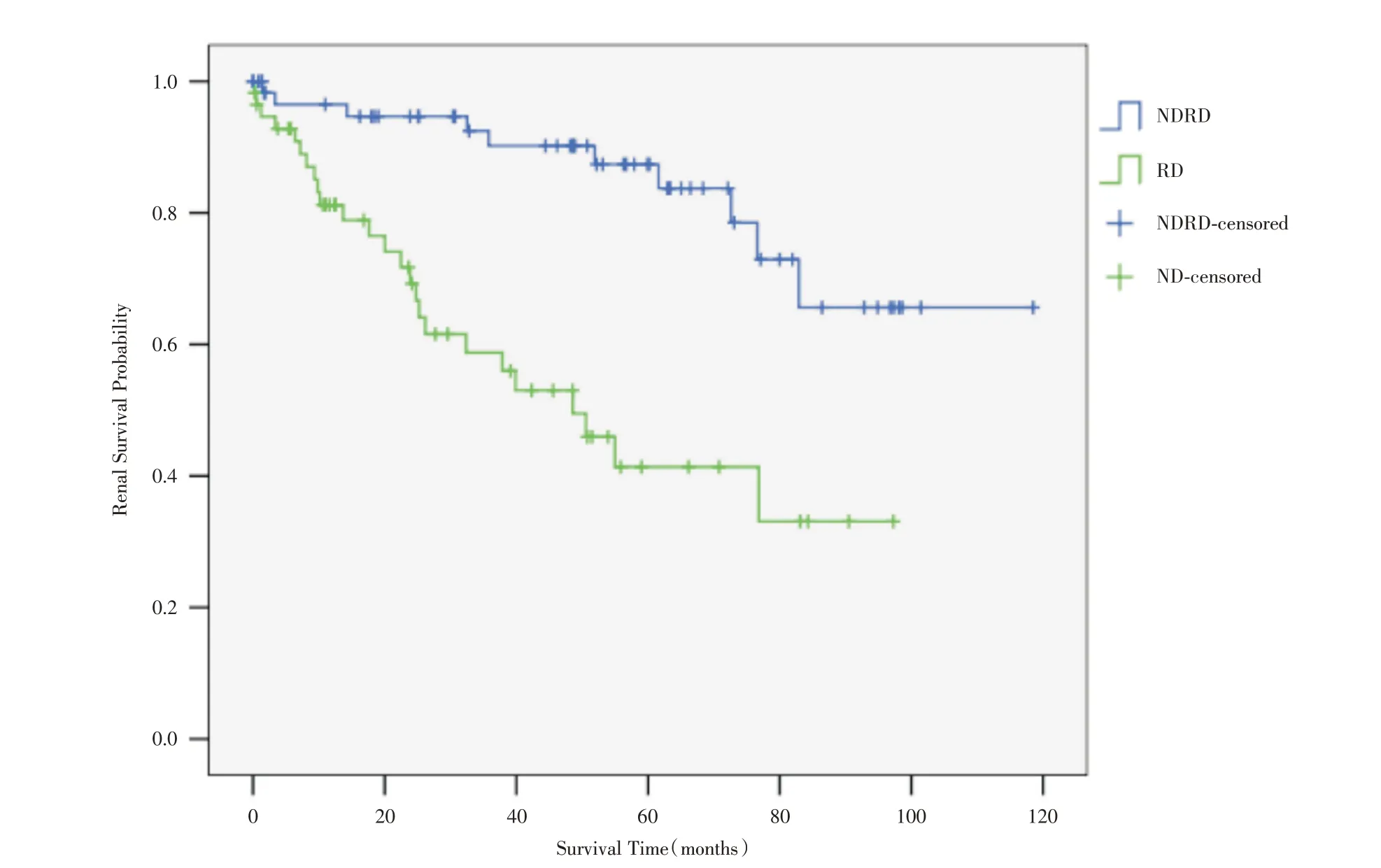
图1 DN组与NDRD组肾脏生存率比较Fig.1 The comparison of renal survival probability in DN group and NDRD group
关于糖尿病肾病及与NDRD 临床鉴别,不少研究指出糖尿病病程、血糖控制不良,合并高血压、血尿、肾功能恶化及合并糖尿病视网膜病变等是几个重要方面。与NDRD组相比,我们发现DN 组肾病综合征水平蛋白尿和eGFR < 60 mL·min-1·(1.73 m2)-1的患者比例更高,提示肾功能减退伴肾病综合征水平蛋白尿在DN 患者中较NDRD 患者更常见。我们也发现NDRD组患者平均24 h 尿蛋白定量>3 g,且伴有白蛋白水平低下,考虑可能与NDRD 组膜性肾病患者比例较高有关。我们的研究还提示非糖尿病肾性肾损害患者大多DM 病程短,多数在5 年以内,而糖尿病肾病患者病程多在5 年以上,与国内外的报道相似[4,17,20]。此外,DN 患者的血红蛋白明显低于NDRD 组,发生贫血的比例更高,多因素logistic 回归分析显示血红蛋白水平是预测糖尿病肾病的独立危险因素。有研究结果提示,患有糖尿病的CKD 患者在肾病的早期即可出现贫血。糖尿病患者内脏神经功能紊乱会导致红细胞生成素(EPO)分泌功能受损,也有学者指出EPO 分泌减少与糖尿病所造成的微血管并发症相关[21-22]。UKPDS 等著名研究强调了血糖控制不良是糖尿病肾病的进展的重要因素,但本研究显示两组患者糖化血红蛋白、空腹血糖的比较上并无差异,考虑可能与本研究所选取的HbA1c 及FBG 为基线值而不是长期均值有关。目前的研究证实,对血糖的严格控制仍是减少各种并发症发生发展的有效措施。
作为糖尿病的两个最主要的微血管病变,两者在病理生理和发病机制上有很多相似之处,不少研究认为DR 对DN 筛查与诊断以及协助判断DN 向ESRD 进展上具有重要的预测价值[12-15]。当肾脏有K-W 结节损害时,视网膜必有微动脉瘤出现。当发现DN 时,很多患者亦出现DR 的改变。有学者对1456 例2 型糖尿病合并肾病的患者行眼底检查或眼底照相,65%患者有视网膜病变[23]。在2007 年糖尿病及慢性肾脏病的临床实践指南(KDOQI)[24]也凸显了糖尿病视网膜病变在诊断糖尿病肾病的重要性,指出大量蛋白尿或者微量白蛋白尿2 型糖尿病患者合并糖尿病视网膜病变大多可以诊断糖尿病肾病。我们也发现DN组患者发生糖尿病视网膜病变的比例明显高于NDRD 组(80.7%比19.1%,P<0.01),且DN 组发生增殖型糖尿病视网膜病变的比例也明显高于NDRD 组(P<0.01)。这提示在DM 患者中眼底检查是鉴别DN 与DNRD 重要手段。但DN 和DR 的相关性并不完全平行,在本研究当中,尚有19.3%的DN 患者无DR,而患有DR 的2 型糖尿病合并CKD 患者中仍有11.4%肾脏病理诊断为NDRD。此外,在RIACE 研究中,41.4%的2 型糖尿病合并DR的患者并没有同时合并糖尿病肾病[25]。
不少研究目前报道糖尿病患者中NDRD 的肾脏预后优于DN[11,16]。本研究也有类似发现,尽管NDRD 和DN 组的基线eGFR 有差异,但进一步的随访显示DN 进展至ESRD 的风险是NDRD 的4.3倍,且进入到ESRD 中位的时间更短,采用COX 多因素包括基线eGFR 校正后仍然提示DN 预后显著差于NDRD。这提示我们在临床上对于糖尿病合并肾脏疾病患者鉴别DN 及NDRD 的重要性。分析DN 患者预后不良的原因,可能一方面与DN患者糖尿病病程较长,合并症较多,肾功能相对较差有关系,另一方面可能与DN 进展较快,且缺乏有效治疗手段也有关系;而NDRD 患者一般糖尿病病程较短,且通过接受激素和(或)免疫抑制剂治疗后,临床上可以达到一定缓解,因此预后好于DN 患者。
本研究尚存在不足之处,首先,本研究是单中心回顾性研究,且样本量偏小,有一定失访率,对结果可靠性有一定的影响。其次,本研究对象为接受肾活检的患者,存在一定的选择性偏倚,结论尚不能完全推广到2 型糖尿病合并CKD 的患者中。
综上,我们中心的数据显示NDRD 在T2DM 患者中很常见,DN 患者预后显著差于NDRD 患者,依据临床表现如糖尿病病程、肾功能状况、糖尿病视网膜病变等诊断DN 容易造成误诊,对于两者的准确鉴别仍需依靠肾脏病理检查。
