CA153、CA199、CA125和FER联合检验在乳腺癌诊断中的价值
2020-10-12张瑾
张 瑾
(许昌市中心医院,河南 许昌 461000)
乳腺癌位居妇科恶性肿瘤之首,严重威胁着患者的生命健康[1]。乳腺癌早期多无明显症状,待临床确诊时多以处于中晚期,不仅增加了治疗难度,同时缩短了患者的生存期,使生存质量下降[2]。以往临床上常采用影像学、病理活检等手段进行乳腺癌筛查,但均有一定的局限性。有研究表明,部分血清肿瘤标志物与乳腺癌的发生发展有一定的相关性[3]。为此本研究以48例乳腺癌患者为研究对象,探讨CA153、CA199、CA125和FER联合检验在乳腺癌诊断中的价值,现进行如下报告。
1 资料与方法
1.1 一般资料
以许昌市中心医院2017年5月~2019年5月48例乳腺癌患者设为乳腺癌组,所有患者均经病理证实为乳腺癌,且排除严重的器官功能障碍、其他恶性肿瘤、凝血功能障碍、传染性疾病及临床资料不全者,年龄33~71岁,平均(57.65±3.48)岁,临床分期:Ⅰ期12例,Ⅱ期14例,Ⅲ期15例,Ⅳ期7例;并以同期收治的51例乳腺良性病变患者设为良性对照组,年龄31~72岁,平均(57.31±3.35)岁,乳腺增生16例,纤维腺瘤12例,导管内乳头状瘤10例,脂肪瘤7例,错构瘤6例;同期的53例健康体检者作为健康对照组,患者年龄32~74岁,平均(58.12±3.52)岁,所有受试者均自愿参与本次研究。
1.2 方法
所有受试者接受检验前均持续空腹8 h以上,于次日晨起空腹条件下抽取外周静脉血5.0 mL,静置30 min后以3 000 r/min转速离心5 min后,分离出血清于-80℃冰箱中保存备用,采用迈瑞2000i的化学发光免疫分析仪及配套试剂,严格按照说明书及操作规程完成糖类抗原(CA153)、糖类抗原(CA199)、糖类抗原(CA125)及铁蛋白(FER)等相关指标的检测,各肿瘤标志物阳性参考标准:CA125≥35 U/mL、CAl99≥39 U/mL、CA153≥25 U/mL、FER≥150 ng/mL则判断为阳性,联合检测时任何一项符合阳性标准即为阳性[4]。a表示真阳性;b表示假阳性;c表示假阴性;d表示真阴性;敏感性=a/(a+b),特异性=c/(c+d),准确性=(a+c)/(a+b+c+d),阳性预测值=a/(a+b)。
1.3 统计学方法
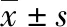
2 结果
2.1 3组各检测指标水平比较(见表1)
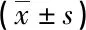
表1 3组各检测指标水平比较
2.2 各检测指标在乳腺癌中的诊断效能比较(见表2)
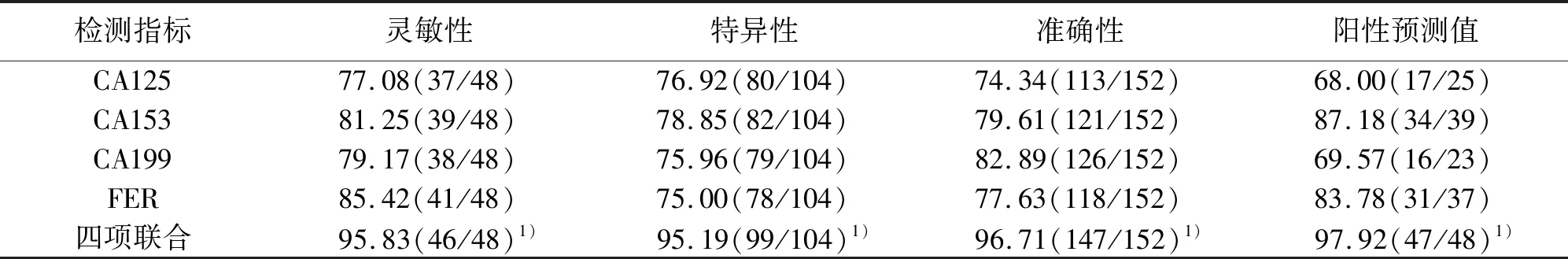
表2 各检测指标在乳腺癌中的诊断效能比较 %(n)
2.3 3组各检测指标的阳性检出率比较(见表3)

表3 3组各检测指标的阳性检出率比较 %
3 讨论
目前除了超声、病理检查以外,血清肿瘤标志物因其在肿瘤的普查、诊断、预后判断、疗效评价方面均有较大的实用价值目前也被临床广泛应用于乳腺癌的诊断。其中以CA153、CA199、CA125和FER为主的肿瘤标志物在乳腺癌诊断中的应用最为广泛[3,4]。CA153广泛存在于乳腺、胰腺、卵巢的恶性肿瘤细胞及正常上皮细胞中,具有一定的器官特异性,在浸润性及转移性乳腺癌中灵敏度较高[3-5]。血清 CA199是存在于人体胃、肠、胰腺等上皮层细胞膜上糖脂质,在乳腺癌中也有一定的阳性率。CA125 是卵巢癌疗效评价及预后判断的敏感指标,在乳腺癌中也有一定的阳性率。FER存在于肝、脾、肠黏膜细胞中,有研究已证实在实体恶性细胞中可合成FER,尤其在早期肺癌诊断中敏感性较高[1,3]。本研究结果表明,与健康对照组与良性对照组相比,乳腺癌组患者的血清CA153、CA199、CA125及FER水平更高;与健康对照组与良性对照组相比,乳腺癌组患者的血清CA153、CA199、CA125及FER的阳性检出率更高;CA153、CA199、CA125和FER联合检验的灵敏性、特异性、准确性及阳性预测值均优于各指标单独检测;差异均有统计学意义(P<0.05)。综上所述,CA153、CA199、CA125和FER联合检验可有效提高乳腺癌阳性检查率及诊断效能,对临床确立治疗方案及预后评估具有积极意义。
