基于网络药理学探讨黄芪-当归药对治疗老年中风机制
2020-10-10魏燕飞
魏燕飞
中风又称脑卒中,包括西医学的脑溢血、脑梗死等脑血管意外所出现的以猝然昏仆、不省人事、半身不遂、口眼歪斜、言语不利为主症的病证。中医认为,该病是由于气血逆乱,产生风火痰瘀上犯于脑,导致脑脉痹阻或迫使血液溢于脉外而致。该病发病率、死亡率均高,给患者及其家庭带来沉重的精神和经济负担。因此,积极有效的治疗极为重要。中医药治疗中风具有丰富的经验及完善的治疗体系,历代医家对本病的治疗提供了宝贵的思路和方法。李毓秋等[1]通过收集名家医案中有效治疗中风的医案资料,系统总结中医治疗中风核心中药的用药规律及药物配伍,发现黄芪-当归药对出现的频次较高,使用尤为广泛。网络药理学能够描述药物与器官、靶点、疾病等生物系统之间复杂的相互作用[2]。本研究基于网络药理学方法,筛选黄芪-当归药对的活性成分,以阐释黄芪-当归药对治疗中风的重要作用靶点和生物过程,从生物复杂系统的角度探讨其治疗中风的潜在机制。
1 资料与方法
1.1 黄芪-当归活性成分的挖掘与筛选采用中药系统药理学数据库和分析平台(Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform,TCMSP)[3]检索出黄芪-当归药对的活性成分。根据吸收分布代谢排泄(absorption distribution metabolism excretion,ADME)的关键参数:口服生物利用度(OB) ≥30%、类药性(DL) ≥ 0.18筛选黄芪-当归药对中有效的活性成分。
1.2 黄芪-当归药对活性成分作用靶点的预测利用 TCMSP 数据库获取黄芪-当归药对中筛选出的每个活性成分对应的潜在靶点信息,并除去没有靶点的成分。借 助 Uniprot (http://www. uniprot. org) 数据库中的 UniprotKB 搜索功能和NCBI中gene查询功能,将靶点名称设定物种为人,将所得到的靶点全部校正为基因名,以解决药物靶点存在的名称不规范等问题。
1.3 黄芪-当归的GO分析和KEGG信号通路富集分析利用DAVID 6.8数据库(https://david. ncifcrf. gov/)对黄芪-当归药对靶点蛋白进行GO分析和KEGG信号通路富集分析。在DAVID的基因列表中粘贴目标基因,并标示为“official gene symbol”,物种为“Homo Sapiens”,背景也为“official gene symbol”,进行分析后得到最终结果。
2 结果
2.1 黄芪-当归药对活性成分以OB ≥30%、DL≥ 0.18为筛选标准,共筛选出25个活性成分,其中黄芪20个,当归5个,另外有4种化学成分,虽然DL≤ 0.18,在已有文献中报道其药理学活性较好,因此将其列为候选化合物。见表1。

表1 黄芪-当归药对活性成分
2.2 黄芪-当归药对活性成分的靶点预测借助 TCMSP、Uniprot 数据库,共得到黄芪-当归药对活性成分对应的靶点141个,通过Cytoscape 3. 6 软件构建活性成分靶点相互作用网络,列出节度点≥3的靶点,即3个及以上化合物对应的靶点共58个。见表2。

表2 黄芪-当归药对中活性成分的靶点

续表2
2.3 黄芪-当归药对治疗中风 GO 分析使用 DAVID 数据库对黄芪-当归药对靶蛋白进行 GO 分析,得到了多个重要生物学过程,表3中列出10个及以上靶蛋白富集的生物学过程,包括细胞外泌体、线粒体、衰老、应对低氧、损伤修复、血管收缩调节、一氧化氮生物合成过程的正向调节、凋亡过程调节等。
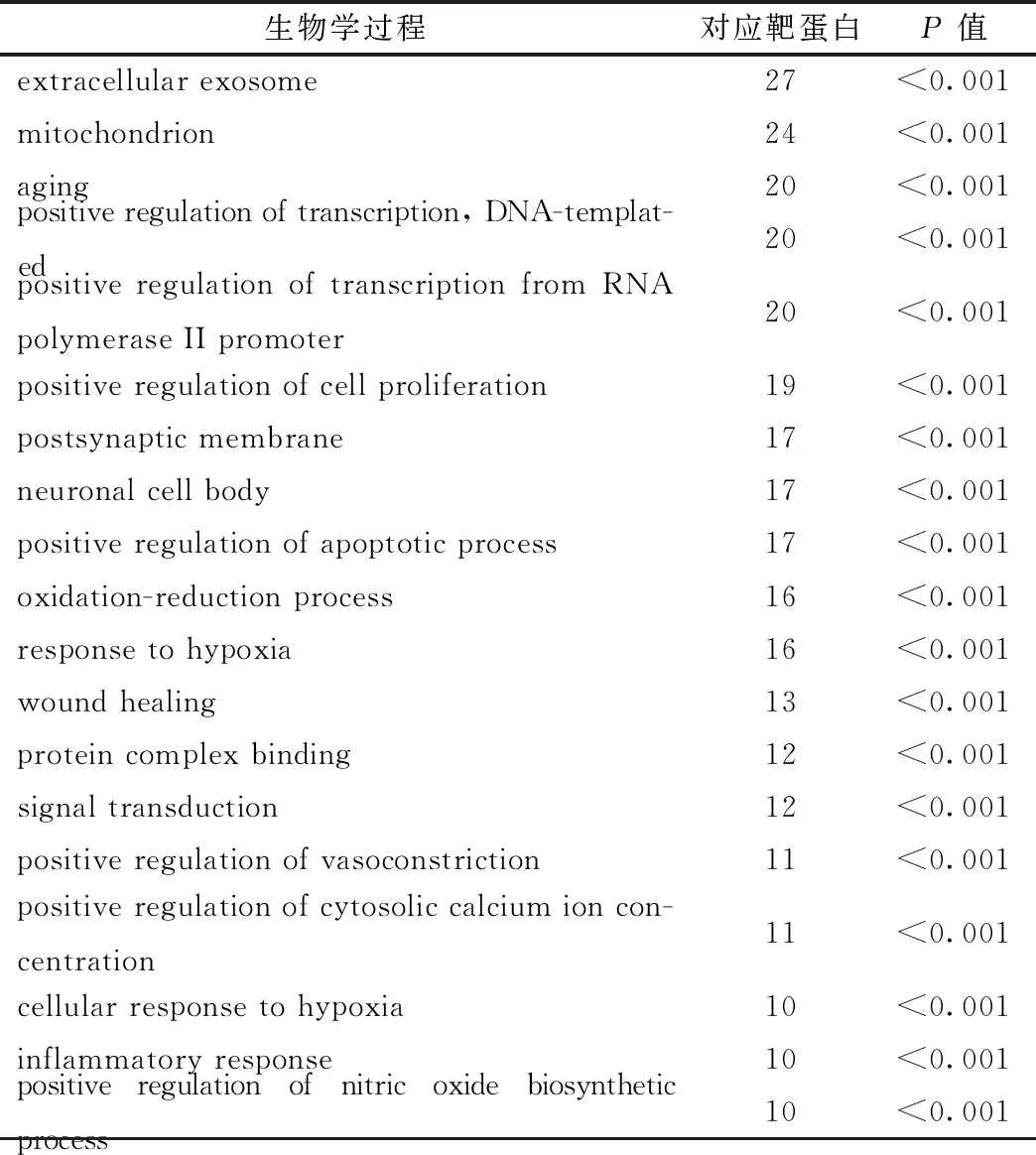
表3 黄芪-当归药对治疗中风的生物学过程
2.4 黄芪-当归药对治疗中风KEGG 信号通路富集分析使用 DAVID 数据库对黄芪-当归药对靶蛋白进行KEGG 信号通路富集分析,得到如下表所示重要生物信号通路,包括神经活性配体-受体相互作用、钙信号通路、胆碱能突触、血管内皮生长因子(VEGF)信号通路、神经营养因子信号通路、肌动蛋白细胞骨架调节、缺氧诱导因子(HIF)-1信号通路等。见表4。

表4 黄芪-当归药对治疗中风的KEGG通路富集分析
3 讨论
中风病名及病因病机首见于《黄帝内经》,为“内虚邪中”所致,为中医“风、痨、膨、膈”四大难病之首。《中医内科学》[4]认为中风病病位在脑,与心肝脾肾密切相关,病机主要是风、火、气、痰、瘀、虚六端,其基本病机为阴阳失调、气血逆乱、上犯于脑。气虚、血瘀是中风病发生发展的根源及核心,最终导致经络闭阻、血脉不利并发为风,故益气活血、祛风通络为其主要治则[5],历代医家都十分重视气虚血瘀这一病理因素,在治疗过程中60% 以上的方剂同时配伍益气药和活血药[6]。清末著名医家张锡纯于《治内外中风方》和《治肢体痿废方》中,详载用于中风治疗的11 首方47味药中,以黄芪、当归使用频率最高,黄芪-当归药对的置信度达100%,故张锡纯治疗中风时黄芪必配当归同用,黄芪补中益气,当归行血活血,两者配伍,功效相得益彰,黄芪用之于当归之中,自能助之以生血也,气血双生、阴阳有制[7]。
现代药理研究表明,黄芪具有调节血脂代谢、降血脂、降血压和增强抗脂质过氧化的作用,也可调节脑血管供血不足,对预防和治疗中风具有重要意义[8]。
当归可改善造血功能,增加心脏血供,维持正常的血液循环,提高机体免疫功能[9]。本研究基于网络药理学,以“生物靶标”模式从网络的角度进行研究[10],对黄芪-当归药对进行化学成分分析,靶点预测,生物学过程和信号通路分析,以探讨黄芪-当归药对治疗中风的作用途径,为临床应用提供依据。
黄芪-当归药对中共发现25个活性较好、生物利用度较高的活性成分,黄芪20个,当归5个,二者并没有重叠的成分,从活性成分的数目上反映了人参-茯苓的主从地位。25个活性成分对应141个靶蛋白,多个成分对应1个靶蛋白,黄芪、当归中活性成分有共同对应的靶蛋白,如PTGS2 靶蛋白,它是刺激炎症反应的重要分子,参与中风的发病过程。因此,黄芪-当归药对在作用靶点水平具有协同增效的作用。为了探索黄芪-当归药对的潜在生物学机制,我们通过GO分析和KEGG通路富集发现,黄芪-当归药对参与多种生物学过程,包括衰老过程、损伤修复、血管收缩调节等,这些生物学过程与中风恢复密切相关,其作用通路与神经活性配体-受体相互作用、钙信号通路、胆碱能突触等信号通路有关。
综上所述,黄芪-当归药对治疗中风具有多靶点、多通路、多途径的特点,通过网络药理学分析,发现其治疗中风与多个潜在靶点和作用途径相关,但仍需体内外实验验证本研究中预测和分析的结果。
