基于网络药理学与分子对接研究四逆散治疗肝癌的作用机制
2020-09-28莫嘉浩许洪彬朱俊霞史佩玉邢万里林丽珠
李 菁,莫嘉浩,许洪彬,朱俊霞,史佩玉,邢万里,钟 崇,林丽珠
1 广州中医药大学 第一临床医学院,广州 510000; 2 湖南中医药大学第一附属医院 肿瘤科,长沙 410007;3 广州中医药大学 第二临床医学院,广州 510405; 4 广州中医药大学第一附属医院,广州 510000
原发性肝癌指发生于肝细胞或肝内胆管细胞的恶性肿瘤[1],位列致死性恶性肿瘤第三名[2]。我国是肝癌的高发地区,发病人数约占全球的一半,且仍呈上升的趋势[3]。西药在病情缓解、提高生存质量和延长生存时间等方面没有显著优势[4],而中医药治疗肝癌的临床疗效显著,并且可以减少肿瘤复发和转移,延长患者的生存时间,改善生存质量[5-6]。作为《伤寒论》的名方,四逆散由柴胡、芍药、枳实、甘草组成,具有解郁疏肝理脾之效[7]。现代研究[8]也表明,四逆散可抑制携带人肝癌基因的裸鼠的移植瘤生长,通过增强其氧化应激能力以促进凋亡。但因四逆散化学成分复杂,目前的研究对于四逆散治疗肝癌的完整的药效机制尚未明确。
网络药理学基于“化合物-靶点-通路-疾病”的相互作用网络,探究四逆散中潜在有效物质与核心治疗靶点,与中医的整体观念相符。而分子对接方法是一种基于配体-受体理论,通过化学计量学方法来模拟小分子配体与蛋白受体的几何匹配、能量匹配,以进行分子间相互作用识别并预测受体-配体复合物结构的一种方法,可用于研究成分与靶点的相互作用[9-10]。因此,本文拟联合网络药理学-分子对接以探究四逆散抗肝癌的有效物质、核心治疗靶点通路及分子机制,为进一步的实验研究提供理论参考。
1 材料与方法
1.1 四逆散化合物与靶标获取 运用中药系统药理学数据库和分析平台(TCMSP,http://lsp.nwu.edu.cn/tcmsp.php)分别查找柴胡、枳实、白芍、甘草,获取相应的化合物。以口服利用度(oral bio-availability,OB)≥30%,类药性(drug likeness,DL)≥0.18为条件进行化合物筛选,并运用TCMSP查找筛选所得化合物对应的靶标信息,将所得靶标信息输入Uniprot(http://www.uniprot.org/)获取靶标对应的基因Symbol。
1.2 肝癌疾病基因获取 以“hepatocellular carcinomas”、“liver cancer”、“hepatoma”、“hepatic cancer”、“hepatic carcinoma”为关键词从人类基因数据库获取肝癌的疾病基因,与四逆散的靶标基因对比后筛选出二者之间的交集基因。
1.3 构建“中药-化合物-治疗靶标”网络图 获取交集基因后,对化合物进行反向筛选,剔除靶标基因中不含交集基因的化合物,运用Cytoscape3.7.1软件绘制“中药-化合物-治疗靶标”网络图,根据软件所提供的“network analyzer”板块进行网络拓扑学分析。
1.4 蛋白质相互作用(PPI)网络构建 将所得交集基因输入STRING(https://string-db.org/)数据分析平台进行PPI网络分析,数据分析模式设定为“Multiple proteins”,物种限制为“Homo sapiens”。对数据进行预读后将置信度设置为≥0.900,并隐藏孤立蛋白,构建PPI网络,利用Cytoscape3.7.1软件对结果进行可视化。
1.5 GO富集以及KEGG通路富集分析 利用R studio软件的cluster profiler包对治疗靶标进行GO和KEGG富集分析,并利用ggplot2包对结果进行可视化。其中输出GO富集条形图展示生物进程、细胞组成、分子功能前十条富集结果。KEGG富集分析先计算靶标集合的每条富集通路的P值(使用Bonferroni法进行校正,P<0.01被认定是富集显著,P值越小富集越显著),输出KEGG富集气泡图。
1.6 活性成分与关键靶点的分子对接验证 在上述活性成分与核心靶点筛选结果的基础上,选择靶点数目最多的活性成分作为配体,取PPI网络中“Degree(度值)”最大的靶点作为受体,进行分子对接。步骤如下:查阅文献,确定需要对接的蛋白晶体结构域,从PDB网站(https://www.rcsb.org/)下载需要对接的蛋白,利用软件PyMol_2.3.0分离配体、受体并去除二者的水分子,将二者导入AutoDockTools_1.5.6并保存为“pdbqt”格式,设置蛋白原配体为对接盒子中心,其盒子大小设定为40×40×40,格子间距设定为0.375A,其余参数均设置为默认值,将下载好的蛋白文件、配体文件、化合物文件导入AutoDock Vina_1.1.2进行分子对接准备,结果导入DISCOVERY STUDIO软件进行结构预处理,并输出2D结构图,导入,最后导入PyMol_2.3.0处理数据,输出3D结构图。
2 结果
2.1 四逆散化学成分及靶标筛选结果 以OB≥30%,DL≥0.18为筛选条件,并对不满足条件但已有文献[11-13]报道具有明显药理活性的化合物进行补充(补充了柴胡皂甙a、柴胡皂甙D),去重后共得到141种活性成分,转换去重后共得到中药靶标基因394个;从数据库获得肝癌疾病基因共565种,取交集后有91个基因重合,为潜在靶标基因,详见图1。剔除不含交集基因(靶标)的化学成分后,筛得相关化学成分141种,其中柴胡19种,枳实23种,甘草93种,白芍13种,以柴胡为例,见表1。
2.2 “中药-化合物-治疗靶标”网络构建 基于91个重合基因相对应的化合物及中药,构建“中药-化合物-治疗靶标”网络,并利用Cytoscape软件对网络进行可视化,见图2。图中三角形、正方形、圆形分别代表中药、化合物、治疗靶标;绿色、红色、深蓝、黄色分别代表甘草、白芍、柴胡、枳实及其化合物,紫色代表治疗靶标,褐色为柴胡和甘草共有的化合物,浅蓝代表甘草和柴胡和白芍共有的化合物,褐色是枳实和甘草共同的化合物;节点的大小代表Degree的大小,按度值排序,前二的化合物是山柰酚与槲皮素。
2.3 PPI网络图构建 将治疗靶点导入string在线数据库,设置highest confidence(0.900),并去除游离靶点后,构建PPI网络,利用Cytoscape对结果进行可视化(图3)。图中节点大小代表Degree,根据Degree进行排序,数值较大的前20位为关键基因(表2)。
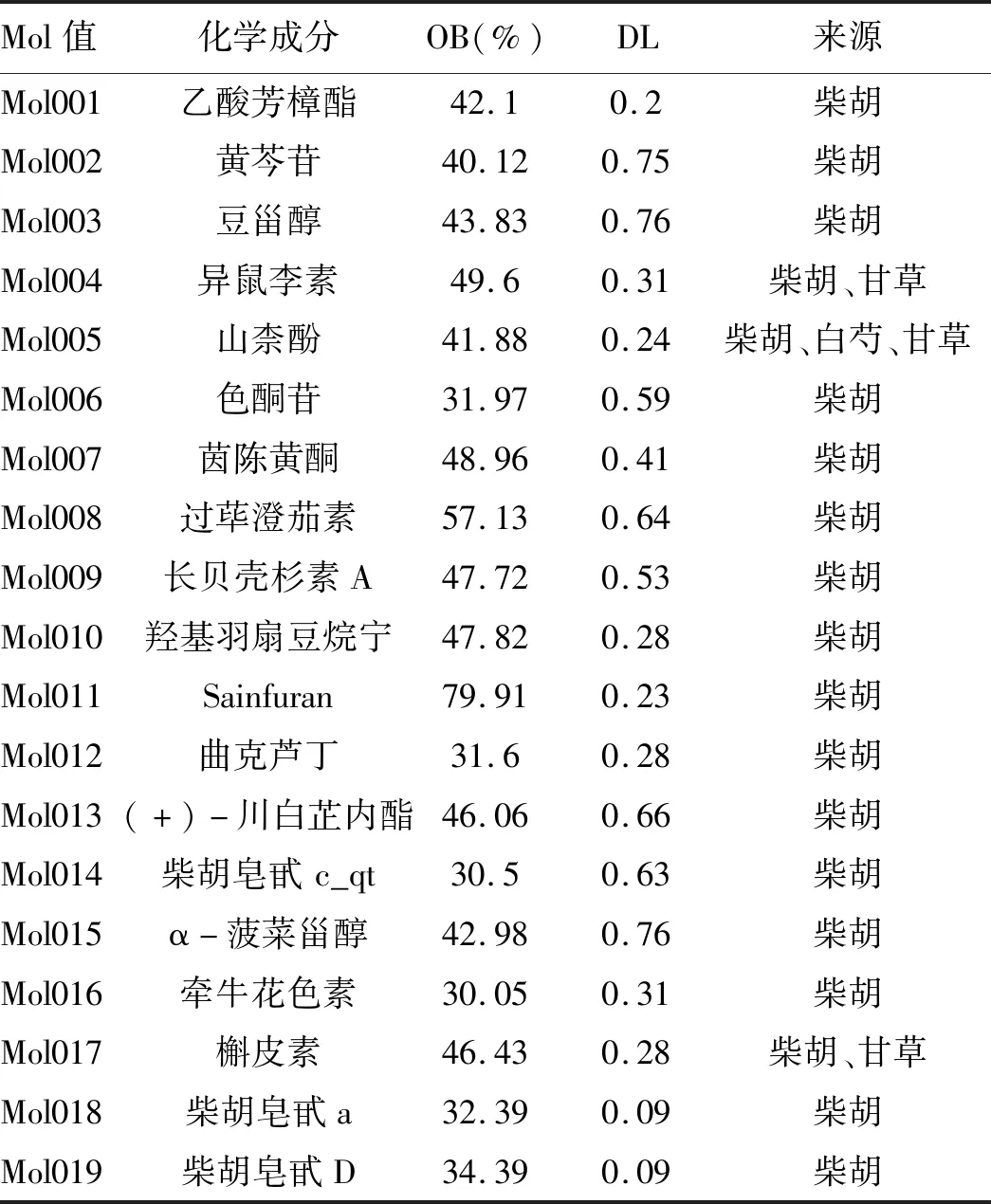
表1 四逆散活性成分基本信息表(以柴胡为例)
2.4 GO和KEGG功能富集分析 共得到GO富集条目1007条,KEGG富集结果102条。GO富集条形图展示生物进程、细胞组成、分子功能,CC,MF前十条富集结果(图4)。KEGG富集分析先计算靶标集合的每条富集通路的P值(使用Bonferroni法进行校正,P<0.01被认定是富集显著,P值越小富集越显著),对P值排序后取前15名进行分析(表3),并绘制KEGG气泡图展示富集通路结果(图5)。此外,对KEGG结果进行预读后发现,与四逆散治疗肝癌密切相关的通路有乙型肝炎通路、丙型肝炎通路、PI3K-Akt信号通路。
2.5 活性成分与关键靶点的分子对接验证 以上结果显示,槲皮素是预测靶点最多的活性成分,TP53为PPI 网络中 Degree最大的靶点,且经“中药-化合物-治疗靶标”网络图可知槲皮素与TP53存在相互作用。为进一步探究二者分子层面的相互作用位点,选择两者分别作为分子对接的配体和受体。
搜索查阅文献后发现,TP53所表达的蛋白P53对肿瘤细胞具有抑制生长、促进凋亡的生物学功能[14],P53容易突变是引起近半数癌症的原因[15],新近国外研究[16]发现6GGA、6GGB、6GGC、6GGD、6GGE、6GGF等结合后稳定且可正常运作,故可通过稳定P53-Y220C突变体以抗癌,由于均是同一个活性位点,故取6GGA进行分子对接验证。从PDB网站(https://www.rcsb.org/)下载槲皮素三维结构(图6)。经对接,结果显示槲皮素能稳定地对接到TP53蛋白结构6GGA的活性口袋中,通过氨基酸残基VAL147、THR150发生π-σ键作用;通过CYS220发生π-硫键作用;通过GLU221发生π-氨基键作用,通过PRO222、PRO223、PRO151发生π-烷基作用。槲皮素与TP53(6GGA)分子对接2D结构结果见图7,3D结构显示结果见图8。

表2 排名前20的关键基因
3 讨论
四逆散为仲景名方,方中柴胡辛散、芍药酸收、甘草甘缓,三药配伍共奏调肝用、补肝体、防肝变之效[17],在抗肝癌的临床研究[18-20]使用频繁。但目前针对四逆散治疗肝癌的网络药理学与分子层面的研究尚有欠缺。因此,本研究拟联合网络药理学-分子对接以进行成分-靶点-通路-分子结合的研究思路,探究四逆散治疗肝癌的机制,为临床研究奠定基础。
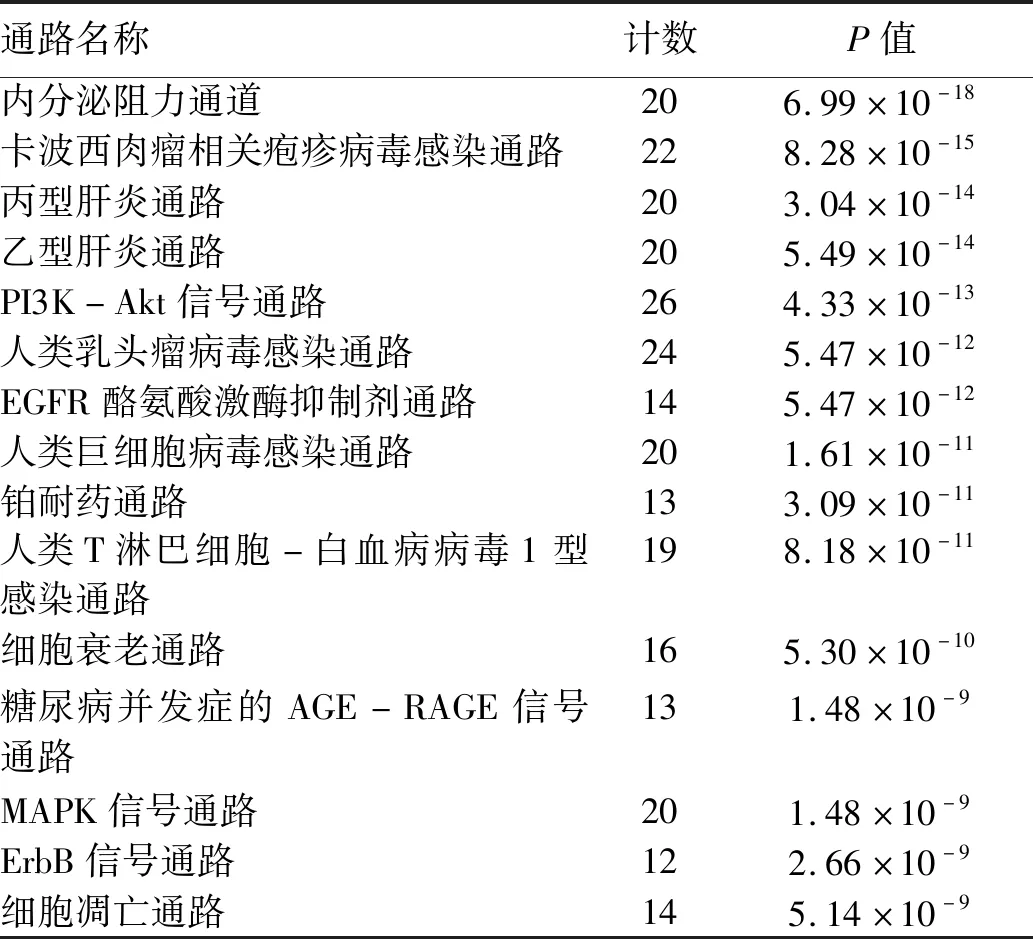
表3 前15位KEGG通路富集表
经过筛选与取交集后,获得治疗靶标基因91个,最终筛得潜在化合物141种,其中部分化合物的有效性及作用机制已被证实。在潜在化合物中,柴胡、白芍、甘草均富含山柰酚;而柴胡、甘草均含有槲皮素,上述两种化合物均处于网络图的核心,并具有较高Degree,提示这些化合物对应的靶标基因可能在四逆散抗肝癌过程中起主要作用。查阅相关文献可知,山柰酚为常见的黄酮类化合物,有国外研究[21]发现,山柰酚可抑制HepG2细胞的增殖、迁移和侵袭以调节肝癌的进程;而槲皮素作为一种强大的自由基清除剂,经证实亦可调节TP53以抑制肝癌细胞增殖,与本研究PPI网络所得的关键基因靶点结果一致[22]。
提取活性成分与交集靶标基因后,由PPI网络图可知TP53、HSP90AA1等靶标为其中心,提示其可能是核心治疗靶标。其中TP53突变在HBV感染导致的肝癌中有重要意义[23],其HBV致癌通路也是本研究后续的KEGG通路富集结果之一;有新近研究[24]发现HSP90AA1在中重度抑郁组肝癌患者中呈高表达,且与肝癌患者的肿瘤临床分期存在一定相关性[25]。
GO功能富集结果主要集中在蛋白丝氨酸-苏氨酸激酶活性调控、细胞应激反应等过程,而KEGG通路富集结果显示,四逆散主要作用于乙型肝炎通路、丙型肝炎通路、PI3K-Akt信号通路等。其中蛋白丝氨酸-苏氨酸激酶的过度表达跟肝癌的发生、分化、转移进程高度相关[26];根据肝癌防治专家指南与近期研究[27-28],乙型肝炎与丙型肝炎是肝癌发生发展的重要病因之一,结合本研究的分析结果,乙型肝炎通路确是四逆散防治肝癌发生发展的重点;根据基因学研究[29]显示,治疗丙型肝炎相关性肝癌可通过调控CCND1靶点以调节肿瘤细胞的分化,而CCND1也是前述PPI网络中的核心靶标之一;PI3K-Akt信号通路参与细胞的生长、增殖、凋亡等过程,对多种癌症存在着重要的调控作用[30]。
基于前述结果,本研究选取预测靶点最多的活性成分槲皮素作为配体,发现其能稳定地对接到Degree最大的关键靶点TP53的抗癌相关蛋白结构(PDBID:6GGA)上,二者通过氨基酸残基VAL147、THR150发生π-σ键作用;通过CYS220发生π-硫键作用;通过GLU221发生π-氨基键作用,通过PRO222、PRO223、PRO151发生π-烷基作用。TP53亦称P53,是一种抑癌基因,其参与槲皮素调控肝脂肪变性进程中线粒体自噬及稳态维持[31],而肝脂肪变性是正常肝组织癌变的其中一个重要过程;另有药理学实验[32]证实,槲皮素可诱导P53非依赖的G2/M细胞周期阻滞以及促进细胞的凋亡进程以抑制人肝癌细胞增殖,均与本研究的分子对接验证结果相符。
综上所述,本研究通过联合网络药理学分析与分子对接验证,发现槲皮素、山柰酚为四逆散的主要活性成分,以TP53、HSP90AA1等为核心靶标,涉及抗氧化反应、蛋白丝氨酸-苏氨酸激酶活性调控等多个生物过程,并通过调控乙型肝炎通路、PI3K-Akt信号通路以防治肝癌,可与新近的关于四逆散中“白芍-柴胡”药对治疗肝癌的研究结果互相印证[33],但该研究仅停留在传统网络药理学的靶标通路,缺少在分子层面的抗癌蛋白结构域研究,故本研究最终通过分子对接验证了槲皮素-TP53的VAL147、CYS220、GLU221、PRO222等靶蛋白晶体结构域的协同抗癌效应,为后续分子层面的中药抗癌研究提供理论支持。
