阿帕替尼治疗二线及以上食管癌的疗效观察
2020-09-23濮忠建孙元鹏王亚军
杨 帆 濮忠建 孙元鹏 王亚军
江苏省海安市中医院肿瘤科 226600
食管癌是常见的恶性肿瘤,其发病率位居全球癌症的第8位,死亡率位于第6位[1]。而在中国,食管癌的发病率和死亡率也居高不下,仅次于肝癌、胃癌、肺癌[2]。该病具有发病隐匿、进展快的特点,多数患者发现时已经处于中晚期。化疗是这类患者的主要治疗手段,一线主要选择紫杉类、氟尿嘧啶类、铂类为基础的联合化疗,但二线及以上治疗无标准的治疗方案。阿帕替尼为我国自主研发的抗VEGGR-2的靶向药物,对晚期食管癌有一定疗效。本文旨在观察阿帕替尼用于治疗一线治疗失败后食管癌的临床疗效和不良反应,并探讨预后影响因素。
1 资料与方法
1.1 临床资料 收集2017年1月—2018年12月于我院肿瘤科诊治的食管癌患者57例,其中食管鳞癌30例,腺癌1例,小细胞癌2例,既往接受食管癌根治术15例,放疗13例,紫杉醇联合奈达铂化疗27例,替吉奥单药化疗30例。常规行胸腹部增强CT、颈部淋巴结彩超、头颅CT或MRI检查。纳入标准:(1)所有患者均经胃镜或术后病理明确为食管恶性肿瘤;(2)既往接受过至少一种化疗方案后出现复发或转移;(3)年龄18~70岁;(4)KPS评分≥70分,预计生存期不少于3个月;(5)血常规中白细胞计数≥4.0×109,血红蛋白≥90g/L,血小板计数≥75×109,无肝肾功能损伤。排除标准:(1)根据实体瘤RECIST1.1评价标准,有可测量的靶病灶,且既往接受过放疗或靶向治疗;(2)不能口服药物者;(3)有经药物难以控制高血压;(4)妊娠及哺乳期妇女。本研究经我院伦理委员会批准并签署相关治疗同意书。
1.2 方法 均行阿帕替尼(江苏恒瑞医药股份公司,规格:250mg/d,国药准字H20140103)单药治疗,药物起始治疗剂量为500mg,早餐后0.5h口服,1次/d,28d为1个治疗周期,根据出现的毒副反应,可酌情降低剂量至200mg,直至出现不可耐受的毒副反应或发生病情进展。治疗1周期后评价疗效。
1.3 评价指标 评价临床疗效,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。ORR=(CR+PR)/总例数×100%,DCR=(CR+PR+SD)/总例数×100%。不良反应根据WHO标准分为0~4级。KPS评分按照体力状况的大小为0~100分,共分10级,每10分为1级,100分为患者体力状况正常,无症状和体征,0分为死亡。
1.4 统计学方法 所得数据采用SPSS20.0软件进行统计学分析,计数资料采用χ2检验,生存分析应用Kaplan-Meier法,采用log-rank检验分析影响PFS的各项因素,多因素生存分析采用Cox回归模型。P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效 本组57例患者均完成评价,其中CR 0例(0%),PR 13例(22.81%),SD 28例(49.12%),PD 16例(28.07%),ORR 为22.81%,DCR为71.93%。
2.2 治疗相关不良反应 治疗期间最常见的副反应是高血压和蛋白尿,高血压发生率为50.88%,蛋白尿发生率为36.84%。见表1。
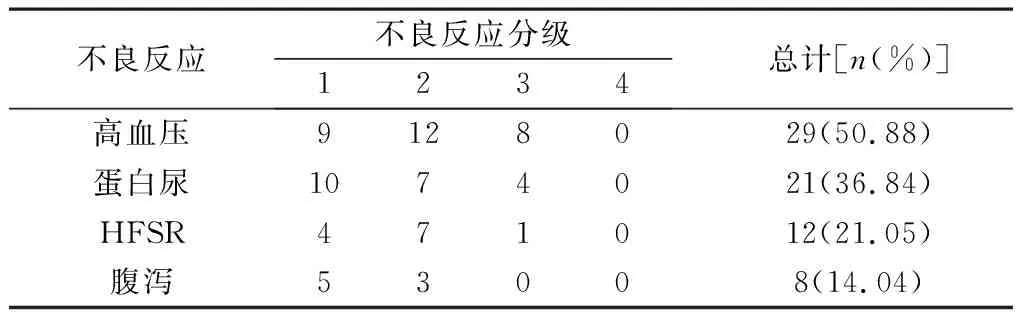
表1 阿帕替尼治疗二线及以上食管癌不良反应发生情况
2.3 阿帕替尼后的无进展生存期(PFS)影响因素 通过χ2检验得知,PFS的影响因素与年龄、性别、吸烟史、饮酒史、蛋白尿、HFSR无关(P>0.05)。KPS评分、高血压与PFS有关联(P<0.05)。见表2。Cox多因素回归分析表示,KPS评分、高血压是患者PFS的独立预后因素。见表3。
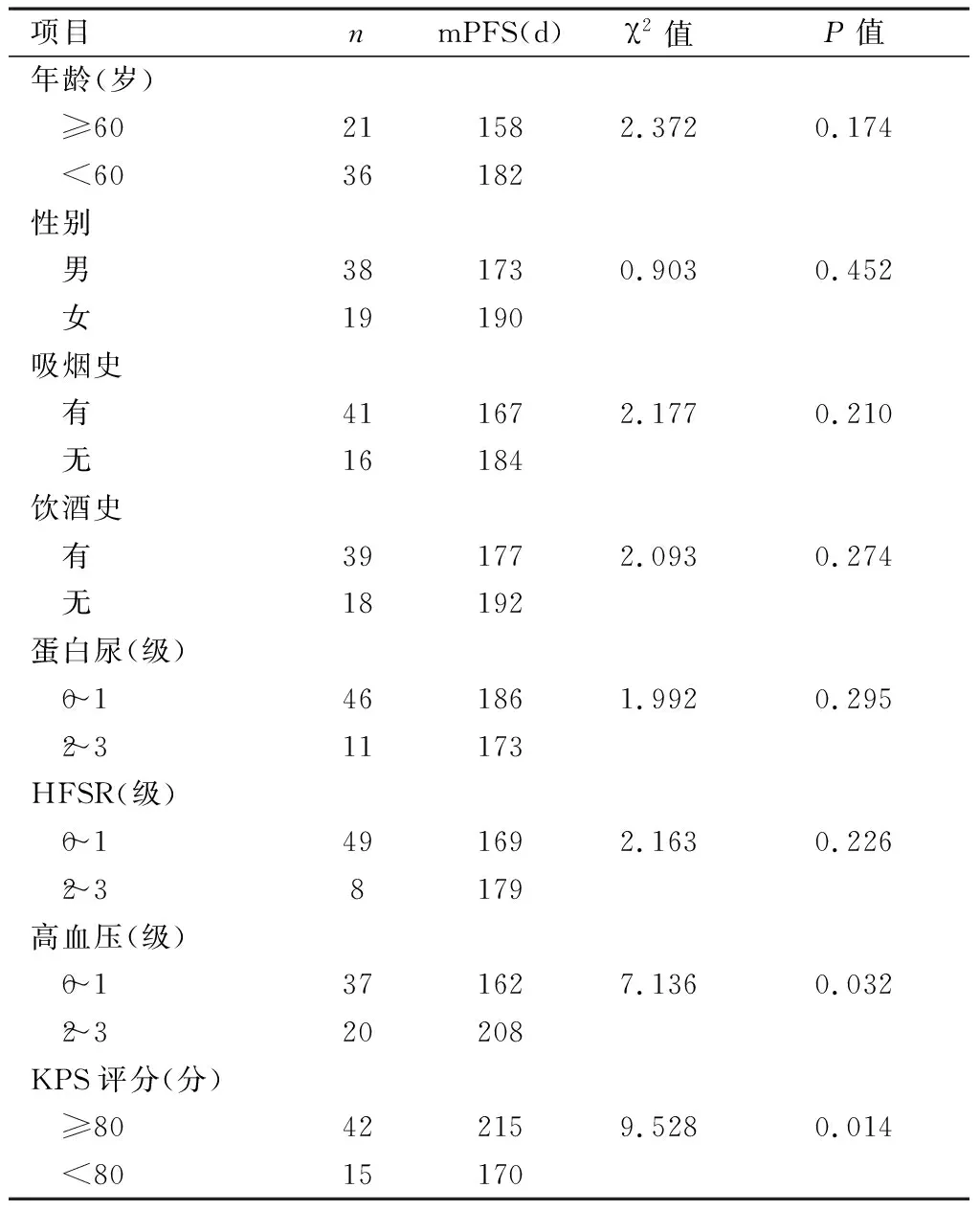
表2 临床特征与PFS关系的单因素分析

表3 PFS关系Cox多因素回归分析
3 讨论
食管癌是我国常见的恶性肿瘤,发病率和死亡率均位居前列,且我国食管癌以食管鳞状细胞癌为多见,食管腺癌及小细胞癌较少见。中晚期食管癌主要的治疗手段是放化疗,但二线及以上治疗没有标准的方案。食管癌的发生与肿瘤血管生成有密切关联,郭晓峰等[3]对153例食管鳞癌组织中血管生成抑制蛋白1(VASH1)和血管内皮生长因子(VEGF)的表达情况进行分析,结果显示癌组织中二者的表达均高于癌旁组织,而VASH1是抑制肿瘤血管生成的重要基因,VEGF可诱导VASH1的表达,这提示食管癌的发生、发展与血管生成密不可分。
甲磺酸阿帕替尼是我国自主研发的新型抗血管生成抗肿瘤靶向药,可拮抗VEGF与VEGFR-2的结合并抑制VEGFR-2的磷酸化,并对抗肿瘤细胞的增殖、迁移,进而起到抗肿瘤作用。周梦耘等[4]建立食管癌裸鼠模型,采用阿帕替尼联合放疗对比单纯放疗的疗效和机制,结果显示,联合组较单纯放疗提高了对VEGFR-2、微血管密度(MVD)表达的抑制。
本文结果显示:ORR达22.81%,DCR为71.93%。不良反应方面,高血压发生率为50.88%,蛋白尿发生率为36.84%,HFSR的发生率为21.05%,腹泻的发生率为14.04%,除高血压的发生率同Song等[5]以及马国军等[6]报道的一致外,蛋白尿、HFSR、腹泻的发生率均低于这两项研究,其原因可能是本研究入组的人群一般状况较好、肿瘤负荷较轻。
预后因素方面,KPS评分及用药后出现高血压是影响患者PFS的独立预后因素,多因素回归分析也表明KPS评分及用药后出现高血压是患者PFS的危险性因素。这与赵青芳等[7]的研究结果一致。对于KPS评分<80的患者,体力状况较差,提示肿瘤分期较晚、肿瘤负荷大、治疗的耐受性较差,进而影响阿帕替尼的疗效。抗血管生成靶向药的常见副反应之一是高血压,在使用该类靶向的患者中,几乎所有患者均会出现血压升高,其中一部分患者发展为高血压[8]。抗血管生成药物不同,其高血压的发生率也不一样。一些荟萃分析显示,诸如贝伐珠单抗、索拉菲尼、舒尼替尼药物治疗相关性高血压的发生率为19%~67%不等[9-10]。Li等[11]采用阿帕替尼联合化疗治疗晚期胃肠道肿瘤患者,高血压发生率为35.2%。目前,有研究显示,抗血管生成靶向药相关性高血压是临床疗效的预测指标之一,出现高血压提示可能会出现更好的治疗效果[12]。Zhong等[13]回顾82例接受贝伐珠单抗治疗的脑胶质瘤患者,出现高血压组患者的PFS和OS均明显高于未出现高血压组,这提示治疗出现高血压可能带来更多的临床获益。本文结果进一步验证了这一观点。
由此可见,甲磺酸阿帕替尼对食管癌具有一定疗效,主要的不良反应是高血压、蛋白尿、HFSR、腹泻等,但不良反应相对较轻,安全可控。治疗相关性高血压、KPS评分是影响疗效的预后因素,值得临床关注。
