纳米零价铁降解水中17β-雌二醇的作用机制
2020-09-23杨硕余薇薇杨伦杜邦昊谢明原赵晨菊万巧玲潘伟亮
杨硕,余薇薇,杨伦,杜邦昊,谢明原,赵晨菊,万巧玲,潘伟亮
(1 重庆交通大学河海学院,水利水运工程教育部重点实验室,重庆400074;2 国家城市供水水质监测网重庆监测站,重庆400060)
随着中国城市化进程和规模化畜禽养殖业的迅猛发展,大量天然类固醇雌激素(NSE)通过污水处理厂、养殖废水排放和沼液灌溉进入周边水体和土壤[1-2],给自然环境带来严重威胁。NSE主要包括雌酮(E1)、17β-雌二醇(17β-E2)、17α-雌二醇(17α-E2)和雌三醇(E3)。因具有强烈的内分泌干扰性,传统污水处理工艺降解效果有限[3],NSE的有效降解已成为世界各国研究的重要环境课题之一。其中17β-E2 具有雌激素活性最高、稳定性较强、自然水体中广泛检出等特点[4],环境危害性最大。近年研究表明,我国长江、珠江等主要地表水体中17β-E2 和E1(17β-E2 主要转化产物)均有较高检出率和检出浓度[5-6]。
目前,光催化氧化[7]、微生物降解[8]、碳纳米管吸附降解[9]等方法被相继用于降解NSE。然而大多数方法仅能在污水处理单元中发挥作用,难以用于NSE 污染水体的修复。纳米零价铁(nZVI)作为一种广泛应用于水体及土壤修复的纳米材料,因其纳米尺寸、高比表面积、高活性、低制备成本和低环境危害性等特点[10],被认为是有机污染物污染水体修复的理想材料。近年来,已有关于nZVI 降解NSE的报道,其中Ali等[11]研究了nZVI对17β-E2的吸附机理;Jarosova等[12]验证了nZVI降解17β-E2的可行性。然而针对nZVI 降解NSE 的作用机制及其作用下NSE降解路径尚不明确。
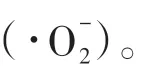
1 实验材料和方法
1.1 仪器、试剂与材料
仪器: 岛津三重四级杆液质联用仪(Shimadzu LC-MS/MS-8060)、日立高效液相色谱(Chromaster 5100,Hitachi)、UV-Vis 分光光度计(HACH DR6000)、场发射扫描电镜(JEOL,JSM-7800F)、X 射线衍射仪(Rigaku Ultima Ⅳ)、电镜能谱仪(ZEISS JSM-6360LV)、12位固相萃取装置(Mediwax-12)、水浴氮吹仪(MTN-2800W-12)、涡旋混匀器(VORTEX-5)等。
试剂:雌酮(E1,纯度≥99%)、17α-雌二醇(17α-E2,纯度≥98%)、17β-雌二醇(17β-E2,纯度≥99%)、雌三醇(E3,纯度≥98.5%)均购于北京百灵威(J&K)科技有限公司;氘代雌酮(E1-d4,纯度≥99.5%)购于加拿大CDN 同位素公司;纳米零价铁(nZVI,纯度>95%,平均粒径80nm)购于上海阿拉丁生物科技有限公司。甲醇、乙腈、异丙醇、三氯甲烷等均为HPLC 级。盐酸、氢氧化钠、乙酸铵等均为分析级。
材料:NH2固相萃取柱(Welchrom® 6cc/500mg)、高纯度氮气(纯度≥99.999%)、自动进样器及柱转换接头等。
1.2 实验方法
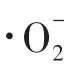
试验后使用高强度钕铁硼(NdFeB)磁体在氮气保护下加速nZVI的沉积,沉积物在氮气保护下干燥并用2mL甲醇淋洗3次后放入充满氮气的玻璃样品瓶。应用XRD及FESEM表征nZVI反应前后的变化。
1.3 检测方法
17β -E2 浓 度 检 测 应 用 带 有C18色 谱 柱(4.6×150mm,5µm)的高效液相色谱仪,流速1.0mL/min,流动相为45%乙腈和55%超纯水,201nm 波长紫外条件。17β-E2 标准曲线呈线性关系(R2>0.999)。
邻菲罗啉分光光度法[13]改进后用于Fe2+浓度测量。0.5mL 样品过0.22µm 尼龙膜,滤液显色后在510nm 下测量吸光度。Fe2+标准曲线的检测范围为0.02~5.00mg/L(R2>0.999)。
应用高效液相色谱串联两级质谱仪(HPLCMS/MS)鉴定17β-E2 可能的降解产物。设两组重复试验,量取50mL 样品过膜后通过NH2固相萃取柱浓缩纯化。活化液为5mL 甲醇和5mL 超纯水,洗脱液为5mL 甲醇/乙酸乙酯(体积比1/1)和5mL 5%氨水甲醇溶液,水浴氮吹后2mL 甲醇重溶解。在ESI(-)模式下分析产物,扫描范围m/z=50~1200,详细参数见表1。17β-E2、17α-E2、E1、E3标准曲线均呈线性关系(R2>0.999),LC-MS/MS检测检出限(LOD)范围为0.07~0.39ng/L,定量限(LOQ)范围为0.24~1.18ng/L。
2 结果与讨论
2.1 17β-E2降解动力学
通过IBM SPSS 25 和Origin 2018 进行伪一级动力学拟合,改进的拟合公式[14]如式(1)所示。
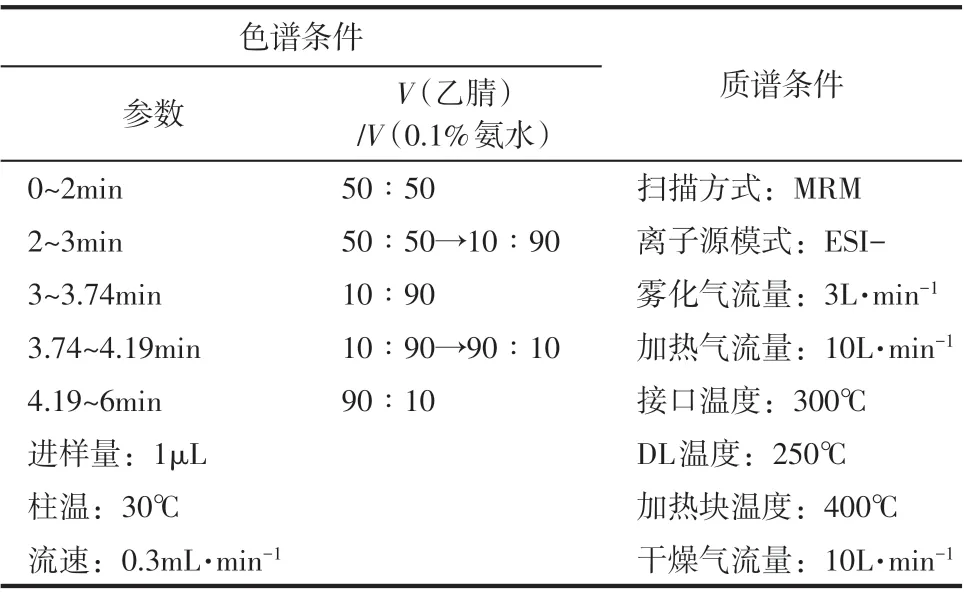
表1 三重四级杆液质联用仪分析参数

式中,R 为t 时刻17β-E2 的降解率,即R=Ct/C0;Rmax为反应器中17β-E2的理论最大降解率,即Rmax=Cmax/C0;k为拟合的一阶速率常数,min-1。
拟合的伪一级动力学曲线如图1所示,相关系数(R2)大于0.95(p<0.01)。说明模型对17β-E2的降解过程拟合良好,可用于评估nZVI对17β-E2的降解动力学。
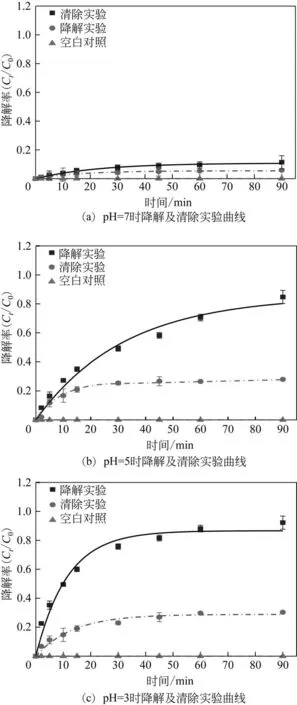
图1 不同pH下nZVI降解17β-E2动力学曲线
nZVI 对17β-E2 的降解效率在pH=5 和3 时较高,分别为84.72%±2.74%和92.3%±4.55%(图2)。总体上,nZVI 在酸性条件(pH=3,5)下可高效降解17β-E2,而中性条件(pH=7)时效率较低,为11.41%±1.25%。
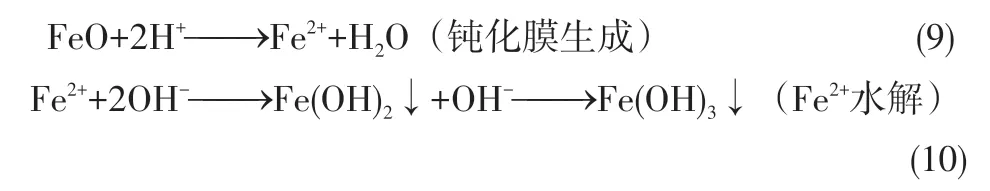
清除实验中,pH=7 时17β-E2 降解率仅为5.47%±0.19%[图1(a)],结合能谱分析结果(后文2.4节)说明该降解体系中17β-E2的降解主要依赖降解而非吸附作用。pH 从5 上升到7 时,体系中17β-E2 的降解率大幅下降。这是由于高pH(pH>6)时,nZVI在溶解氧和OH-的作用下[式(2)]表面被致密的钝化膜、铁离子水解产物和其他沉淀物覆盖,活性点位减少,材料与污染物的接触受到限制,从而导致其降解性能的下降[15-17]。而图3中,pH=7时Fe2+浓度的快速下降至趋于0也证实了体系中离子水解的存在。相比之下,pH从5下降到3时降解率仅有小幅上升。较低pH时,体系中17β-E2的降解呈现一定程度抑制的现象,一方面归结于nZVI过快的酸腐蚀不利于H2O2的生成[式(3)],另一方面体系中产生的氢(H2)在nZVI 表面形成密集的微小气泡[式(6)],阻碍nZVI 在低pH 条件时的反应[18]。虽然pH=3时17β-E2的降解率受一定影响,但其降解速率却大幅提升(表2)。这是由于酸性条件下Fe2+的加速产生,进一步加速ROS的生成[式(4)、式(5)]。且H+在nZVI 作用下转化为H2的过程中可能导致更多活性氢原子([H])的生成[19][式(6)],从而加快反应速度。在nZVI/H2O2降解诺氟沙星报道中[20],也发现了低pH 下存在类似趋势。
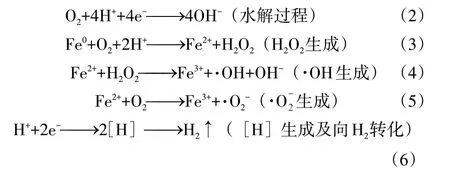
2.2 ∙OH和的贡献
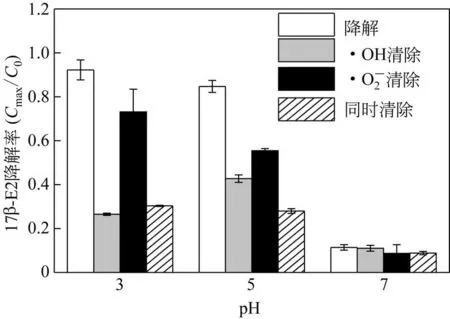
图2 反应90min后不同pH下17β-E2降解率
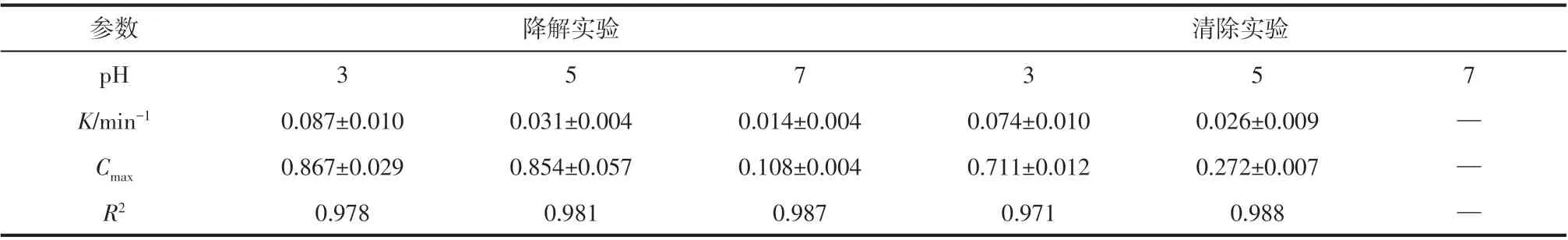
表2 降解及清除动力学曲线拟合数据

图3 不同pH下nZVI降解17β-E2过程中Fe2+浓度
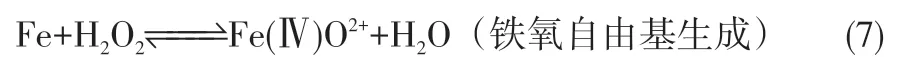

2.3 nZVI的腐蚀及Fe2+的产生
对降解实验和清除实验中Fe2+浓度进行连续监测,以评估体系中nZVI腐蚀情况对17β-E2降解的影响(图3)。pH=7 时,反应前期Fe2+浓度少量增加后迅速下降至趋近于零,证实了中性条件下17β-E2的降解被nZVI 的表面钝化所阻。pH=5时,Fe2+浓度先快速升高后缓慢降低至平衡,且最高浓度仅有pH=3时的61.61%±0.002%。这是因为pH>4时,酸性条件对nZVI 表面氧化膜的抑制作用[式(9)]降低,氧化膜限制Fe2+的产生;另一方面,Fe(OH)3的生成[式(10)]在消耗Fe2+的同时促进Fe2+向Fe3+的转化。pH=3时,Fe2+浓度在前15min内快速增加后趋于稳定,与17β-E2 在前15min 的快速降解一致;15min 后,Fe0向Fe2+的转化以及Fe2+向Fe3+的转化达到动态平衡,17β-E2 的降解速率降低并趋于平衡。总体上,17β-E2 的降解率和降解速率和Fe2+的浓度和生成速度相关[24]。
清除实验中,Fe2+浓度均略低于降解实验,这是因为∙OH和∙O2-被捕获后促进了式(4)和式(5)的反应平衡向生成Fe3+的方向移动,而非淬灭剂和Fe2+的直接作用。清除和降解实验反应0~40min 阶段Fe2+的浓度差值较大,从而表明pH=5时17β-E2 较高的降解率主要依赖于Fe2+引导的Fenton反应。
2.4 反应前后nZVI表征
对反应前后的nZVI 进行EDS 表征结果见表3,实验中使用的nZVI 含有微量的Cu 和C,为液相还原法制备。反应后,样品中出现了Cl,C含量的增加,说明nZVI 对氯仿等有机物有少量吸附。当nZVI 投加量大于0.4g/L 时开始表现对NSEs 的降解[11],大于1g/L时表现出对NSEs的明显吸附[12],而实验所用0.5g/L nZVI 对17β-E2 的降解以降解为主。
对nZVI 反应前后的XRD 表征见图4,分析表明实验所用nZVI 为体心立方结构,反应后仅观察到微弱的FeO峰,且存在许多细小杂峰。微弱的氧化峰,可能因为nZVI 表面致密的钝化膜阻止了其进一步氧化。对XRD 进行全谱拟合,nZVI 平均粒径计算为80nm,反应后nZVI 的平均粒径大于100nm 且晶面间距减小,表明反应后nZVI 颗粒发生了一定的磁性聚集。
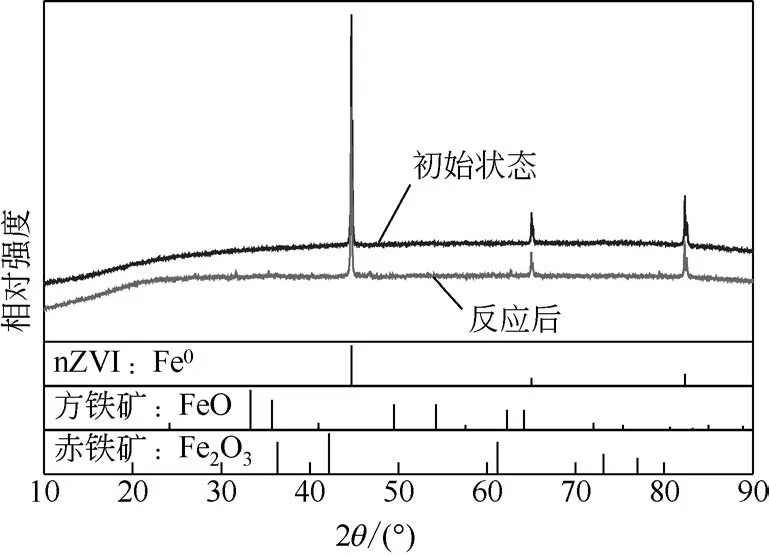
图4 反应前后nZVI的XRD图谱

表3 反应前后nZVI能谱检测数据

图5 反应前后nZVI的扫描电镜图
应用FESEM 对反应后nZVI 的形貌变化进行表征(图5),放大5 万和10 万倍观察nZVI 的形貌特征。nZVI 颗粒呈规则的球形,平均粒径在80~100nm之间,材料呈现簇状聚集但分散性良好。反应后,nZVI的球形结构因腐蚀和氧化作用而坍塌,颗粒呈明显的聚集,并产生鳞片状和棱锥状结构[26]。这说明nZVI可通过自身腐蚀产生Fe2+等进一步诱导产生ROS,其降解污染物的能力受钝化和磁性聚集所限制。
2.5 17β-E2降解产物和路径分析
通过贝农表-相对丰度法分析降解产物可能的分子结构[27]。3 种已知转化产物(E1、17α-E2 和E3)可定量分析(表4),其中17α-E2、E3均未检出,说明17β-E2 的D 环除了C17 处的羟基易转化为酮基外相对稳定(图6)。在所有实验中E1 均有检出,浓度见表4,表明17β-E2 易被nZVI 转化为E1,而自然条件下E1 也是17β-E2 的主要转化产物[1,28]。随着pH值的降低,E1的产率降低,说明转化生成的E1 可在较低pH 值下被nZVI 进一步降解。
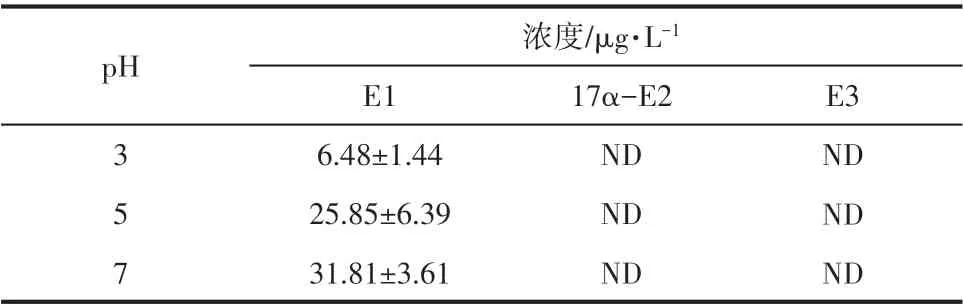
表4 3种已知转化产物定量浓度

图6 类固醇雌激素分子结构
pH=7 时,检测到负离子碎片m/z=255(MW=256,C18H24O)、m/z=273 (MW=274,C18H26O2)、m/z=289 (MW=290,C18H26O3)、m/z=293 (MW=294,C18H30O3)和m/z=307(MW=308,C18H28O4),可能的降解路径如图7所示。

图7 不同(pH=3、5、7)时17β-E2可能的降解路径
17β-E2转化为E1后未检测到进一步的降解产物。17β-E2 的主要降解路径为A 环基团的替换、断裂和开环。Du 等[29]通过软件计算17β-E2 的Fukui指数,得出17β-E2 A环的C2和C4位具有最高的Fukui 指数(0.102 和0.101),而高的Fukui 指数表明它们相较其他点位更易失去电子,被·OH和∙O2-等强亲电子基团取代[30]。17β-E2可能的降解路径为A环(芳香环)失去电子(MW=284),羟基或酮基取代(MW=290),A环的开环(MW=308)以及脱羟基(MW=294)。
pH=3 和5 时,未检测到到负离子碎片m/z=293,新检出m/z=285(MW=86,C18H22O3)、m/z=303(MW=304,C18H24O4)、m/z=541(MW=542,C36H46O4)和m/z=811(MW=812,C54H68O6),可能的降解路径如图7所示。
17β-E2转化为E1后在酸性条件下可被进一步降解,其可能的降解路径为A 环的羟基取代和开环。自然条件下,E1(19h)与17β-E2(13h)相比半衰期更长,因此更稳定[31]。当pH 升高,ROS产率下降时,ROS优先攻击相对不稳定的17β-E2。pH=3 时,新检出m/z=249(MW=250,C17H30O)和m/z=279(MW=280,C18H32O2)。在低pH 时,17β-2E A 环开环后可进一步降解,表现为脱羟基及A环的彻底断裂。此外不排除17β-E2 在Fenton 反应作用下彻底矿化的可能[32]。
由图7 可知,产物17β-E2 二聚体和三聚体表明nZVI 体系在酸性条件下可进行仿漆酶反应,将底物活化为有机自由基进行自由基偶联或相互共价偶联[33]。而17β-E2 二聚体最有可能在C2-C4',C4-C2'和C2-C2'之间偶联,三聚体则最有可能在C4-C2',C2-C2'和C2-C2',C4-C4'之间偶联[34]。
3 结论
酸性条件下,17β-E2可被nZVI迅速降解;而中性条件下,钝化膜和铁离子的水解产物包裹nZVI 表面,限制其降解污染物能力。17β-E2的降解率和降解速率与Fe2+浓度及生成速度呈正相关。Fe2+主导的Fenton 反应在nZVI 体系中占有重要地位。

