缺血后处理对大鼠脊髓缺血再灌注损伤的保护作用及对钙敏感受体和Caspase-12表达的影响
2020-09-21张睿孙继芾陈谦曹苏成黄永辉
张睿,孙继芾,陈谦,曹苏成,黄永辉
(1. 江苏大学医学院,江苏 镇江 212013; 2. 江苏大学附属医院脊柱一科,江苏 镇江 212001)
脊髓缺血再灌注损伤(spinal cord ischemia-reperfusion injury,SCIRI) 是指临床上由于脊柱骨折、胸腹主动脉瘤压迫等情况下,脊髓在特定时间段进入相对缺血的状态,医生通过手术解除压迫后,脊髓组织得以恢复灌注,但是其功能并没有恢复,反而在之前的功能障碍上逐渐加重,出现难以逆转的神经功能损害,甚至导致肢体瘫痪等严重后果[1-2]。脊髓神经细胞对缺氧缺血的反应相当敏感,短时间内即可引起明显的脊髓损伤,目前临床上仍没有有效的预防措施[3]。近年来有学者发现,缺血后处理(ischemic post-conditioning,IPC)对SCIRI具有保护效果[4],然而其保护机制尚无定论。钙敏感受体(calcium-sensing receptor,CaSR)在机体多个组织器官广泛表达,参与维持胞内钙离子稳态[5]。发生SCIRI过程中,神经细胞内钙超载是关键环节,而CaSR在其调节中举足轻重[6]。研究证实CaSR在大鼠脊髓神经细胞的胞质内广泛表达,并且在缺血再灌注损伤时表达增加[7]。同时Caspase-12是钙超载诱导内质网应激导致细胞凋亡这条信号通路中的特异性蛋白[8],因此Caspase-12表达变化能间接反映CaSR变化。本实验通过建立大鼠SCIRI模型,观察IPC对SCIRI的保护作用及IPC后脊髓组织中CaSR和Caspase-12表达的变化。
1 材料与方法
1.1 动物与试剂
清洁级SD大鼠50只,雌性,体重220~250 g,由江苏大学动物实验中心提供,合格证号:NO.201905966,许可证号:SCXK(苏)2018- 0012。β-肌动蛋白抗体、CaSR抗体(兔抗鼠)及Caspase-12抗体(美国CST公司);羊抗兔二抗(美国Abcam公司);GdCl3(美国Sigma公司);NPS2390(美国Tocris公司);EnVision免疫组化试剂盒(丹麦Dako公司);TUNEL检测试剂盒(瑞士Roche公司)。
1.2 动物分组
采用SRS抽样法将50只SD大鼠平均分为5组:假手术组,缺血再灌注模型组(IR组),IR模型+IPC组(IPC组),IR模型+IPC+激动剂组(IPC-GdCl3组)和IR模型+抑制剂组(NPS2390组)。
1.3 建立SCIRI模型
IPC-GdCl3组和NPS2390组,提前2天经大鼠尾静脉分别注射CaSR激动剂GdCl3或CaSR抑制剂NPS2390,剂量分别为30 μmol/kg、10 μmol/kg,注射2天。术前充分禁食禁水。假手术组大鼠予腹腔麻醉(7%水合氯醛),手术开腹游离腹主动脉,不进行其他处理,暂不完全缝合切口,待30 min左右关腹。其余各组大鼠麻醉后均采用改良Zivin法建立SCIRI模型[9-10]:腹腔注射麻醉,待麻药起效后(约数分钟)予腹部备皮,将大鼠牢靠固定于手术台,予皮肤消毒并铺巾;取腹正中线切开约3 cm切口,轻轻掀开大网膜及肠管,钝性分离软组织,显露腹主动脉,沿其主干找到肠系膜前动脉及右肾动脉,游离之间的腹主动脉段,使用清洁的金属动脉夹将其夹闭。为保护大鼠胃肠道等其他内脏器官,先用生理盐水冲洗局部腹腔,将外翻的大网膜、肠管理顺后小心纳入切口,切口暂不完全缝合,将动脉夹柄部留于腹腔以外,周围填盖清洁温水打湿的棉球以保暖。25 min后,小心取出动脉夹,恢复血流灌注,予腹腔滴注适量青霉素预防感染,缝合切口,碘伏消毒。IPC组和IPC-GdCl3组在恢复灌注3 min后再次夹上动脉夹3 min,然后松开动脉夹2 min后再次夹闭2 min,最后夹闭1 min后彻底取出动脉夹,缝合。再灌注24 h后(SCIRI后24 h为CaSR受体表达高峰[11])开始BBB(Basso Beattie Bresnahan locomotor rating scale)评分及提取脊髓组织。
1.4 BBB评分
各组大鼠再灌注24 h后分别予BBB评分,判断大鼠脊髓损伤情况。总共21个分级[12],无可见后肢运动为0分;持续的掌面移动和协调步态,足趾保持抓地,主动爪始终平行于稳定的躯干,尾巴持续翘起为21分。评分完成后,每组取9只平均分别用于蛋白质印迹、免疫组化以及TUNEL法检测。
1.5 蛋白质印迹检测大鼠脊髓组织中CaSR和Caspase-12的表达
处死大鼠,取L2~L4节段脊髓,采用裂解法提取蛋白,并测定蛋白浓度。配置分离胶、浓缩胶,连夹板放入电泳装置,加电泳液,点样孔内加蛋白定量标志物4 μL,其余每孔加样本15~20 μL;电泳电压70 V,当蛋白泳至分离胶、浓缩胶分界线时,将电压调至120 V,待蛋白泳至凝胶底部时关闭电源;将凝胶上的蛋白转至PVDF膜,脱脂牛奶封闭;加一抗(CaSR 1 ∶500;Caspase-12 1 ∶500;β-肌动蛋白1 ∶1 000),4 ℃慢摇过夜;TBST洗脱,加二抗(1 ∶5 000),常温慢摇1 h并洗脱;曝光显影,测定灰度值并定量分析。
1.6 免疫组织化学检测大鼠脊髓组织中CaSR和Caspase-12的表达
各组大鼠麻醉,打开腹腔,心尖部插入细管,先用PBS灌洗,然后4%低聚甲醛固定,分离取出L2~L4节段脊髓组织,甲醛浸泡12 h后用PBS充分洗净;适当修剪组织,予脱水、二甲苯透明,而后制备石蜡切片。使用试剂盒分别进行免疫组化染色。石蜡切片脱蜡,PBS冲洗;3%H2O2孵育10 min;冲洗后稀释山羊血清封闭10 min;倒去血清滴加一抗CaSR(1 ∶400)和Caspase-12(1 ∶400)室温孵育2 h;PBS冲洗后,二抗工作液显色剂复合物孵育30 min,再水洗、复染、脱水、透明、封片。镜下观察阳性表达,CaSR阳性呈棕色或褐色,Caspase-12阳性呈蓝色。
1.7 TUNEL法检测大鼠脊髓组织中神经细胞凋亡
大鼠处理及制备石蜡切片同免疫组化,各组操作均按照TUNEL荧光染色试剂盒说明书(罗氏)。荧光显微镜下观察脊髓组织,细胞核呈绿色即为TUNEL染色阳性细胞,各组予阳性细胞计数。
1.8 统计学分析
2 结果
2.1 各组大鼠再灌注后24 h BBB评分比较
假手术组、IR组、IPC组、IPC-GdCl3组和NPS2390组大鼠BBB评分分别为20.80±0.422、9.30±0.949、15.20±0.919、9.00±0.667、14.40±0.843,总体差异有统计学意义(F=384.173,P<0.01);其中,各建模组BBB评分均明显高于假手术组(P<0.05),说明建模后大鼠后肢运动功能明显损伤,建模有效;IPC组、NPS2390组BBB评分均明显高于IR组(P<0.05),说明IPC、抑制剂NPS2390预处理这两种干预方法均能使大鼠后肢运动功能损伤减轻,IPC与NPS2390均具有相似的保护作用;IPC组BBB评分明显高于IPC-GdCl3组(P<0.05),说明经激动剂GdCl3预处理的大鼠IPC治疗效果较差。
2.2 各组大鼠脊髓组织中CaSR和Caspase-12蛋白表达比较
蛋白质印迹结果显示,各模型组CaSR和Caspase-12表达明显高于假手术组;IPC组较IR组CaSR及Caspase-12表达量明显降低,且NPS2390组较IR组CaSR及Caspase-12表达量也明显降低;IPC-GdCl3组较IPC组CaSR和Caspase-12表达量明显增加。说明IPC抑制了CaSR和Caspase-12的表达。见图1。
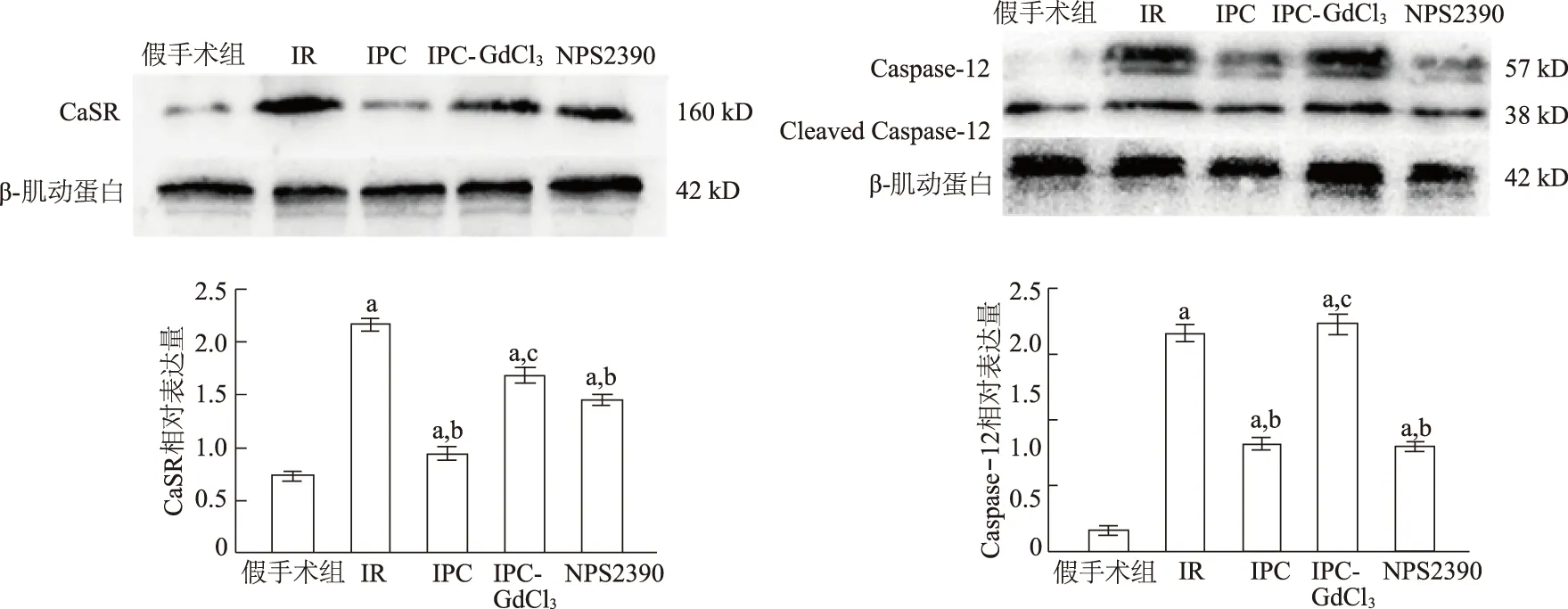
a:P<0.05,与假手术组比较;b:P<0.05,与IR组比较;c:P<0.05,与IPC组比较
2.3 各组大鼠脊髓组织CaSR和Caspase-12免疫组化结果比较
与假手术组相比,各模型组CaSR和Caspase-12表达均明显增加,说明各组建立SCIRI模型有效。与IR组相比,IPC组、NPS2390组CaSR和Caspase-12表达均明显降低;与IPC-GdCl3组相比,IPC组CaSR和Caspase-12表达也明显降低。说明IPC抑制了CaSR和Caspase-12的表达。见图2、表1。

图2 免疫组化观察大鼠脊髓组织CaSR和Caspase-12表达(×400)
2.4 各组大鼠脊髓组织神经细胞凋亡情况
TUNEL染色结果显示,假手术组可见极少凋亡染色阳性神经细胞。IR组凋亡神经细胞数相比IPC组明显增加(P<0.05),较NPS2390组也明显增加(P<0.05);IPC组较IPC-GdCl3组凋亡神经细胞数量明显减少(P<0.05)。见图3、表1。

图3 TUNEL荧光染色观察各组大鼠脊髓组织细胞凋亡情况(×200)

表1 各组大鼠脊髓组织免疫组化与TUNEL染色定量结果
3 讨论
SCIRI的发生和发展是包含多种机制的复杂病理过程,多年来一直没有成熟的治疗措施。缺血后适应最早发现并应用于心肌缺血再灌注损伤过程中,通过在损伤早期及时给予几个短暂的缺血再灌注循环,从而降低心肌耗氧量、改善心肌代谢,获得了良好的治疗作用[13]。近年来随着对IPC研究的深入,IPC开始应用于机体多个重要脏器中,相关研究表明在再灌注最早期即采取IPC治疗可能获得更好的效果[14]。受此启发,本研究在再灌注3 min立即行IPC治疗,并且以阶梯形式逐渐减少再灌注时间,结果证实这种方法确实显著提高了BBB评分,改善了大鼠后肢运动功能损伤。
CaSR是一种特殊跨膜受体,是G蛋白耦联受体超家族C家族成员,可调节细胞内钙离子的稳态,在细胞的增殖、凋亡等过程中起到关键作用[15-16]。有研究报道CaSR 激活增加了氧自由基产生,使组织缺血再灌注损伤加重[17]。为了探究IPC对CaSR的影响,本研究首先需要选择CaSR的特异性激动剂和抑制剂。多数研究者认为只需要在实验前2日连续大鼠尾静脉注射氯化钆(GdCl3)试剂,即可有效激活CaSR,增加其表达量[18],剂量以大鼠体重为指标30 μmol/kg为宜[19];在抑制剂方面,有报道称小剂量精胺可以抑制CaSR,不过其抑制作用与代谢有关系,难以精准把控,而NPS2390的组织富集作用较为稳定[20-21],以10 μmol/kg提前2日注射可减少CaSR表达,所以本研究将CaSR的抑制剂确定为NPS2390。TUNEL染色结果显示,建模各组细胞凋亡数均明显多于假手术组,说明SCIRI是一种短时间内难以逆转的损伤;IPC组及NPS2390组神经细胞凋亡数均明显低于IR组,说明IPC对大鼠SCIRI起到一定程度的保护作用,且与抑制剂保护作用相似。
本课题组前期的实验已经证实在大鼠SCIRI过程中,CaSR表达增加导致钙超载从而加速细胞凋亡,并且CaSR激动剂会加重大鼠SCIRI,CaSR抑制剂则一定程度缓解大鼠SCIRI[7,11]。本实验蛋白质印迹及免疫组化结果显示,建模各组CaSR表达均高于假手术组,说明大鼠SCIRI模型建立成功;IPC组及NPS2390组较IR组CaSR表达均明显减少,且IPC-GdCl3组CaSR表达量明显高于IPC组,反映出IPC与CaSR抑制剂作用性质相同,与CaSR激动剂则有拮抗作用,即IPC抑制了CaSR表达。
Caspase-12位于内质网外膜,是内质网应激介导的凋亡的关键蛋白酶[22]。内质网应激通过Caspase-12独立诱导细胞凋亡。当内质网受到损伤时,无活性的Caspase-12酶原被激活,具有活性的Caspase-12可以激活Caspase-9、Caspase-3等酶原,通过Caspase级联反应促使细胞凋亡,因此Caspase-12在启动内质网凋亡途径中具有核心作用[23]。本研究结果显示,IPC组Caspase-12表达明显低于IR组,可以看出IPC能够抑制Caspase-12表达;其余各组比较结果几乎与CaSR表达的组间比较一致。这是由于在大鼠脊髓缺血再灌注过程中,CaSR过表达引起神经细胞内钙超载,破坏了钙的稳态,从而诱发过度内质网应激,Caspase-12活化片段表达增多,经一系列复杂的信号转导最终发生神经细胞凋亡,因此IPC抑制了CaSR表达,继而同步抑制了Caspase-12的表达。另外,本研究发现IPC与CaSR抑制剂NPS2390具有类似的保护作用,但是临床上CaSR抑制剂几乎无应用,可能是由于CaSR存在于机体较多组织器官,盲目用药会引起难以预知的毒副作用。但IPC治疗效果是否优于抑制剂或者两者之间是否有预防及治疗上的协同作用,有待深入研究。
近年来关于大鼠脑组织缺血再灌注损伤的研究证实,远隔缺血后处理能够抑制神经细胞的CaSR表达[24],但是IPC调控CaSR表达的机制尚不明朗。我们推测其可能机制为:在脊髓发生缺血再灌注后第一时间进行IPC操作,使细胞很快适应灌注状态,部分已经激活的CaSR重新失去活性,这就解释了IPC使CaSR蛋白表达下调的原因。关于CaSR与Caspase-12的表达调控关系,目前认为CaSR的表达下调使Ca2+内流也相应减少,细胞内钙稳态相对平衡,诱发的内质网应激较少或者应激持续时间较短,继而Caspase-12活化减少,所以Caspase-12蛋白相应下调。
综上所述,IPC对大鼠SCIRI具有保护作用,且抑制脊髓组织中CaSR及Caspase-12的表达,其保护机制或可能与内质网应激减少有关。但IPC减轻脊髓缺氧复氧损伤的机制和信号转导途径错综复杂,仍需进一步探究。
